文档内容
1.3.1 氧化还原反应
本节课是高中化学的重要理论基础。氧化还原反应在中学化学阶段的知识中处于非常重要的地位,是
整个高中化学教学重点之一,是高中化学反应理论的基础,该知识点的应用贯穿于中学化学教材的始终,
同时也是日常生活、工农业生产和现代科技中经常遇到的一类重要的化学反应。在学习本节课之前,学生
在初中化学学习中已经接触了许多反应,并已经掌握对反应类型的分类方法(四个基本反应类型);也能
够从具体的反应去理解氧化反应和还原反应,但并没认识到氧化还原反应的本质特征;学生也学习了化合
价,能够判断简单物质的化合价,可以理解物质中化合价的变化,但并没有了解化合价变化的实质以及化
合价的变化与得失电子之间的关系。在这节课的学习中,学生要掌握好氧化还原反应的基本概念,深入理
解氧化还原反应的本质特征,才能在后续的元素化合物学习中理解化学反应的实质。
宏观辨识与微观探析:从宏观上理解化合价变化是氧化还原反应的表观现象,从微观上明确在氧化还
原反应中物质发生化合价变化的本质原因是电子的转移(得失和共用电子对偏移)。
证据推理与模型认知:建立氧化还原反应中的电子转移模型,并利用该模型理解氧化还原反应的本质。
科学探究与创新意识:学习氧化还原反应从得氧失氧的原始特征到化合价升降的表面现象,再到电子
转移的本质原因,层层推进,逐步探究深入的发展过程。通过对氧化还原反应的特征和本质的分析,学习
由表及里以及逻辑推理的科学探究方法。
科学精神与社会责任:形成氧化还原反应的化学概念,知道化学概念源于生活源于社会,而化学知识
又服务生活服务社会,体验化学概念从生活经验到理性规范的演变过程。
理解氧化还原反应的概念,能够用电子转移模型解释氧化还原反应。能够运用化合价的变化判断电子
的转移。
学生复习初中化学中氧化反应和还原反应的概念,复习初中关于元素化合价的知识,预习本课内容;
教师准备多媒体课件。
【引入】苹果削皮后放置一段时间会变黄色(或褐色),喝红酒之前要先把红酒倒入醒酒器中,敞口放置一段时间,喝起来更加绵柔滑润,更加可口;以上都是生活中不起眼的小常识,但是在这些常识中实际蕴
含着一些重要的化学理论。本节课,我们就要以这些常识为开端,学习一种新的反应类型。(展示切开一
段时间的苹果和刚刚切开的苹果)
【设疑】本章中同学们一直在学习分类,比如,同学们初中学习了将化学反应分为四个基本反应类型,上
一节课学习了离子反应,那么同学们想想你还知道其他的反应类型吗?(氧化反应和还原反应)
【设疑】通过初中的学习,同学们了解了氧化反应和还原反应两种反应类型,什么是氧化反应,什么是还
原反应呢?(物质得氧的反应是氧化反应,物质失氧的反应是还原反应)
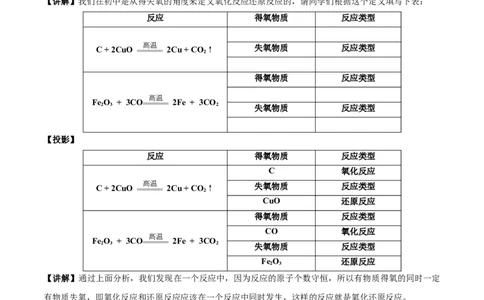
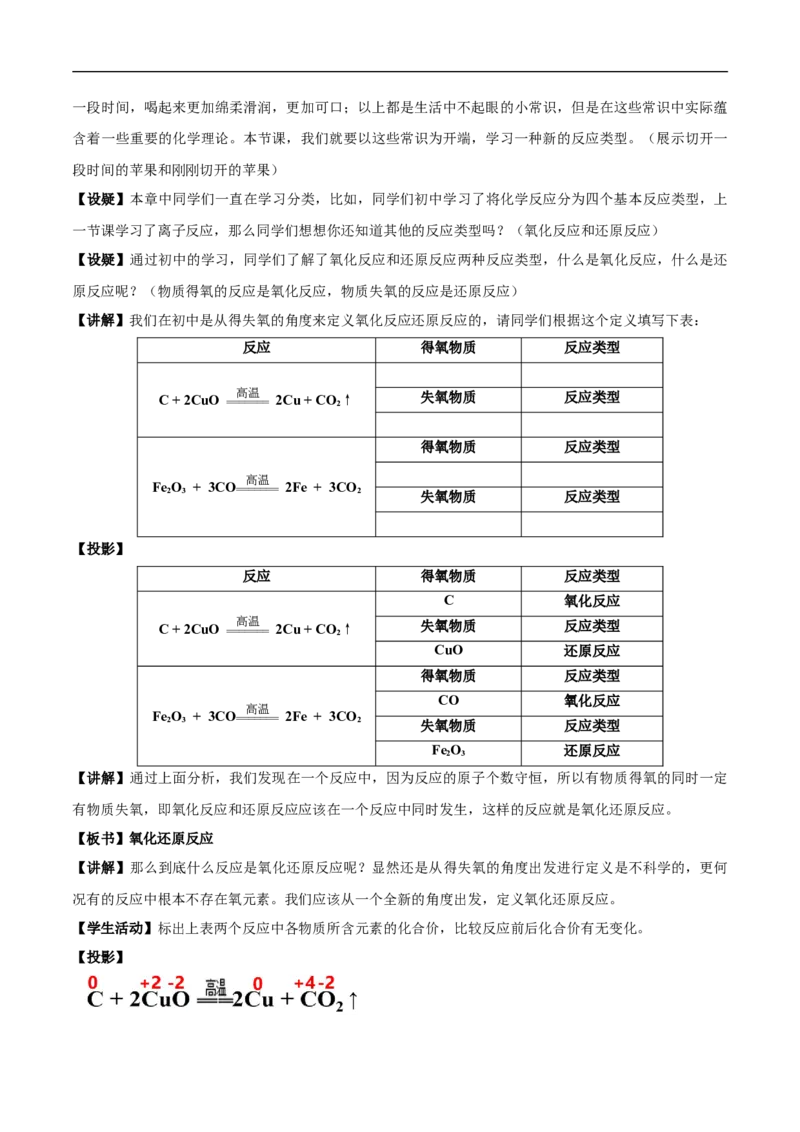
【讲解】我们在初中是从得失氧的角度来定义氧化反应还原反应的,请同学们根据这个定义填写下表:
反应 得氧物质 反应类型
C + 2CuO == 高 == 温 === 2Cu + CO 2 ↑ 失氧物质 反应类型
得氧物质 反应类型
高温
Fe
2
O
3
+ 3CO======= 2Fe + 3CO
2 失氧物质 反应类型
【投影】
反应 得氧物质 反应类型
C 氧化反应
C + 2CuO == 高 == 温 === 2Cu + CO 2 ↑ 失氧物质 反应类型
CuO 还原反应
得氧物质 反应类型
CO 氧化反应
高温
Fe
2
O
3
+ 3CO======= 2Fe + 3CO
2 失氧物质 反应类型
FeO 还原反应
2 3
【讲解】通过上面分析,我们发现在一个反应中,因为反应的原子个数守恒,所以有物质得氧的同时一定
有物质失氧,即氧化反应和还原反应应该在一个反应中同时发生,这样的反应就是氧化还原反应。
【板书】氧化还原反应
【讲解】那么到底什么反应是氧化还原反应呢?显然还是从得失氧的角度出发进行定义是不科学的,更何
况有的反应中根本不存在氧元素。我们应该从一个全新的角度出发,定义氧化还原反应。
【学生活动】标出上表两个反应中各物质所含元素的化合价,比较反应前后化合价有无变化。
【投影】【讲解】根据方程式中物质所含元素的化合价,同学们明显可以发现反应中存在化合价的变化。根据这种
变化,同学们模仿下表的第一行,将表格补充完整。
反应 得氧物质的转化 化合价变化 反应类型
C→CO 升高(0→+4) 氧化反应
2
高温
C + 2CuO ======= 2Cu + CO 2 ↑ 失氧物质的转化 化合价变化 反应类型
得氧物质的转化 化合价变化 反应类型
高温
Fe
2
O
3
+ 3CO======= 2Fe +
3CO 失氧物质的转化 化合价变化 反应类型
2
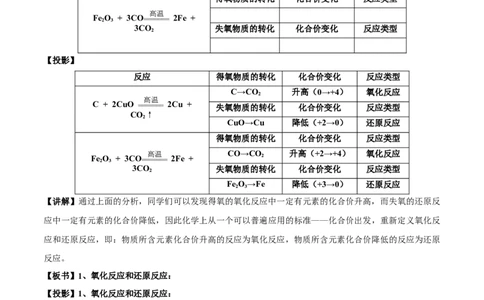
【投影】
反应 得氧物质的转化 化合价变化 反应类型
C→CO 升高(0→+4) 氧化反应
2
高温
C + 2CuO ======= 2Cu + 失氧物质的转化 化合价变化 反应类型
CO↑
2
CuO→Cu 降低(+2→0) 还原反应
得氧物质的转化 化合价变化 反应类型
高温 CO→CO 升高(+2→+4) 氧化反应
Fe
2
O
3
+ 3CO======= 2Fe + 2
3CO 失氧物质的转化 化合价变化 反应类型
2
FeO→Fe 降低(+3→0) 还原反应
2 3
【讲解】通过上面的分析,同学们可以发现得氧的氧化反应中一定有元素的化合价升高,而失氧的还原反
应中一定有元素的化合价降低,因此化学上从一个可以普遍应用的标准——化合价出发,重新定义氧化反
应和还原反应,即:物质所含元素化合价升高的反应为氧化反应,物质所含元素化合价降低的反应为还原
反应。
【板书】1、氧化反应和还原反应:
【投影】1、氧化反应和还原反应:
氧化反应:物质所含元素化合价升高的反应
还原反应:物质所含元素化合价降低的反应
【讲解】根据上述的分析,我们将氧化反应和还原反应的概念进行了扩大,不再看物质得失氧,而是观察
反应前后物质所含元素的化合价的变化。
【练习】判断下列过程是氧化反应还是还原反应:
(1)Cu→CuO ( ) (2)Cu→CuCl ( )
2
(3)N→NH ( ) (4)FeCl →FeCl ( )
2 3 2 3【投影】判断下列过程是氧化反应还是还原反应:
(1)Cu→CuO (氧化反应) (2)Cu→CuCl (氧化反应)
2
(3)N→NH (还原反应) (4)FeCl →FeCl (氧化反应)
2 3 2 3
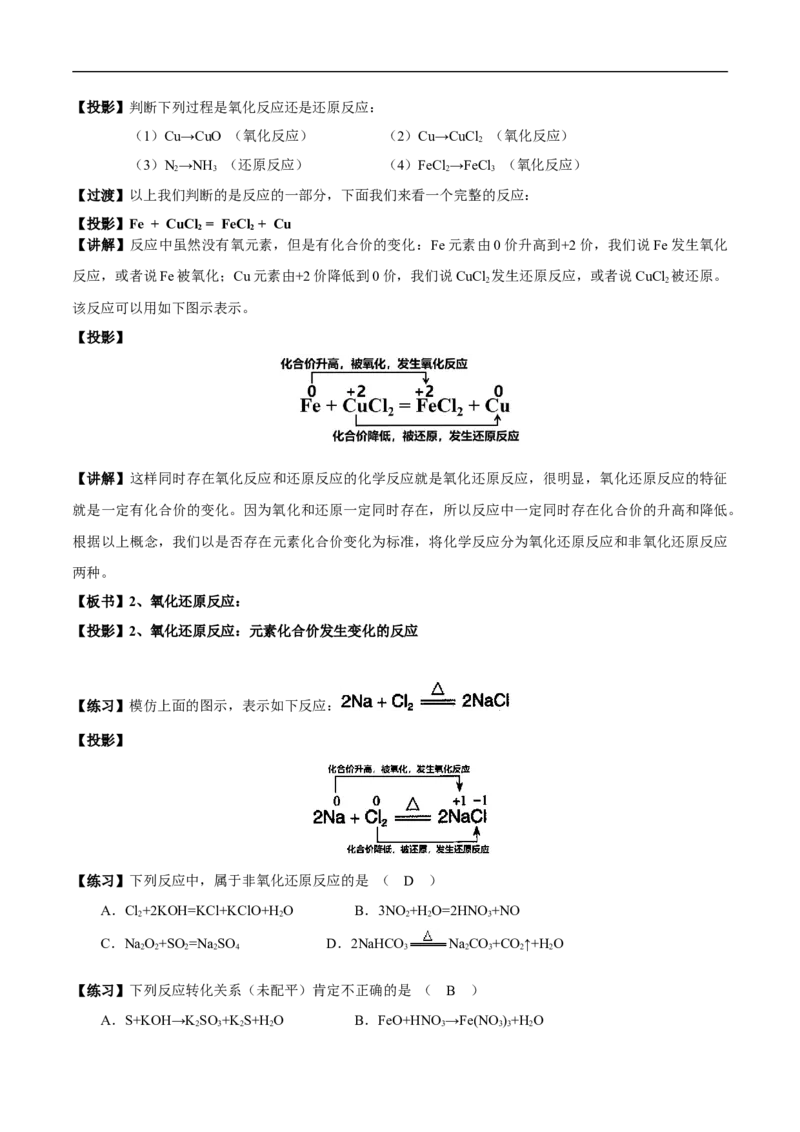
【过渡】以上我们判断的是反应的一部分,下面我们来看一个完整的反应:
【投影】Fe + CuCl = FeCl + Cu
2 2
【讲解】反应中虽然没有氧元素,但是有化合价的变化:Fe元素由0价升高到+2价,我们说Fe发生氧化
反应,或者说Fe被氧化;Cu元素由+2价降低到0价,我们说CuCl 发生还原反应,或者说CuCl 被还原。
2 2
该反应可以用如下图示表示。
【投影】
【讲解】这样同时存在氧化反应和还原反应的化学反应就是氧化还原反应,很明显,氧化还原反应的特征
就是一定有化合价的变化。因为氧化和还原一定同时存在,所以反应中一定同时存在化合价的升高和降低。
根据以上概念,我们以是否存在元素化合价变化为标准,将化学反应分为氧化还原反应和非氧化还原反应
两种。
【板书】2、氧化还原反应:
【投影】2、氧化还原反应:元素化合价发生变化的反应
【练习】模仿上面的图示,表示如下反应:
【投影】
【练习】下列反应中,属于非氧化还原反应的是 ( D )
A.Cl+2KOH=KCl+KClO+H O B.3NO +H O=2HNO +NO
2 2 2 2 3
C.NaO+SO=Na SO D.2NaHCO NaCO+CO ↑+H O
2 2 2 2 4 3 2 3 2 2
【练习】下列反应转化关系(未配平)肯定不正确的是 ( B )
A.S+KOH→KSO +K S+HO B.FeO+HNO →Fe(NO )+H O
2 3 2 2 3 3 3 2C.Cu O+HSO →CuSO +Cu+H O D.NH NO →NO+H O
2 2 4 4 2 4 3 2 2
【讲解】现在我们回到最初的问题,苹果削皮后放置一段时间会变黄色(或褐色),切开的苹果中的某些
化学物质与空气中的氧气接触,该化学物质被氧化,颜色发生了变化导致的;而红酒喝之前需要醒酒,其
中一个重要的原因是让红酒与氧气充分接触,使某些化学物质被氧化,从而使口感更柔和。这些都是氧化
还原理论在生活中的实际应用。
【过渡】既然氧化还原反应的重要特征是有元素的化合价变化,那么氧化还原反应中为什么会出现元素化
合价的变化呢?即氧化还原反应的本质是什么呢?
【板书】3、氧化还原反应的本质:
【投影】3、氧化还原反应的本质:
【讲解】首先,我们来研究一个刚才讨论过的氧化还原反应: 。反应中Na的化合
价由0价升高为+1价,这个过程是如何实现的呢?在离子反应的章节中,我们已经知道了NaCl中实际存
在的是Na+和Cl-,反应中,Na的化合价为0价,转化为Na+其化合价就变为+1价了。根据初中化学中原子
结构的知识,同学们可以明确,这种转化是因为Na原子失去了最外层的一个电子。
【设疑】反应中Na原子失去了一个最外层电子,那么失去的电子去哪里了?(给了Cl)
【讲解】反应中Cl得到了Na失去的一个电子转化为Cl-其化合价也由0价转化为-1价。
【投影】演示反应中Na原子和Cl原子的得失电子情况。
【讲解】根据上面的分析,反应的化合价变化的过程可以进行如下的表述:Na原子的最外层只有1个电子,
Cl原子的最外层有7个电子,Na失去最外层的1个电子转化为Na+,达到最外层8电子的稳定结构;Cl原
子得到Na原子失去的1个电子,转化为Cl-也达到8电子的稳定结构。反应中Na失电子,化合价升高,被
氧化,发生氧化反应;Cl得电子,化合价降低,被还原,发生还原反应。因此我们说,该反应的本质是电
子的得失。
【投影】反应的电子得失可以进行如下的表示:
【讲解】上面的图示中,得失电子使用了m×ne-的形式进行表示,其中m代表发生电子得失的原子个数,n
代表每个原子得失的电子数(当m或n为1时要省略)。这种表示形式就是氧化还原反应的双线桥表示。
【练习】以上面的双线桥表示形式为例,对下面的反应进行双线桥分析:
(1)Zn + 2H+ = Zn2+ + H ↑ (2)2K + S = K S
2 2
【投影】【讲解】除了上面的情况以外,在电解质的章节中,同学们还知道有的电解质是以分子的形式存在的,溶
于水时在水分子作用下,才会电离为可移动的阴阳离子,既然该物质不是以离子形式存在的,那么形成该
物质的过程发生的就不会是电子的转移。下面我们以H 和Cl 反应生成HCl为例,来分析此类物质形成过
2 2
程中化合价变化的原因。
【投影】
【讲解】氢原子最外层有1个电子,氯原子最外层有7个电子,两者都倾向于得到1个电子达到稳定结构,
所以并没有进行电子得失,而是两者各以最外层1个电子组成一个共用电子对。该电子对受到两个原子核
的共同吸引,两个原子可以共同占有这1对电子,从而使两个原子都达到了稳定结构。
【投影】演示共用电子对的形成过程
【过渡】那么这种形成共用电子对的反应中,化合价是如何发生变化的呢?
【讲解】H和Cl通过形成共用电子对转化为HCl分子,由于氯原子吸引共用电子对的能力强于氢原子,共
用电子对偏向于氯原子而偏离于氢原子,所以在HCl中H的化合价为+1,Cl的化合价为-1。从而得到,在
该反应中,H元素的化合价由0价升高至+1价,H 被氧化;Cl元素的化合价由0价降低至-1价,Cl 被还
2 2
原。反应发生化合价变化的原因是:发生了共用电子对的偏移。
【设疑】根据上面的分析,同学们互相讨论回答下面的问题:NH 中N和H的化合价为什么分别是-3和
3
+1?(NH 中N原子和H原子之间形成了3个共用电子对,其中3个共用电子对都偏向于N原子,所以N
3
显-3价;3个H原子中每个H原子都有1个共用电子对偏离,所以3个H都显+1价)
【总结】由上,氧化还原反应的本质是电子的转移(电子得失或共用电子对偏移)。失电子(或电子对偏
离),化合价升高,被氧化,发生氧化反应;得电子(或电子对偏向),化合价降低,被还原,发生还原
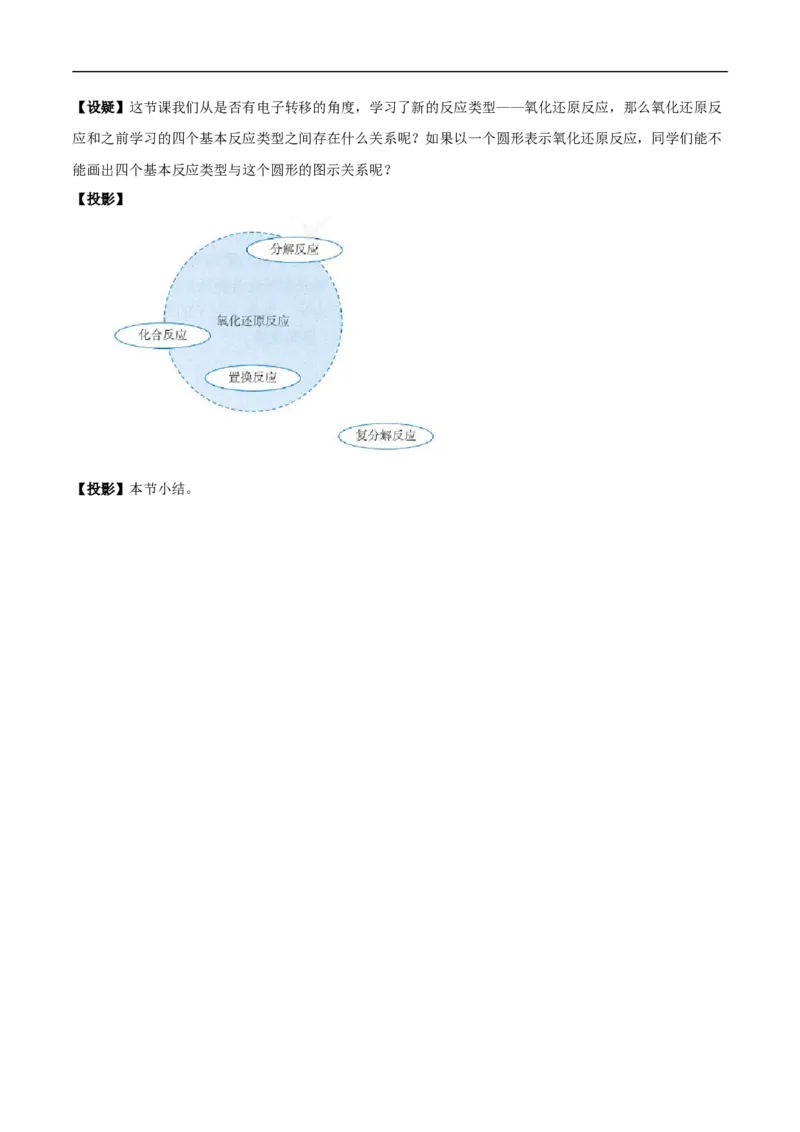
反应。【设疑】这节课我们从是否有电子转移的角度,学习了新的反应类型——氧化还原反应,那么氧化还原反
应和之前学习的四个基本反应类型之间存在什么关系呢?如果以一个圆形表示氧化还原反应,同学们能不
能画出四个基本反应类型与这个圆形的图示关系呢?
【投影】
【投影】本节小结。