文档内容
格致课堂
第一课时 活泼的金属单质—钠(学案)
1、了解钠的物理性质
2、掌握钠与氧气的反应与现象
3、掌握钠与水的反应与现象
钠与氧气、钠与水的反应及现象
初中学习的金属活动性顺序为: ,氧化还原反应
中氧化剂的定义是 ;还原剂的定义
是 ;
钠的单质
从物质分类的角度分析,钠属于 ;
从氧化还原的角度分析,钠一定具有 ;
根据金属活动性分析,钠是 ;
总结: 。
从原子结构的角度分析,钠有强还原性的原因是 。
【实验2-1】操作:用 取一小块钠,用滤纸吸干表面的 后,用刀切去一端的外皮,观察钠
的光泽和颜色,并注意新切开的钠的表面所发生的变化。
现象:金属钠的状态为 ,保存在 中,用小刀切开,其表面有
一、钠的物理性质:
二、钠的化学性质:
1、与氧气的反应:新切开的金属钠光亮的表面 ,是因为钠与 发生了反
应,在钠的表面形成了一薄层 ,这种氧化物是 色的 。
方程式为:
【思考】钠为什么需要保存在煤油中?
【思考】钠为什么可以保存在煤油中?格致课堂
在实验室中通常把金属钠保存在 中
【实验2-2】将一个干燥的坩埚加热,同时切取一块绿豆大的钠,迅速投到热坩埚中。继续加热坩埚片刻,
待钠熔化后立即撤掉酒精灯,观察现象。
观察到的现象
化学方程式:
钠是一种具有强还原性的金属单质,可以与很多非金属单质反应,如: 等。
2、钠与水的反应:
【交流讨论】从物质组成和氧化还原的角度分析预测一下,钠与水反应的产物应该是什么?
(钠与水反应应该得到 )
【分组实验】向水槽中加入一定量的水,滴加几滴酚酞,投入一块绿豆大的钠,待实验完后,观察实验现
象。
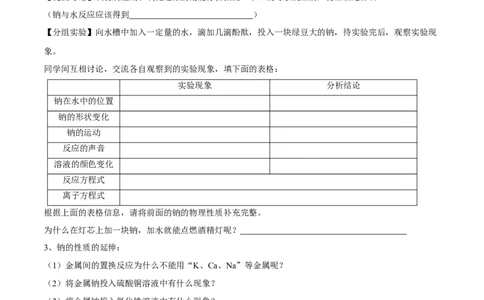
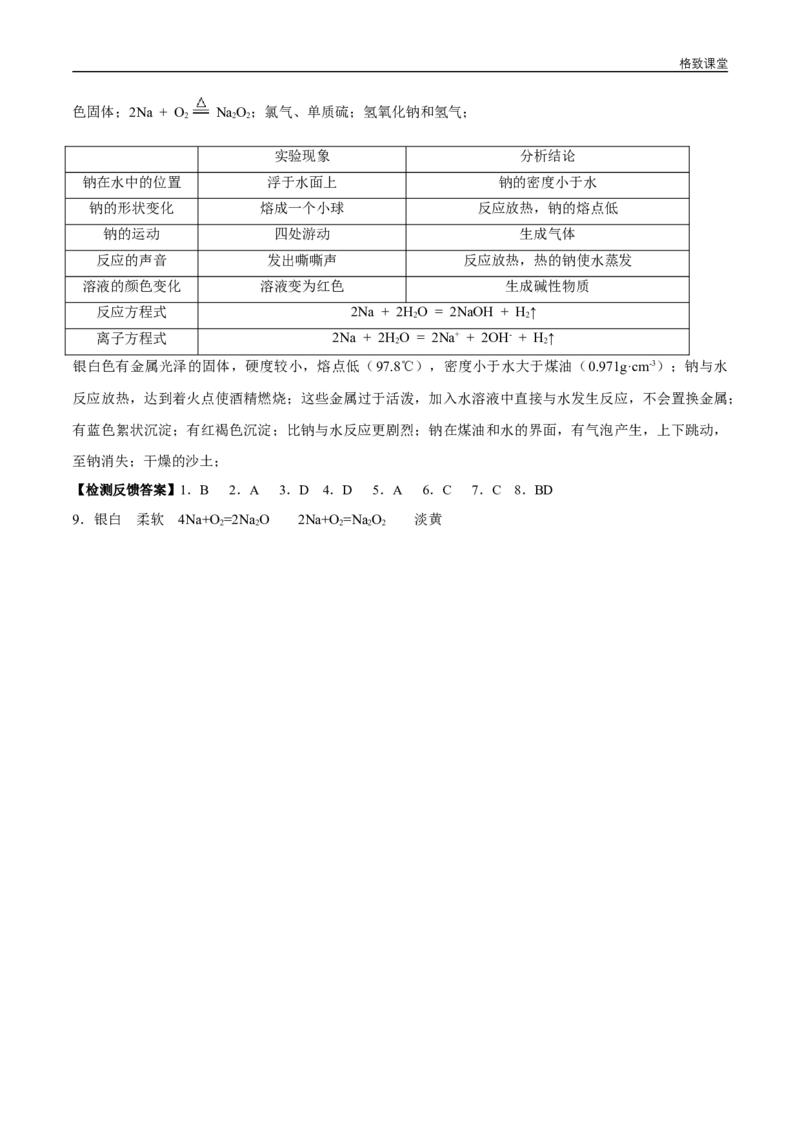
同学间互相讨论,交流各自观察到的实验现象,填下面的表格:
实验现象 分析结论
钠在水中的位置
钠的形状变化
钠的运动
反应的声音
溶液的颜色变化
反应方程式
离子方程式
根据上面的表格信息,请将前面的钠的物理性质补充完整。
为什么在灯芯上加一块钠,加水就能点燃酒精灯呢?
3、钠的性质的延伸:
(1)金属间的置换反应为什么不能用“K、Ca、Na”等金属呢?
(2)将金属钠投入硫酸铜溶液中有什么现象?
(3)将金属钠投入氯化铁溶液中有什么现象?
(4)预测钠与浓盐酸反应的现象。
(5)预测钠投入煤油和水的混合物中的现象。
(6)金属钠失火应该用什么灭火? 。
1.下列关于钠的叙述中,不正确的是( )
A.钠燃烧时发出黄色的火焰格致课堂
B.钠燃烧时生成氧化钠
C.钠有很强的还原性
D.钠原子的最外层只有一个电子
2.下列物质放置在空气中,因发生氧化还原反应而变质的是( )
A.Na B.NaCl C.NaOH D.NaO
2
3.取一小块钠放在玻璃燃烧匙里加热,下列实验现象正确的是( )
①金属先熔化 ②在空气中燃烧火焰呈黄色 ③燃烧时火星四射 ④燃烧后生成淡黄色固体
⑤燃烧后生成白色固体
A.①②③ B.①②④ C.①②⑤ D.①③⑤
4.在烧杯中加入水和苯(密度:0.88g/cm3)各50mL,将一小粒钠投入烧杯中,观察到的现象是
A.钠在水层中反应并四处游动 B.钠停留在苯层中不发生反应
C.钠在苯的上面并四处游动 D.钠在苯与水的界面处反应并可能上下跳动
5.下列反应的离子方程式书写正确的是( )
A.氢氧化钠溶液和稀硫酸反应:H++OH-===H O
2
B.氯化镁溶液中加入澄清石灰水:Mg2++Ca(OH) ===Mg(OH) ↓+Ca2+
2 2
C.碳酸钙加入过量盐酸中:CO+2H+===CO ↑+HO
2 2
D.钠和水反应:Na+HO===Na++OH-+H↑
2 2
6.当钠着火时,应选用灭火的是( )
A.煤油 B.水 C.沙土 D.泡沫灭火器
7.2.3g纯净金属钠在干燥空气中被氧化后得到3.5g固体,由此可判断其氧化物是( )
A.只有NaO B.只有NaO C.NaO和NaO D.无法确定
2 2 2 2 2 2
8.钠离子的性质是( )
A.有强还原性 B.有弱氧化性 C.有碱性 D.比钠原子稳定
9.金属钠是_______色固体,质地__________,将钠放在空气中一会儿,会发现金属钠的表面变暗,原因
是(用化学方程式表示)_____________________________________________;将钠放在空气中燃烧,其
反应的化学方程式是_____________________________,生成物的颜色是___________色。
【知识点填空答案】金属单质;还原性;很活泼的金属;钠是一种具有较强还原性的金属单质;钠原子的
最外层只有1个电子,容易失去,达到最外层8电子稳定结构;镊子;煤油;吸干表面的煤油;玻璃片;
固体;煤油;银白色金属光泽;银白色有金属光泽的固体,硬度较小;很快变暗了;氧气;氧化物;白;
氧化钠(NaO);4Na + O = 2NaO;钠与空气中的氧气快速反应,需要隔绝空气保存;钠不与煤油反
2 2 2
应且钠的密度大于煤油,即大于0.8g·cm-3;煤油或者石蜡油;钠先熔化再燃烧,发出黄色火焰,生成淡黄格致课堂
色固体;2Na + O NaO;氯气、单质硫;氢氧化钠和氢气;
2 2 2
实验现象 分析结论
钠在水中的位置 浮于水面上 钠的密度小于水
钠的形状变化 熔成一个小球 反应放热,钠的熔点低
钠的运动 四处游动 生成气体
反应的声音 发出嘶嘶声 反应放热,热的钠使水蒸发
溶液的颜色变化 溶液变为红色 生成碱性物质
反应方程式 2Na + 2HO = 2NaOH + H↑
2 2
离子方程式 2Na + 2HO = 2Na+ + 2OH- + H↑
2 2
银白色有金属光泽的固体,硬度较小,熔点低(97.8℃),密度小于水大于煤油(0.971g·cm-3);钠与水
反应放热,达到着火点使酒精燃烧;这些金属过于活泼,加入水溶液中直接与水发生反应,不会置换金属;
有蓝色絮状沉淀;有红褐色沉淀;比钠与水反应更剧烈;钠在煤油和水的界面,有气泡产生,上下跳动,
至钠消失;干燥的沙土;
【检测反馈答案】1.B 2.A 3.D 4.D 5.A 6.C 7.C 8.BD
9.银白 柔软 4Na+O=2Na O 2Na+O=Na O 淡黄
2 2 2 2 2