文档内容
第二章 海水中的重要元素——钠和氯
第一节 钠的几种化合物
钠的重要化合物是本章教材的重点之一,本节知识是钠单质性质的延伸和发展,钠单质在化学反应中
易失电子转变为钠的化合物,所以钠单质和钠的化合物之间存在着必然的因果关系。只有既了解了钠单质
的性质又了解了钠的化合物性质,才会比较全面的了解钠这种金属。通过钠单质及钠的重要化合物的学习,
既复习巩固了氧化还原反应和离子反应,又为学习其他几种重要金属化合物奠定基础和提供理论模式。
教学目标
1. 掌握氧化钠和过氧化钠的化学性质。
2. 掌握NaCO 和NaHCO 的共性和差异性。通过探究实验,比较碳酸钠和碳酸氢钠在水中的溶解性及热稳
2 3 3
定性,从而掌握鉴别它们的方法;培养学生的观察能力;训练学生运用对比的方法认识事物和全面地分析
事物的逻辑思维能力;完善学生的实验能力和创造思维能力。
核心素养
1. 通过探究氧化纳和过氧化钠性质的探究,建立通过实验得到性质结论的认知模型。
2. 通过掌握氧化钠和过氧化钠的化学性质、NaCO 和NaHCO 的共性和差异性,让学生明白性质
2 3 3
决定用途。
氧化钠和过氧化钠的化学性质,NaCO 和NaHCO 的共性和差异性。
2 3 3
查阅资料了解钠的化合物在生产生活中的应用;查阅关于侯氏制碱法相关内容,教师准备多媒体课件。
【引入】钠是一种活泼的金属元素,在自然界中不存在游离态的钠,钠元素都是以化合态存在于自然界的。
常见的钠的化合物有很多,如氢氧化钠是我们初中就学过一种常见的强碱,上节课我们学过的氧化钠和过
氧化钠,还有钠盐-----氯化钠、碳酸钠、碳酸氢钠、硫酸钠等。这节课我们重点学习氧化钠和过氧化钠以
及碳酸钠和碳酸氢钠。
【板书】1. 氧化钠和过氧化钠【阅读】教材中【思考与交流】
【学生板演】1. 4Na+ O ===2Na O(白色) 2Na+ O ====== Na O(淡黄色)
2 2 2 2 2
2. CaO + H O ==== Ca(OH) NaO + HO ====2 NaOH
2 2 2 2
【讲述】氧化钠是一种常见碱性氧化物,具有碱性氧化物的性质,如能跟水反应生成碱-----氢氧化钠;能
跟酸反应生成水和相应的盐。请写出氧化钠与盐酸反应的化学方程式。
【生板演】NaO + 2HCl=== 2NaCl+H O
2 2
【过渡】过氧化钠也是碱性氧化物吗?它具有哪些性质呢?下面我们一起来探究。
【板书】NaO 的性质:①物理性质:淡黄色固体。②化学性质
2 2
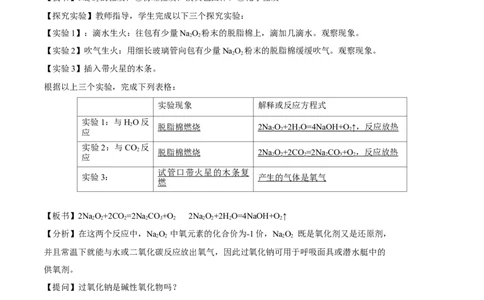
【探究实验】教师指导,学生完成以下三个探究实验:
【实验1】:滴水生火:往包有少量NaO 粉末的脱脂棉上,滴加几滴水。观察现象。
2 2
【实验2】吹气生火:用细长玻璃管向包有少量NaO 粉末的脱脂棉缓缓吹气。观察现象。
2 2
【实验3】插入带火星的木条。
根据以上三个实验,完成下列表格:
实验现象 解释或反应方程式
实验1:与HO反
2 脱脂棉燃烧 2NaO+2H O=4NaOH+O ↑ ,反应放热
应 2 2 2 2
实验2:与CO 反
2 脱脂棉燃烧 2NaO+2CO =2Na CO+O ,反应放热
应 2 2 2 2 3 2
试管口带火星的木条复
实验3: 产生的气体是氧气
燃
【板书】2NaO+2CO =2Na CO+O 2Na O+2H O=4NaOH+O ↑
2 2 2 2 3 2 2 2 2 2
【分析】在这两个反应中,NaO 中氧元素的化合价为-1价,NaO 既是氧化剂又是还原剂,
2 2 2 2
并且常温下就能与水或二氧化碳反应放出氧气,因此过氧化钠可用于呼吸面具或潜水艇中的
供氧剂。
【提问】过氧化钠是碱性氧化物吗?
【学生回答】
【教师点拨】不是,因为过氧化钠与水反应除了生成氢氧化钠外,还有氧气。
【追问】过氧化钠与盐酸反应产物又会是什么?请试着写出反应的方程式。
【板书】NaO+2HCl===2NaCl+H O+ O↑
2 2 2 2
【小结】氧化钠是碱性氧化物,过氧化钠不是碱性氧化物。
【过渡】日常生活中在做面包、馒头时,为了疏松可口,要加入哪些食品添加剂?
【生思考、回答】
【师追问】发酵粉、食用碱的主要成分是什么?【生思考、回答】
【师】这节课我们一起来共同探究碳酸钠和碳酸氢钠的性质。
【板书】2. 碳酸钠和碳酸氢钠
【师展示样品】
【教师讲解】观察一下,可以获得哪些信息?强调注意二者之间在外观上细小的差异。
【学生活动】观察、对比,完成下列表格。
物质 碳酸钠 碳酸氢钠
俗名 纯碱、苏打 小苏打
化学式 NaCO NaHCO
2 3 3
颜色、状态 白色粉末 细小白色晶体
【教师活动】引导学生猜想假设:碳酸钠和碳酸氢钠可能具有哪些性质?
【学生讨论】猜想假设,并将想法相互交流。
【教师总结】可溶于水、具有热稳定性、可与酸反应、可与碱反应、可与某些盐溶液反应等。
【过渡】根据刚才的猜想,我们一起来完成下列三个探究实验:
【展示】实验探究1 碳酸钠和碳酸氢钠的溶解性
实验步骤为:⑴在2支试管里分别加入少量碳酸钠和碳酸氢钠(各约1克);⑵滴入1mL水,
振荡,用手摸试管底部,观察现象。
⑶加入10mL水,用力振荡,观察现象;⑷向试管内滴入1-2滴酚酞溶液,观察现象。
【学生活动】记录实验现象、思考、交流、讨论、分析、得出结论。回答现象、笔记:
步骤 NaCO NaHCO
2 3 3
滴1mL水 加水结块变成晶体放热 加水部分溶解,感受不到热量变化
加10mL水 可溶解 部分溶解
滴 1-2 滴酚酞溶 溶液变红色 ( 较深 ) 溶液变微红色
液
结论 易溶于水,溶液呈碱性 易溶于水 ( 比 N aCO 略小 ) ;溶液呈碱性
2 3
( 比 Na CO 弱 )
2 3
【提问】根据实验你得到什么结论?
【学生思考总结】
【教师总结并板书】溶解性:NaCO>NaHCO
2 3 3
【展示】实验探究2:碳酸钠和碳酸氢钠的热稳定性
【学生阅读】图3-13碳酸钠和碳酸氢钠固体受热分解实验装置图。
【教师活动】引导:与实验室制备什么气体的反应装置相同?实验时要注意哪些问题?【学生活动】观看、分析、交流。与制备氧气的装置相同。
【强调】实验时要注意:1.试管口要略低于试管底;铁夹要夹在试管的中上部。
2.固体药品要平铺试管底部,加热时要先均匀受热再集中加热。
3.使用前要检查装置的气密性。
【教师演示】碳酸钠和碳酸氢钠固体分别受热分解实验
【学生活动】观察实验、对比实验现象。通过观察实验推导出碳酸氢钠受热方程式并得出碳酸钠固体比碳
酸氢钠固体热稳定性强的结论记录、领悟鉴别方法:
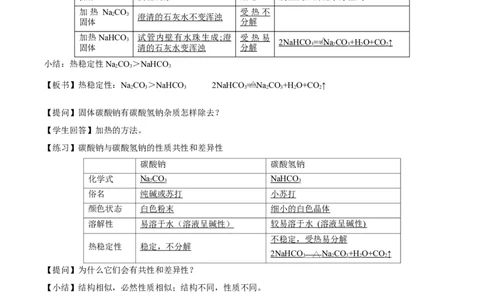
操作 实验现象 结论 发生反应的化学方程式
加热 NaCO 受热不
2 3 澄清的石灰水不变浑浊
固体 分解
加热NaHCO 试管内壁有水珠生成 ; 澄 受热易
3 2NaHCO ==Na CO+H O+CO↑
固体 清的石灰水变浑浊 分解 3 2 3 2 2
小结:热稳定性NaCO>NaHCO
2 3 3
【板书】热稳定性:NaCO>NaHCO 2NaHCO ==Na CO+H O+CO↑
2 3 3 3 2 3 2 2
【提问】固体碳酸钠有碳酸氢钠杂质怎样除去?
【学生回答】加热的方法。
【练习】碳酸钠与碳酸氢钠的性质共性和差异性
碳酸钠 碳酸氢钠
化学式 NaCO NaHCO
2 3 3
俗名 纯碱或苏打 小苏打
颜色状态 白色粉末 细小的白色晶体
溶解性 易溶于水(溶液呈碱性) 较易溶于水 ( 溶液呈碱性 )
不稳定 , 受热易分解
热稳定性 稳定 , 不分解
2NaHCO NaCO+H O+CO↑
3====== 2 3 2 2
【提问】为什么它们会有共性和差异性?
【小结】结构相似,必然性质相似;结构不同,性质不同。
【教师活动】大家知道节日燃放的五彩缤纷的烟花是怎么来的吗?
很多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色,这在化学上叫做焰色反应。
【演示实验:焰色反应】洗 → 烧 → 蘸 → 烧 → 洗
现象:灼烧Na2CO3溶液时,火焰呈黄色;当灼烧K2CO3溶液时,透过蓝色钴玻璃可观察到火焰呈紫色。
结论:钠元素的焰色为黄色,钾元素的焰色为紫色。
【教师活动】焰色反应的注意事项
【课堂小结投影】
一、Na2O与Na2O2性质比较二、碳酸钠和碳酸氢钠的性质
三、焰色反应