文档内容
格致课堂
1.3.2 氧化剂和还原剂(学案)
1、理解氧化还原反应的中氧化剂、还原剂、氧化产物和还原产物的概念
2、理解氧化性和还原性的概念,能判断常见物质有的性质
3、能利用氧化还原反应方程式判断物质氧化性和还原性强弱
3、能用单线桥表示简单的氧化还原反应
1、氧化剂、还原剂、氧化产物和还原产物的判断;
2、能正确书写氧化还原反应的单线桥
氧化还原反应的本质是 ,反应中物质中元素化合价升高的原因是
;而物质中元素化合价降低的原因是 ;
对下面的反应进行双线桥分析:
通过上面分析,我们发现在反应中电子转移的方向为: 。我们可
以用如下的形式表示该反应的电子转移:
这个式子直观的表示了反应中电子的转移,2个Na原子转变为Na+一共失去2个电子,这2个电子给
了Cl,Cl 得到2个电子转变为2个Cl-,所以说反应中电子转移的方向是 ,电子转移
2 2
的数目为 。这种式子是反应的单线桥表示式。
【练习】模仿上面的单线桥表示式,写出下列反应的单线桥:
(1)Zn + 2H+ = Zn2+ + H ↑ (2)2K + S = K S
2 2
与双线桥相比单线桥需要注意的是:
1、 ;
2、 ;
3、 。格致课堂
1、氧化剂和还原剂:
氧化剂:
还原剂:
【练习】根据上面的定义,判断下面反应的氧化剂、还原剂、氧化产物和还原产物:
Zn + 2H+ = Zn2+ + H ↑
2
(氧化剂: ;还原剂: ;氧化产物: ;还原产物: )
根据上面的判断,我们可以得到,氧化还原反应可以表示成如下的过程:
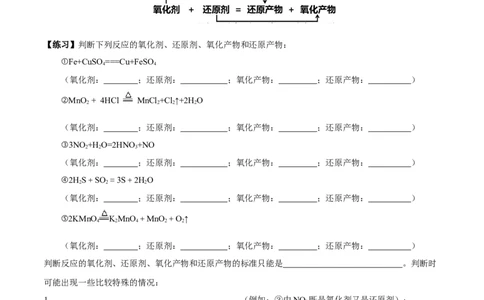
【练习】判断下列反应的氧化剂、还原剂、氧化产物和还原产物:
①Fe+CuSO===Cu+FeSO
4 4
(氧化剂: ;还原剂: ;氧化产物: ;还原产物: )
②MnO + 4HCl MnCl +Cl↑+2H O
2 2 2 2
(氧化剂: ;还原剂: ;氧化产物: ;还原产物: )
③3NO +H O=2HNO +NO
2 2 3
(氧化剂: ;还原剂: ;氧化产物: ;还原产物: )
④2HS+SO =3S+2HO
2 2 2
(氧化剂: ;还原剂: ;氧化产物: ;还原产物: )
⑤2KMnO KMnO +MnO +O↑
4 2 4 2 2
(氧化剂: ;还原剂: ;氧化产物: ;还原产物: )
判断反应的氧化剂、还原剂、氧化产物和还原产物的标准只能是 。判断时
可能出现一些比较特殊的情况:
1、 (例如:③中NO 既是氧化剂又是还原剂);
2
2、 (例如:⑤中还原产物是KMnO 和MnO )。
2 4 2
2、氧化性和还原性:
氧化性:
还原性:
如何判断物质是否具有氧化性或者还原性呢?
【练习】判断下列物质具有氧化性还是还原性:
H+ ( ) Fe ( ) S ( )格致课堂
【小知识】红酒的某些成分在储存的过程中会被氧气氧化,而使红酒的口感变差。所以我们应该在红酒中
加入一些 。二氧化硫就是这种加入的 ,所以我们说二氧化硫应该具
有 。同学们去查阅资料会发现,很多资料称加入的二氧化硫为抗氧化剂,你理解什么
是抗氧化剂? 。
化学上比较常见的氧化剂有: 等;
比较常见的还原剂有: 等。
【练习】HCl有氧化性还是还原性?( );MnO 有氧化性还是还原性?
2
( )判断反应MnO + 4HCl MnCl +Cl↑+2H O中的氧化剂是
2 2 2 2
,还原剂是 。为什么在这个反应里,HCl是还原剂而MnO 是氧化剂呢?
2
3、氧化性还原性强弱的判断:
判断氧化性和还原性强弱的方法是: 。
例如,在反应Fe+CuSO==Cu+FeSO 中氧化剂是 ,氧化产物是 ,就可以得
4 4
到结论:氧化性是 ;还原剂是 ,还原产物是 ,就可以得到
结论:还原性是 。
【练习】根据下列反应,判断氧化性强弱正确的是( )
(1)2HS+O===2S↓+2H O (2)4NaI+O+2H O===4NaOH+2I (3)NaS+I ===2NaI+S↓
2 2 2 2 2 2 2 2
A.O>I>S B.O>S>I C.I>O>S D.S>I>O
2 2 2 2 2 2 2 2
【交流讨论】在初中化学中,同学们学习过金属的置换反应:金属活动性较强的金属可以将金属活动性较
差的金属从其盐溶液中置换出来。请同学们互相讨论,用氧化还原的理论解释一下如上的结论。
1.根据下列反应:
(1)2Fe3++2I-===2Fe2++I
2
(2)Br +2Fe2+===2Fe3++2Br-
2
判断相关物质的氧化性由强到弱的顺序是( )
A.Fe3+>I >Br B.I>Fe3+>Br
2 2 2 2
C.Br >I >Fe3+ D.Br >Fe3+>I
2 2 2 2
2.在反应2KMnO =====KMnO +MnO +O↑中,还原产物是( )
4 2 4 2 2
A.只有KMnO B.只有MnO
2 4 2格致课堂
C.KMnO 和MnO D.O
2 4 2 2
3.发射“神舟”十号的长三丙火箭由三个子级构成。其中一子级上部装有液体四氧化二氮(N O),下部装
2 4
有液体偏二甲肼(C HN)(C为-1价,N为-3价)。发动机内燃烧的化学方程式为C HN +2NO===3N ↑
2 8 2 2 8 2 2 4 2
+2CO↑+4HO,该反应中( )
2 2
A.C HN 发生还原反应 B.C HN 是氧化剂
2 8 2 2 8 2
C.NO 发生氧化反应 D.NO 是氧化剂
2 4 2 4
4.用硫酸酸化的三氧化铬(CrO )遇酒精后,其颜色由红变为蓝绿色,用这种现象可测得司机是否酒后驾车,
3
反应如下:2CrO+3C HOH+3HSO ===Cr (SO )+3CHCHO+6HO。此反应的还原剂是( )
3 2 5 2 4 2 4 3 3 2
A.HSO B.CrO
2 4 3
C.Cr (SO ) D.C HOH
2 4 3 2 5
5.实验室常用热的 NaOH溶液洗去试管壁上的硫黄,其反应为 6NaOH+3S=====2NaS+NaSO +
2 2 3
3HO。在此反应中硫表现的性质是( )
2
A.氧化性 B.还原性
C.既无氧化性又无还原性 D.既有氧化性又有还原性
7.(1)写出铝粉与盐酸溶液反应的化学方程式并用单线桥法标出电子转移的方向和数目
________________________________________________________________________。
(2)上述反应过程中,发生还原反应的是________,判断的依据是________;发生氧化反应的是
________,判断的依据是______________。
(3)上述反应中,氧化剂是________,表现出________性,还原剂是________,表现出________性。
【知识点填空答案】 ;从Na转移到了Cl中;由Na到Cl;2e-;
; ;1、只标注在反应物一侧;2、指明电子转移的方向和数目;3、电子转移数目不需要用
m×ne-的形式表示;得电子化合价降低的物质,生成还原产物;失电子化合价升高的物质,生成氧化产物;
(氧化剂:H+;还原剂:Zn;氧化产物:Zn2+;还原产物:H);
2
;(氧化剂:CuSO ,还原剂:Fe,氧化产物:FeSO ,还原产物:
4 4
Cu);(氧化剂:MnO ,还原剂:HCl,氧化产物:Cl,还原产物:MnCl );(氧化剂:NO,还原剂:
2 2 2 2
NO,氧化产物:HNO,还原产物:NO);(氧化剂:SO ,还原剂:HS,氧化产物:S,还原产物:
2 3 2 2
S);(氧化剂:KMnO ,还原剂:KMnO ,氧化产物:O,还原产物:KMnO 和MnO );化合价的变
4 4 2 2 4 2格致课堂
化;某种物质有两种“身份”;某些物质的“身份”相同;物质得电子的能力;物质失电子的能力;判断
物质的化合价是否能升高或者降低;氧化性;还原性;氧化性和还原性;还原剂;还原剂;还原性;还原
剂;O、Cl、浓硫酸、HNO、KMnO 、FeCl ;金属单质(Al、Zn、Fe)、C、H、CO、KI;氧化性和还
2 2 3 4 3 2
原性;氧化性和还原性;MnO ;HCl;说明两者比较,HCl的还原性相对较强,MnO 的氧化性相对较强;
2 2
氧化剂的氧化性强于氧化产物,还原剂的还原性强于还原产物;CuSO ;FeSO ;CuSO >FeSO ;Fe;
4 4 4 4
Cu;Fe>Cu;A;这里金属活动性可以认为代表金属还原性,只有活动性强的金属置换活动性差的金属,
才能保证反应中,还原剂的还原性强于还原产物;
【检测反馈答案】1.D 2.C 3.D 4.D 5.D
6. (1) (2)HCl 因为氢元素的化合价降低,得到电子 Al 因为铝
元素的化合价升高,失去电子 (3)HCl 氧化 Al 还原