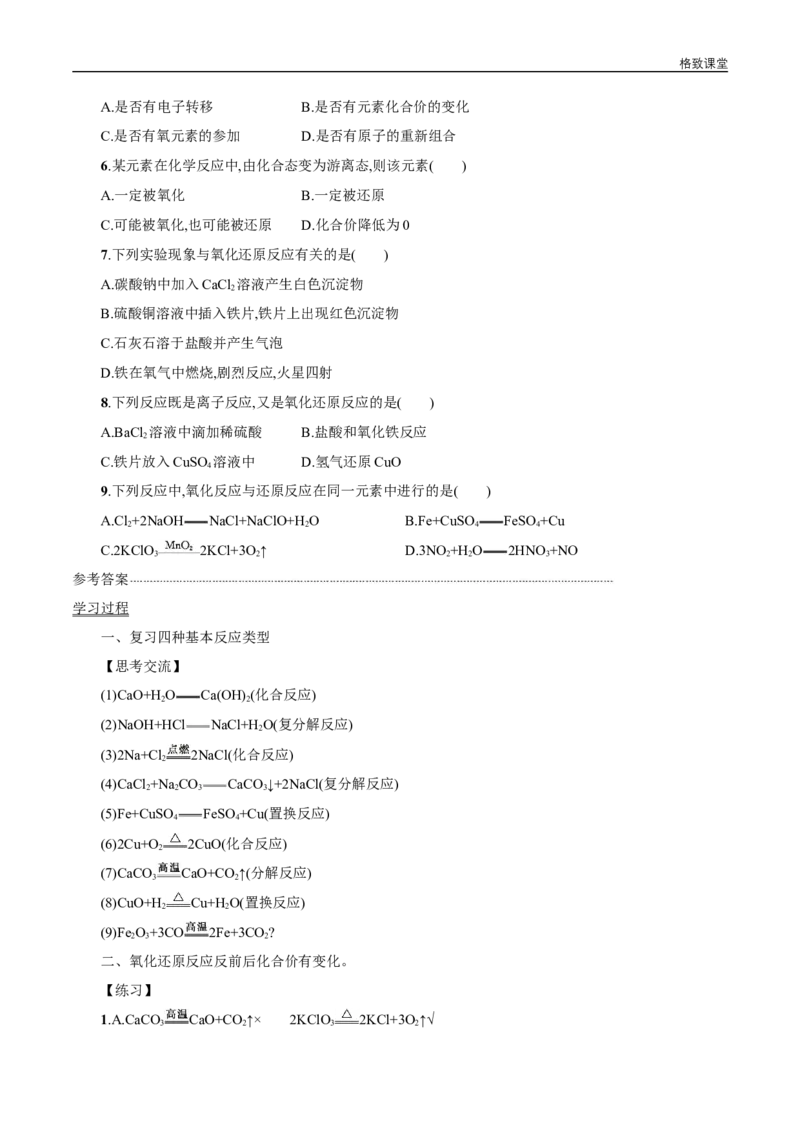文档内容
格致课堂
第一章 物质及其变化
第 3 节 氧化还原反应
3.1 氧化还原反应
1.了解氧化还原反应的特征。
2.了解氧化还原反应的实质。
3.了解氧化还原反应与四种基本反应类型的关系。
重点:氧化还原反应的判断方法
难点:氧化还原反应电子转移的分析
四种基本反应类型及氧化反应和还原反应
一、复习四种基本反应类型:
【思考交流】
下列9个化学反应分别属于什么类型?
(1)CaO+HO Ca(OH)
2 2
(2)NaOH+HCl NaCl+H O
2
(3)2Na+Cl 2NaCl
2
(4)CaCl +Na CO CaCO ↓+2NaCl
2 2 3 3
(5)Fe+CuSO FeSO +Cu
4 4
(6)2Cu+O 2CuO
2
(7)CaCO CaO+CO ↑
3 2
(8)CuO+H Cu+H O
2 2
(9)Fe O+3CO 2Fe+3CO
2 3 2
二、以化合价的表观现象分析氧化还原反应:
标出上述反应中各种元素的化合价,观察同种元素化合价前后变化情况,试归纳氧化还原反应及非氧化格致课堂
还原反应与元素化合价前后变化有何种关系?
【练习】
1.下列反应是否为氧化还原反应?
A.CaCO CaO+CO ↑ 2KClO 2KCl+3O ↑
3 2 3 2
B.CaCO +H O+CO Ca(HCO ) C+O CO
3 2 2 3 2 2 2
C.Zn+HSO ZnSO+H ↑
2 4 4 2
D.NaOH+HNO NaNO +H O
3 3 2
2.在反应MnO +4HCl(浓) MnCl +2H O+Cl ↑中, 元素化合价升高,被 (填“氧化”或
2 2 2 2
“还原”),发生 (填“氧化”或“还原”)反应; 元素化合价降低,被 (填“氧
化”或“还原”),发生 (填“氧化”或“还原”)反应。
三、分析氧化还原反应与四种基本反应类型的关系
(1)氧化还原反应与四种基本反应类型的关系如何?
(2)氧化还原反应与基本反应类型的关系及一般规律:
随堂检测
1.判断一个反应是否为氧化还原反应的标准是( )
A.是否有氧元素参加反应
B.是否为置换反应
C.同一元素的化合价在反应前后是否发生变化
D.是否为化合反应或分解反应
2.古诗词是古人为我们留下的宝贵精神财富。下列诗句中不涉及氧化还原反应的是( )
A.野火烧不尽,春风吹又生
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.粉身碎骨浑不怕,要留清白在人间
D.爆竹声中一岁除,春风送暖入屠苏
3.下列类型的反应,一定发生电子转移的是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
4.以元素化合价升降的观点分析下列各化学反应,其中不属于氧化还原反应的是( )
A.Mg+2HCl MgCl +H ↑ B.H +Cl 2HCl
2 2 2 2
C.CuO+H Cu+H O D.CaCl +Na CO CaCO ↓+2NaCl
2 2 2 2 3 3
5.有关氧化还原反应实质的说法中正确的是( )格致课堂
A.是否有电子转移 B.是否有元素化合价的变化
C.是否有氧元素的参加 D.是否有原子的重新组合
6.某元素在化学反应中,由化合态变为游离态,则该元素( )
A.一定被氧化 B.一定被还原
C.可能被氧化,也可能被还原 D.化合价降低为0
7.下列实验现象与氧化还原反应有关的是( )
A.碳酸钠中加入CaCl 溶液产生白色沉淀物
2
B.硫酸铜溶液中插入铁片,铁片上出现红色沉淀物
C.石灰石溶于盐酸并产生气泡
D.铁在氧气中燃烧,剧烈反应,火星四射
8.下列反应既是离子反应,又是氧化还原反应的是( )
A.BaCl 溶液中滴加稀硫酸 B.盐酸和氧化铁反应
2
C.铁片放入CuSO 溶液中 D.氢气还原CuO
4
9.下列反应中,氧化反应与还原反应在同一元素中进行的是( )
A.Cl +2NaOH NaCl+NaClO+H O B.Fe+CuSO FeSO +Cu
2 2 4 4
C.2KClO 2KCl+3O ↑ D.3NO +H O 2HNO+NO
3 2 2 2 3
参考答案
学习过程
一、复习四种基本反应类型
【思考交流】
(1)CaO+HO Ca(OH) (化合反应)
2 2
(2)NaOH+HCl NaCl+H O(复分解反应)
2
(3)2Na+Cl 2NaCl(化合反应)
2
(4)CaCl +Na CO CaCO ↓+2NaCl(复分解反应)
2 2 3 3
(5)Fe+CuSO FeSO +Cu(置换反应)
4 4
(6)2Cu+O 2CuO(化合反应)
2
(7)CaCO CaO+CO ↑(分解反应)
3 2
(8)CuO+H Cu+H O(置换反应)
2 2
(9)Fe O+3CO 2Fe+3CO ?
2 3 2
二、氧化还原反应反前后化合价有变化。
【练习】
1.A.CaCO CaO+CO ↑× 2KClO 2KCl+3O ↑√
3 2 3 2格致课堂
B.CaCO +H O+CO Ca(HCO )× C+O CO√
3 2 2 3 2 2 2
C.Zn+HSO ZnSO+H ↑√
2 4 4 2
D.NaOH+HNO NaNO +H O×
3 3 2
2.氯 氧化 氧化 锰 还原 还原
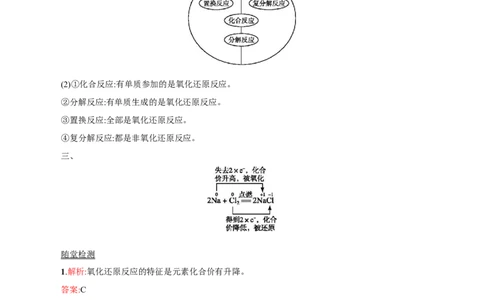
(1)
(2)①化合反应:有单质参加的是氧化还原反应。
②分解反应:有单质生成的是氧化还原反应。
③置换反应:全部是氧化还原反应。
④复分解反应:都是非氧化还原反应。
三、
随堂检测
1.解析:氧化还原反应的特征是元素化合价有升降。
答案:C
2.解析:A、B、D均有可燃物的燃烧,是氧化还原反应;C中:CaCO CaO+CO ↑,是非氧化还原反应。
3 2
答案:C
3.解析:置换反应一定属于氧化还原反应,一定有电子转移。
答案:C
4.解析:只要反应前后存在元素化合价升降的化学反应,都属于氧化还原反应。
答案:D
5.解析:氧化还原反应的实质是电子转移(包括电子得失和偏移),而外部特征是元素化合价发生变化。只格致课堂
要有元素化合价升降的反应就是氧化还原反应,与是否有氧元素参加无关。
答案:A
6.解析:元素以单质形态(游离态)存在时,化合价为0,元素以化合物形态(化合态)存在时,化合价有正价或
负价之分。当元素由游离态变为化合态时,元素的化合价升高和降低都有可能,所以可能被氧化,也可能被还
原。
答案:C
7.解析:A、B、C、D四项发生反应的化学方程式分别为:
A项,Na CO+CaCl CaCO ↓+2NaCl;
2 3 2 3
B项,CuSO +Fe FeSO +Cu;
4 4
C项,CaCO +2HCl CaCl +CO ↑+H O;
3 2 2 2
D项,3Fe+2O Fe O。
2 3 4
通过分析元素化合价升降结果可知A、C项中元素化合价没有发生变化,B、D项中有元素化合价发生
变化,属于氧化还原反应。
答案:BD
8.解析:A、B、C项对应的反应为离子反应,但A、B中的反应为复分解反应,C中的反应为置换反
应,Fe+CuSO FeSO +Cu或Fe+Cu2+ Fe2++Cu。
4 4
答案:C
9.解析:分析各反应元素化合价的变化可知:A项中被氧化和被还原的元素均为氯。B项中被氧化的元素
为铁,被还原的元素为铜。C项中被氧化的元素为氧,被还原的元素为氯。D项中被氧化和被还原的元素均为
氮。
答案:AD