文档内容
格致课堂
第四章 元素周期律
4.2.1 元素性质的周期性变化规律
1、知道元素原子结构的周期性变化。
2、能够以第三周期元素为例,说明同周期元素性质的递变情况。
3、在理解元素周期律的内容和实质的基础上,形成结构决定性质的学科思想。
1、以第三周期元素为例,说明同周期元素性质的递变情况。
2、微粒半径大小比较。
碱金属元素、卤素的原子结构和性质的,同主族元素的性质有着相似性和递变性。
一、探究核外电子排布、原子半径、化合价的周期性变化
【思考与交流】
观察表4-5,思考并讨论:随着原子序数的递增,元素原子的核外电子排布、原子半径和化合
价各呈现什么规律性的变化?
【总结】
同一周期元素,随着原子序数的递增,元素原子核外电子排布的变化规律是
;元素化合价的变化规律是 , 负 价 呈 现 由
的周期性变化;元素的原子半径呈现 的周期性变化。格致课堂
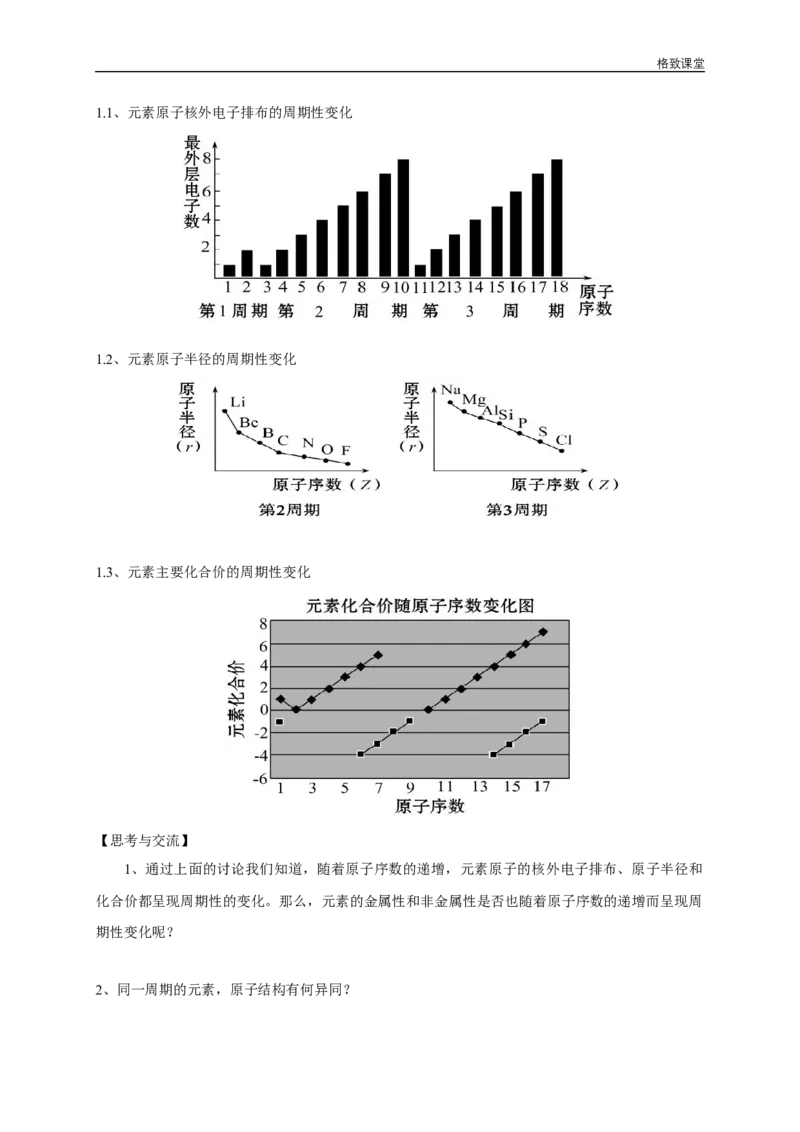
1.1、元素原子核外电子排布的周期性变化
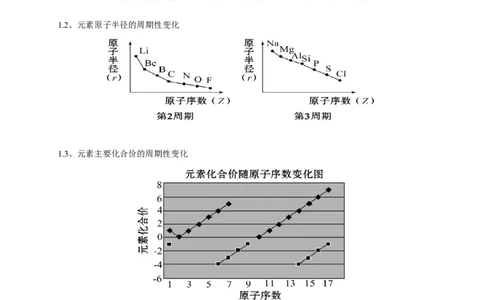
1.2、元素原子半径的周期性变化
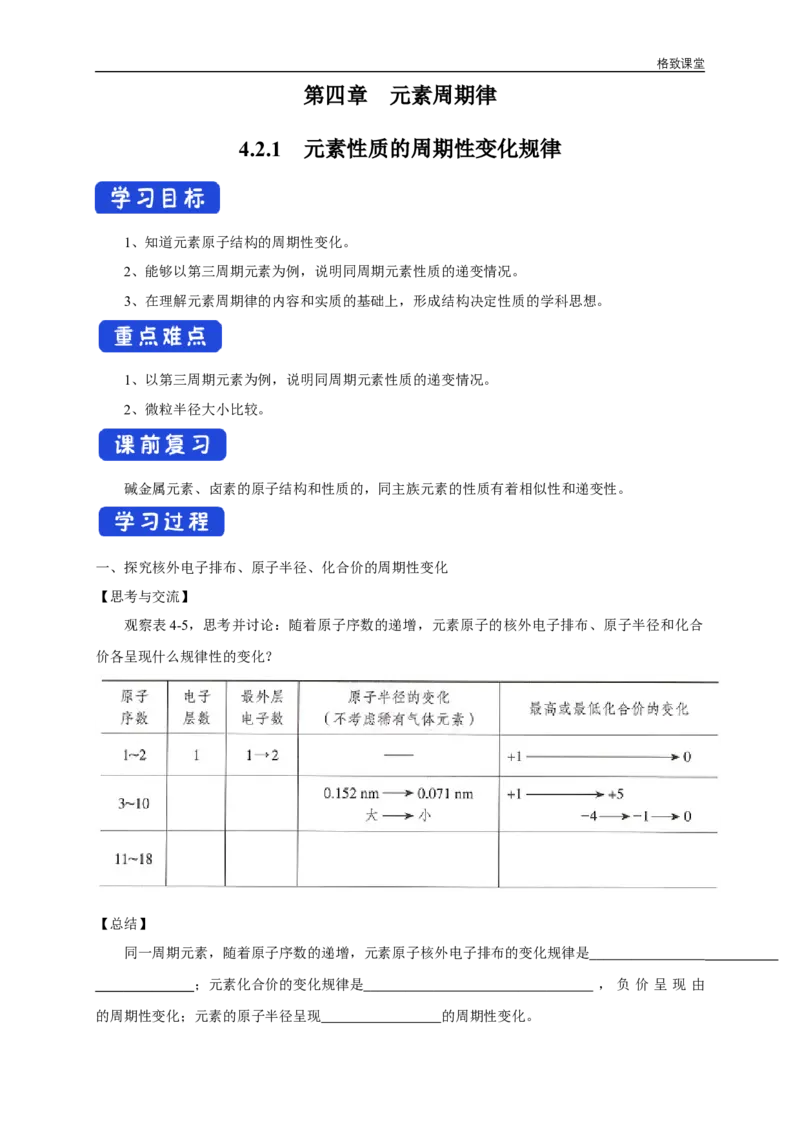
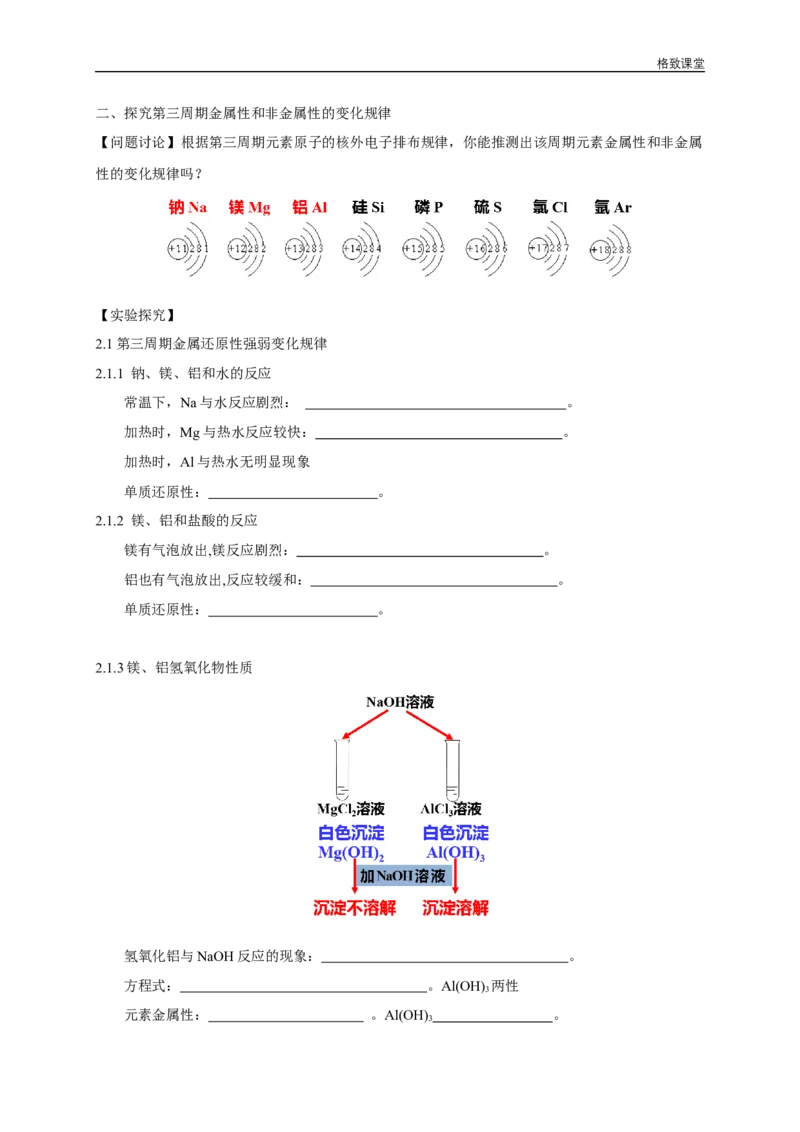
1.3、元素主要化合价的周期性变化
【思考与交流】
1、通过上面的讨论我们知道,随着原子序数的递增,元素原子的核外电子排布、原子半径和
化合价都呈现周期性的变化。那么,元素的金属性和非金属性是否也随着原子序数的递增而呈现周
期性变化呢?
2、同一周期的元素,原子结构有何异同?格致课堂
二、探究第三周期金属性和非金属性的变化规律
【问题讨论】根据第三周期元素原子的核外电子排布规律,你能推测出该周期元素金属性和非金属
性的变化规律吗?
【实验探究】
2.1第三周期金属还原性强弱变化规律
2.1.1 钠、镁、铝和水的反应
常温下,Na与水反应剧烈: 。
加热时,Mg与热水反应较快: 。
加热时,Al与热水无明显现象
单质还原性: 。
2.1.2 镁、铝和盐酸的反应
镁有气泡放出,镁反应剧烈: 。
铝也有气泡放出,反应较缓和: 。
单质还原性: 。
2.1.3镁、铝氢氧化物性质
氢氧化铝与NaOH反应的现象: 。
方程式: 。Al(OH) 两性
3
元素金属性: 。Al(OH) 。
3格致课堂
【总结】
第三周期金属还原性强弱变化规律
① 钠、镁、铝置换出水(或酸)中的氢时,由易到难的顺序为 ;
② 钠、镁、铝的最高价氧化物对应的水化物的碱性由强到弱的顺序为 ;
③ 钠、镁、铝的金属性由强到弱的顺序为 。
2.2 第三周期非金属单质氧化性强弱变化规律
【总结】第三周期非金属单质氧化性强弱变化规律
①硅、磷、硫、氯单质与氢气化合时条件由易到难的顺序为 ;
②硅、磷、硫、氯最高价氧化物对应水化物的酸性由强到弱的顺序为 ;
③硅、磷、硫、氯元素非金属性由强到弱的顺序为 。
【课堂练习】
1.已知下列原子的半径:
原子 N S O Si
半径r/10-10 m 0.75 1.02 0.74 1.17
根据以上数据,P原子的半径可能是( )
A.1.10×10-10 m B.0.80×10-10 m C.1.20×10-10 m D.0.70×10-10 m
2.下列各组元素性质或原子结构递变情况错误的是( )格致课堂
A. Li、Be、B原子最外层电子数依次增多
B. P、S、Cl元素最高正化合价依次升高
C. N、O、F原子半径依次增大
D. Na、K、Rb的电子层数依次增多
3.已知X、Y、Z是三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱的顺序是
HXO>HYO >HZO,则下列判断正确的是( )
4 2 4 3 4
A. 气态氢化物的稳定性:HX>HY>ZH
2 3
B. 非金属活泼性:Y<X<Z
C. 原子半径:X>Y>Z
D. 原子最外层电子数:XMg2+>Na+ C.Rb>K>Na D.P>S>O