文档内容
格致课堂
4.2.1 元素周期律(学案)
1、了解第三周期元素的递变规律
2、了解氢氧化铝的两性
3、了解元素周期律的成因
第三周期元素性质的递变规律
在元素周期表中同周期元素是指 ,金属
钠与水反应的现象是 ;方程式为 ;
元素周期律
一、元素性质的周期性变化规律:
【思考与交流】
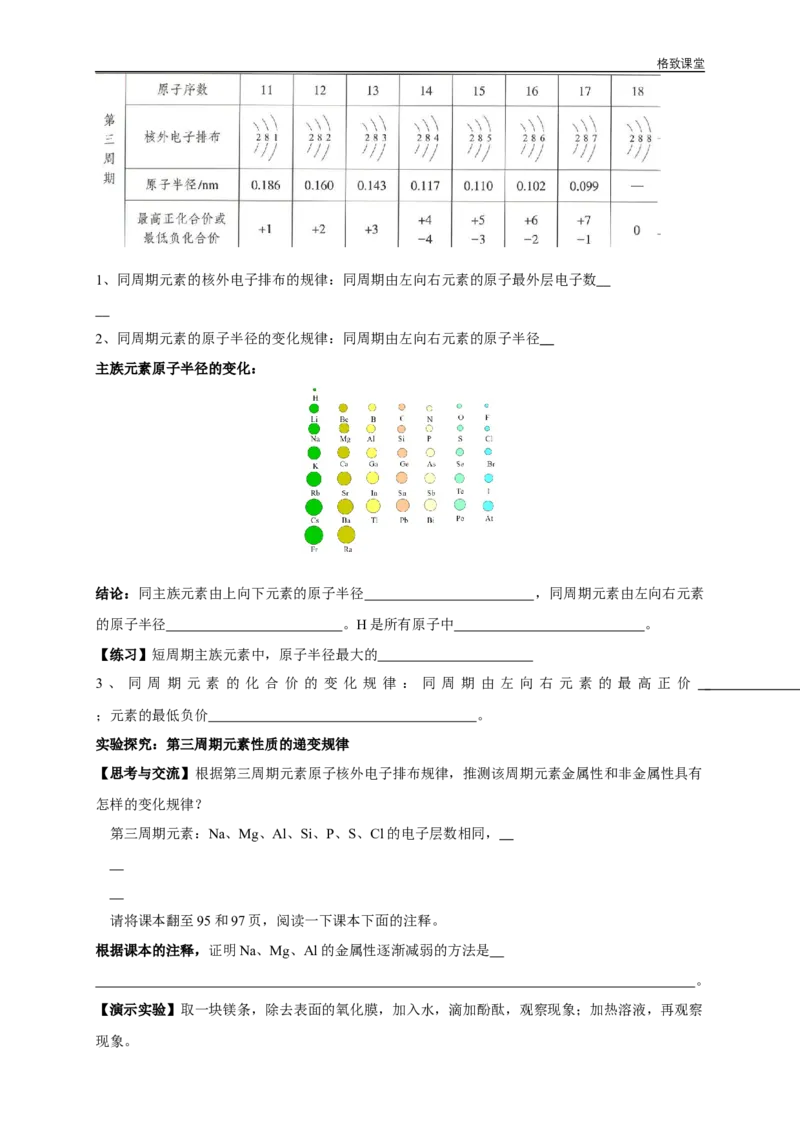
【思考与交流】观察下面表格中的数据,判断随着原子序数的递增,元素原子的核外电子排布、原
子半径和化合价的变化规律是什么?格致课堂
1、同周期元素的核外电子排布的规律:同周期由左向右元素的原子最外层电子数
2、同周期元素的原子半径的变化规律:同周期由左向右元素的原子半径
主族元素原子半径的变化:
结论:同主族元素由上向下元素的原子半径 ,同周期元素由左向右元素
的原子半径 。H是所有原子中 。
【练习】短周期主族元素中,原子半径最大的
3 、 同 周 期 元 素 的 化 合 价 的 变 化 规 律 : 同 周 期 由 左 向 右 元 素 的 最 高 正 价
;元素的最低负价 。
实验探究:第三周期元素性质的递变规律
【思考与交流】根据第三周期元素原子核外电子排布规律,推测该周期元素金属性和非金属性具有
怎样的变化规律?
第三周期元素:Na、Mg、Al、Si、P、S、Cl的电子层数相同,
请将课本翻至95和97页,阅读一下课本下面的注释。
根据课本的注释,证明Na、Mg、Al的金属性逐渐减弱的方法是
。
【演示实验】取一块镁条,除去表面的氧化膜,加入水,滴加酚酞,观察现象;加热溶液,再观察
现象。格致课堂
现象:
。
方程式为 。与金属钠相比较,该反应明显困难,说明
【演示实验】向氯化铝溶液中加入氨水,将生成的沉淀分装在两个试管中,分别加入盐酸和氢氧化
钠溶液,观察现象。
现象:向氯化铝溶液中加入氨水, 。反应方程式为: 。
向氢氧化铝沉淀中加入盐酸溶液, ,方程式为: ;
向氢氧化铝沉淀中加入氢氧化钠溶液, ,方
程式为: 。氢氧化铝与酸碱都反应
生成盐和水,所以氢氧化铝是典型的 。
【演示实验】将氯化铝溶液换成氯化镁溶液,重复上述实验。
现象:氯化镁溶液中加入氨水得到 ,该沉淀加盐酸 ,加氢
氧化钠溶液 。
【科学事实】钠、镁、铝是金属元素,都能形成氢氧化物,NaOH是 ,Mg(OH) 是
2
,而Al(OH) 是 ,说明钠镁铝的金属性 。
3
【练习】下列说法能证明钾元素比镁元素金属性强的是( )
A.金属钾与冷水剧烈反应,镁与冷水几乎没有现象。
B.KOH的碱性比Mg(OH) 强
2
C.金属钾与MgCl 的水溶液反应可置换出金属镁
2
D.在化学反应中,钾失去1个电子,镁失去2个电子
根据课本的注释,证明Si、P、S、Cl的非金属性逐渐增强的方法是
。
【科学事实】
硅、磷、硫、氯所对应的的最高价氧化物的水化物的酸性 ,所以硅、磷、
硫、氯的非金属性 。
【练习】下列说法能够证明氯元素的非金属性比硫元素强的是( )
A.氯气与氢气化合的条件比硫与氢气化合的条件更容易
B.HCl的酸性比HS强
2格致课堂
C.HCl的稳定性比HS强
2
D.HClO 的酸性比HSO 强
3 2 3
结论:在同一周期中,虽然各元素的原子核外电子层数相同,但由左向右,核电荷数依次
,原子半径 ,失电子能力 ,得电子能力
,因此金属性,非金属性 。元素的金属性和非金属随着原子序数的递增,
而呈现 。
元素周期律:元素的性质随着元素原子序数的递增而呈周期性的变化。
元素性质的周期性变化是 的必然结果。
1.要使AlCl 溶液中的Al3+完全转化成Al(OH) 沉淀,应选的最佳试剂是( )
3 3
A.NaOH溶液 B.稀盐酸
C.AgNO 溶液 D.氨水
3
2.下列离子方程式书写错误的是( )
A.铝粉投入到NaOH溶液中:2Al+2HO+2OH-===2AlO+H↑
2 2
B.Al(OH) 溶于NaOH溶液中:Al(OH) +OH-===AlO+2HO
3 3 2
C.Al(OH) 溶于盐酸溶液中:Al(OH) +3H+===Al3++3HO
3 3 2
D.Al O 粉末溶于NaOH溶液中:Al O+2OH-===2AlO+HO
2 3 2 3 2
3.元素的以下性质中,随着原子序数递增不呈周期性变化的是( )
A.相对原子质量 B.化合价
C.原子半径 D.元素的金属性和非金属性
4.下列关于11~17号元素性质的比较中,正确的是( )
①元素的最高正化合价依次升高 ②元素的非金属性逐渐增强 ③元素的金属性逐渐减弱
④元素的最高价氧化物的水化物的碱性逐渐减弱,酸性逐渐增强
A.只有①② B.只有③④ C.全都不正确 D.全都正确
5.已知下列元素的原子半径:
原子 N S Si
半径r/10-10 m 0.75 1.02 1.17
根据上表数据分析,磷原子的半径可能是( )
A.1.10×10-10 m B.0.70×10-10 m C.1.20×10-10 m D.0.80×10-10 m
6.碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,根据碱金属元素性质的递变规律
预测其性质,其中不正确的是( )
A.在碱金属元素中它具有最大的原子半径格致课堂
B.钫在空气中燃烧时,只生成化学式为Fr O的氧化物
2
C.它的氢氧化物化学式为FrOH,这是一种极强的碱
D.它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸
7.现有原子序数依次增大的A、B、C、D、E、F六种同周期元素。已知:A、C、F三种元素
原子的最外层共有11个电子,其最高价氧化物的水化物之间,两两皆能反应且均能生成盐和水;D
和E各有如下表所示的电子层结构。
元素 最外层电子数 次外层电子数
D x x+4
E x+1 x+4
按要求填空:
(1)写出各元素的元素符号:A________,B________,C________,D________,E________,
F________。
(2)D的氢化物的化学式为_______,E的氢化物的化学式为______,两者的稳定性:______>
________。
(3)F与C两元素的最高价氧化物的水化物反应的离子方程式为____________________________。
【知识点填空答案】逐渐增加(第一周期是 1→2,第二周期和第三周期都是 1→8);逐渐减小
(不包括稀有气体);逐渐增大;逐渐减小;半径最小的;Na;逐渐升高(+1→+7,O和F无最高
正价);由ⅣA族的-4价逐渐升高至ⅦA族的-1价;随着核电荷数的递增,原子半径逐渐减小,
导致失电子能力逐渐减弱,得电子能力逐渐增强,金属性减弱,非金属性增强;单质与水(或酸)
反应的难易;最高价氧化物的水化物——氢氧化物的碱性强弱;常温下镁与水的反应较缓慢,镁条
表面有一些红色;加热后反应剧烈,镁条表面有大量气泡,溶液变为红色;Mg + 2H O Mg(OH)
2 2
+ H ↑;钠的金属性强于镁;生成白色絮状沉淀;Al3+ + 3NH ·H O = Al(OH) ↓+ 3NH +;沉淀溶解;
2 3 2 3 4
Al(OH) + 3H+ = Al3+ + 3H O;沉淀溶解;Al(OH) + OH-= AlO -+ 2H O;两性氢氧化物;氢氧化镁
3 2 3 2 2
白色沉淀;溶解;不溶解;强碱;中强碱;两性氢氧化物;逐渐减弱;AB;单质与氢气反应生成
气态氢化物的难易;最高价氧化物的水化物的酸性强弱;气态氢化物的稳定性;依次增强;逐渐增
强;AC;递增;逐渐减小;逐渐减弱;逐渐增强;逐渐减弱;逐渐增强;周期性的变化;元素原
子的核外电子排布的周期性变化;
【检测反馈答案】1.D 2.A 3.A 4.D 5.A 6.B
7.(1)Na;Mg;Al;Si;P;Cl
(2)SiH;PH ;PH ;SiH
4 3 3 4
(3)Al(OH) +3H+===Al3++3HO
3 2格致课堂