文档内容
格致课堂
第四章 元素周期律
第 2 节 元素周期性表和元素周期律的应用(二课时)
1、知道 元素周期表的简单分区。
2、进一步认识元素周期表是元素周期律的具体表现形式。
3、学会运用元素周期表、元素周期律的有关知识,指导科学研究和工农业生产。
1、对元素周期表结构和规律的认知。
2、金属性和非金属性的判断和归纳。
3、对“位”“构”“性”的认识。
4、元素周期律在工农业和研究中的应用。
第三周期的元素周期性的变化。
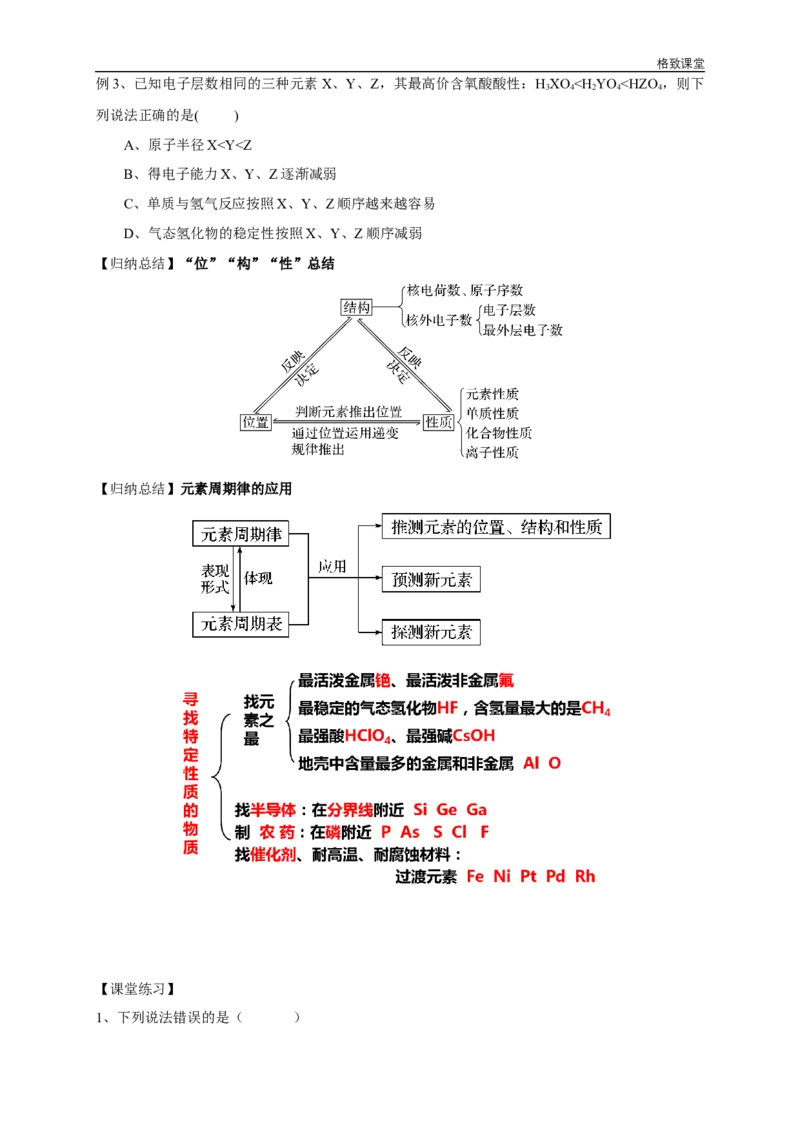
一、元素的金属性、非金属性与元素在周期表中位置的关系
认真观察下表,填空并画出金属与非金属的交界线,标出其附近的元素符号。
【总结】1、 。
2、 。
3、 。
二、金属性与非非金属性的比较总结格致课堂
1、金属性的比较
比较金属性的强弱,其实质是看元素原子 电子的难易程度,越易 电子,金属性越 。
(1)根据元素周期表判断
①同一周期,从左到右,随着原子序数的递增,元素的金属性逐渐 ;
②同一主族,从上到下,随着原子序数的递增,元素的金属性逐渐 。
(2)根据元素单质及其化合物的相关性质判断
①金属单质与水(或酸)反应越剧烈,元素的金属性 。如Zn与盐酸反应比Fe与盐酸反应更容
易,则金属性:Zn>Fe;
②最高价氧化物对应水化物的碱性越强,元素的金属性 。如碱性:NaOH>Mg(OH) ,则
2
金属性:Na>Mg;
③金属单质间的置换反应。如Zn+Cu2+=Zn2++Cu,则金属性:Zn>Cu;
④元素的原子对应阳离子的氧化性越强,则元素的金属性 。如氧化性:Mg2+>Na+,则
金属性:Mg<Na。
(3)根据金属活动性顺序判断
一般来说,排在前面的金属元素其金属性比排在后面的强。如Fe排在Cu的前面,则金属性:Fe>
Cu。
【注意】金属性强弱的比较,关键是比较原子失去电子的难易,而不是失去电子数的多少。如Na
失去一个电子,而Mg失去两个电子,但Na的金属性比Mg强。
2、非金属性的比较
比较元素非金属性的强弱,其实质是看元素原子 电子的难易程度,越易 电子,非金属性
越 。
(1)根据元素周期表判断
①同一周期,从左到右,随着原子序数的递增,元素的非金属性逐渐 ;
②同一主族,从上到下,随着原子序数的递增,元素的非金属性逐渐 。
(2)根据元素单质及其化合物的相关性质判断
①非金属单质越易跟H 化合,其非金属性 。如F 与H 在暗处即可反应,Br 与H 在加热条
2 2 2 2 2
件下才能反应,则非金属性:F>Br;
②气态氢化物越稳定,其非金属性 。如稳定性:HF>HCl,则非金属性:F>Cl;
③最高价氧化物对应水化物的酸性越强,其非金属性 。如酸性:HSO >HPO ,则非金属性:
2 4 3 4
S>P;
④非金属单质间的置换反应。如Cl2+2KI=2KCl+I,则非金属性:Cl>I;
2
⑤元素的原子对应阴离子的还原性越强,其非金属性就 。如还原性:S2->Cl-,则非金属格致课堂
性:Cl>S。
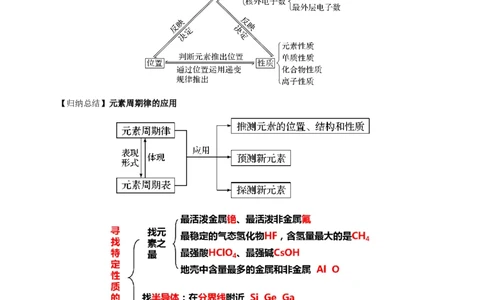
三、元素的化合价与元素在周期表中的位置关系
主族元素的最高正化合价等于原子所能 的最外层电子数(价电子),
而非金属的最低负化合价则等于使原子达到8电子稳定结构所需 的电子数。所以,非金属
元素的最高正化合价和它的最低负化合价的绝对值之和等于 。
(1)最高正化合价= 序数=原子 电子数(O、F除外)。
(2)最高正化合价+|最低负化合价|= 。
【归纳总结】元素金属性、非金属性递变与其在周期表中的位置关系
碱性最强的是 ,酸性最强的含氧酸是 。
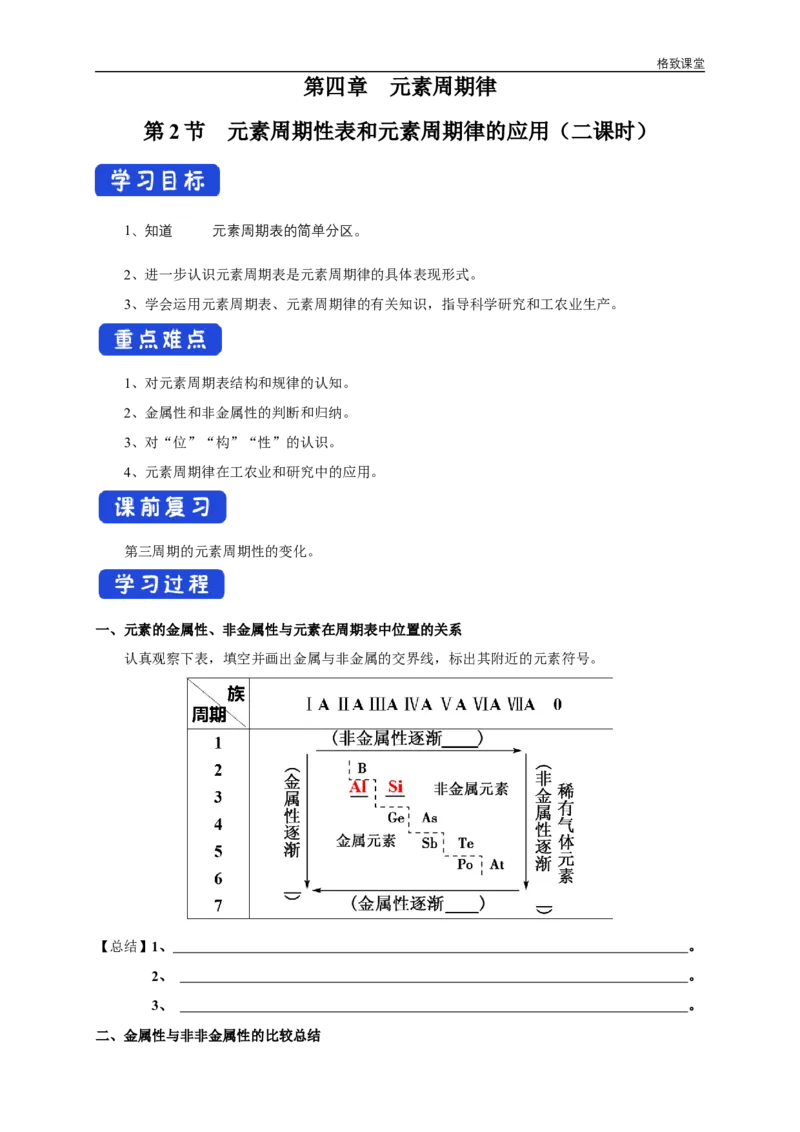
四、元素周期表和元素周期律的应用
(1)指导其他与化学相关的科学技术
①在周期表中__________________,可以找到半导体材料。
②在__________中寻找催化剂和耐高温、耐腐蚀的合金材料。
③寻找制取农药的元素 。
(2)元素周期表和元素周期律的理论应用
① 预测元素的性质
例1、镭是第7周期第ⅡA族元素,下列关于镭的性质的描述中不正确的是( )
A.镭比钙金属性更强 B.氢氧化物呈两性
C.在化合物中呈+2价 D.碳酸盐难溶于水
② 比较元素的性质
例2、下列说法正确的是( )
A. C、N、O、F原子半径依次增大
B. NH 、HO(g)、HF 稳定性依次增强
3 2
C. HClO比HSO 酸性强。
2 4
D.甲、乙两种非金属元素与金属钠反应时,甲得电子的数目多,所以甲活泼。格致课堂
例3、已知电子层数相同的三种元素X、Y、Z,其最高价含氧酸酸性:HXO