文档内容
第五章 化工生产中的重要非金属元素
第 2 节 氮及其化合物
第 2 课时 氨和铵盐
1、认识氨的物理性质,掌握并能熟练应用氨的化学性质。
2、理解喷泉实验的原理。
3、掌握铵盐的性质和铵根离子的检验。
4、掌握氨气的实验室制法,了解氨的工业制法及实验室中其他简易方法。
1、氨气和铵盐的化学性质,铵根离子的检验。
2、喷泉实验,实验室制备氨气。
氮气的性质和NOx之间的转化。
一、氨
1、物理性质
颜色状态 气味 密度 溶解性 特性
_____溶于水,1体积水能溶
_____气体 _______气味 _____空气 易液化
解____体积的氨气
【思考】氨作为制冷剂,是利用了它的什么性质? 试分析它有什么缺点?
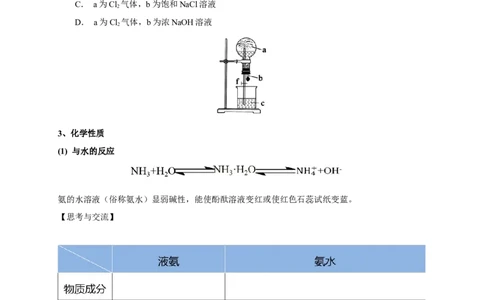
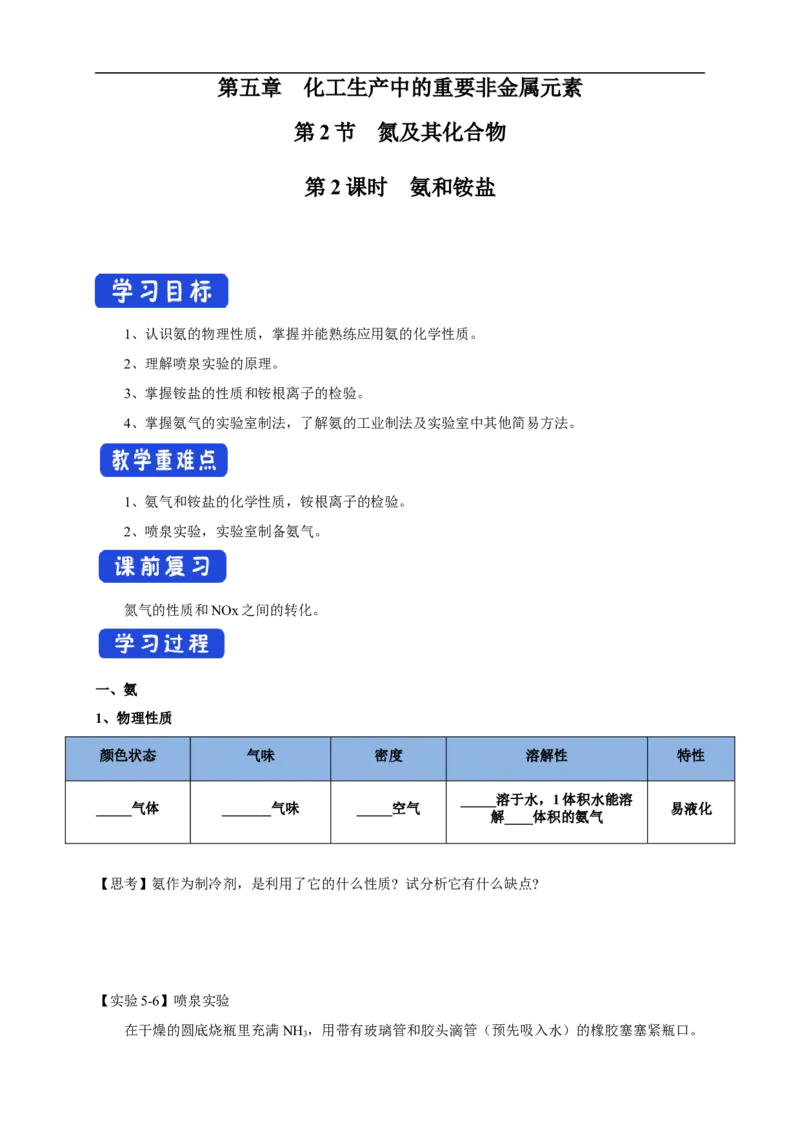
【实验5-6】喷泉实验
在干燥的圆底烧瓶里充满NH ,用带有玻璃管和胶头滴管(预先吸入水)的橡胶塞塞紧瓶口。
3倒置烧瓶,使玻璃管插入盛有水的烧杯中(预先在水里滴入少量酚酞溶液)。打开弹簧夹,挤压胶
头滴管,使水进入烧瓶。观察并描述现象,分析出现这些现象的可能原因。
现象:
结论:
方程式:
【思考与交流】
(1)根据以上实验,探究形成喷泉的原因是什么?
(2)某同学做该实验时,打开止水夹后将胶头滴管内的水挤入烧瓶内,可并未产生喷泉,试分析实验
失败可能的原因是什么?
(3)若将NH 换为NO ,能否形成喷泉?若能形成,则实验后液体能否充满烧瓶?
3 2
【总结】喷泉实验的原理及应用
(1) 喷泉形成原理
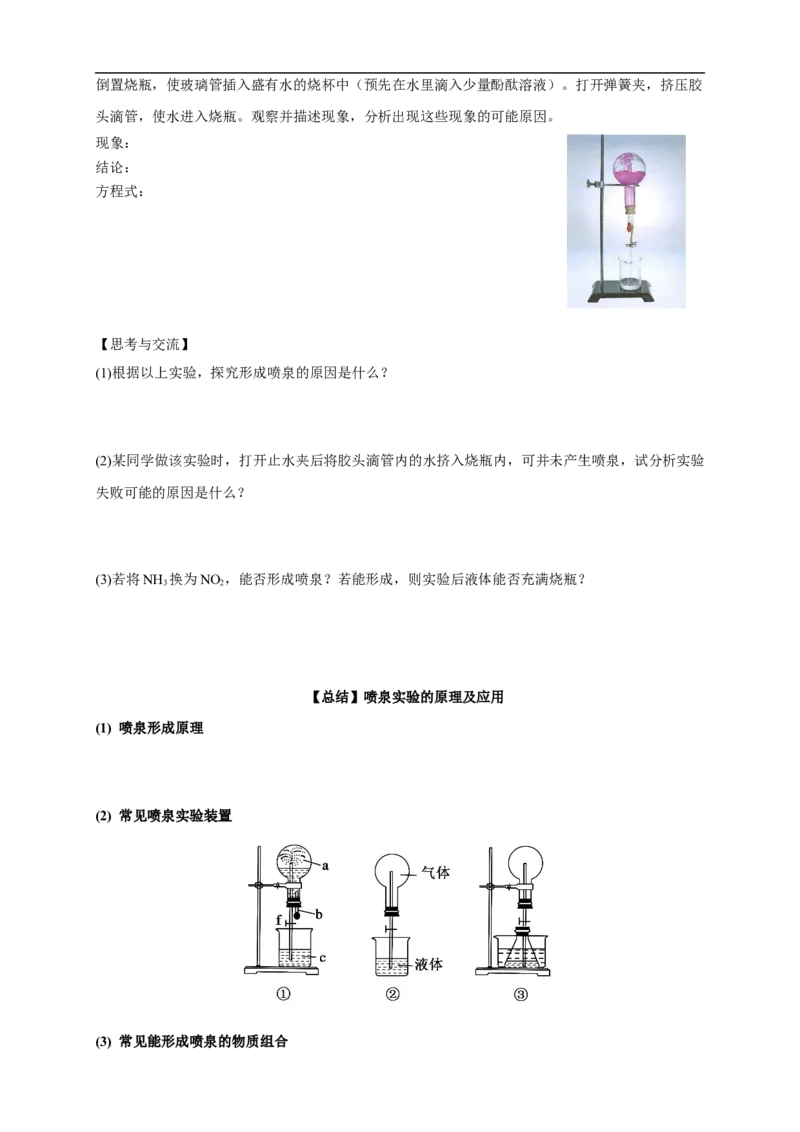
(2) 常见喷泉实验装置
(3) 常见能形成喷泉的物质组合【课堂练习】
例1. 如图所示:烧瓶中充满干燥气体a,将胶头滴管中的液体b挤入烧瓶内,轻轻震荡烧瓶,
然后打开弹簧夹,烧杯中的液体呈喷泉状喷出,则a、b不可能是( )
A. a为HCl气体,b为HO
2
B. a为CO 气体,b为浓NaOH溶液
2
C. a为Cl 气体,b为饱和NaCl溶液
2
D. a为Cl 气体,b为浓NaOH溶液
2
3、化学性质
(1) 与水的反应
氨的水溶液(俗称氨水)显弱碱性,能使酚酞溶液变红或使红色石蕊试纸变蓝。
【思考与交流】
(2) 与酸的反应原理:
现象:
原因:
【思考与交流】
a 浓氨水遇浓硫酸、浓硝酸也会产生白烟吗?
b 氨与其他酸的反应:
(3) 氨的还原性
氨的催化氧化: 。氨的催化氧化是工业_______的基础。
与氯气的反应: 。
【思考与交流】工业制硝酸原理
【总结】
(1)氨水的性质
(2) 氨气的性质
【课堂练习】例2、 下列反应中说明氨气具有还原性和碱性的是( )
A. 2NH +3CuO === 3Cu+N+3HO
3 2 2
B. 8NH +3Cl === 6NH Cl+N
3 2 4 2
C.4NH +5O ===4NO+6HO
3 2 2
D.NH +HCl === NH Cl
3 4
二、铵盐
1. 物理性质 。
2. 化学性质
(1) 受热易分解
【实验5-7】
向盛有少量NH Cl溶液、NH NO 溶液和(NH )SO 溶液的三支试管中分别加入NaOH溶液并加
4 4 3 4 2 4
热(注意通风),用镊子夹住一片湿润的红色石蕊试纸放在试管口。观察现象,分析现象产生的原
因,写出反应的离子方程式。
(2)与碱反应
在实验室中,常利用铵盐与强碱反应产生氨这一性质来检验铵根离子的存在和制取氨。
【小结】铵盐的检验方法
(1) 。
(2) 。
【思考与讨论】
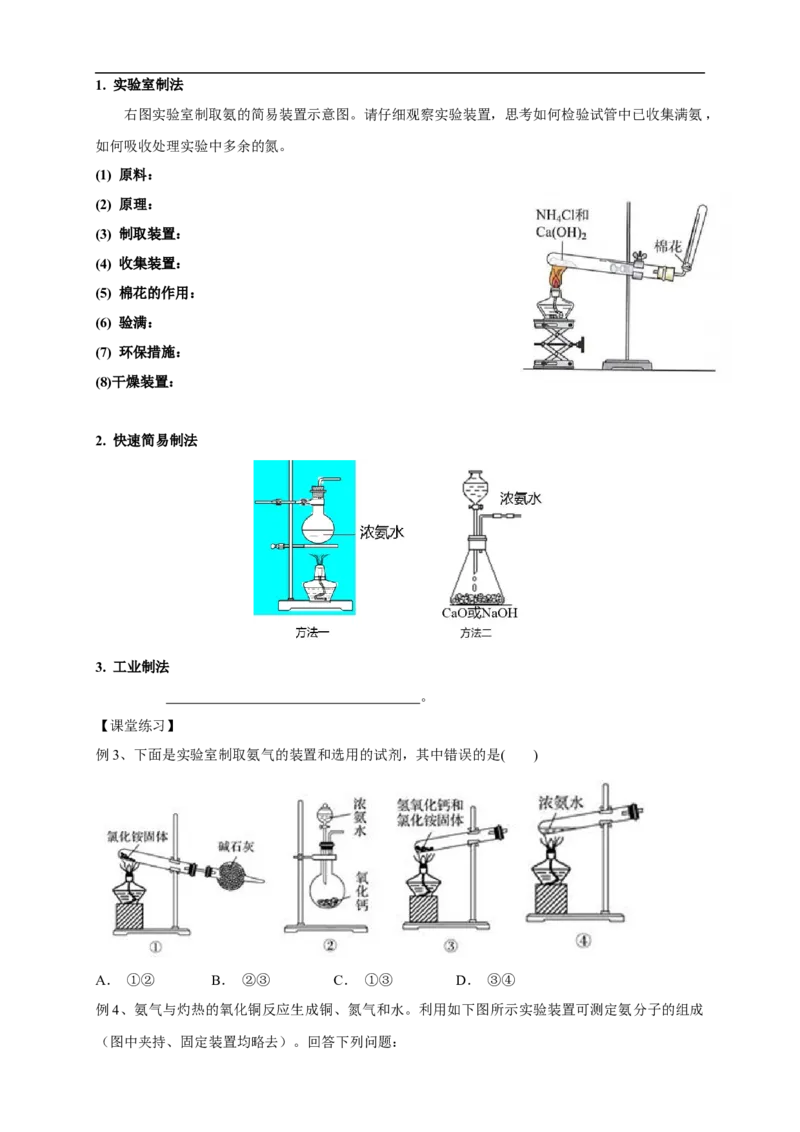
三、氨气的制法1. 实验室制法
右图实验室制取氨的简易装置示意图。请仔细观察实验装置,思考如何检验试管中已收集满氨,
如何吸收处理实验中多余的氮。
(1) 原料:
(2) 原理:
(3) 制取装置:
(4) 收集装置:
(5) 棉花的作用:
(6) 验满:
(7) 环保措施:
(8)干燥装置:
2. 快速简易制法
3. 工业制法
。
【课堂练习】
例3、下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
A. ①② B. ②③ C. ①③ D. ③④
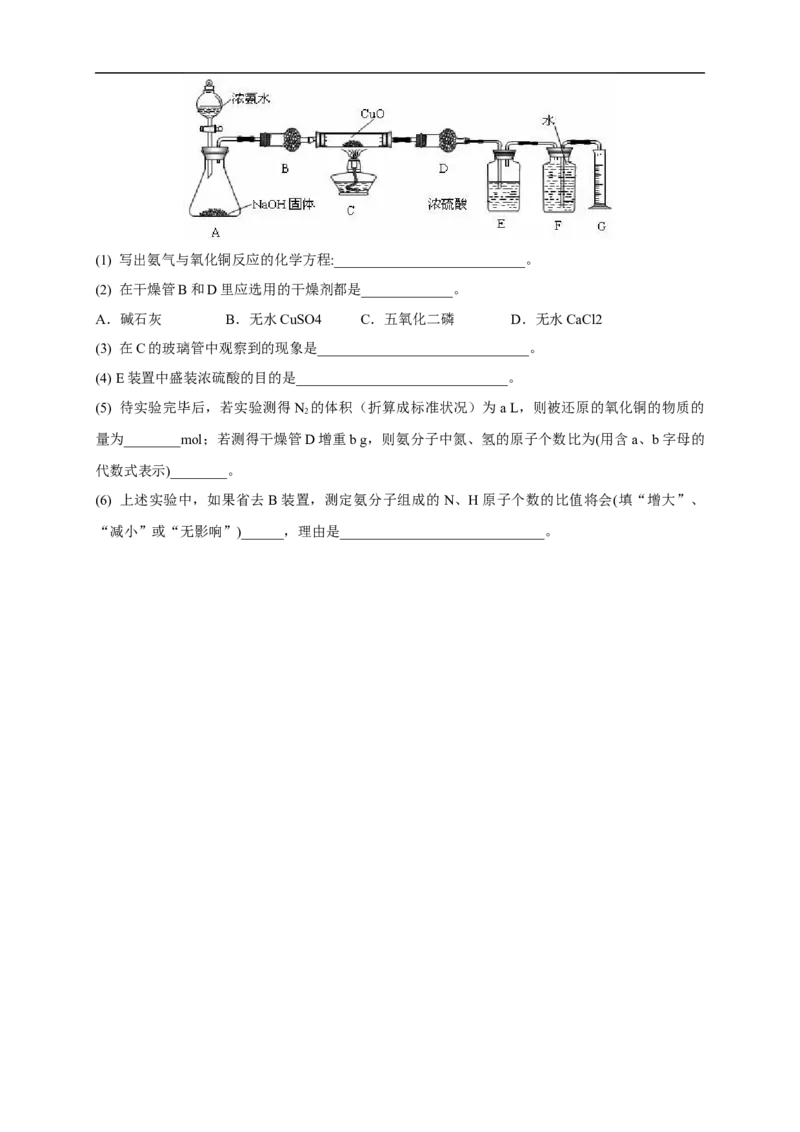
例4、氨气与灼热的氧化铜反应生成铜、氮气和水。利用如下图所示实验装置可测定氨分子的组成
(图中夹持、固定装置均略去)。回答下列问题:(1) 写出氨气与氧化铜反应的化学方程:___________________________。
(2) 在干燥管B和D里应选用的干燥剂都是_____________。
A.碱石灰 B.无水CuSO4 C.五氧化二磷 D.无水CaCl2
(3) 在C的玻璃管中观察到的现象是______________________________。
(4) E装置中盛装浓硫酸的目的是______________________________。
(5) 待实验完毕后,若实验测得N 的体积(折算成标准状况)为a L,则被还原的氧化铜的物质的
2
量为________mol;若测得干燥管D增重b g,则氨分子中氮、氢的原子个数比为(用含a、b字母的
代数式表示)________。
(6) 上述实验中,如果省去B装置,测定氨分子组成的N、H原子个数的比值将会(填“增大”、
“减小”或“无影响”)______,理由是_____________________________。