文档内容
第五章 化工生产中的重要非金属元素
第 2 节 氮及其化合物
第 2 课时 氨和铵盐
本节是人教版第五章第二节氮及其化合物的内容。本节内容主要包括:氮及氮的固定、一氧化
氮和二氧化氮、氨和铵盐、硝酸、酸雨及其防治。教材首先根据氮的原子结构知识,应用前一节掌
握的研究非金属单质性质的基本思路预测氮的化学性质,渗透条件对化学反应的影响,引出氮的固
定对人类生存的重要意义。之后,根据物质类别研究氮的化合物,包括一氧化氮、二氧化氮、硝酸、
氨和铵盐的化学性质。以工业合成氨、工业制硝酸的生产原理为载体,应用氧化还原反应原理,设
计含氮化合物的转化,使学生认识到从一种原料转化成多种产品,路径之一是通过氧化还原反应改
变主要元素的化合价,提升“变化观念”等学科核心素养。教材设置铵根离子的检验、实验室制取
氨的实验活动,让学生根据氨、铵根离子的性质和反应,选择合适的试剂,设计检验或者制取物质
的方案,提升其科学探究的能力。最后,教材编入“酸雨及其防治”内容以及“测定雨水的 pH”的
研究与实践活动,综合运用硫和氮及其化合物的相关知识,寻求证据参与社会性议题的讨论,分析
硫酸工业、合成氨工业对社会发展的价值和对环境的影响,有意识地渗透资源合理利用和环境保护
的意识。
《普通高中化学课程标准(2017版)》对本节的要求:结合真实情境中的应用实例或通过实验探
究,了解氮及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。结合
实例认识金属、非金属及其化合物的多样性,了解通过化学反应可以探索物质性质、实现物质转化,
认识物质及其转化在自然资源综合利用和环境保护中的重要价值。其情景素材建议为:“雷雨发庄
稼”;氮的循环与氮的固定;工业合成氨、工业制硫酸(或硝酸);氮肥的生产与合理使用;氯气、
氨气等泄漏的处理;酸雨的成因与防治;汽车尾气的处理。因此内容安排三个课时:第一课时为氮
气与氮的固定,一氧化氮和二氧化氮,第二课时为氨和铵盐,第硝酸和酸雨及防治。本节为第二课
时的内容:氨和铵盐。
【学习目标】
1、认识氨的物理性质,掌握并能熟练应用氨的化学性质。
2、理解喷泉实验的原理。3、掌握铵盐的性质和铵根离子的检验。
4、掌握氨气的实验室制法,了解氨的工业制法及实验室中其他简易方法。
【核心素养】
1、通过学习氨的知识培养学生论据推理与模型认知的化学核心素养。
2、通过对喷泉实验原理、实验室制备氨气的探讨培养学生科学探究与实验创新的化学核心素养,
理解氨的喷泉实验原理,体会性质决定用途的核心观念。
1、氨气和铵盐的化学性质,铵根离子的检验。
2、喷泉实验,实验室制备氨气。
多媒体、氨气、硝酸铵、硫酸铵、碳酸铵、氯化铵、NaOH、试管、圆底烧瓶等
【阅读理解】阅读教材p13的内容,完成表格,总结氨气的物理性质。
【讲解】
一、氨
1、物理性质
颜色状态 气味 密度 溶解性 特性
_____溶于水,1体积水能溶
_____气体 _______气味 _____空气 易液化
解____体积的氨气
【思考交流】
制冷剂为液态,在一定的温度下又可以变为气态,即能够在制冷系统的蒸发器内蒸发并从被冷
却物体中吸取热量而汽化,然后在冷凝器内将热量传递给周围介质(水或空气)而变为液体的媒介物。
制冷剂的种类很多,空调常用的制冷剂有氨、氟利昂等。氨是目前使用最为广泛的一种中压中温制
冷剂。
【思考】氨作为制冷剂,是利用了它的什么性质? 试分析它有什么缺点?
氨气易液化变为液体,且液氨变为气体时会吸收大量的热。缺点是有刺激性气味、有毒、可以
燃烧和爆炸。
【实验探究】
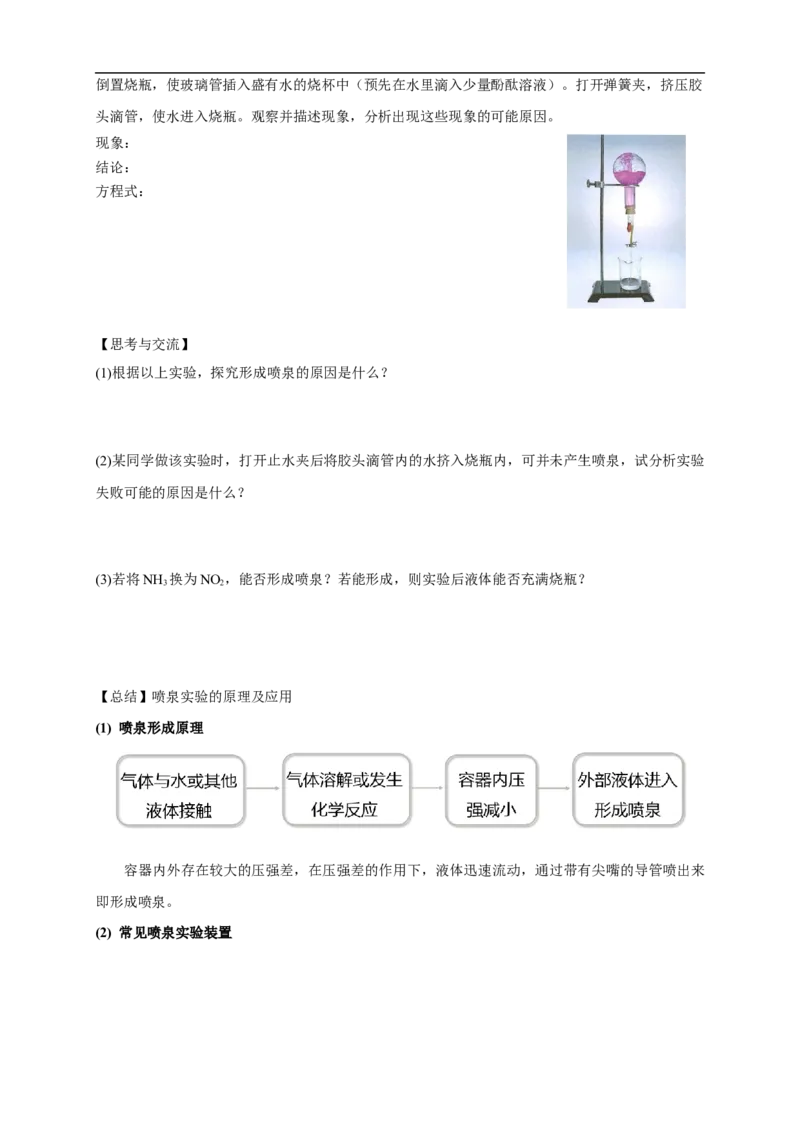
【实验5-6】喷泉实验
在干燥的圆底烧瓶里充满NH ,用带有玻璃管和胶头滴管(预先吸入水)的橡胶塞塞紧瓶口。
3倒置烧瓶,使玻璃管插入盛有水的烧杯中(预先在水里滴入少量酚酞溶液)。打开弹簧夹,挤压胶
头滴管,使水进入烧瓶。观察并描述现象,分析出现这些现象的可能原因。
现象:
结论:
方程式:
【思考与交流】
(1)根据以上实验,探究形成喷泉的原因是什么?
(2)某同学做该实验时,打开止水夹后将胶头滴管内的水挤入烧瓶内,可并未产生喷泉,试分析实验
失败可能的原因是什么?
(3)若将NH 换为NO ,能否形成喷泉?若能形成,则实验后液体能否充满烧瓶?
3 2
【总结】喷泉实验的原理及应用
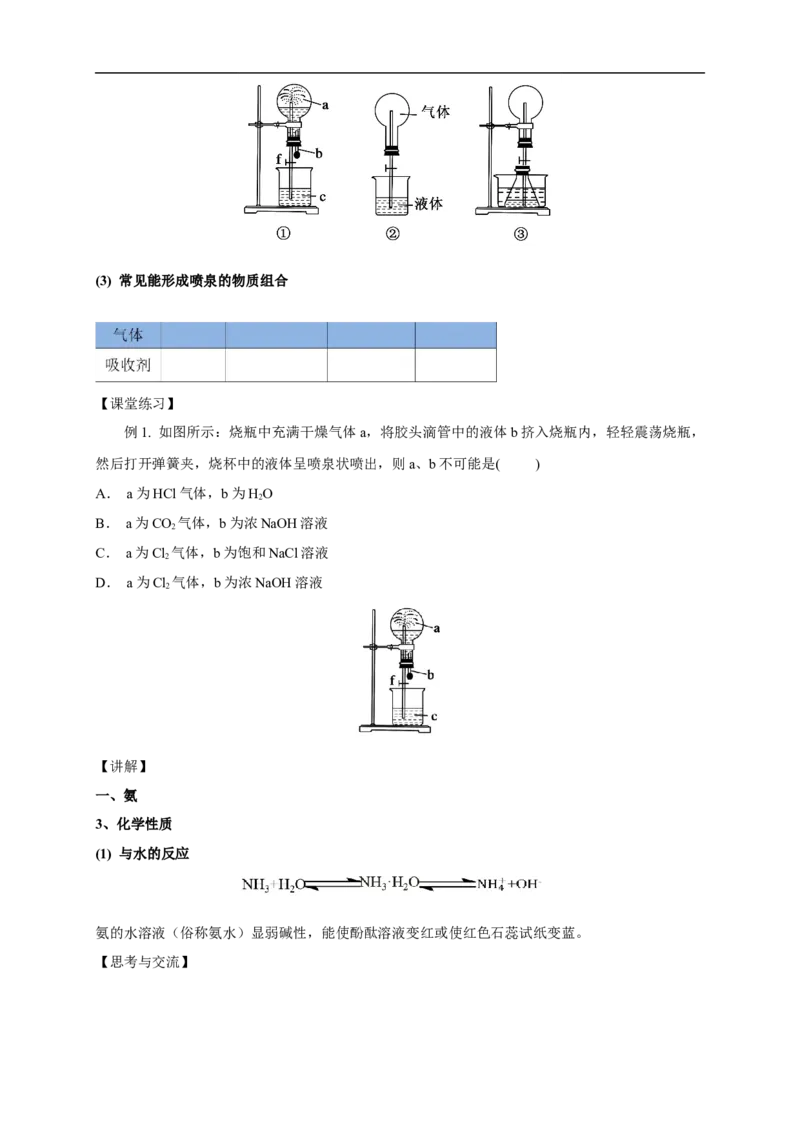
(1) 喷泉形成原理
容器内外存在较大的压强差,在压强差的作用下,液体迅速流动,通过带有尖嘴的导管喷出来
即形成喷泉。
(2) 常见喷泉实验装置(3) 常见能形成喷泉的物质组合
【课堂练习】
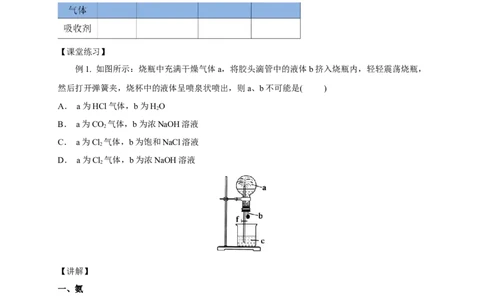
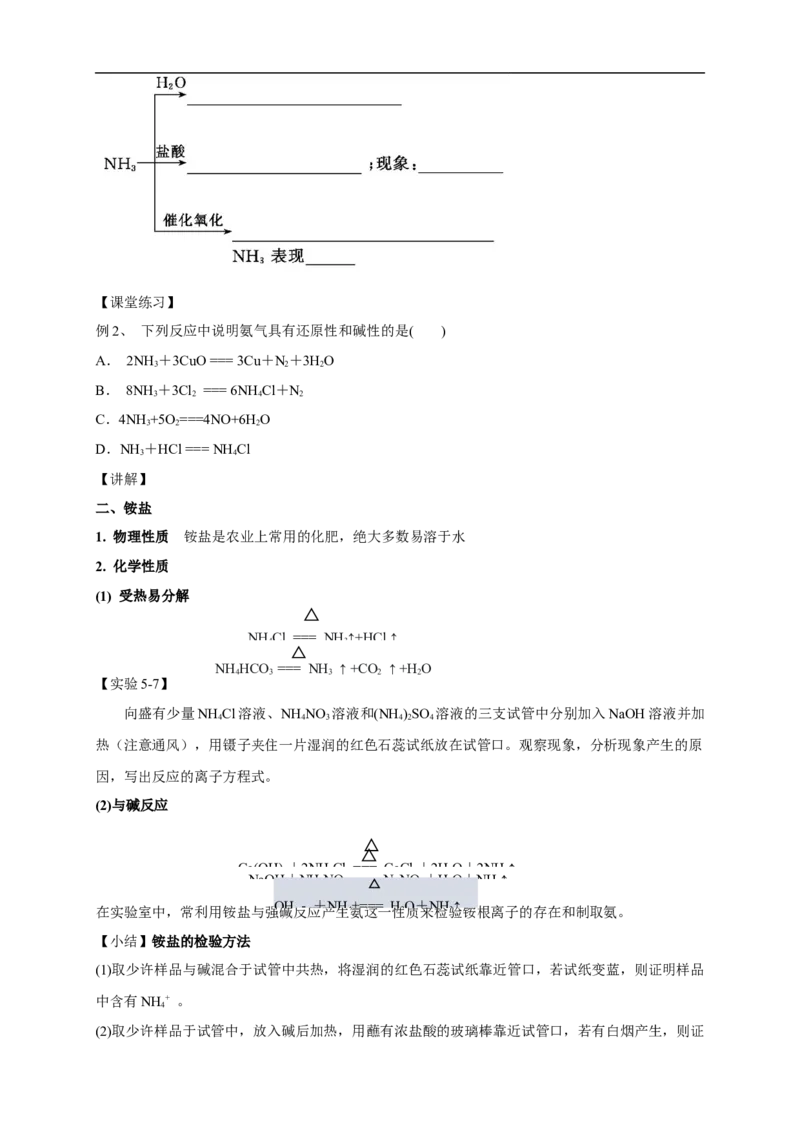
例1. 如图所示:烧瓶中充满干燥气体a,将胶头滴管中的液体b挤入烧瓶内,轻轻震荡烧瓶,
然后打开弹簧夹,烧杯中的液体呈喷泉状喷出,则a、b不可能是( )
A. a为HCl气体,b为HO
2
B. a为CO 气体,b为浓NaOH溶液
2
C. a为Cl 气体,b为饱和NaCl溶液
2
D. a为Cl 气体,b为浓NaOH溶液
2
【讲解】
一、氨
3、化学性质
(1) 与水的反应
氨的水溶液(俗称氨水)显弱碱性,能使酚酞溶液变红或使红色石蕊试纸变蓝。
【思考与交流】(2) 与酸的反应
原理:
现象:
原因:
【思考与交流】
a 浓氨水遇浓硫酸、浓硝酸也会产生白烟吗?
b 氨与其他酸的反应:
(3) 氨的还原性
氨的催化氧化: 。氨的催化氧化是工业_______的基础。
与氯气的反应: 。
【思考与交流】工业制硝酸原理
【总结】
(1)氨水的性质
(2) 氨气的性质【课堂练习】
例2、 下列反应中说明氨气具有还原性和碱性的是( )
A. 2NH +3CuO === 3Cu+N+3HO
3 2 2
B. 8NH +3Cl === 6NH Cl+N
3 2 4 2
C.4NH +5O ===4NO+6HO
3 2 2
D.NH +HCl === NH Cl
3 4
【讲解】
二、铵盐
1. 物理性质 铵盐是农业上常用的化肥,绝大多数易溶于水
2. 化学性质
(1) 受热易分解
NH Cl === NH ↑+HCl ↑
4 3
NH HCO === NH ↑ +CO ↑ +H O
4 3 3 2 2
【实验5-7】
向盛有少量NH Cl溶液、NH NO 溶液和(NH )SO 溶液的三支试管中分别加入NaOH溶液并加
4 4 3 4 2 4
热(注意通风),用镊子夹住一片湿润的红色石蕊试纸放在试管口。观察现象,分析现象产生的原
因,写出反应的离子方程式。
(2)与碱反应
Ca(OH) +2NH Cl === CaCl +2HO+2NH ↑
2 4 2 2 3
NaOH+NH NO === NaNO +HO+NH ↑
4 3 3 2 3
OH - +NH +=== HO+NH ↑
在实验室中,常利用铵盐与强碱反应产生4氨这一性2质来检验3 铵根离子的存在和制取氨。
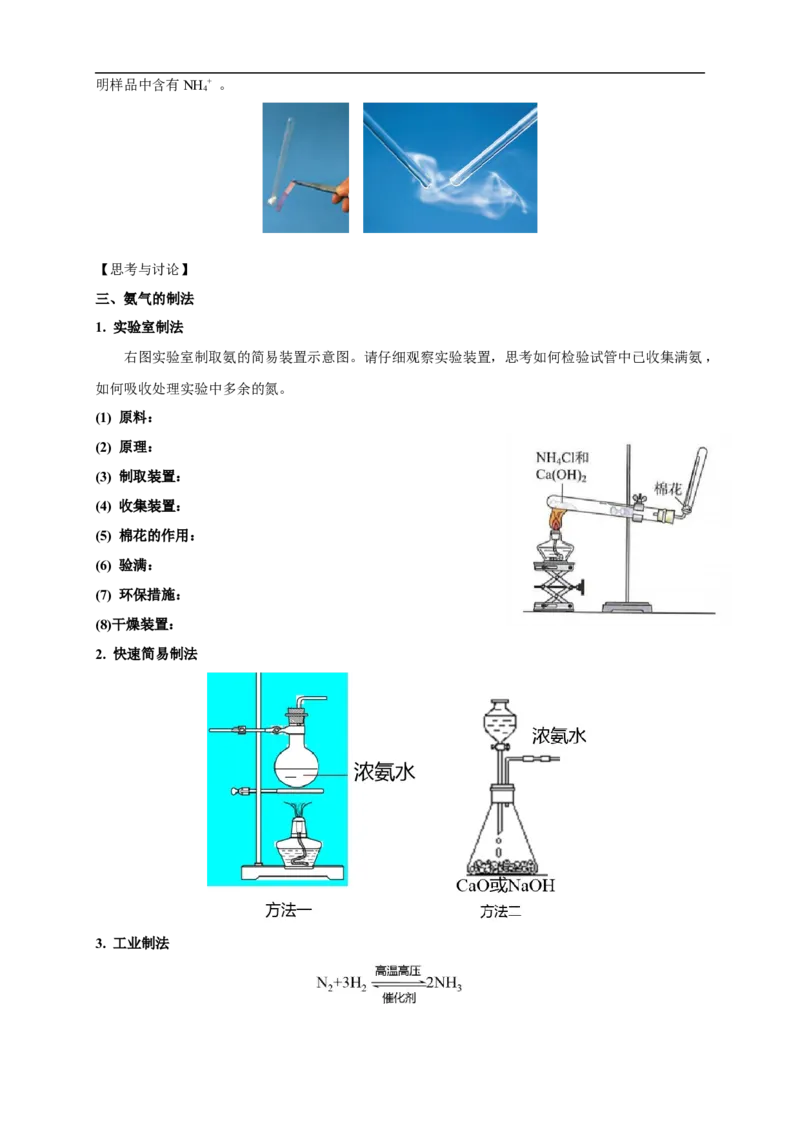
【小结】铵盐的检验方法
(1)取少许样品与碱混合于试管中共热,将湿润的红色石蕊试纸靠近管口,若试纸变蓝,则证明样品
中含有NH + 。
4
(2)取少许样品于试管中,放入碱后加热,用蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,则证明样品中含有NH + 。
4
【思考与讨论】
三、氨气的制法
1. 实验室制法
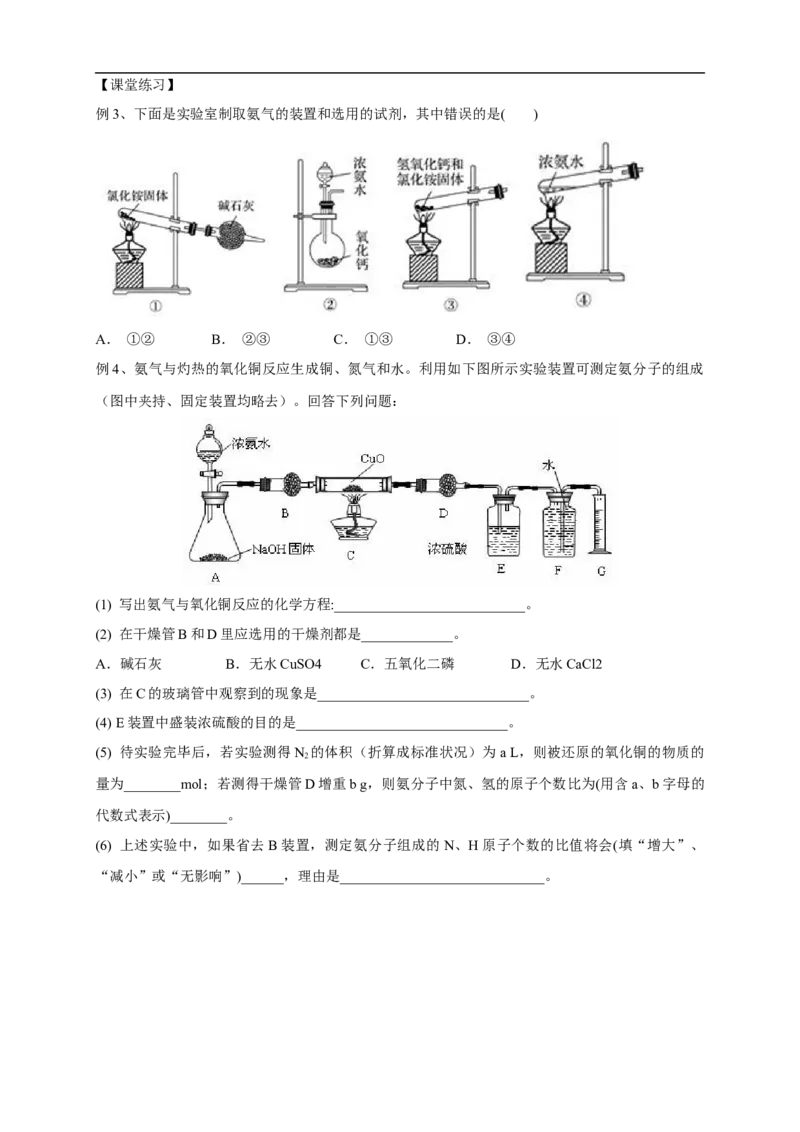
右图实验室制取氨的简易装置示意图。请仔细观察实验装置,思考如何检验试管中已收集满氨,
如何吸收处理实验中多余的氮。
(1) 原料:
(2) 原理:
(3) 制取装置:
(4) 收集装置:
(5) 棉花的作用:
(6) 验满:
(7) 环保措施:
(8)干燥装置:
2. 快速简易制法
3. 工业制法【课堂练习】
例3、下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
A. ①② B. ②③ C. ①③ D. ③④
例4、氨气与灼热的氧化铜反应生成铜、氮气和水。利用如下图所示实验装置可测定氨分子的组成
(图中夹持、固定装置均略去)。回答下列问题:
(1) 写出氨气与氧化铜反应的化学方程:___________________________。
(2) 在干燥管B和D里应选用的干燥剂都是_____________。
A.碱石灰 B.无水CuSO4 C.五氧化二磷 D.无水CaCl2
(3) 在C的玻璃管中观察到的现象是______________________________。
(4) E装置中盛装浓硫酸的目的是______________________________。
(5) 待实验完毕后,若实验测得N 的体积(折算成标准状况)为a L,则被还原的氧化铜的物质的
2
量为________mol;若测得干燥管D增重b g,则氨分子中氮、氢的原子个数比为(用含a、b字母的
代数式表示)________。
(6) 上述实验中,如果省去B装置,测定氨分子组成的N、H原子个数的比值将会(填“增大”、
“减小”或“无影响”)______,理由是_____________________________。