文档内容
第五章 化工生产中的重要非金属元素
第 1 节 硫及其化合物
第 2 课时 硫酸
1、了解浓硫酸的三大特性。
2、能运用氧化还原反应知识理解浓硫酸的氧化性。
3、认识硫酸在相关反应中体现的性质。
1、浓硫酸的三大特性(强氧化性、吸水性、脱水性)。
2、浓硫酸与金属单质、非金属单质、还原性物质的氧化还原理论的分析。
二氧化硫的性质(漂白性、氧化性、还原性、酸性氧化物的通行)。
一、硫酸的用途与工业制备
(1) 用途:
① 重要的化工原料,可用于制___________、炸药、染料、盐类等。
② 用于精炼石油、金属加工前的酸洗及制取各种挥发性酸、作干燥剂等。
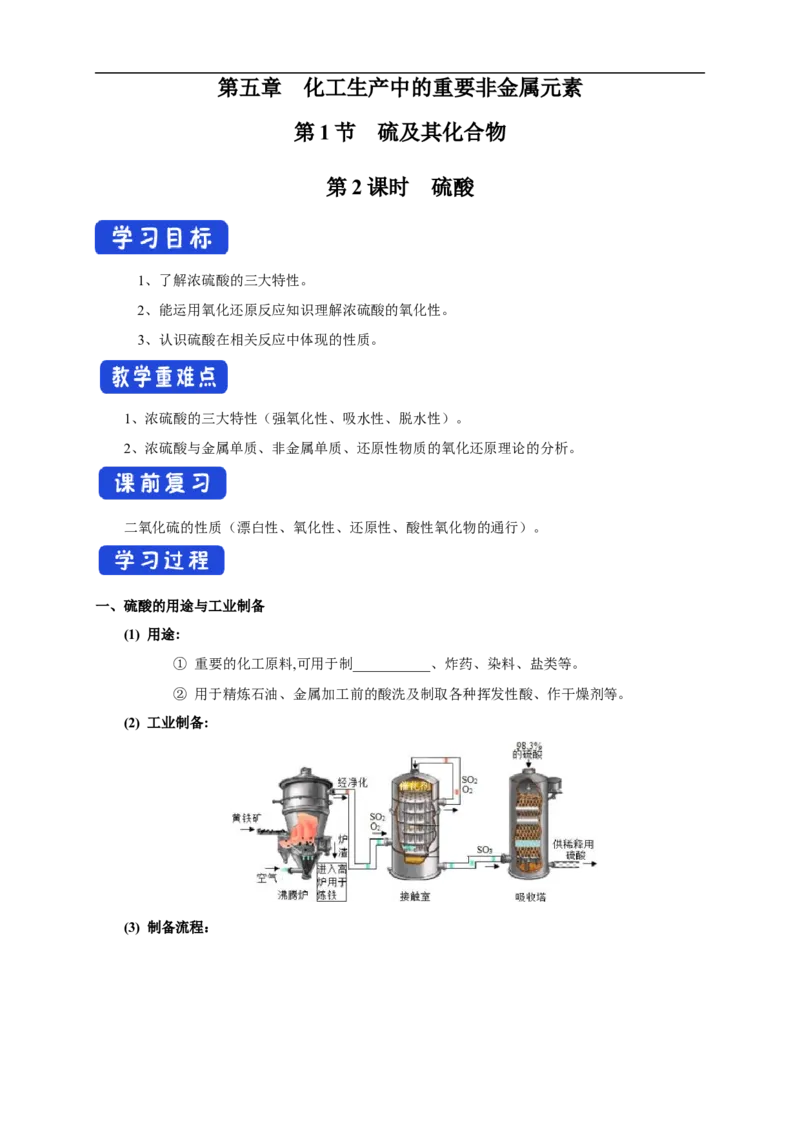
(2) 工业制备:
(3) 制备流程:【课堂练习】1、写出下列流程的化学方程式。
① 制备_________________________________或S+O2= SO ;
2
② 制备SO :___________________________;
3
③ 吸收SO :___________________________。
3
二、硫酸的化学性质
(1) 酸的通性
电离方程式 。
【课堂练习】2、写出下列流程的离子方程式。
(1) 稀硫酸与活泼金属反应,如Zn:______________________。
(2) 稀硫酸与金属氧化物反应,如CuO:______________________。
(3) 稀硫酸与碱反应,如NaOH: ____________________________。
(4) 稀硫酸与部分盐反应,如NaCO: _______________________。
2 3
(2) 浓硫酸的特性——吸水性与脱水性
【实验探究】“黑面包”实验
(1) 吸水性:浓硫酸能吸收存在于周围环境中的水分,常用做
(2) 脱水性:浓硫酸能将有机物中的 元素按水的组成比脱去【思考讨论】1、吸水性与脱水性的区别
吸水性 脱水性
浓硫酸能够吸收______________________ 浓硫酸能把有机物中
及固体 ________________________脱
原理
中的结晶水 去,剩余黑色的炭
区别
应用
2、浓硫酸能使蓝色胆矾变为白色,该过程体现了浓硫酸的脱水性还是吸水性?
【实验探究】
(3) 浓硫酸的特性——强氧化性
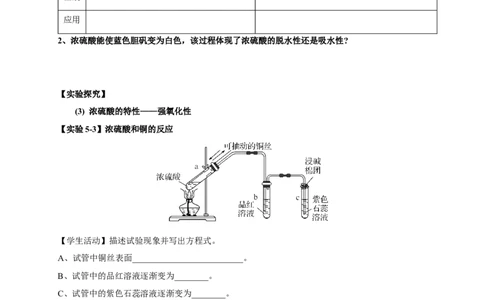
【实验5-3】浓硫酸和铜的反应
【学生活动】描述试验现象并写出方程式。
A、试管中铜丝表面__________________________。
B、试管中的品红溶液逐渐变为________。
C、试管中的紫色石蕊溶液逐渐变为________。
D、将a试管里的溶液慢慢倒入水中,溶液变为_____。
【思考交流】
(1) 该方程式中,谁是氧化剂,谁是还原剂?
(2) 浓硫酸在这个反应中体现了什么性质?(3) 实验室用金属和酸反应制取氢气时,往往用稀硫酸、而不用浓硫酸,这是为什么?
【思考交流】浓硫酸能和金属反应,为什么可用铝罐车和铁罐车来运输浓硫酸?
3. 浓硫酸的特性
(3) 强氧化性
① 与金属的反应
② 与 非金属反应:
③ 与具有还原性的化合物反应,如 等
【学生总结】浓硫酸特性——强氧化性
【课堂练习】1.浓硫酸具有A.强酸性,B.强氧化性,C.高沸点、难挥发性,D.脱水性,E.吸水性等性质。以下过
程主要表现了浓硫酸的哪些性质?请将答案的字母分别填入括号中。
(1)用NaCl固体和浓硫酸在加热条件下制氯化氢气体( )
(2)用磷矿物[主要成分是Ca (PO )]和硫酸反应制磷酸( )
3 4 2
(3)浓硫酸干燥H、O、Cl、HCl和SO 等气体( )
2 2 2 2
(4)常温下可以用铁或铝的容器贮存浓硫酸( )
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末( )
(6)不能用浓硫酸干燥HBr、HI和HS等气体( )
2
(7)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑( )
2.实验证明铜在低温下不能和氧气发生反应,也不能和稀硫酸共热发生反应,但工业上却是将废铜
屑倒入热的稀硫酸中并不断地通入空气来制取硫酸铜溶液的。铜屑在此状态下发生的一系列化学反
应的方程式为____________________________________________。
利用铜和浓硫酸在加热条件下也能制备硫酸铜溶液,其化学方程式为________________。
以上两种方法哪种好?________,原因是________________________________________。