文档内容
第五章 化工生产中的重要非金属元素
第 1 节 硫及其化合物
第 2 课时 硫酸
本节是人教版第五章第一节硫及其化合物的内容。本节内容主要包括:硫、二氧化硫和硫酸的
性质,硫酸根离子的检验,不同价态含硫物质的转化。教材首先根据硫在元素周期表中的位置,利
用原子结构和元素周期律的相关知识,从化学变化的视角考虑硫单质能否与金属单质、非金属单质、
化合物等发生反应,使学生掌握研究非金属单质性质的基本思路;之后,根据物质类别研究硫的化
合物(包括二氧化硫、硫酸)的化学性质。教材以工业制硫酸的生产原理为载体,从氧化还原的角
度来综合认识含硫化合物的氧化性和还原性,并结合浓硫酸与铜反应的实验,基于证据探究浓硫酸
的氧化性。接下来,设计“硫酸根离子的检验”实验,对构成物质的离子进行检验,提升学生“宏
观辨识与微观探析”的学科核心素养。最后,设置“不同价态含硫物质的转化”探究活动,要求学
生从物质类别和元素价态变化的角度,应用氧化还原反应原理设计实验方案,选择适当的实验试剂,
探究不同价态含硫物质的转化,提升学生“变化观念”等学科核心素养。
《普通高中化学课程标准(2017版)》对本节的要求:结合真实情境中的应用实例或通过实验探
究,了解硫及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。其情
景素材建议为:火山喷发中含硫物质的转化;“雷雨发庄稼”;工业制硫酸;食品中适量添加二氧
化硫的作用(去色、杀菌、抗氧化);酸雨的成因与防治。实验及探究活动:浓、稀硝酸的性质;
二氧化硫的性质;浓硫酸的性质;溶液中SO 2-等离子的检验。因此内容安排三个课时:第一课时
4
为硫和二氧化硫,第二课时为硫酸,第三课时为硫酸根离子的检验,不同价态含硫物质的转化。本
节为第二课时的内容。
【学习目标】
1、了解浓硫酸的三大特性。
2、能运用氧化还原反应知识理解浓硫酸的氧化性。
3、认识硫酸在相关反应中体现的性质。
【核心素养】
1、通过对浓硫酸性质的学习,培养学生论据推理与模型认知的化学核心素养。
2、通过对化学实验的设计及操作的学习,培养学生科学探究与创新意识的化学核心素养。1、浓硫酸的三大特性(强氧化性、吸水性、脱水性)。
2、浓硫酸与金属单质、非金属单质、还原性物质的氧化还原理论的分析。
多媒体、浓硫酸、铜片、品红溶液,石蕊溶液、NaOH溶液、酒精灯、玻璃管、橡胶塞、导气
管、试管夹、试管、胶头滴管、铁架台等
【引入】
硫酸是重要的化工原料,工业上硫酸是怎么制备的呢?
【讲解】
一、硫酸的用途与工业制备
(1) 用途:
① 重要的化工原料,可用于制___________、炸药、染料、盐类等。
② 用于精炼石油、金属加工前的酸洗及制取各种挥发性酸、作干燥剂等。
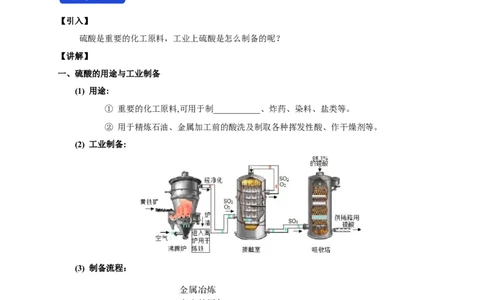
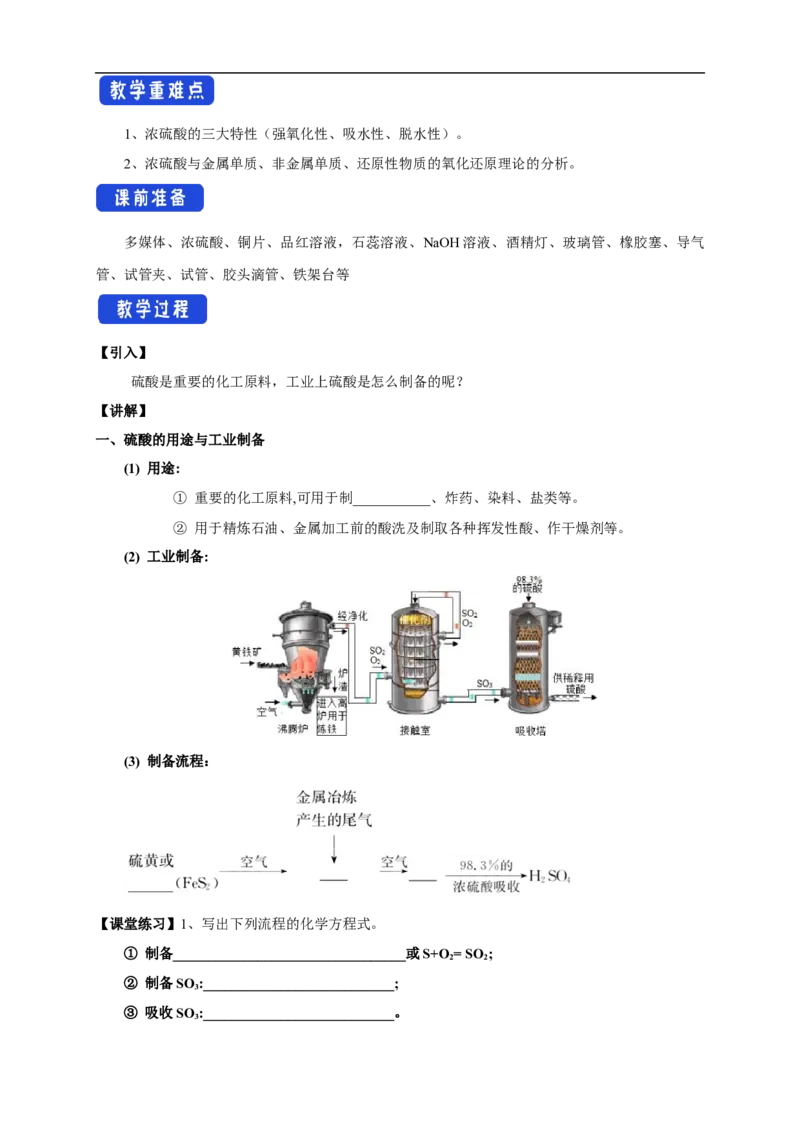
(2) 工业制备:
(3) 制备流程:
【课堂练习】1、写出下列流程的化学方程式。
① 制备_________________________________或S+O = SO ;
2 2
② 制备SO :___________________________;
3
③ 吸收SO :___________________________。
3【讲解】
二、硫酸的化学性质
(1) 酸的通性
电离方程式
【课堂练习】2、写出下列流程的离子方程式。
(1) 稀硫酸与活泼金属反应,如Zn:______________________。
(2) 稀硫酸与金属氧化物反应,如CuO:______________________。
(3) 稀硫酸与碱反应,如NaOH: ____________________________。
(4) 稀硫酸与部分盐反应,如NaCO: _______________________。
2 3
(2) 浓硫酸的特性——吸水性与脱水性
【实验探究】“黑面包”实验
(1) 吸水性:浓硫酸能吸收存在于周围环境中的水分,常用做干燥剂
(2) 脱水性:浓硫酸能将有机物中的氧、氢元素按水的组成比脱去
【思考讨论】1、吸水性与脱水性的区别
吸水性 脱水性
浓硫酸能够吸收______________________ 浓硫酸能把有机物中
原理 及固体 ________________________脱中的结晶水 去,剩余黑色的炭
区别
应用
2、浓硫酸能使蓝色胆矾变为白色,该过程体现了浓硫酸的脱水性还是吸水性?
【实验探究】
(3) 浓硫酸的特性——强氧化性
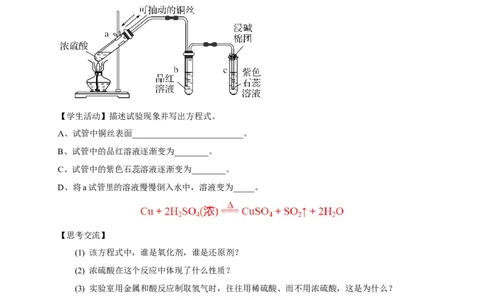
【实验5-3】浓硫酸和铜的反应
【学生活动】描述试验现象并写出方程式。
A、试管中铜丝表面__________________________。
B、试管中的品红溶液逐渐变为________。
C、试管中的紫色石蕊溶液逐渐变为________。
D、将a试管里的溶液慢慢倒入水中,溶液变为_____。
【思考交流】
(1) 该方程式中,谁是氧化剂,谁是还原剂?
(2) 浓硫酸在这个反应中体现了什么性质?
(3) 实验室用金属和酸反应制取氢气时,往往用稀硫酸、而不用浓硫酸,这是为什么?
【思考交流】浓硫酸能和金属反应,为什么可用铝罐车和铁罐车来运输浓硫酸?
【讲解】3. 浓硫酸的特性
(3) 强氧化性
① 与金属的反应② 与 非金属反应:
Δ
C+2HSO (浓) CO↑+2SO ↑+2HO
2 4 2 2 2
③ 与具有还原性的化合物反应,如H
2
S、 HI、HBr、FeCl
2
等
【学生总结】浓硫酸特性——强氧化性
【板书设计】
浓硫酸的特性
(1)吸水性:浓硫酸可以吸收空气或其他气体中的水蒸气、混在固体中的湿存水、结晶水合物中的结
晶水。在实验室里常用浓硫酸作干燥剂。
(2)脱水性: 浓硫酸可以使有机化合物中的氢、氧元素按水的组成从有机物中“脱离”出来,结合
生成水分子。
(3)强氧化性
①浓硫酸能与大多数金属反应,生成高价态金属的硫酸盐,本身一般被还原为SO 。
2
②常温下,浓硫酸能使铁、铝钝化。
③浓硫酸可将碳、磷等非金属单质氧化成高价态的氧化物或含氧酸,本身被还原为SO 。
2
【课堂练习】
1.浓硫酸具有A.强酸性,B.强氧化性,C.高沸点、难挥发性,D.脱水性,E.吸水性等性质。以下过
程主要表现了浓硫酸的哪些性质?请将答案的字母分别填入括号中。
(1)用NaCl固体和浓硫酸在加热条件下制氯化氢气体( )
(2)用磷矿物[主要成分是Ca (PO )]和硫酸反应制磷酸( )
3 4 2
(3)浓硫酸干燥H、O、Cl、HCl和SO 等气体( )
2 2 2 2(4)常温下可以用铁或铝的容器贮存浓硫酸( )
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末( )
(6)不能用浓硫酸干燥HBr、HI和HS等气体( )
2
(7)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑( )
2.实验证明铜在低温下不能和氧气发生反应,也不能和稀硫酸共热发生反应,但工业上却是将废铜
屑倒入热的稀硫酸中并不断地通入空气来制取硫酸铜溶液的。铜屑在此状态下发生的一系列化学反
应的方程式为____________________________________________。
利用铜和浓硫酸在加热条件下也能制备硫酸铜溶液,其化学方程式为________________。
以上两种方法哪种好?________,原因是________________________________________。
整节课讲练结合,讲能阐述清楚概念的内涵和外延,练起到了加深学生对概念的理解,探究如
何能深入到学生学习化学的整个过程之中,让“探究”常态化,而不流于形式,还需要对知识点,
对学生进行深层次了解。本节课趣味性比较强,通过对浓硫酸性质的学习,培养学生论据推理与模
型认知的化学核心素养。通过对化学实验的设计及操作的学习,培养学生科学探究与创新意识的化
学核心素养。在本节课还注重“教”“学”“评”一体化,在对学生回答做评价时,如何给予艺术
性的评价,做到既准确,又能很好把握激励的度,让学生的心智得以健康发展,做为教师,语言功
底还要加深。如何能在教师演示实验中,引导学生探究,做到教师“手动”,学生“脑动”,也是
一个值得研究的问题。