文档内容
第五章 化工生产中的重要非金属元素
第 2 节 氮及其化合物
第 1 课时 氮气与氮的固定 一氧化氮和二氧化氮
1、了解氮元素的存在及氮的固定。
2、掌握NO、NO 的性质。
2
3、了解NO、NO 、O 溶于水的简单计算(对生成硝酸的启示)。
2 2
1、氮气、一氧化氮、二氧化氮的化学性质为重点。
2、NO 溶于水的计算为难点。
x
不同价态含硫物质的转化。
氮元素位于元素周期表的第 周期, 族。氮原子的最外层有5个电子,既不容易得到3
个电子,也不容易失去5个电子。一般通过共用电子对与其他原子结合。
一、氮气
(1) 氮气的物理性质
颜色 状态 气味 密度 溶解性
_____ 气体 _____ 密度与空气接近 ___溶于水(2) 氮气的化学性质 氮气的结构 。
氮气的化学性质_____,通常很难与其他物质发生化学反应。
① 还原性:氮气与氧气的反应,其化学方程式为 。
② 氧化性:
a. N 与H 反应生成NH ,化学方程式为 。
2 2 3
b. 在点燃条件下与Mg反应,方程式为 。
二、氮的固定
(1) 含义: 将大气中_______的氮转化为___________的过程叫做氮的固定。
(2) 分类:
三、一氧化氮和二氧化氮
(1) 物理性质
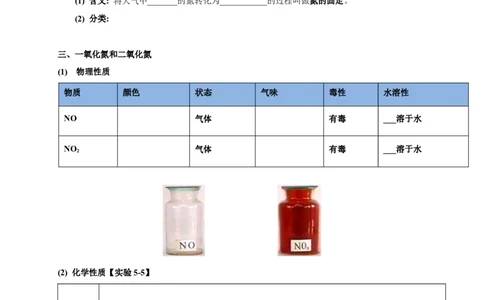
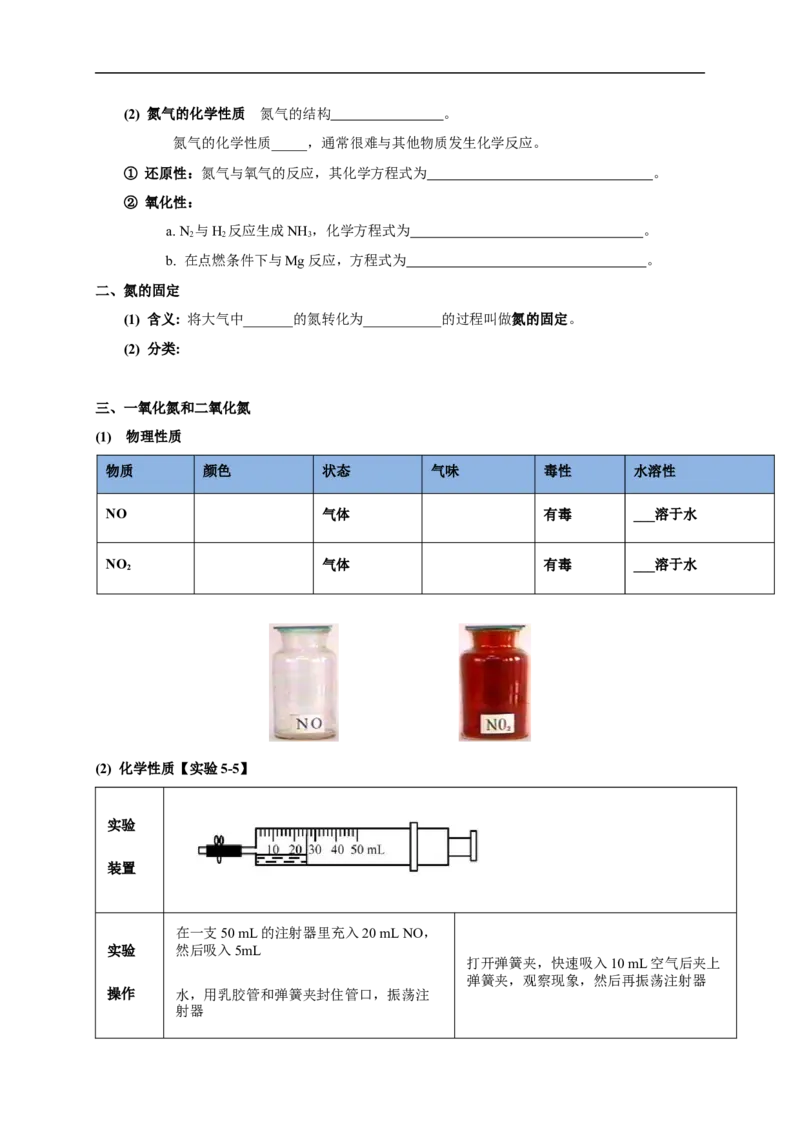
物质 颜色 状态 气味 毒性 水溶性
NO 气体 有毒 ___溶于水
NO 气体 有毒 ___溶于水
2
(2) 化学性质【实验5-5】
实验
装置
在一支50 mL的注射器里充入20 mL NO,
实验 然后吸入5mL
打开弹簧夹,快速吸入10 mL空气后夹上
弹簧夹,观察现象,然后再振荡注射器
操作 水,用乳胶管和弹簧夹封住管口,振荡注
射器现象
振荡后________________
结论:在一定条件下,NO与NO 可以相互转化。
2
反应的化学方程式为
①NO→NO : _____________________;
2
②NO →NO: __________________________(工业制取硝酸)。
2
【思考与讨论】
实验5-5发生了哪些化学反应?如果将注射器中的NO充分转化,可以采取什么措施?上述实
验对工业生成硝酸有什么启示?
工业生成硝酸的启示
(1) 原理
解答氮的氧化物溶于水的计算问题首先明确原理,无论是单一气体(NO ),还是NO、NO 、
2 2
O 中的两者或三者的混合气体,反应的实质是 ,故
2
若有气体剩余只能是NO或O,不能是NO 。
2 2
如何把NO和O 混合全部溶于水呢?
2
如何把NO 和O 混合全部溶于水呢?
2 2【思考与讨论】
(1) NO和NO 分别采用什么方法收集?
2
(2)NO 转化为NO的变化中,NO 只能作氧化剂吗?
2 2
【总结】
【课堂练习】
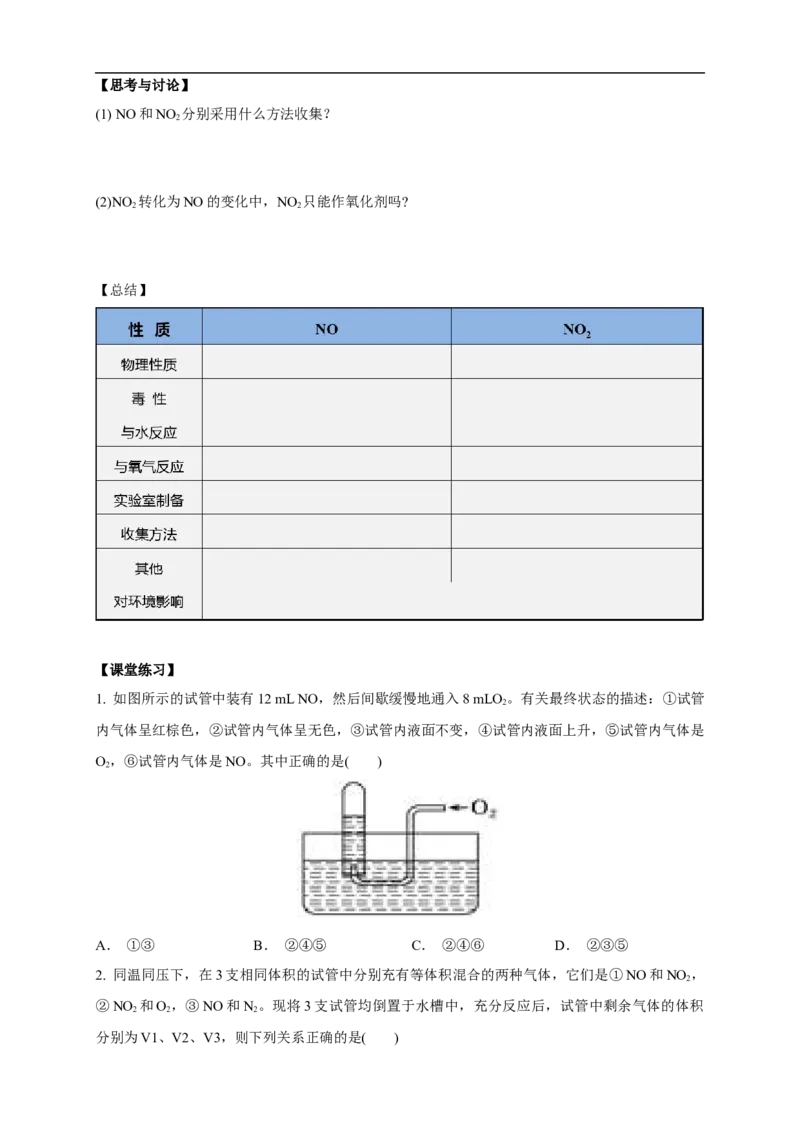
1. 如图所示的试管中装有12 mL NO,然后间歇缓慢地通入8 mLO。有关最终状态的描述:①试管
2
内气体呈红棕色,②试管内气体呈无色,③试管内液面不变,④试管内液面上升,⑤试管内气体是
O,⑥试管内气体是NO。其中正确的是( )
2
A. ①③ B. ②④⑤ C. ②④⑥ D. ②③⑤
2. 同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是①NO和NO ,
2
②NO 和O ,③NO和N 。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积
2 2 2
分别为V1、V2、V3,则下列关系正确的是( )A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V3>V1>V2
3. 在容积为672 mL的烧瓶中充满NO和NO 的混合气体,将其倒立在水槽里,去塞后再通入280
2
mL氧气,恰好完全反应,且液体充满烧瓶(气体体积都已折合为标准状况下的体积),下列有关叙
述正确的是( )
A. 总反应为NO+NO +O+HO === 2HNO
2 2 2 3
B. 总反应为4NO+8NO +5O+6HO === 12HNO
2 2 2 3
C. 生成硝酸的物质的量浓度均为0.030 mol·L-1
D. 生成硝酸的物质的量浓度约为0.060 mol·L-1
4. 用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO +NO+2NaOH===2NaNO +HO
2 2 2
2NO +2NaOH===NaNO +NaNO +HO
2 2 3 2
现有V L某NaOH溶液能完全吸收n mol NO 和m mol NO 组成的大气污染物。
2
(1)所用烧碱溶液的物质的量浓度至少为 mol·L-1
(2)若所得溶液中(NO -:NO -)=1:9,则原混合气体中NO 和NO的物质的量之比n:m=
3 2 2
。