文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
第一课时 化学反应与热能
作为高中必修阶段的化学课程,本章内容的编写力图在初中化学相关知识的基础上,使学生进
一步加深对化学反应相关知识的了解,初步形成较为全面的认识。本节内容主要包括化学反应中的
热能。对于化学反应中的热能,教材除引出化学反应中的吸热、放热反应等热量变化现象和概念外,
主要是借助化学反应中的热量变化揭示化学反应中能量变化的本质,并探讨其与社会、生产、生活
的联系。
教学目标
1.理解化学反应中能量变化的主要原因—化学键的断裂和形成。
2.了解吸热反应和放热反应的概念,熟知常见的吸热反应和放热反应。
核心素养
1.宏观辨识:理解化学反应中能量的变化取决于反应物与生成物的总能量相对大小。
2.微观探析:从化学键的断裂和形成,在本质上认识化学能量与化学变化的本质。
重点:理解化学反应中能量变化的主要原因—化学键的断裂和形成。
难点:理解化学反应中能量变化的主要原因—化学键的断裂和形成。
查找相关资料,准备实验仪器。
一、放热反应与吸热反应
教师设问:生活中哪些事实说明了化学反应伴随着能量变化?
学生交流。
设计意图:强化学生深刻理解化学、技术、社会和环境之间的相互关系,赞赏化学对社会 发展的
重大贡献,能运用已有知识和方法综合分析化学过程对自然可能带来的各种影响,权衡利弊,勇于承担责任,和积极与有关化学问题的社会决策。
教师活动:演示实验
【实验6-1】在一支试管中加入2mL2mol/L盐酸,并用温度计测量其温度。再向试管中放入用砂纸
打磨光亮的镁条,观察现象,并测量溶液温度的变化。
【实验6-2】将20gBa(OH) ·8H O品体研细后与10gNH CI品体一起放入烧杯中,并将烧杯放在
2 2 4
滴有几滴水的木片上。用玻璃棒快速搅拌,闻到气味后迅速用玻骑片盖上烧杯,用手触模杯壁下部,
试着用手拿起烧杯,观察现象。
学生活动:根据【实验6-1】【实验6-2】这两个实验总结一下生活中哪些反应属于放热反应,哪些
反应属于吸热反应?
设计意图:拓展学生知识面。
教师小结:上述两个实验中,反应前后的温度变化说明反应过程中伴有热量的释放或吸收。化学上
把释放热量的化学反应称为放热反应,如镁条、铝片与盐酸的反应,木炭、氢气、甲烷等在氧气中
的燃烧,氢气与氯气的化合等都是放热反应;把吸收热量的化学反应称为吸热反应,如氢氧化钡与
氯化铵的反应,盐酸与碳酸氢钠的反应,灼热的炭与二氧化碳的反应等都是吸热反应。
设计意图:拓展学生知识面,强化要点内容。
二、化学反应的实质
教师设问:化学反应过程中为什么会有能量变化?
学生交流:学生交流讨论
教师小结: 一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程。
三、一个化学反应吸收能量还是放出能量的决定因素
教师设问:在化学反应中,随着物质的变化,既有反应物中化学键的断裂,又有生成物中化学键的
形成,化学能也随之而改变。那么,一个化学反应吸收能量还是放出能量是由什么决定的呢?
学生活动:在25 ℃和101 kPa的条件下,断裂1 mol H-H需要吸收436 kJ能量,断裂1 mol Cl-Cl
键需要吸收242 kJ能量,形成1 mol H-Cl会放出431 kJ能量,通过计算说明化学反应 H+Cl ==
2 2
2HCl是吸热反应还是放热反应。
学生交流总结:
1、微观:化学反应中能量变化的原因——化学键的断裂和形成2、宏观:化学反应中能量变化的原因——反应物和生成物的总能量相对大小
设计意图:能初步学会收集各种证据,对物质的性质及其变化提出可能的假设;基于证据进行分析
推理,证实或证伪假设;能解释证据与结论之间的关系,确定形成科学结论所需要的证据和 寻找
证据的途径。
教师小结:
宏观解释
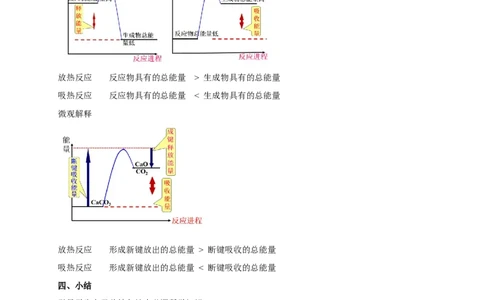
一个化学反应是释放能量还是吸收能量取决于反应物总能量与生成物总能量的相对大小
放热反应 反应物具有的总能量 > 生成物具有的总能量
吸热反应 反应物具有的总能量 < 生成物具有的总能量
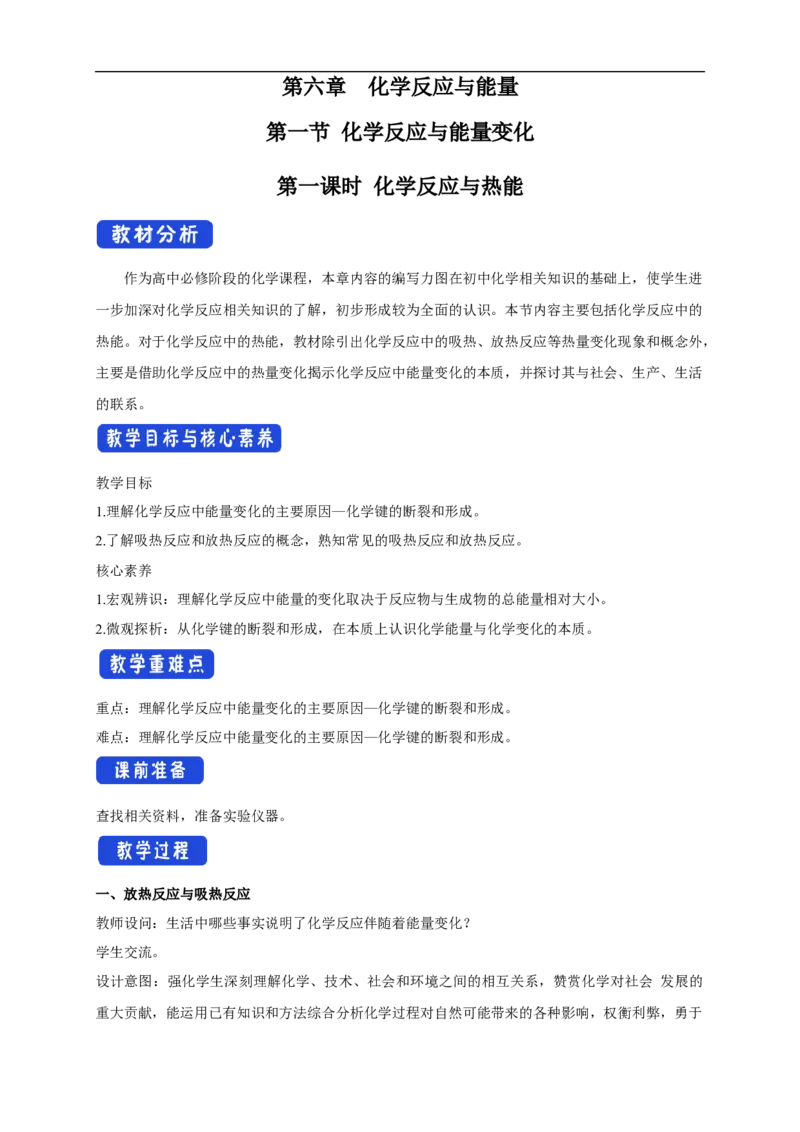
微观解释
放热反应 形成新键放出的总能量 > 断键吸收的总能量
吸热反应 形成新键放出的总能量 < 断键吸收的总能量
四、小结
引导学生自己总结归纳本节课所学知识
设计意图:透过现象引发学生深层次的思考,培养学生的归纳能力。培养学生思维的深刻性,提升
对元素及其化合物知识的认知水平。