文档内容
5.2.3 硝酸 酸雨及防治(学案)
1、结合实验探究,了解硝酸的主要性质——不稳定性和强氧化性,知道硝酸是重要的化工原料。
2、了解酸雨的概念,知道酸雨形成的主要原因是二氧化硫和二氧化氮进入大气,知道酸雨会严重
危害环境,增强环保意识,培养社会责任感。
重点:硝酸的不稳定性和强氧化性,酸雨的概念。
难点:硝酸的强氧化性。
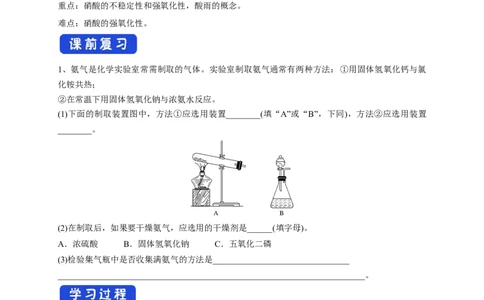
1、氨气是化学实验室常需制取的气体。实验室制取氨气通常有两种方法:①用固体氢氧化钙与氯
化铵共热;
②在常温下用固体氢氧化钠与浓氨水反应。
(1)下面的制取装置图中,方法①应选用装置________(填“A”或“B”,下同),方法②应选用装置
________。
(2)在制取后,如果要干燥氨气,应选用的干燥剂是______(填字母)。
A.浓硫酸 B.固体氢氧化钠 C.五氧化二磷
(3)检验集气瓶中是否收集满氨气的方法是________________________________
________________________________________________________________________。
1、为什么浓硝酸一般将其保存在棕色试剂瓶中,并放置在阴凉处。为什么有的浓硝酸看起来有颜
色呢!
2、硝酸的强氧化性:【实验5-8】学生活动:观察并比较实验现象。书写相关化学方程式。3、浓硝酸的氧化性很强,为什么运输浓硝酸时还是用铁罐车和铝槽车运输?
4、硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。工业上制硝酸的原理是将氨经过
一系列反应得到硝酸。
(1)写出每一步反应的化学方程式。
(2)请分析上述反应中的物质类别和氮元素化合价的变化情况,以及每一步反应中含氮物质发生
的是氧化反应还是还原反应。
5、根据上图酸雨的形成过程,写一写相关的化学方程式。
1、酸雨形成的最主要原因是( )
A.森林遭乱砍滥伐,破坏了生态平衡
B.工业上大量燃烧含硫燃料
C.大气中二氧化碳的含量增多
D.汽车排出大量尾气
2、下列关于硝酸的叙述正确的是( )
A.常温下,浓硝酸可以使金属镁钝化
B.稀硝酸与活泼金属反应主要放出氢气
C.浓硝酸和稀硝酸都是强氧化剂
D.室温下,铜能与浓硝酸反应,不能与稀硝酸反应
3、0.3 mol Cu和含1.2 mol HNO 的浓硝酸,充分反应后,生成NO 的量为( )
3 2
A.0.2 mol B.0.6 mol
C.小于0.6 mol D.大于0.6 mol