文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
第 1 课时 化学反应与热能
1、理解化学反应中能量变化的主要原因——化学键的断裂和形成。
2、知道化学反应中的能量变化和物质具有的能量之间的关系。
3、了解吸热反应和放热反应的概念,熟知常见的吸热反应和放热反应。
重点:化学反应中能量变化的本质;
难点:化学键断裂和形成简单计算放热反应和吸热反应。
能量守恒定律。
一、吸热反应与放热反应
【实验6-1】镁和盐酸的反应
在一只试管中加入2 mL 2 mol/L 盐酸,并用温度计测量其温度。再向试管中放入用砂纸打磨
光亮的镁条,观察现象,并测量溶液温度的变化。
现象: 。
结论: 。
【实验6-2】Ba(OH) •8HO和NH Cl
2 2 4
将20g Ba(OH) •8H O晶体研细后与10gNH Cl在烧杯中混合,并将烧杯放在滴有几滴水的木片
2 2 4
上,用玻璃棒快速搅拌,闻到气味后迅速用玻璃片盖上烧杯,用手触摸烧杯下部,试着用手拿起烧杯。观察现象。
现象: 。
结论: 。
1. 吸热反应与放热反应
放热反应:把释放热量的化学反应称为放热反应。
常见的放热反应
吸热反应:把吸收热量的化学反应称为吸热反应。
常见的吸热反应
【思考与交流】化学反应过程中为什么会有能量的变化?为什么有的化学反应释放热量,有的化学
反应吸收热量?
2.化学反应的能量变化的本质
(1) 在1 mol氢分子中,含有 mol氢原子,含有 mol H—H键。
(2) 已知在25 ℃和101 kPa条件下,由2 mol H原子形成1 mol H—H键时,放出436 kJ的能量。若
要使1 mol氢分子变为2 mol氢原子时,需要断开1 mol H—H键,其能量变化是 。
(3) CH 的结构式是 ,1 mol CH 分子中含有 mol C—H键。
4 4
(4) 在CH 中,断开1 mol C—H键要吸收415 kJ的能量。若要形成1 mol CH 中的C—H键其能量
4 4
变化是 。
结论:在相同条件下,由原子形成1 mol化学键时所 ,与断开1 mol相同化学
键所 是相等的。【思考与交流】
H + Cl = 2HCl
2 2
断开1 mol H-H 键要吸收 436 kJ 的能量
断开1 mol Cl-Cl 键要吸收 243 kJ 的能量
生成1 mol H-Cl 键要释放 431 kJ 的能量
E吸收= kJ E放出= kJ
E E 反应
1 2
2.化学反应的能量变化的本质
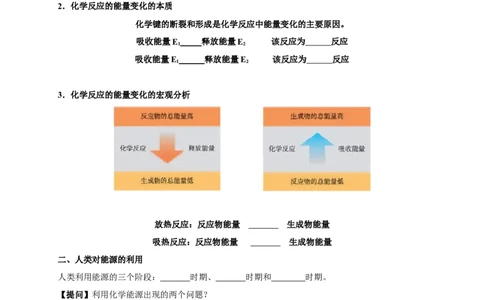
化学键的断裂和形成是化学反应中能量变化的主要原因。
吸收能量E 释放能量E 该反应为 反应
1 2
吸收能量E 释放能量E 该反应为 反应
1 2
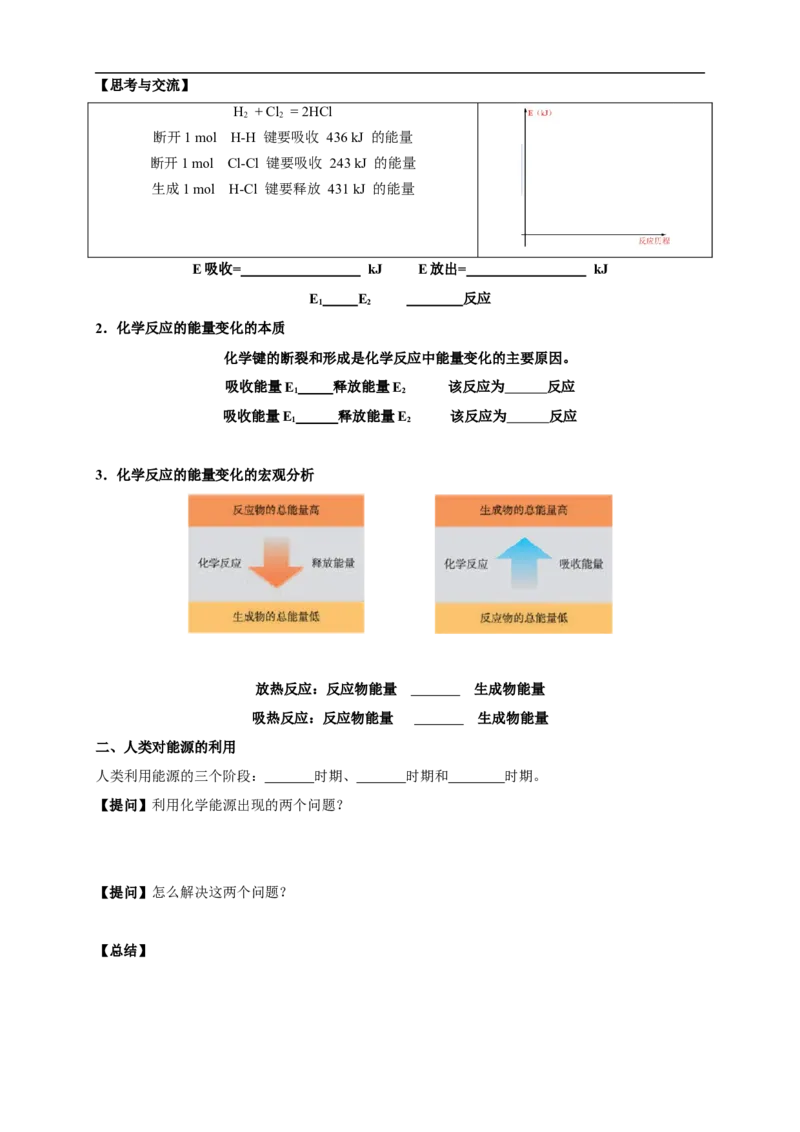
3.化学反应的能量变化的宏观分析
放热反应:反应物能量 生成物能量
吸热反应:反应物能量 生成物能量
二、人类对能源的利用
人类利用能源的三个阶段: 时期、 时期和 时期。
【提问】利用化学能源出现的两个问题?
【提问】怎么解决这两个问题?
【总结】【课堂练习】
1.下列说法正确的是( )
①需要加热才能发生的反应一定是吸热反应 ②放热反应在常温下一定很容易发生 ③反应是放出
能量还是吸收能量必须看反应物和生成物所具有的总能量的相对大小 ④有的放热反应加热到一定
温度引发后,停止加热反应也能继续进行
A.只有③④ B.只有①② C.①②③④ D.②③④
2.已知反应A +B = 2AB,破坏1 mol A 中的化学键消耗的能量为Q kJ,破坏1 mol B 中的化学键
2 2 2 1 2
消耗的能量为 Q kJ,形成1 mol AB中的化学键释放的能量为 Q kJ,则下列说法正确的是(
2 3
)
A.若A 和B 的总能量之和大于生成的AB的总能量,则反应放热
2 2
B.若A 和B 的总能量之和小于生成的AB的总能量,则反应放热
2 2
C.若该反应放出能量,则Q+Q>Q
1 2 3
D.若该反应吸收能量,则Q+Q