文档内容
第六章 化学反应与能量
第一节 化学反应与能量变化
第 1 课时 化学反应与热能
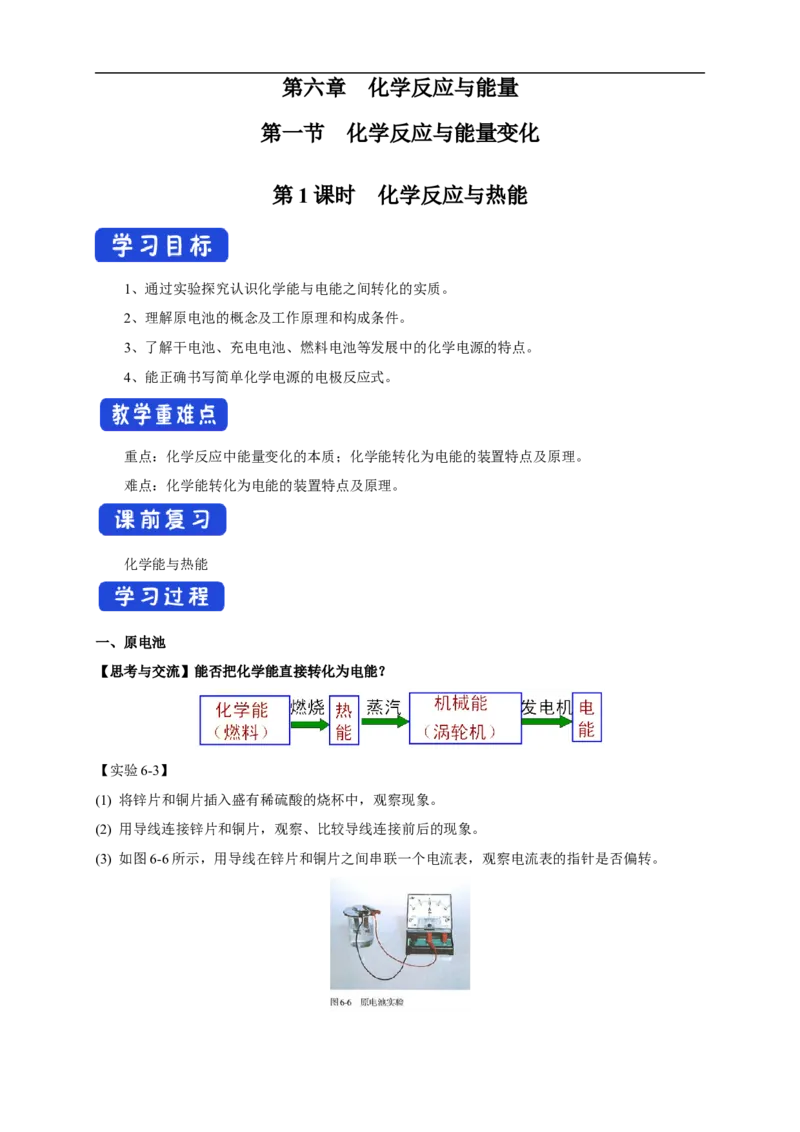
1、通过实验探究认识化学能与电能之间转化的实质。
2、理解原电池的概念及工作原理和构成条件。
3、了解干电池、充电电池、燃料电池等发展中的化学电源的特点。
4、能正确书写简单化学电源的电极反应式。
重点:化学反应中能量变化的本质;化学能转化为电能的装置特点及原理。
难点:化学能转化为电能的装置特点及原理。
化学能与热能
一、原电池
【思考与交流】能否把化学能直接转化为电能?
【实验6-3】
(1) 将锌片和铜片插入盛有稀硫酸的烧杯中,观察现象。
(2) 用导线连接锌片和铜片,观察、比较导线连接前后的现象。
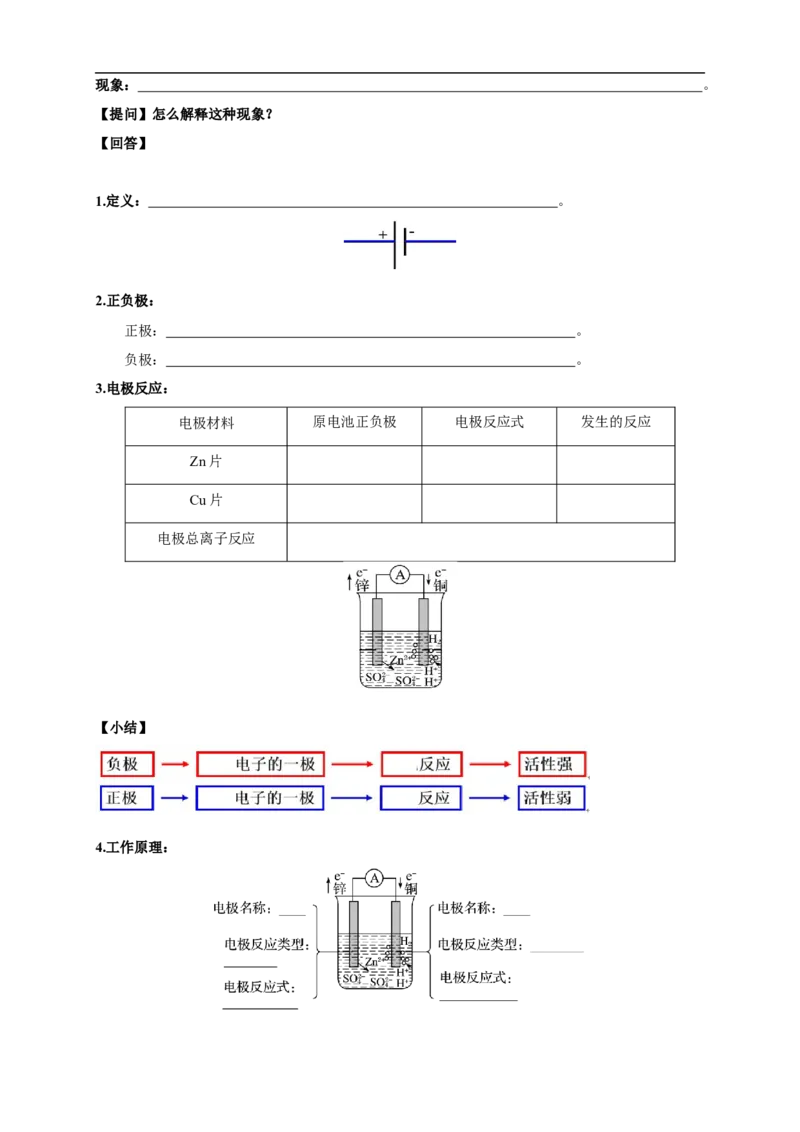
(3) 如图6-6所示,用导线在锌片和铜片之间串联一个电流表,观察电流表的指针是否偏转。现象: 。
【提问】怎么解释这种现象?
【回答】
1.定义: 。
2.正负极:
正极: 。
负极: 。
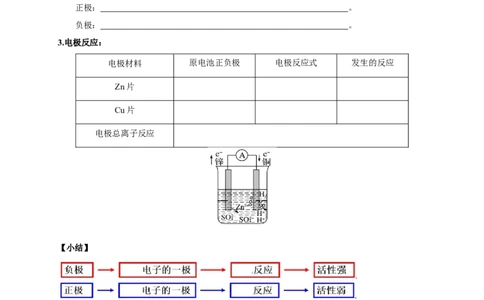
3.电极反应:
电极材料 原电池正负极 电极反应式 发生的反应
Zn片
Cu片
电极总离子反应
【小结】
4.工作原理:原电池总反应式: ;
5.构成条件
理论上,自发的 反应均可构成原电池。
具体条件是:
①具有 的两个电极(金属与金属或金属与能导电的非金属);
②溶液:两电极均插入 溶液中;
③导线:两极用导线相连,形成闭合回路。
【课堂练习】
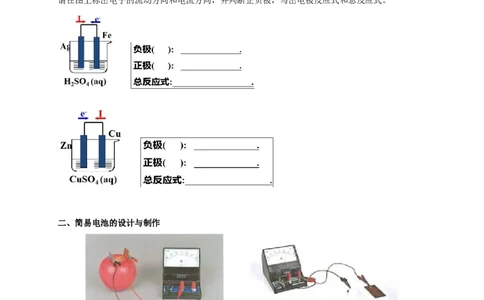
请在图上标出电子的流动方向和电流方向,并判断正负极,写出电极反应式和总反应式。
二、简易电池的设计与制作
【课堂练习】
1、一个电池反应的离子方程式是 Zn+Cu2+=Zn2+ +Cu, 该反应的的原电池正确组合是( )
A B C D
正极 Zn Cu Cu Fe负极 Cu Zn Zn Zn
电解质溶液 CuCl HSO CuSO HCl
2 2 4 4
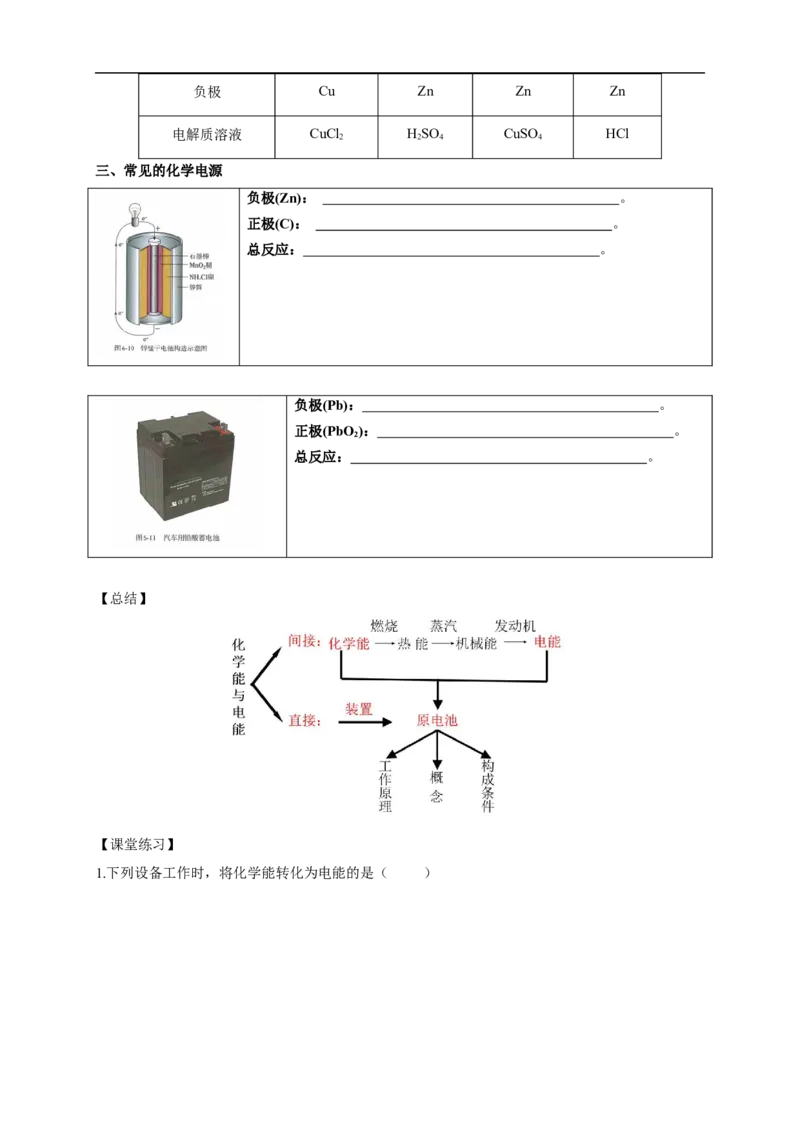
三、常见的化学电源
负极(Zn): 。
正极(C): 。
总反应: 。
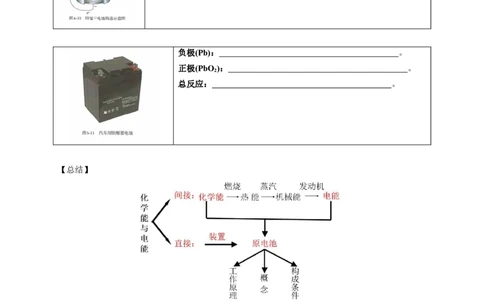
负极(Pb): 。
正极(PbO ): 。
2
总反应: 。
【总结】
【课堂练习】
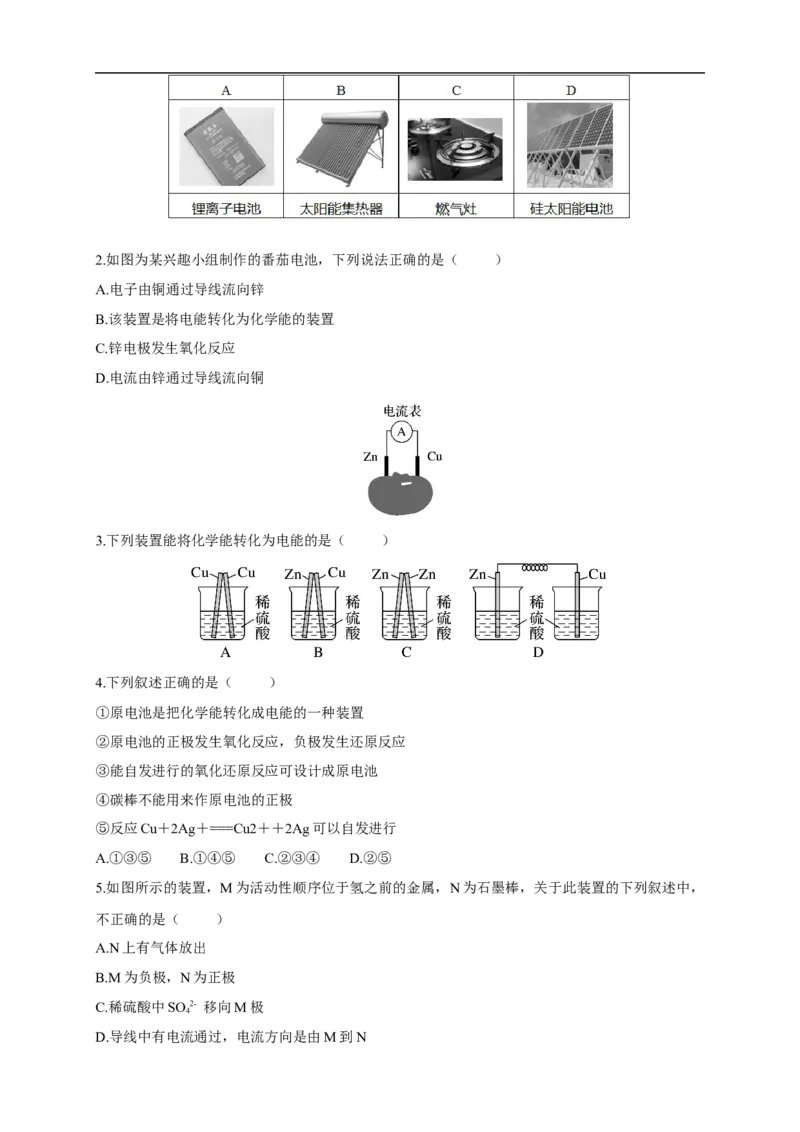
1.下列设备工作时,将化学能转化为电能的是( )2.如图为某兴趣小组制作的番茄电池,下列说法正确的是( )
A.电子由铜通过导线流向锌
B.该装置是将电能转化为化学能的装置
C.锌电极发生氧化反应
D.电流由锌通过导线流向铜
3.下列装置能将化学能转化为电能的是( )
4.下列叙述正确的是( )
①原电池是把化学能转化成电能的一种装置
②原电池的正极发生氧化反应,负极发生还原反应
③能自发进行的氧化还原反应可设计成原电池
④碳棒不能用来作原电池的正极
⑤反应Cu+2Ag+===Cu2++2Ag可以自发进行
A.①③⑤ B.①④⑤ C.②③④ D.②⑤
5.如图所示的装置,M为活动性顺序位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,
不正确的是( )
A.N上有气体放出
B.M为负极,N为正极
C.稀硫酸中SO 2- 移向M极
4
D.导线中有电流通过,电流方向是由M到N6.下列几种化学电池中,不属于可充电电池的是( )
A.碱性锌锰电池 B.手机用锂电池
C.汽车用铅蓄电池 D.玩具用镍氢电池
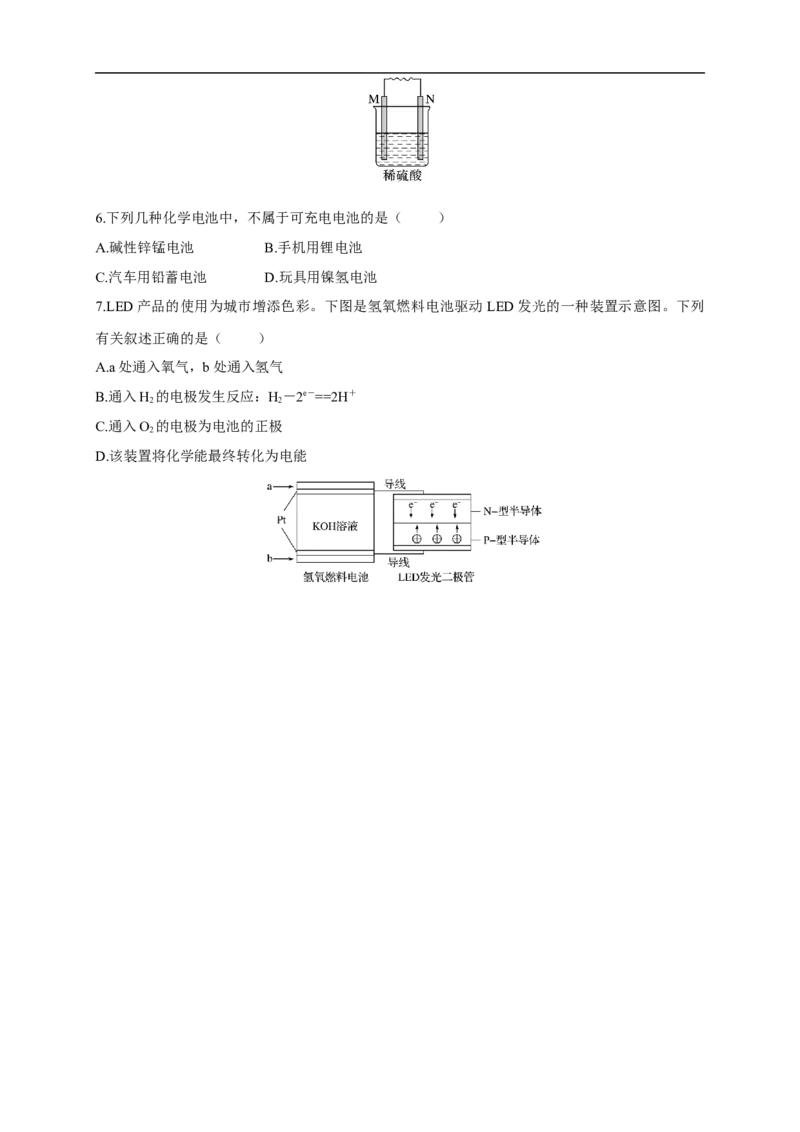
7.LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列
有关叙述正确的是( )
A.a处通入氧气,b处通入氢气
B.通入H 的电极发生反应:H-2e-==2H+
2 2
C.通入O 的电极为电池的正极
2
D.该装置将化学能最终转化为电能