文档内容
第六章 化学反应与能量
第二节 化学反应的速率和限度
第一课时 化学反应的速率
考虑到通过初中和高中的化学学习,学生对化学反应速率与反应条件相关,改变反应条件(如使用催
化剂)可调控反应速率等知识已有所了解。教材中化学反应速率影响因素的内容,以新旧兼容、详略有别
的方式编排。教材结合学生学过的相关知识,补充一些生活、生产中需要通过反应条件调控反应速率的实
例,说明认识化学反应速率影响因素的重要性,并借此体现调控反应速率的意义和价值。在已知催化剂这
一反应速率影响因素的基础上,通过“探究”,重点引导学生探讨反应温度和反应物浓度对化学反应速率
的影响,并结合浓度影响因素,针对气体反应说明压强的影响。
“探究”中安排的两个实验和一个讨论,教材采取了学生自主参与度不同的设计。对反应温度的影响的探
究给出了具体步骤,学生只需自主操作并观察、比较;对反应物浓度的影响的探究只给出探究设计提示,
学生需要根据要求选择实验用品,设计并实施实验。“问题与讨论”则需要学生自主提出问题、进行假设、
设计实验方案。这种探究水平的进阶式设计,意在体现一定探究性的前提下保证可操作性,同时也照顾到
全国范围内化学教学的实际可行性。
除“探究”之外,教材还利用“思考与讨论”引导学生探讨得出影响化学反应速率的其他一些因素,如反
应物颗粒大小、反应物接触面积等。这样将教材中提及的各种不同影响因素分层次处理,既突出浓度(压
强)、温度、催化剂的影响因素等重点内容,又不局限于这几个因素,表明影响化学反应速率的因素还有
很多。
教学目标
1.了解化学反应速率的概念和表示方法。
2.能够进行化学反应速率的简单计算。
3.理解影响化学反应速率的因素及规律。
核心素养
1.变化观念:认识反应条件对化学反应速率的影响。
2.模型认知:能用一定的理论模型说明外界条件改变对反应速率的影响。重点:化学反应速率的概念及其影响因素。
难点:化学反应速率的概念及其影响因素。
查找相关资料,准备实验仪器。
学生活动:思考与交流:化学反应的快慢是相对的!不同的化学反应,快慢不同。你了解下列化学变化过
程进行的快慢吗?反应的快慢与我们有什么关系?
设计意图:抛出问题,引出新课内容,激发学生学习欲望。
教师小结:
A. 定性观察法(粗略)
①冒气泡快慢
②固体量减少
③溶液浑浊程度
④溶液颜色变化等
B. 定量表示法(准确)——化学反应速率
一、化学反应速率
教师活动:教师抛出问题:化学反应速率是如何定义的呢?回忆一下物理中是怎么描述物体运动的快慢?
学生活动:化学反应速率:单位时间内反应物浓度的减少量或生成物浓度的增加量。
设计意图:增强师生互动
学生活动:【问题】用∆t来表示时间,∆c表示浓度变化,v表示反应速率,你能用字母符号来表示化学反
应速率吗?
教师小结:概念:单位时间内反应物浓度的减少量或生成物浓度的增加量。
数学表达式:。v(B)=∆C(B)/∆t
Δc —— 某一反应物或生成物浓度的变化量,常用单位:mol/L;
Δt —— 变化所用时间,常用单位:s,min,h;
V —— 化学反应速率,常用单位:
mol/(L·s),mol/(L·min)等。
学生活动:在某一化学反应里,反应物A的浓度在10 s内从4.0 mol/L变成1.0 mol/L。在这10 s内A的化学反应速率为多少?
教师小结:注意:反应速率指10s内的平均速率!
二、“三段法”计算化学反应速率:
学生活动:在2 L的密闭容器中,加入1 mol N 和3 mol H ,发生 N+3H == 2NH ,在2s末时,测得容
2 2 2 2 3
器中含有0.4 mol的NH ,求该反应的化学反应速率。
3
教师小结: “三段法”计算化学反应速率:
“三段法”基本步骤:
(1)写出有关反应的化学方程式;
(2)标出各物质的起始量、变化量、某时刻量;
(3)根据已知条件列方程式计算。
例: m A + n B p C + q D
起始: a b 0 0
变化: mx nx px qx
某时刻:a-mx b-nx 0+px 0+qx
基本关系:①变化量与方程式中各物质的化学计量数成比例
②这里a、b可指 物质的量、浓度、体积等
③反应物:某时刻量=起始量-变化量
生成物:某时刻量=起始量+变化量
④转化率α
三、影响化学反应速率的因素
学生活动:有哪些条件会影响化学反应速率呢?你能以HO 制O 为例,设计实验探究吗?
2 2 2
探究温度对反应速率的影响:
【假设】
影响化学反应速率的因素可能有反应温度、反应物浓度等。
【用品】
5%H,O,溶液、1mol/LFeCl,溶液、0.1mol/L盐酸、1mol/L盐酸、大理石碎块、冷水、热水、试管、试
管夹、烧杯。
【实验】
(1)反应温度的影响不同温度环境 实验现象
冷水
热水
反应物浓度的影响:
步骤: 。
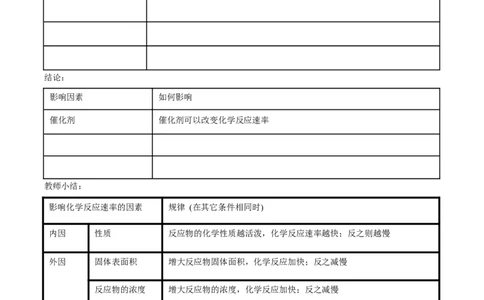
结论:
影响因素 如何影响
催化剂 催化剂可以改变化学反应速率
教师小结:
影响化学反应速率的因素 规律 (在其它条件相同时)
内因 性质 反应物的化学性质越活泼,化学反应速率越快;反之则越慢
外因 固体表面积 增大反应物固体面积,化学反应加快;反之减慢
反应物的浓度 增大反应物的浓度,化学反应加快;反之减慢
温度 升高温度,化学反应速率加快;反之减慢
催化剂 使用催化剂,化学反应速率加快
设计意图:加强学生发现和提出有探究价值的化学问题,能依据探究目的设计并优化实验方案,完成实验
操 作,能对观察记录的实验信息进行加工并获得结论;能和同学交流实验探究的成果,提出进 一步探究
或改进实验的设想;能尊重事实和证据,不迷信权威,具有独立思考、敢于质疑和批判的创新精神。四、小结
引导学生自己总结归纳本节课所学知识
设计意图:透过现象引发学生深层次的思考,培养学生的归纳能力。培养学生思维的深刻性,提升对元素
及其化合物知识的认知水平。