文档内容
第七章 有机化合物
第二节 乙烯与有机高分子材料
第 1 课时 乙烯
乙烯是石油化学工业重要的基本原料,通过有机化学反应可以由乙烯得到多种烃的衍生物及高
分子材料;同时,乙烯也是较简单的含有官能团的有机物。通过对乙烯的学习,学生可以更深人地
了解有机物的结构、性质、用途及相互转化规律,并将初步接触决定有机物分类与化学性质的特征
基团(官能团)。基于此,本节教材在编排上依次从物理性质、分子结构、化学性质和用途这几个方
面介绍乙烯,给出在中学阶段认识有机物的一般流程,建立认知模型,使学生进一步认识有机物的
结构特点,体会物质结构对性质和用途的决定作用。
本节教材在介绍乙烯的物理性质后,给出乙烯的分子式、结构式和分子结构模型,让学生直观
地了解乙烯与烷烃在结构上的差异,引出下文对二者化学性质差异的讨论。乙烯的化学性质围绕碳
碳双键展开。氧化反应先讲学生熟悉的燃烧氧化(有机物的共性),再讲被高锰酸钾等氧化剂氧化(含
双键等不饱和基团的有机物的特性)。由于后者的反应产物较为复杂,教材只介绍反应现象,不涉
及产物和化学方程式。
介绍加成反应时,教材选择乙烯与溴反应的实验,使用四氯化碳作为溶剂,明确了反应产物,
避免在教材和教学中解释使用溴水时的副产物。教材通过实验和化学方程式中结构式的变化引入加
成反应的概念,同时指出乙烯还可与其他试剂发生加成反应,生成一系列产物, 借此体现有机物
转化的思想。
初中化学曾简单介绍过小分子相互连接形成高分子的聚合反应,因此教材在这里侧重通过化学
方程式、结构式和分子结构模型具体展示化学键与有机物的分子结构在聚合反应前后的变化,使学
生初步认识加成反应与聚合反应的关系,了解聚合物的分子结构,深化对结构决定性质这一化学基
本观念的理解。同时,教材还以聚乙烯为例介绍了链节、单体、聚合度等高分子基本概念,以利于
接下来学习合成高分子与生物高分子。
在学习了甲烷和乙烯这两种饱和烃和不饱和烃的代表性物质之后,学生对烃的结构与性质已经
有了初步的认识。在此基础上,教材给出烃、饱和烃、不饱和烃等概念,并结合树状图和代表物的
结构式介绍烃的分类:一种是根据分子中的特征性基团分类,另一种是根据碳骨架类型分类。由此体现辨识有机物的两个基本视角(碳骨架与官能团)和物质分类的学科思想,提升学生的认识水平。
课程标准对乙炔和苯的要求较低,只要求学生知道其基本结构特征,不涉及性质。因此教材只
简单描述二者分子中碳原子的成键特点,并通过栏目让学生用模型探究乙炔的分子结构。“科学史
话”中有关芳香族化合物和苯的拓展性内容,供学有余力的学生自行阅读,不作教学要求。
【学习目标】
1、会写乙烯的分子式、结构式、结构简式、电子式。
2、知道乙烯能够发生氧化反应、加成反应、聚合反应。
3、理解加成反应的概念。
【核心素养】
1、微观探析:认识乙烯的组成、结构、性质和变化,形成“结构决定性质”的观念
2、证据推理:通过分析、推理认识乙烯发生加成反应时的断键和成键情况。
重点:从宏观和微观两个方面研究乙烯的结构如何决定其性质;
难点:乙烯加成反应、加聚反应的基本规律。
球棍模型,乙烯,高锰酸钾,溴的四氯化碳。
【引入】
为了促进香蕉成熟,可在密封袋子中放一些成熟的苹果
乙烯是石油化学工业重要的基本原料,通过一系列化学反应,可以从乙烯得到有机高分子材料、
药物等成千上万种有用的物质。乙烯的用途广泛,其产量可以用来衡量一个国家石油化学工业的发
展水平。【讲解】
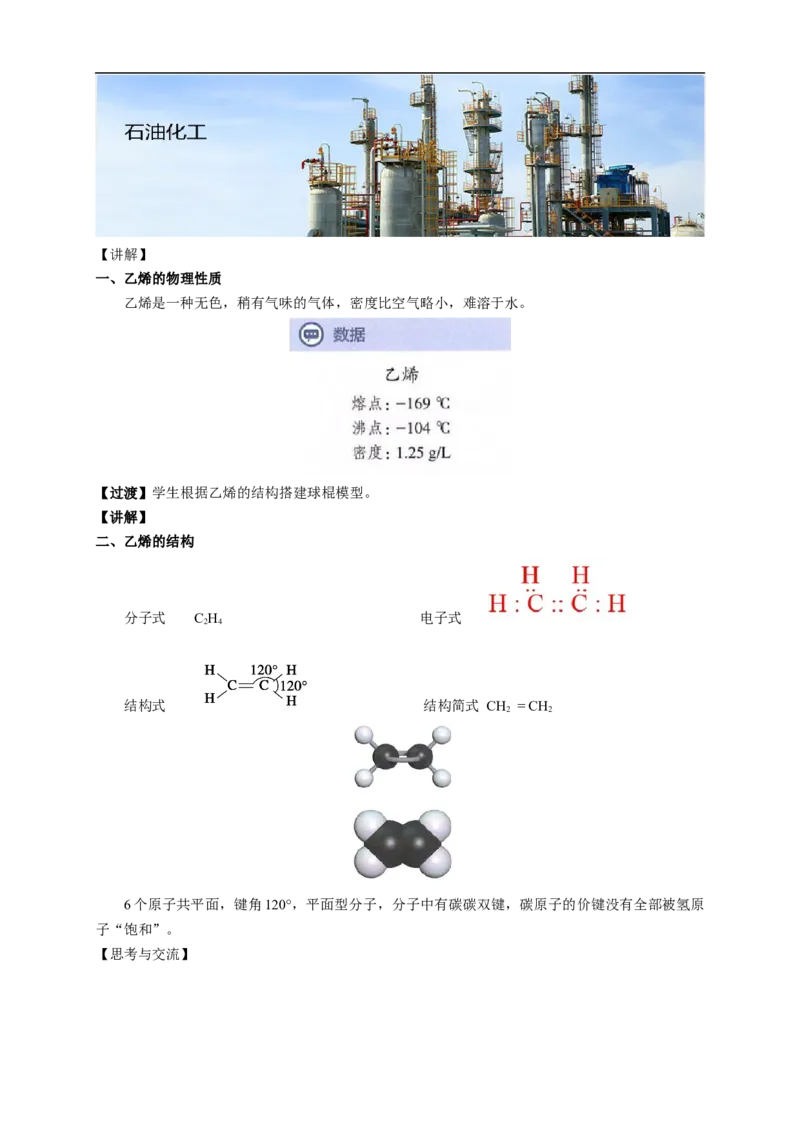
一、乙烯的物理性质
乙烯是一种无色,稍有气味的气体,密度比空气略小,难溶于水。
【过渡】学生根据乙烯的结构搭建球棍模型。
【讲解】
二、乙烯的结构
分子式 C H 电子式
2 4
结构式 结构简式 CH = CH
2 2
6个原子共平面,键角120°,平面型分子,分子中有碳碳双键,碳原子的价键没有全部被氢原
子“饱和”。
【思考与交流】乙烯分子中含有碳碳双键,在组成和结构上与只含碳碳单键和碳氢键的烷烃有较大差异,因此
在性质上也有很多不同。碳碳双键使乙烯表现出较活泼的化学性质。
【实验探究】
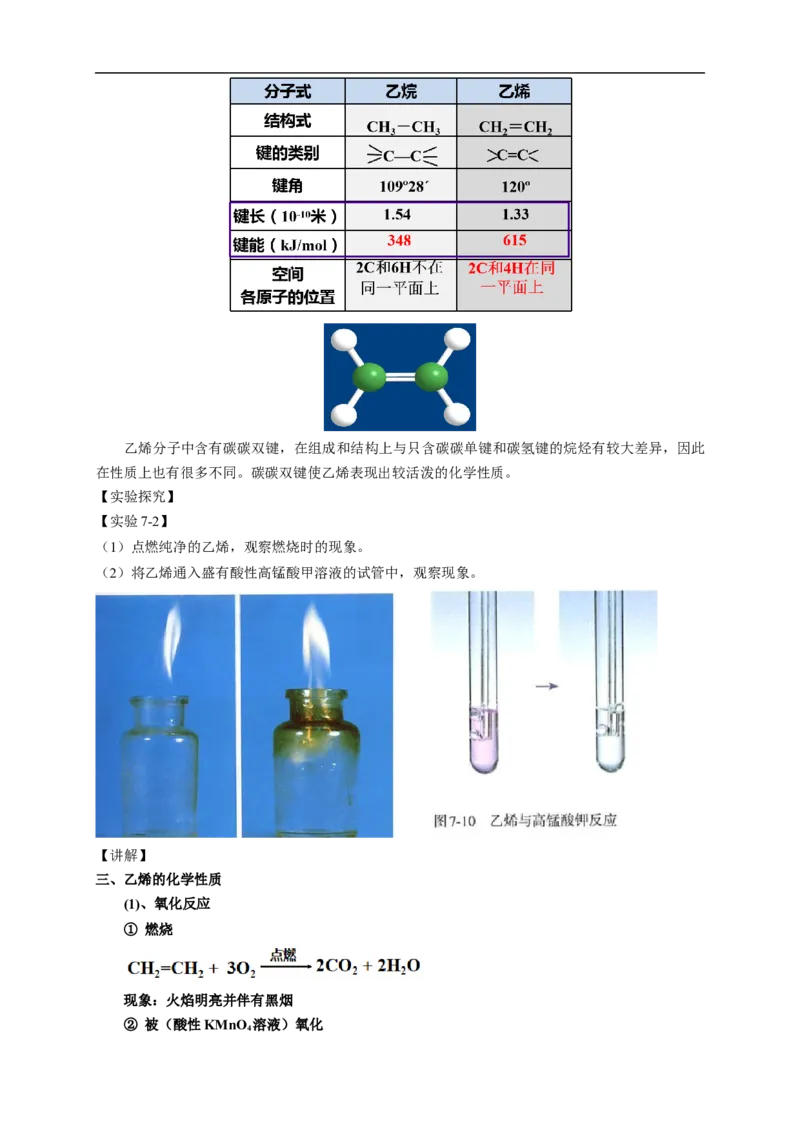
【实验7-2】
(1)点燃纯净的乙烯,观察燃烧时的现象。
(2)将乙烯通入盛有酸性高锰酸甲溶液的试管中,观察现象。
【讲解】
三、乙烯的化学性质
(1)、氧化反应
① 燃烧
现象:火焰明亮并伴有黑烟
② 被(酸性KMnO 溶液)氧化
4现象:溶液的紫色褪去
应用:鉴别乙烯(与烷烃比)
【思考】能不能用于除去烷烃中的乙烯?
【实验探究】
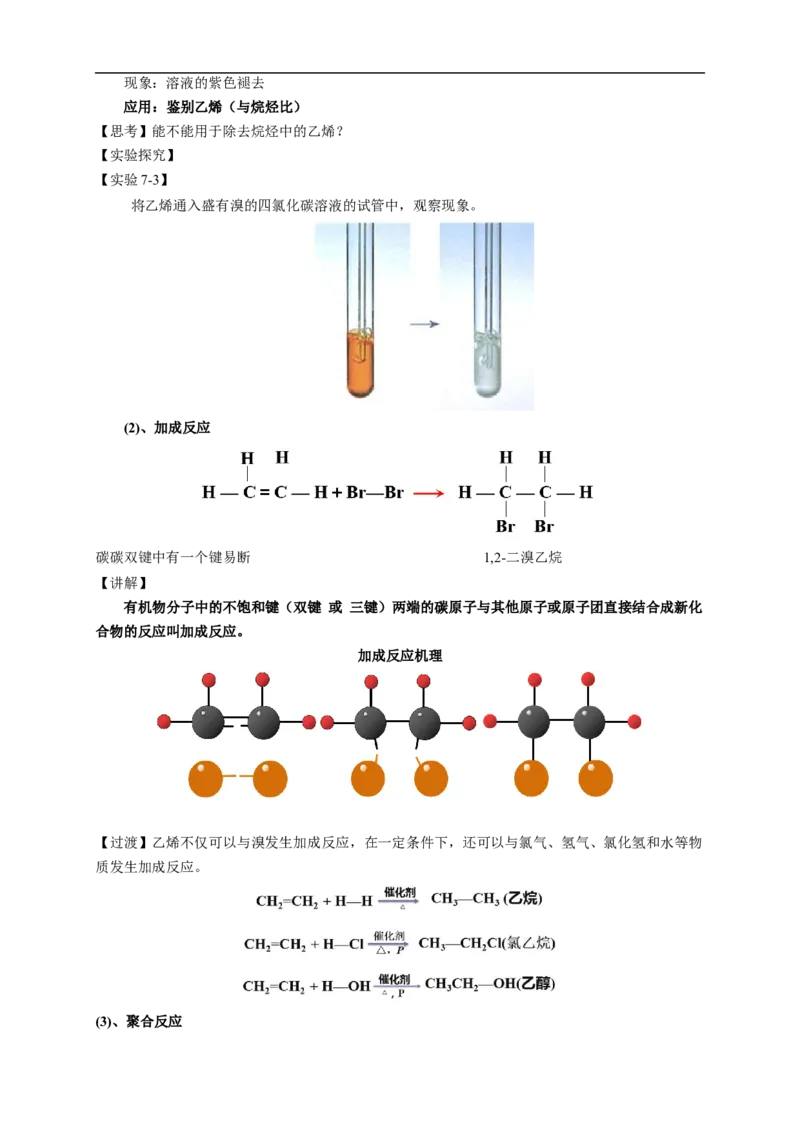
【实验7-3】
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
(2)、加成反应
碳碳双键中有一个键易断 1,2-二溴乙烷
【讲解】
有机物分子中的不饱和键(双键 或 三键)两端的碳原子与其他原子或原子团直接结合成新化
合物的反应叫加成反应。
加成反应机理
【过渡】乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物
质发生加成反应。
(3)、聚合反应在适当的温度、压强和催化剂存在的条件下,乙烯分子中碳碳双键中的一个键断裂,分子间通
过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物聚乙烯。
像这样,由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合
反应。聚合反应在有机高分子材料的生产中有着广泛的应用。乙烯的聚合反应同时也是加成反应,
这样的反应又被称为加成聚合反应,简称加聚反应。
【信息搜索】
除了被用作化工原料,乙烯还是一种植物生长调节剂,可用于催熟果实。在两个透明的塑料袋
中各放一个未成熟的水果,向其中的一个袋子里再放一个成熟的水果,将袋口密封,观察并比较水
果的变化。请查阅资料,与同学交流,解释以上现象。
【归纳总结】
乙烷与乙烯的分子结构和化学性质对比
分子式 C H C H
2 6 2 4
分
结构式
子
结
碳碳键类别 碳碳单键 碳碳双键
构
分子内原子
C、H不全在一个平面内 6个原子都在同一平面内
的相对位置
燃烧 2C H+7O――→4CO+6HO C H+3O――→2CO+2HO
2 6 2 2 2 2 4 2 2 2
化
CH==CH+
学 2 2
特征反应 C H+Cl――→C HCl+HCl
2 6 2 2 5
Br ―→CHBrCHBr
性 2 2 2
与酸性高锰
质
不反应 因发生氧化反应而使其褪色
酸钾溶液
【课堂练习】
1.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )
A.澄清石灰水,浓硫酸
B.溴水,浓硫酸
C.酸性高锰酸钾溶液,浓硫酸D.浓硫酸,酸性高锰酸钾溶液
2. 下列说法错误的是( )
A.无论是乙烯与Br 的加成反应,还是乙烯使酸性KMnO 溶液褪色,都与分子内含有的碳碳双键有
2 4
关
B.溴的四氯化碳溶液和酸性KMnO 溶液都可以鉴别乙烯和甲烷
4
C.相同质量的乙烯和甲烷完全燃烧后生成水的质量相同
D.乙烯的化学性质比乙烷的化学性质活泼
3.长途运输水果时,常常将浸泡有高锰酸钾溶液的硅土放置在盛放水果的容器中,其目的是
( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
4.能证明乙烯分子中含有一个碳碳双键的事实是( )
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO 和HO的物质的量相等
2 2
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO 溶液褪色
4
5.含有碳碳双键的有机物很多,其性质和乙烯相似,写出下列要求的方程式。
(1)丙烯与溴水反应:_______________________________。
(2)丙烯在一定条件下加聚生成聚丙烯:_______________________________。
乙烯是最具有工业价值的石油化工基础原料,也是最简单的不饱和烃。对乙烯结构和性质的学
习,其重点是从化学键和官能团视角认识有机化合物的结构决定性质的学科思想,帮助学生发展
“宏观辨识与微观探析”的学科核心素养。同时,乙烯的机构和性质的学习模型也可以帮助学生认
识不饱和烃的结构和性质特点。