文档内容
6.2.2 化学反应的限度 化学反应条件的控制(学案)
1.了解可逆反应。
2.理解化学平衡状态。
3.了解控制反应条件在生产生活和科学研究中的作用。
重点:化学平衡状态的特征和判断。
难点:化学平衡状态的特征和判断。
(1)在反应A(g)+3B(g)===2C(g)中,若以物质A表示该反应的化学反应速率为0.2 mol·L-1
·min-1,则以物质B表示此反应的化学反应速率为 mol·L-1·min-1。
(2)在2 L的密闭容器中,充入2 mol N 和3 mol H ,在一定条件下发生反应,3 s后测得N 的物质的量为
2 2 2
1.9 mol,则以H 的浓度变化表示的反应速率为 。
2
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在
最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s 时,容器中有 mol A,此时C的物
质的量浓度为 。
1、思考与交流:一个化学反应在实际进行时,反应物能否完全转变为生成物?阅读:P48 科学史话,从
这一材料中,你得到什么启示?
2、思考与交流:水的生成(H + O )与电解,二次电池的放电与充电,CO 和HO在生物体中通过光合
2 2 2 2
作用合成糖与糖在人体内氧化生成CO 和HO,它们是否属于“可逆反应”?谈谈你的见解。
2 2
3、交流与讨论:分析合成氨反应中正、逆反应的反应速率、反应物和生成物的浓度随时间的变化情况。4、【例题】 可逆反应2NO 2NO+O 在体积不变的密闭容器中反应,达到平衡状态的标志是( )
2 2
①单位时间内生成n mol O 的同时生成2n mol NO
2
②单位时间内生成n mol O 的同时生成2n mol NO
2 2
③用NO 、NO、O 的物质的量浓度变化表示的反应速率之比为2∶2∶1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
A.①④ B.②④
C.①③④D.②③⑤
5、对于在一定条件下的可逆反应: N+3H 2NH
2 2 3
判断以下哪些叙述说明V =V ?
(正) (逆)
(1)单位时间内,消耗1molN ,同时生成1molN
2 2
(2)单位时间内,消耗3molH ,同时消耗2molNH
2 3
(3)单位时间内,生成1molN ,同时有2molNH 生成
2 3
(4)单位时间内,消耗1molN2,同时有2molNH3生成
6、反应mA(g)+nB (g) pC(g) ,达到平衡的标志为:
①、A的消耗速率与A的生成速率
—————
②、A的消耗速率与C的 速率之比等于
。
③、B的生成速率与C的 速率之比等于
。
④、A的生成速率与B的 速率之比等于
。
7、思考与交流现在,假设你是一名工程师,你要提高你工厂煤的燃烧效率,你认为应该从哪些方面进行
分析?• 煤的状态与燃烧的速率有何关系?与煤的充分燃烧有何关系?
• 空气的用量对煤的充分燃烧有什么影响?原因是什么?
• 应选用什么样的炉膛材料?
• 如何充分利用煤燃烧后的废气中的热量?
1、某可逆反应达到平衡状态时,下列说法正确的是( )
①正反应和逆反应同时进行,两者的速率完全相等
②反应物和生成物同时存在,两者的浓度相同
③混合物的组成比例不会随时间而改变
A.① B.①③ C.② D.①②③
2、在体积固定的容器中,对于反应A(g)+B(g) 3C(g)(正反应为放热反应),下列叙述为平衡状态标志
的是( )
①单位时间内A、B生成C的分子数与分解C的分子数相等
②外界条件不变时,A、B、C浓度不随时间变化
③体系温度不再变化
④体系的压强不再变化
⑤体系的分子总数不再变化
A.①② B.①②③ C.①②③④ D.①②③④⑤
3、将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧,这样处理的目的是( )
①使煤充分燃烧,提高煤的利用率 ②减少SO 的产生,避免造成“酸雨” ③减少有毒的CO产生,避
2
免污染空气 ④减少CO 的产生,避免“温室效应”
2
A.①②③ B.②③④
C.①③④ D.①②③④
4、下列措施可以提高燃料燃烧效率的是( )
①提高燃料的着火点 ②降低燃料的着火点 ③将固体燃料粉碎 ④将液体燃料雾化处理
⑤将煤进行气化处理 ⑥通入适当过量的空气
A.①③④⑤ B.②③⑤⑥C.③④⑤⑥ D.①②③④
5、向一密闭容器中放入1 mol X,进行可逆反应2X(g) 3Y(g),反应过程中的反应速率(v)与时间(t)的关
系曲线如图所示,下列叙述正确的是( )
A.t 时,只有正反应
1
B.t~t 时,反应不再发生
2 3
C.t 时,容器内有1.5 mol Y
2
D.t~t 时,X、Y的物质的量均没有发生变化
2 3
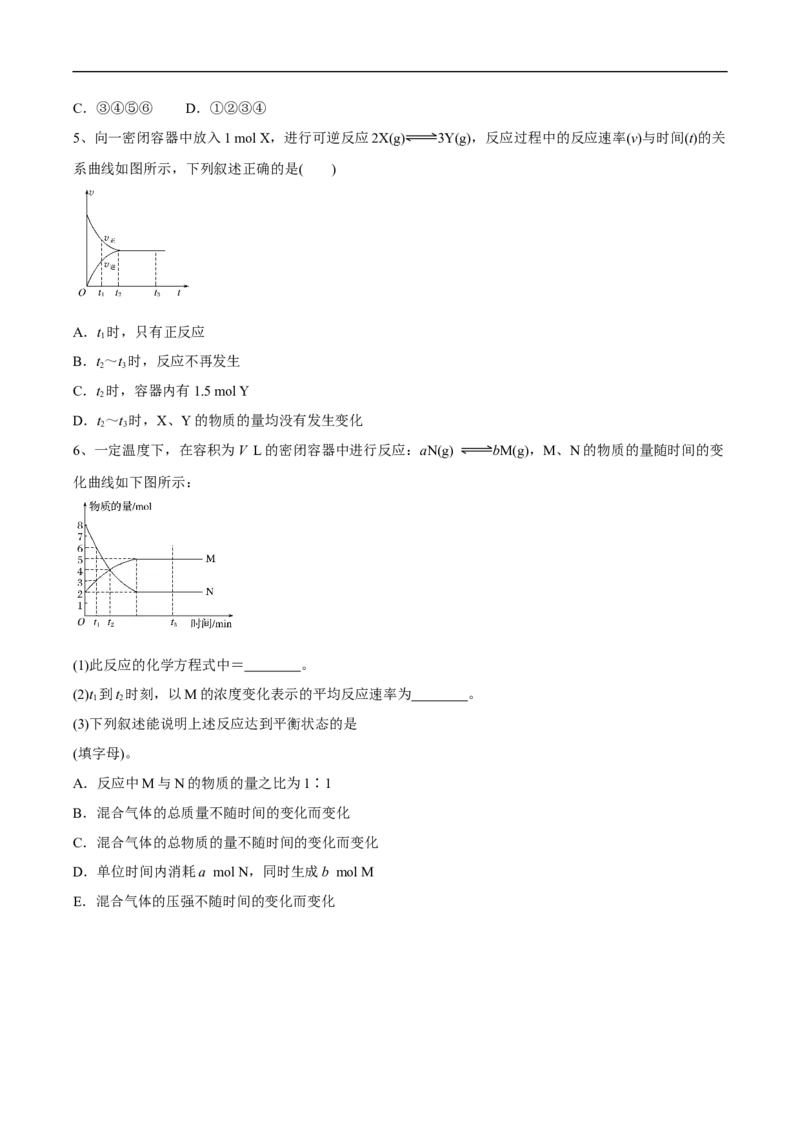
6、一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变
化曲线如下图所示:
(1)此反应的化学方程式中= 。
(2)t 到t 时刻,以M的浓度变化表示的平均反应速率为 。
1 2
(3)下列叙述能说明上述反应达到平衡状态的是
(填字母)。
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化