文档内容
第七章 有机化合物
第二节 乙烯与有机高分子材料
第 1 课时 乙烯
1、会写乙烯的分子式、结构式、结构简式、电子式。
2、知道乙烯能够发生氧化反应、加成反应、聚合反应。
3、理解加成反应的概念。
重点:从宏观和微观两个方面研究乙烯的结构如何决定其性质;
难点:乙烯加成反应、加聚反应的基本规律。
烷烃的结构和性质。
一、乙烯的物理性质
乙烯是一种 ,稍有气味的 ,密度比空气略 ,难溶于 。
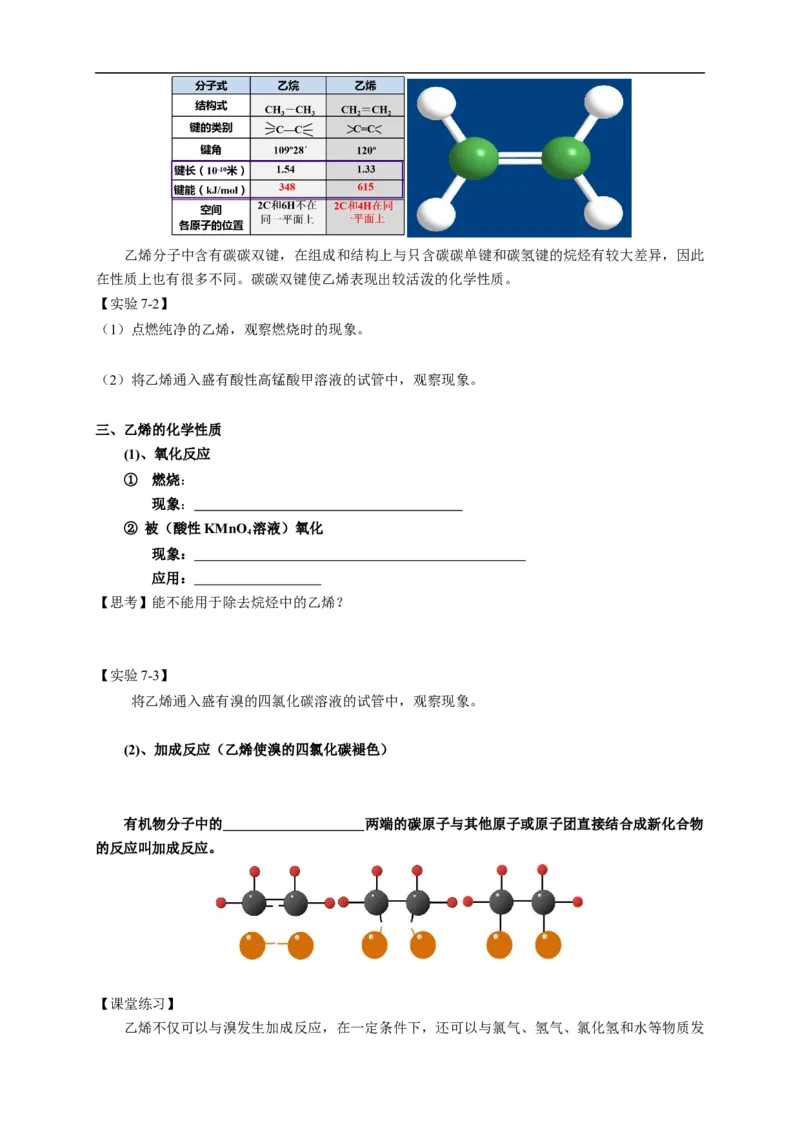
二、乙烯的结构
分子式 电子式
结构式 结构简式
6个原子 ,键角 , 型分子,分子中有 ,碳原子的价键 被氢原子“饱
和”。
【思考与交流】乙烯分子中含有碳碳双键,在组成和结构上与只含碳碳单键和碳氢键的烷烃有较大差异,因此
在性质上也有很多不同。碳碳双键使乙烯表现出较活泼的化学性质。
【实验7-2】
(1)点燃纯净的乙烯,观察燃烧时的现象。
(2)将乙烯通入盛有酸性高锰酸甲溶液的试管中,观察现象。
三、乙烯的化学性质
(1)、氧化反应
① 燃烧:
现象:
② 被(酸性KMnO 溶液)氧化
4
现象:
应用:
【思考】能不能用于除去烷烃中的乙烯?
【实验7-3】
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
(2)、加成反应(乙烯使溴的四氯化碳褪色)
有机物分子中的 两端的碳原子与其他原子或原子团直接结合成新化合物
的反应叫加成反应。
【课堂练习】
乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应。
(3)、聚合反应
【归纳总结】
乙烷与乙烯的分子结构和化学性质对比
分子式 C H C H
2 6 2 4
分
结构式
子
结 碳碳键类别
构 分子内原子
的相对位置
燃烧
化
学
特征反应
性
与酸性高锰
质
酸钾溶液
【课堂练习】
1.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )
A.澄清石灰水,浓硫酸
B.溴水,浓硫酸
C.酸性高锰酸钾溶液,浓硫酸
D.浓硫酸,酸性高锰酸钾溶液
2. 下列说法错误的是( )
A.无论是乙烯与Br 的加成反应,还是乙烯使酸性KMnO 溶液褪色,都与分子内含有的碳碳双键有
2 4
关
B.溴的四氯化碳溶液和酸性KMnO 溶液都可以鉴别乙烯和甲烷
4
C.相同质量的乙烯和甲烷完全燃烧后生成水的质量相同
D.乙烯的化学性质比乙烷的化学性质活泼
3.长途运输水果时,常常将浸泡有高锰酸钾溶液的硅土放置在盛放水果的容器中,其目的是
( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
4.能证明乙烯分子中含有一个碳碳双键的事实是( )
A.乙烯分子中碳、氢原子的个数比为1∶2B.乙烯完全燃烧生成的CO 和HO的物质的量相等
2 2
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO 溶液褪色
4
5.含有碳碳双键的有机物很多,其性质和乙烯相似,写出下列要求的方程式。
(1)丙烯与溴水反应:_______________________________。
(2)丙烯在一定条件下加聚生成聚丙烯:_______________________________。