文档内容
第七章 有机化合物
第三节 乙醇和乙酸
第2课时 乙酸
1、知道乙酸的组成、结构、官能团、物理性质及用途。
2、会运用乙酸的结构分析其化学性质。
3、掌握制备乙酸乙酯的实验
重点:乙酸的结构和性质;
难点:乙酸的酯化反应。
乙醇的结构和性质。
一、乙酸的物理性质
食醋含醋酸 。
(1) 乙酸俗称 ,是一种有 的无色液体,易溶于 。
(2) 熔点:16.6 ℃,温度低于熔点时,乙酸凝结成晶体,所以纯净的乙酸又称 。
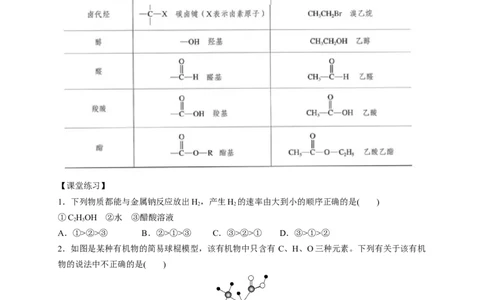
二、乙酸的结构官能团: ,-COOH
三、乙酸的性质
1、酸性 乙酸是一元弱酸,具有酸的通性。
【课堂练习】
1、写出乙酸与下列物质反应的离子方程式:
①Na: 。
②NaOH: 。
③NaO: 。
2
④NaCO: 。
2 3
【思考与讨论】
1、用食醋浸泡有水垢(主要成分是CaCO )的暖水瓶或水壶,可以清除其中的水垢。这是利用了
3
醋酸的什么性质?请写出相应的化学方程式?
2、如何比较乙酸与碳酸、盐酸的酸性强弱?请查阅资料,与同学们讨论,根据生活经验设计
实验方案。
【实验探究】
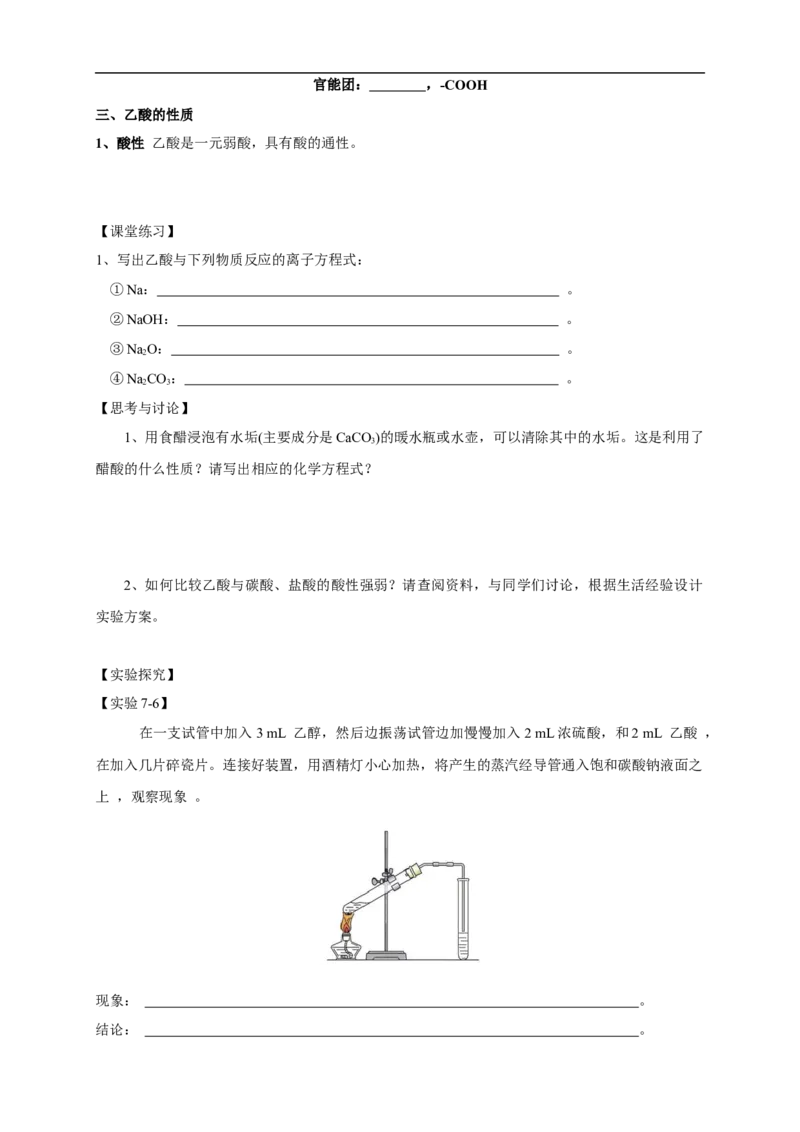
【实验7-6】
在一支试管中加入3 mL 乙醇,然后边振荡试管边加慢慢加入2 mL浓硫酸,和2 mL 乙酸 ,
在加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸汽经导管通入饱和碳酸钠液面之
上 ,观察现象 。
现象: 。
结论: 。2、酯化反应
化学方程式: 。
酯化反应(取代反应):酸和醇起作用,生成 和 的反应。
酯化反应是 ,乙酸乙酯会与水反应生成 和 。
酯基: 。
注意事项:
用酒精灯加热的目的:加快反应速率;将生成的乙酸乙酯及时
酒精灯
蒸出,有利于乙酸乙酯的生成
仪器
试管 作反应器的大试管倾斜45°角的目的:增大受热面积
导气管 导气管末端的位置:不能伸入液面以下,防止倒吸
反应物
试剂 催化剂
吸收剂
操作
【思考与交流】
(1) 导管末端为什么不能插入饱和NaCO 溶液中?
2 3
(2) 浓硫酸的作用是什么?
(3) 饱和NaCO 溶液的作用是什么?
2 3
(4) 碎瓷片的作用是什么?
(5) 酯的分离方法是什么?
(6) 酯化反应可能哪些脱水方式?如何确定?
四、官能团与有机化合物的分类【课堂练习】
1.下列物质都能与金属钠反应放出H,产生H 的速率由大到小的顺序正确的是( )
2 2
①C HOH ②水 ③醋酸溶液
2 5
A.①>②>③ B.②>①>③ C.③>②>① D.③>①>②
2.如图是某种有机物的简易球棍模型,该有机物中只含有 C、H、O三种元素。下列有关于该有机
物的说法中不正确的是( )
A.分子式是C HO B.不能和NaOH溶液反应
3 6 2
C.能发生酯化反应 D.能使紫色石蕊溶液变红
3.将1 mol乙醇(其中的羟基氧用18O标记)在浓硫酸存在并加热下与足量乙酸充分反应。下列叙述
不正确的是( )
A.生成的水分子中一定含有18O
B.生成的乙酸乙酯中含有18O
C.可能生成45 g乙酸乙酯
D.不可能生成相对分子质量为88的乙酸乙酯4.下列物质和乙酸为同系物的是( )
A. B.CH =CH—COOH
2
C. D.
5.某有机物的结构简式如图所示:
(1)1 mol该有机物和过量的金属钠反应最多可以生成________H。
2
(2)该物质最多消耗Na、NaOH、NaHCO 的物质的量之比为________。
3
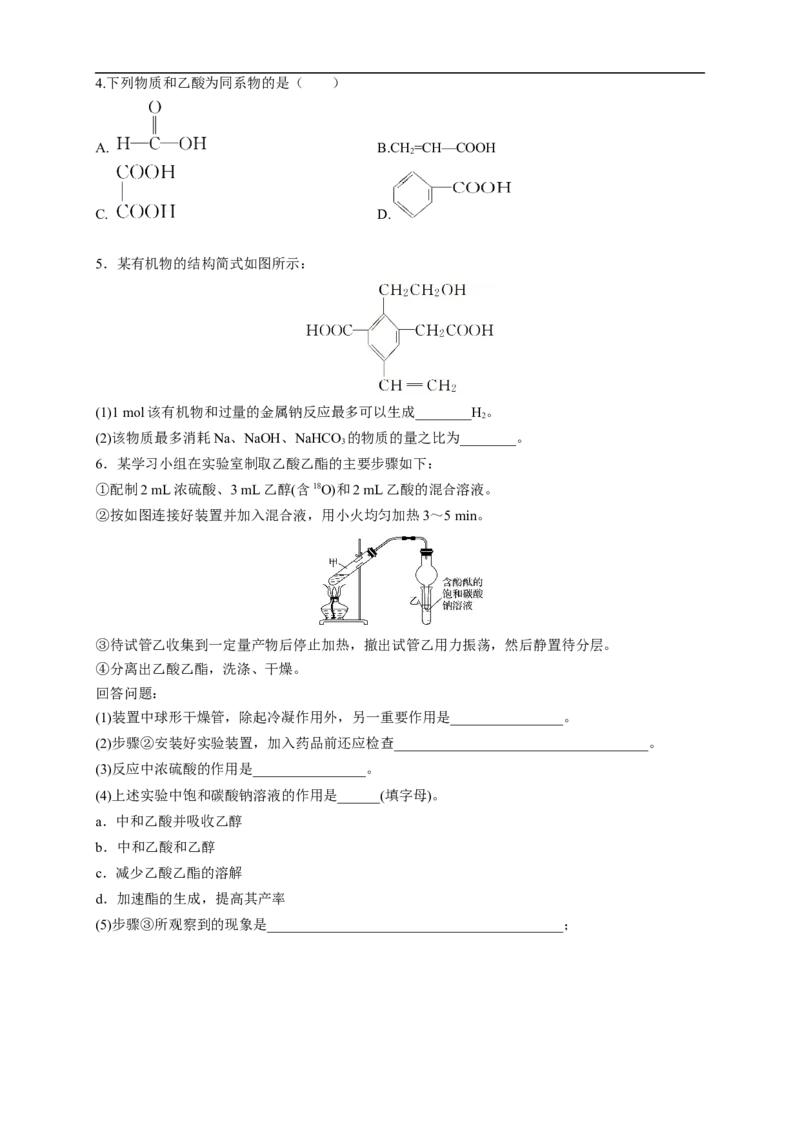
6.某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按如图连接好装置并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
回答问题:
(1)装置中球形干燥管,除起冷凝作用外,另一重要作用是________________。
(2)步骤②安装好实验装置,加入药品前还应检查____________________________________。
(3)反应中浓硫酸的作用是________________。
(4)上述实验中饱和碳酸钠溶液的作用是______(填字母)。
a.中和乙酸并吸收乙醇
b.中和乙酸和乙醇
c.减少乙酸乙酯的溶解
d.加速酯的生成,提高其产率
(5)步骤③所观察到的现象是__________________________________________;