文档内容
第七章 有机化合物
第三节 乙醇和乙酸
第 1 课时 乙醇
乙醇与乙酸是人类较早发现、制备和应用的有机化合物,在生活和生产中的用途广泛,学生
十分熟悉:二者也是醇类和羧酸这两类经的含氧衍生物的典型代表。教材在第二节介绍了乙烯。反
应产物中涉及卤代烃,学生已经初步接触了含有官能团的有机物。本节在此基础上,结合乙醇的实
例给出官能团的概念,让学生从结构的角度理解决定有机物分类与化学性质的特征基团,并从官能
团转化和物质类别变化的角度认识有机物之间的转化,初步认识有机合成。同时,教材在本节最后
结合官能团的作用,从结构和性质的角度对常见有机物进行分类,通过“方法导引”栏目初步总结
认识有机物的一般思路,使学生掌握方法,进一步强化有机物的认知模型。
本节教材从化学史实和生活实例引入乙醇,学生容易就此根据经验总结出乙醇的物理性质。
然后再通过分析分子结构引入取代基和烃的衍生物概念,指出衍生物的分子中含有官能团,与母体
化合物烃的结构不同,因此性质也有所区别,深化学生对“结构决定性质”这一化学基本观念的理
解。教材编入乙醇与钠反应的实验,并分析乙醇与乙烷具有不同化学性质的原因,由此引入官能团
的概念。这样既介绍了代表性物质的化学性质,又让学生认识到官能团对有机物化学性质的决定作
用。
教材中乙醇的氧化反应重点在于催化氧化,其中包含了生物体内酶催化的氧化反应,以及乙
醇与高锤酸钾等氧化剂的反应,由此打通了从乙烯到乙醇、乙醛、乙酸的物质转化链。教材在本节
和本章最后编入相关习题和“整理与提升”,帮助学生分析这一转化过程中的官能团和物质类别变
化,深化其对有机物性质与转化关系的认识。
【学习目标】
1、知道乙醇的组成、结构、官能团、物理性质及用途。
2、了解烃的衍生物的概念及官能团与性质的关系,认识羟基与其性质的关系。
3、会运用乙醇的结构分析其化学性质。
【核心素养】1、微观探析:从官能团的角度认识乙醇的组成、结构、性质和变化,形成“结构决定性质”
的观念。
2、科学探究:设计实验探究乙醇的结构与性质。
重点:乙醇的结构和性质;
难点:乙醇的催化氧化。
球棍模型,无水乙醇,金属钠,铜丝等。
【引入】
早在几千年前,人类就掌握了发酵法酿酒的技术。各种酒类都含有浓度不等的乙醇。
【过渡】请同学们说一些含有酒的诗句?
【学生活动】借问酒家何处有,牧童遥指杏花村(杜甫)
花间一壶酒,独酌无相亲。
举杯邀明月,对影成三人 (李白)
劝君更尽一杯酒,西出阳关无故人 (李白)
【讲解】
一、乙醇的物理性质
乙醇,俗称酒精。无色,有特殊香味的液体,密度比水小,易挥发,能溶解多种有机物和无机
物,能跟水以任意比例互溶。
二、乙醇的结构分子式:C HO
2 6
结构式:
结构简式:CH CH OH或CHOH
3 2 2 5
—OH (羟基)
【讲解】
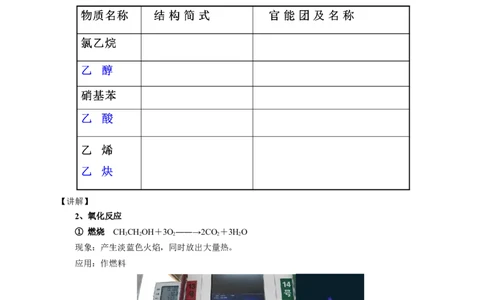
烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。如
CHCl、CHCHOH、CHCOOH等。
3 3 2 3
【实验探究】
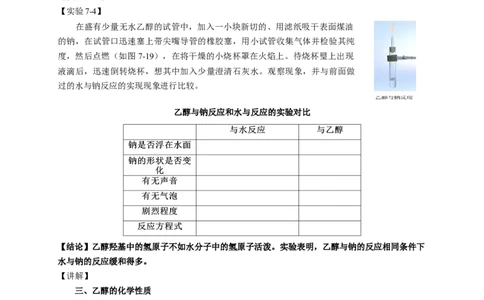
【实验7-4】
在盛有少量无水乙醇的试管中,加入一小块新切的、用滤纸吸干表面煤油
的钠,在试管口迅速塞上带尖嘴导管的橡胶塞,用小试管收集气体并检验其纯
度,然后点燃(如图7-19),在将干燥的小烧杯罩在火焰上。待烧杯璧上出现
液滴后,迅速倒转烧杯,想其中加入少量澄清石灰水。观察现象,并与前面做
过的水与钠反应的实现现象进行比较。
乙醇与钠反应和水与反应的实验对比
【结论】乙醇羟基中的氢原子不如水分子中的氢原子活泼。实验表明,乙醇与钠的反应相同条件下
水与钠的反应缓和得多。
【讲解】
三、乙醇的化学性质
1、与活泼金属(如Na)反应
根据与水和乙醇反应的剧烈程度得出:H—OH > C H—OH
2 5
由于羟基所连的原子或原子团不一样,从而导致羟基氢的活泼性不一样。H—OH > C H—
2 5
OH
水是弱电解质,乙醇为非电解质。
2CHCHOH+2Na―→2CHCHONa+H↑
3 2 3 2 2
【课堂练习】
1、关于乙醇结构与性质方面的说法中正确的是( )
A.乙醇结构中有—OH,所以乙醇溶解于水,可以电离出OH-B.乙醇能电离出H+,所以是电解质
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
【讲解】官能团和基团的概念
像这种决定有机化合物特性的原子或原子团叫做官能团。羟基是醇类物质的官能团,碳碳双键
和碳碳三键分别是烯烃和炔烃的官能团。
烃分子失去1个氢原子后所剩余的部分叫做烃基,可以用一 R来表示。如一CH 叫甲基,一
3
CHCH ,叫乙基。烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的。例如,乙醇分
2 3
子可以看成是由乙基和羟基组成的:CHCH-OH。
3 2
【课堂练习】
【讲解】
2、氧化反应
① 燃烧 CHCHOH+3O――→2CO+3HO
3 2 2 2 2
现象:产生淡蓝色火焰,同时放出大量热。
应用:作燃料
② 催化氧化
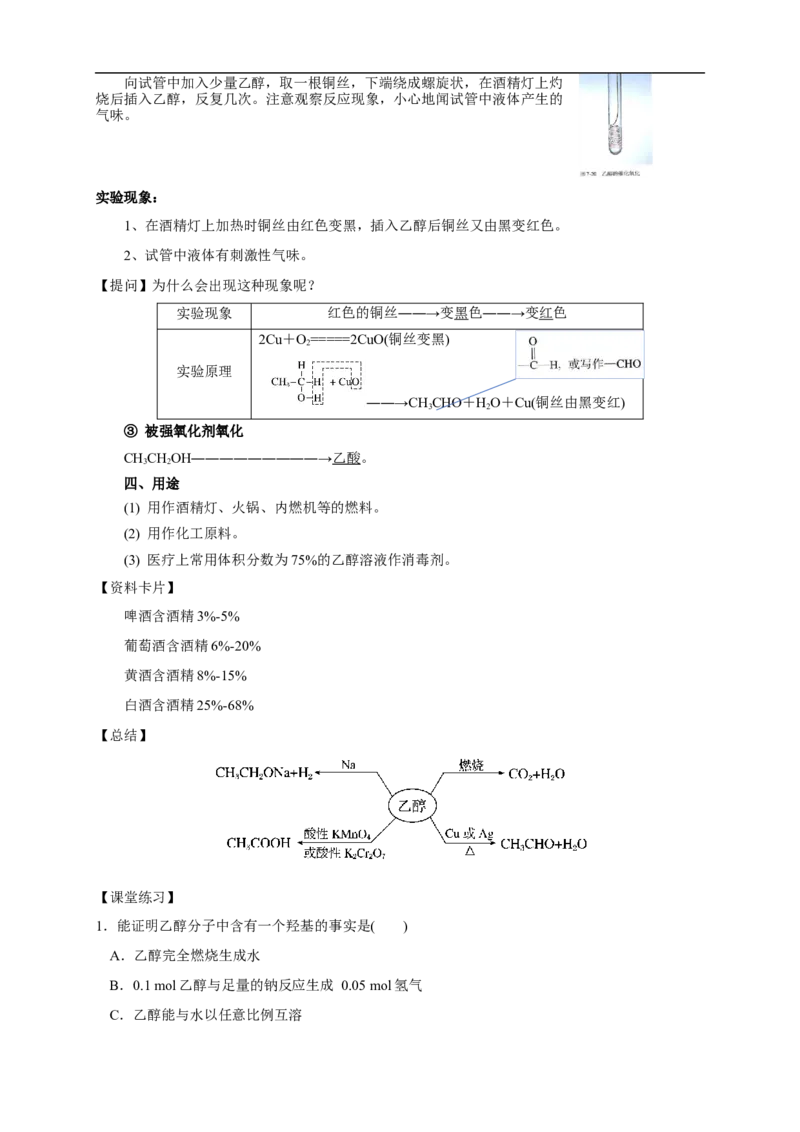
【实验7-5】向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼
烧后插入乙醇,反复几次。注意观察反应现象,小心地闻试管中液体产生的
气味。
实验现象:
1、在酒精灯上加热时铜丝由红色变黑,插入乙醇后铜丝又由黑变红色。
2、试管中液体有刺激性气味。
【提问】为什么会出现这种现象呢?
实验现象 红色的铜丝――→变黑色――→变红色
2Cu+O=====2CuO(铜丝变黑)
2
实验原理
――→CHCHO+HO+Cu(铜丝由黑变红)
3 2
③ 被强氧化剂氧化
CHCHOH―――――――――→乙酸。
3 2
四、用途
(1) 用作酒精灯、火锅、内燃机等的燃料。
(2) 用作化工原料。
(3) 医疗上常用体积分数为75%的乙醇溶液作消毒剂。
【资料卡片】
啤酒含酒精3%-5%
葡萄酒含酒精6%-20%
黄酒含酒精8%-15%
白酒含酒精25%-68%
【总结】
【课堂练习】
1.能证明乙醇分子中含有一个羟基的事实是( )
A.乙醇完全燃烧生成水
B.0.1 mol乙醇与足量的钠反应生成 0.05 mol氢气
C.乙醇能与水以任意比例互溶D.乙醇容易挥发
2. 乙醇分子中不同的化学键如下图,下列关于乙醇在各种反应中断裂键的说法不正确的是( )
A.乙醇和钠反应,键①断裂
B.在Ag催化下和O 反应,键①③断裂
2
C.在Cu催化下和O 反应,键④⑤不可能断裂
2
D.乙醇是电解质,在水中键①断裂能电离出氢离子
3. 下列有机物中,不属于烃的衍生物的是( )
4. 将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是
( )
A.硝酸 B.无水乙醇 C.石灰水 D.盐酸
5. 某物质的分子式是C H O,它能被氧化生成具有相同碳原子数的醛,则该物质的结构可能有( )
4 10
A.2种 B.3种 C.4种 D.5种
教学设计的重点是让学生在探究乙醇的化学性质(与钠的反应、催化氧化反应)的过程中,
认识有机化合物中羟基的特点,帮助学生建立有机化合物中官能团决定其化学性质的学科思想。主
要教学策略一是在教学设计上层层递进,逐渐深人,先感知,再深入,后运用;二是充分发挥学生
在课堂学习活动中的主体作用,创设环境给予学生任务驱动,学生小组合作实验探究,全班交流讨
论,激发学生学习的兴趣和解决问题的动力,最终达到促进全体学生素养发展的目标。