文档内容
1.2 反应热的计算(精练)
题组一 盖斯定律
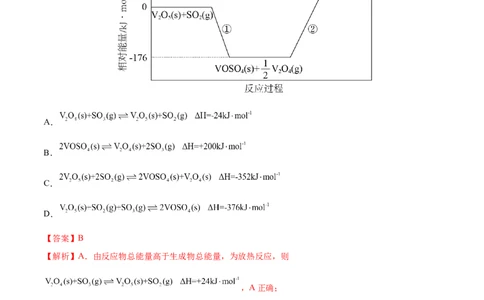
1.(2022·河南南阳·高二期末)硫酸工业中的钒催化剂参与反应的相对能量变化如图所示,下列热化学方
程式错误的是
A.
B.
C.
D.
【答案】B
【解析】A.由反应物总能量高于生成物总能量,为放热反应,则
,A正确;
B.途径2的∆H=24-(-176)=200kJ/mol, ,B错误;
C.途径1的反应物总能量大于生成物总能量,为放热反应,2molV O 反应放出能量为2×176=352kJ,则
2 5
,C正确;
D.根据盖斯定律,由反应 加上可得
,则
,D正确;故选:B。
2.(2022·广西·柳州市第三中学高二期中)已知298K时:C(s)+ O(g)=CO(g) H=−110.5 mol∙L−1;
2 1
△
C(s)+O(g)=CO (g) H=−393.5 mol∙L−1;则C(s)+CO(g)=2CO(g)的△H为
2 2 2 2
A.+283 mol∙L−1 △B.+172.5 mol∙L−1 C.−172.5 mol∙L−1 D.−504 mol∙L−1
【答案】B
【解析】根据题意,根据盖斯定律第一个方程式的2倍减去第二个方程式得到C(s)+CO(g)=2CO(g)的
2
△H=−110.5 mol∙L−1×2−(−393.5 mol∙L−1)= +172.5 mol∙L−1,故B符合题意。
综上所述,答案为B。
3.已知下列热化学方程式:
HO(g)=H O(l) H=QkJ·mol-1;
2 2 1
C
2
H
5
OH(g)=C
2
H△5 OH(l) H=Q
2
kJ·mol-1;
C
2
H
5
OH(g)+3O
2
(g)=2CO△2 (g)+3H
2
O(g) H=Q
3
kJ·mol-1
。
若46g液体酒精完全燃烧,最后恢复到△室温,放出的热量为(单位:kJ)
A.3Q+Q +Q B.-(3Q +Q +Q ) C.-3Q +Q -Q D.3Q-Q +Q
1 2 3 1 2 3 1 2 3 1 2 3
【答案】C
【解析】液体酒精完全燃烧的方程式为C HOH(l)+3O (g)=2CO (g)+3HO(l),记①HO(g)=H O(l)
2 5 2 2 2 2 2
ΔH=QkJ·mol-1;②C HOH(g)=C HOH(l) ΔH=QkJ·mol-1;③C HOH(g)+3O (g)=2CO (g)+3HO(g)
1 2 5 2 5 2 2 5 2 2 2
ΔH=QkJ·mol-1 则根据盖斯定律,由3×①-②+③可得C HOH(l)+3O (g)=2CO (g)+3HO(l),则C HOH(l)
3 , 2 5 2 2 2 2 5
+3O (g)=2CO (g)+3HO(l)的ΔH=3×ΔH -ΔH +ΔH =(3Q -Q +Q )kJ/mol,因此46g液体酒精(1mol)完全燃
2 2 2 1 2 3 1 2 3
烧,最后恢复到室温,放出的热量为-(3Q -Q +Q )=-3Q+Q -Q ,故选C;
1 2 3 1 2 3
答案选C。
4.已知下列热化学方程式:
①
②③
④
现有由2mol上述四种烃中的两种组成的气体混合物,经充分燃烧后放出2988kJ热量,则下列组合中不可
能的是
A. 和 B. 和 C. 和 D. 和
【答案】B
【解析】题给四种烃的燃烧热分别为 、 、 、 。
2mol混合气体完全燃烧放出的热量为2988kJ,所以平均燃烧热为 。根据平均值的意义可知混
合物中两种烃的燃烧热应该分别在该数值的两侧,即一个大于 、一个小于 。所
以上述选项中,只有B项符合题意。答案选B。
5.(2022·云南保山·高二期中)完成下列问题。
(1)常温下,0.1molCl 与焦炭、TiO 完全反应,生成一种还原性气体和一种易水解成TiO·xH O的液态化合
2 2 2 2
物,放热4.28kJ,该反应的热化学方程式为_______。
(2)联氨(又称肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。已知:
2 4
①2O(g)+N(g)=NO(1) H
2 2 2 4 1
②N
2
(g)+2H
2
(g)=N
2
H
4
(1) △H
2
③O
2
(g)+2H
2
(g)=2H
2
O(g) △H
3
④2N
2
H
4
(l)+N
2
O
4
(l)=3N
2
(g)△+4H
2
O(g) H
4
=-1048.9kJ/mol
上述反应热效应之间的关系式为△H
4
=△_______,联氨和N
2
O
4
可作为火箭推进剂的主要原因为_______。
(3)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
①与汽油相比,氢气作为燃料的优点是_______(至少答出两点)。
②利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
【答案】(1)2Cl (g)+TiO (s)+2C(s)=TiCl (l)+2CO(g) H=-85.6kJ/mol
2 2 4
(2) 2 H
3
-2 H
2
- H
1
反应放热量大、产生大量气△体
(3) 污△染小;△可再△生;来源广;资源丰富;燃烧热值高 光能转化为化学能
【解析】(1)0.1molCl 与焦炭、TiO 完全反应,生成一种还原性气体和一种易水解成 的液态化合
2 2
物,放热4.28kJ,配平方程式,可知2molCl 反应放热85.6kJ,由此可得该反应的热化学方程式为
2;
(2)根据盖斯定律,反应热效应之间的关系式为△H=2 H-2 H- H 联氨有强还原性, 有强氧化性,
4 3 2 1.
△ △ △
两者在一起易发生自发的氧化还原反应,反应放热量大、产生大量气体,所以联氨和 可作为火箭推
进剂;
(3)①与汽油相比,氢气作为燃料的优点有污染小;来源广;资源丰富;燃烧热值高等。
②利用太阳能直接分解水制氢气,是将光能转化为化学能。
6.氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH(g)+HO(g)=CO(g)+3H (g) ΔH=206.2 kJ·mol-1①
4 2 2
CH(g)+CO (g)=2CO(g)+2H(g) ΔH=247.4 kJ·mol-1②
4 2 2
又知CH 的燃烧热为890.3 kJ·mol-1。
4
(1)利用上述已知条件写出表示CH 燃烧热的热化学方程式:_______。
4
(2)以甲烷为原料制取氢气是工业上常用的制氢方法。CH(g)与HO(g)反应生成CO(g)和H(g)的热化学方
4 2 2 2
程式为_______。
(3)若在相同温度下,1 mol H O按下列两种途径转化为氢原子与氧原子。
2
则ΔH、ΔH、ΔH 三者之间的关系是_______。
1 2 3
【答案】(1)CH (g)+2O(g)=CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1
4 2 2 2
(2)CH (g)+2HO(g)=CO(g)+4H(g) ΔH=+165.0 kJ·mol-1
4 2 2 2
(3)ΔH=ΔH+ΔH
3 1 2
【解析】(1)燃烧热是在101KPa时,1mol纯物质完全燃烧生成指定产物时放出的热量,表示某物质燃烧
热的热化学方程式中,可燃物的系数为1。1mol甲烷完全燃烧生成二氧化碳气体和液态水,放出890.3kJ
的热量,则表示甲烷燃烧热的热化学方程式为CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1。
4 2 2 2
(2)由盖斯定律,①×2-②即可得出CH(g)+2HO(g)=CO(g)+4H(g) ΔH=+206.2 kJ·mol-1×2-247.4
4 2 2 2
kJ·mol-1=+165.0 kJ·mol-1。
(3)盖斯定律的含义是化学反应的发生不管是一步完成还是分几步完成,其反应热是相同的。不管1mol
水直接分解为氢原子和氧原子,还是1mol水先分解为氢气和氧气,然后氢气和氧气再分别转化为氢原子
和氧原子,其反应热是相同的,所以ΔH=ΔH+ΔH。
3 1 2题组二 反应热的计算
1.回答下列问题
(1)甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水放出热量222.5kJ,则甲烷燃烧的热化
学方程式为___________。
(2)已知:2SO (g)+O(g)=2SO(g) ΔH=-xkJ·mol-1
2 2 3
2NO(g)+O(g)=2NO (g) ΔH=-ykJ·mol-1
2 2
则反应NO (g)+SO (g)=SO(g)+NO(g)的ΔH=___________kJ·mol-1。
2 2 3
(3)已知:2H(g)+O(g)=2HO(g) ΔH=-483.6kJ·mol-1,
2 2 2
查阅文献资料,化学键的键能如下表:
化学键 H—H键 N≡N键 N—H键
E/(kJ·mol-1) 436 946 391
①氨分解反应NH (g)= N(g)+ H(g)的活化能E =300kJ·mol-1,则合成氨反应 N(g)+ H(g)=NH (g)的
3 2 2 al 2 2 3
活化能E =___________kJ·mol-1。
a2
②氨气完全燃烧生成N(g)和气态水的热化学方程式为___________。
2
(4)研究氮氧化物与悬浮的大气中海盐粒子的相互作用时,涉及如下反应:
Ⅰ.2NO(g)+NaCl(s)=NaNO (s)+ClNO(g) ΔH<0
2 3 1
Ⅱ.2NO(g)+Cl(g)=2ClNO(g) ΔH<0
2 2
则反应4NO (g)+2NaCl(s)=2NaNO (s)+2NO(g)+Cl(g)的ΔH=___________(用ΔH、ΔH 表示);
2 3 2 1 2
【答案】(1)CH (g)+2O=CO (g)+2HO(l) ΔH=-890kJ/mol
4 2 2 2
(2)
(3) 254 4NH (g)+3O(g) 2N(g)+6HO(g) ΔH=-1266.8kJ/mol
3 2 2 2
(4)2ΔH 1 -ΔH 2 ⇌
【解析】(1)0.25mol甲烷完全燃烧生成液态水放出热量222.5kJ,则1mol甲烷完全燃烧生成液态水放出的
热量为 =890kJ/mol,则甲烷燃烧的热化学方程式CH(g)+2O=CO (g)+2HO(l) ΔH=-890kJ/mol;
4 2 2 2
(2)依次将所给的两个热化学方程式编号为①、②,根据盖斯定律 ×(②-①)得SO (g)+NO (g) SO (g)
2 2 3
⇌
+NO(g)的ΔH= kJ/mol;(3)①根据键能数据,可求出NH (g) N(g)+ H(g)的ΔH=3×391kJ/mol-( ×946kJ/mol+ ×436kJ/
3 2 2
⇌
mol)=46kJ/mol。NH (g) N(g)+ H(g)的活化能E =300kJ/mol,则其逆反应 N(g)+ H(g) NH (g)的
3 2 2 a1 2 2 3
⇌ ⇌
活化能E =E -ΔH=300kJ/mol-46kJ/mol=254kJ/mol;
a2 a1
②把反应NH (g) N(g)+ H(g)的系数扩大4倍,其ΔH=+46kJ/mol×4=+184kJ/mol,把反应2H(g)
3 2 2 2
⇌
+O (g)=2HO(g)的系数扩大3倍,其ΔH=-483.6kJ./mol×3=-1450.8kJ/mol,把两反应相加,得总反应:
2 2
4NH (g)+3O(g) 2N(g)+6HO(g),其ΔH=+184kJ/mol-1405.8kJ/mol=-1266.8kJ/mol;
3 2 2 2
(4)根据盖斯定律⇌,Ⅰ×2-Ⅱ得:4NO
2
(g)+2NaCl(s)=2NaNO
3
(s)+2NO(g)+Cl
2
(g),ΔH=2ΔH
1
-ΔH
2
。
2.回答下列问题:
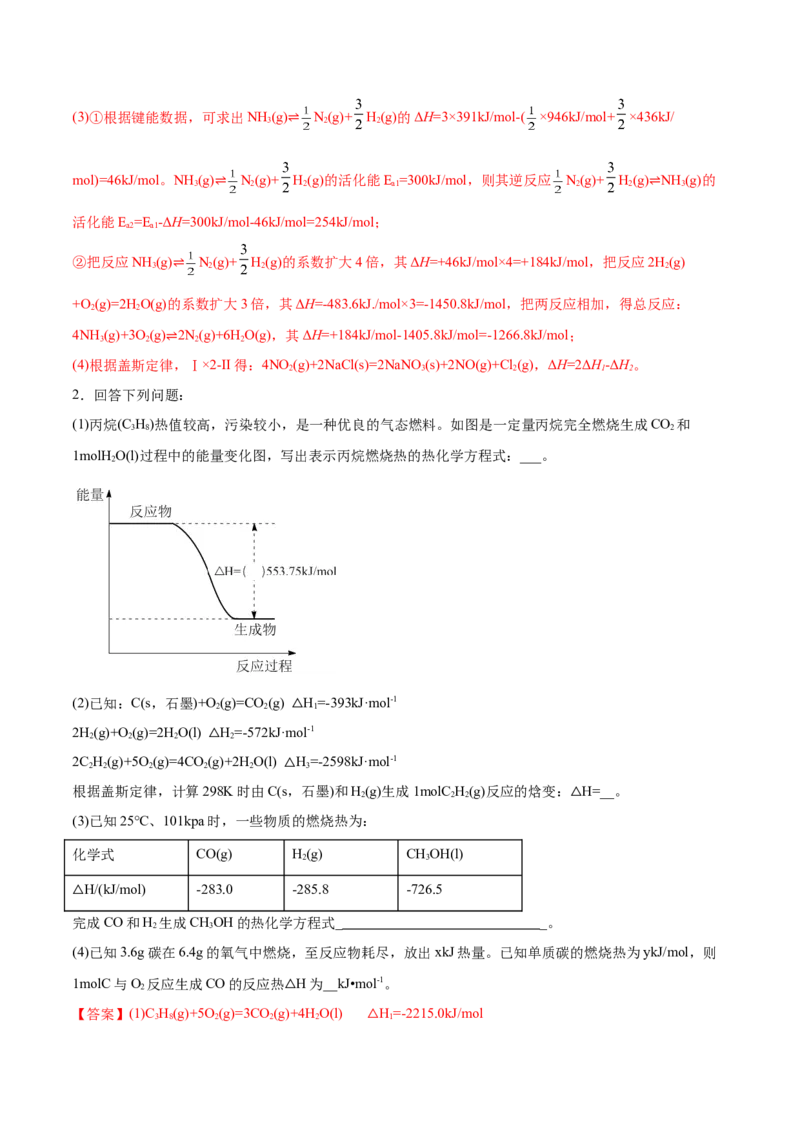
(1)丙烷(C H)热值较高,污染较小,是一种优良的气态燃料。如图是一定量丙烷完全燃烧生成CO 和
3 8 2
1molH O(l)过程中的能量变化图,写出表示丙烷燃烧热的热化学方程式:___。
2
(2)已知:C(s,石墨)+O (g)=CO (g) H=-393kJ·mol-1
2 2 1
2H
2
(g)+O
2
(g)=2H
2
O(l) H
2
=-572kJ·m△ol-1
2C
2
H
2
(g)+5O
2
(g)=4CO
2
(△g)+2H
2
O(l) H
3
=-2598kJ·mol-1
根据盖斯定律,计算298K时由C(s△,石墨)和H
2
(g)生成1molC
2
H
2
(g)反应的焓变: H=__。
(3)已知25℃、101kpa时,一些物质的燃烧热为: △
化学式 CO(g) H(g) CHOH(l)
2 3
H/(kJ/mol) -283.0 -285.8 -726.5
△完成CO和H 生成CHOH的热化学方程式_ _。
2 3
(4)已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,放出xkJ热量。已知单质碳的燃烧热为ykJ/mol,则
1molC与O 反应生成CO的反应热 H为__kJ•mol-1。
2
【答案】(1)C
3
H
8
(g)+5O
2
(g)=3CO
2
(g△)+4H
2
O(l) H
1
=-2215.0kJ/mol
△(2) H=227kJ/mol
(3)△CO(g)+2H
2
(g)=CH
3
OH(l) H=-128.1kJ•mol-1
(4)-(5x-0.5y) △
【解析】(1)由图可知,反应物总能量大于生成物总能量,该反应为放热反应;一定量丙烷完全燃烧生成
CO 和1molH O(l),放出热量为553.75kJ,所以1molC H(g)完全燃烧,生成4mol HO(l)时,放出的热量为
2 2 3 8 2
4×553.75kJ=2215.0kJ,表示丙烷燃烧热的热化学方程式:C H(g)+5O(g)=3CO (g)+4HO(l)
3 8 2 2 2
H=-2215.0kJ/mol;
1
△(2)①C(s,石墨)+O
2
(g)=CO
2
(g) H
1
=-393kJ·mol-1
②2H
2
(g)+O
2
(g)=2H
2
O(l) H
2
=-5△72kJ·mol-1
③2C
2
H
2
(g)+5O
2
(g)=4CO
2
(△g)+2H
2
O(l) H
3
=-2598kJ·mol-1
△
根据盖斯定律,①×2+②× -③× 可得:2C(s,石墨)+H (g)= C H(g) H=2 H+ H-
2 2 2 1 2
△ △ △
H=2×(-393)+ ×(-572)- ×(-2598)= 227kJ/mol;
3
△
(3)一氧化碳燃烧的热化学方程式:①CO(g)+ O(g)=CO (g) H=-283.0kJ·mol-1
2 2 1
△
氢气燃烧的热化学方程式:②2H(g)+O(g)=2HO(l) H=-571.6kJ·mol-1
2 2 2 2
△
甲醇燃烧的热化学方程式:③CHOH(l) + O(g)=CO (g)+2HO(l) H=-726.5kJ·mol-1
3 2 2 2 3
△
根据盖斯定律:①+②-③可得:CO(g)+2H(g)=CH OH(l) H=-283.0+(-571.6)-( -726.5)=-128.1kJ•mol-1;
2 3
△
(4)3.6g碳的物质的量为 =0.3mol,6.4g氧气的物质的量为 =0.2mol;根据氧气不足:
2C+O 2CO,氧气足量:C+O CO 分析,n(C):n(O )=3:2,介于2:1与1:1之间,上述反应都发生;
2 2 2 2
设生成CO为xmol,CO 为ymol;根据碳元素守恒:x+y=0.3,根据氧元素守恒:x+2y=0.2×2,联立方程解
2
得x=0.2mol,y=0.1mol;单质碳的燃烧热为ykJ/mol,所以生成0.1molCO 放出热量为0.1ykJ,生成
2
0.2molCO放出的热量为x kJ-0.1ykJ,由于碳燃烧为放热反应,所以△H的符号为“-”,故1molC与氧气反
应生成CO的反应热△H=- =-(5x-0.5y) kJ·mol-1。
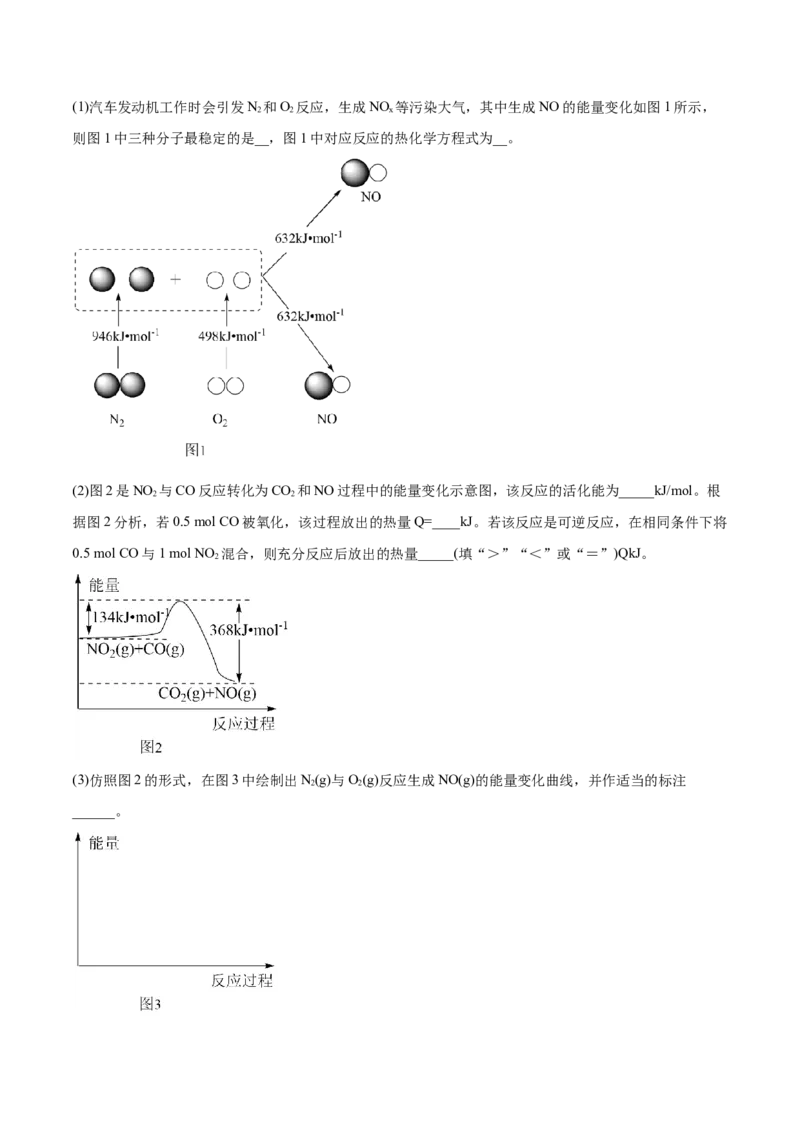
3.回答下列问题:(1)汽车发动机工作时会引发N 和O 反应,生成NO 等污染大气,其中生成NO的能量变化如图1所示,
2 2 x
则图1中三种分子最稳定的是__,图1中对应反应的热化学方程式为__。
(2)图2是NO 与CO反应转化为CO 和NO过程中的能量变化示意图,该反应的活化能为_____kJ/mol。根
2 2
据图2分析,若0.5 mol CO被氧化,该过程放出的热量Q=____kJ。若该反应是可逆反应,在相同条件下将
0.5 mol CO与1 mol NO 混合,则充分反应后放出的热量_____(填“>”“<”或“=”)QkJ。
2
(3)仿照图2的形式,在图3中绘制出N(g)与O(g)反应生成NO(g)的能量变化曲线,并作适当的标注
2 2
______。(4)FeSO 可转化为FeCO,FeCO 在空气中加热反应可制得铁系氧化物材料。已知25℃,101kPa时:
4 3 3
4Fe(s)+3O (g)=2Fe O(s) ΔH=-1648 kJ/mol
2 2 3
C(s)+O(g)=CO (g) ΔH=-393 kJ/mol
2 2
2Fe(s)+2C(s)+3O (g)=2FeCO (s) ΔH=-1480 kJ/mol
2 3
则,4FeCO(s)+O(g)=2Fe O(s)+4CO(g) ΔH=__。
3 2 2 3 2
【答案】(1) N N(g)+O(g)=2NO(g) H=+180 kJ/mol
2 2 2
(2) 134 117 < △
(3)
(4)-260 kJ/mol
【解析】(1)化学键的键能越大,断裂该化学键变为气态单个原子需吸收能量就越高,含有该化学键的物质
就越稳定性。根据图示可知:N 中化学键的键能为946 kJ/mol,O 中化学键的键能为498 kJ/mol,NO分子
2 2
中化学键的键能为632 kJ/mol,因此三种物质分子中N 的化学键的键能最大,N 最稳定;
2 2
反应热等于断裂反应物化学键吸收的总能量与形成生成物化学键释放的总能量的差,则图示反应的热化学
方程式为:N(g)+O(g)=2NO(g) H=946 kJ/mol+498 kJ/mol-2×632 kJ/mol=+180 kJ/mol;
2 2
(2)活化能是物质发生化学反应需吸△收的最低能量,则根据图示可知该反应的活化能为134 kJ/mol;
根据图②可知该反应的热化学方程式为:CO(g)+NO2(g) =CO(g)+NO(g), H=(134 kJ/mol-368kJ/mol)=-234
2
△
kJ/mol,若0.5 mol CO被氧化,放出Q kJ热量,则Q= =117 kJ;若该反应是可逆反应,可逆反应的
特点是可逆性,反应物不能完全转化为生成物,则在相同条件下将0.5 mol CO与1 mol NO 混合充分反应
2
后放出的热量<Q kJ;
(3)断裂1 mol N 和1 mol O 的化学键吸收能量946 kJ+496kJ=1444 kJ,生成2 mol NO放出能量
2 2
632kJ×2=1264 kJ,由于反应物能量低于生成物,因此该反应是吸热反应,据此画出的能量变化曲线为:;
(4)已知25℃,101kPa时:①4Fe(s)+3O (g)=2Fe O(s) ΔH=-1648 kJ/mol,
2 2 3
②C(s)+O(g)=CO (g) ΔH=-393 kJ/mol,
2 2
③2Fe(s)+2C(s)+3O (g)=2FeCO (s) ΔH=-1480 kJ/mol,
2 3
则根据盖斯定律,将①+②×4-③×2,整理可得热化学方程式4FeCO(s)+O(g)=2Fe O(s)+4CO(g) ΔH=-260
3 2 2 3 2
kJ/mol。
4.(2021·甘肃·永昌县第一高级中学高二期末)化学反应同时存在着物质和能量的变化,依据化学反应与
能量变化回答下列问题:
(1)已知汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。反应的化学方程式为2NO(g)+
2CO(g) N(g)+2CO(g)。已知部分化学键的键能如下:
2 2
分子式/结构式 NO/N≡O CO/C=O CO/O=C=O N/N≡N
2 2
化学键 N≡O C=O C=O N≡N
键能/(kJ/mol) 632 1072 750 946
请计算上述反应的ΔH=_____kJ/mol。
(2)1gH 气体完全燃烧生成液态水放出143kJ热量,其热化学方程式为:_____。
2
(3)已知①2O(g)+N(g)=NO(l)ΔH;
2 2 2 4 1
②N(g)+2H(g)=NH(l)ΔH;
2 2 2 4 2
③O(g)+2H(g)=2HO(g)ΔH
2 2 2 3
④2NH(l)+N O(l)=3N (g)+4HO(g)ΔH =-1048.9kJ·mol-1
2 4 2 4 2 2 4
上述反应热效应之间的关系式为ΔH=_____。
4
(4)已知稀溶液中,H+(aq)+OH-(aq)=H O(l)ΔH=-57.3kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol水
2
时放出的热量比57.3kJ_____(填“大”“小”)。
(5)将1molCH 与Cl 发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗Cl 的物
4 2 2
质的量为_____。
【答案】(1)-538(2)H (g)+ O(g)=HO(l)ΔH=-286kJ·mol-1
2 2 2
(3)2ΔH -2ΔH -ΔH
3 2 1
(4)小
(5)2.5mol
【解析】(1)由表格中键能数据及2NO(g)+2CO(g)=N (g)+2CO (g)可知,ΔH=2×632kJ/mol+2×1072kJ/
2 2
mol-946kJ/mol-2×2×750kJ/mol=-538kJ/mol,故答案为:-538。
(2)1g氢气完全燃烧生成液态水时放出热量143kJ,故1mol氢气燃烧生成1mol液态水时放出热量为
1mol×2g/mol×143kJ=286kJ,故热化学方程式为H(g)+ O(g)=HO(l)ΔH=-286kJ·mol-1。
2 2 2
(3)①2O(g)+N(g)=NO(l)ΔH;
2 2 2 4 1
②N(g)+2H(g)=NH(l)ΔH;
2 2 2 4 2
③O(g)+2H(g)=2HO(g)ΔH ;
2 2 2 3
从题给四个方程式分析,“④=③×2-②×2-①”,可得④2NH(l)+N O(l)=3N (g)
2 4 2 4 2
+4H O(g)ΔH =-1048.9kJ·mol-1,则有ΔH=2ΔH -2ΔH -ΔH 。
2 4 4 3 2 1
(4)醋酸为弱酸,其电离是吸热过程,因此稀醋酸与稀氢氧化钠反应生成lmol水时放出的热量小于57.3kJ。
(5)1mol甲烷与氯气发生取代反应,生成的四种有机物的物质的量相等,根据碳原子守恒可知CHCl、
3
CHCl、CHCl 、CCl 四种物质的物质的量均为:0.25mol,根据取代反应的特点可知有机物中氯原子的物
2 2 3 4
质的量等于氯气的物质的量,则消耗氯气的物质的量为:n(Cl )=0.25×1+0.25×2+0.25×3+0.25×4=0.5mol,答
2
案为:2.5mol。
5.(2021·北京市第三中学高二期中)书写下列化学方程式
(1)下图是1 mol NO 和1mol CO反应生成CO 和NO过程中能量变化示意图,请写出NO 和CO反应的热
2 2 2
化学方程式___________。
(2)已知:C(s) + O(g) = CO (g) ΔH=-437.3 kJ•mol-1
2 2
H(g) +1/2O(g) = HO(g) ΔH=-285.8 kJ•mol-1
2 2 2CO(g) +1/2O (g) = CO (g) ΔH=-283.0 kJ•mol-1
2 2
则固态碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是___________。
(3)已知拆开1mol H-H键、1molN≡N和1mol N—H键分别需要的能量是436kJ、948kJ、391 kJ。则N、H
2 2
合成NH 的热化学方程式为:___________。
3
(4)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢
的方法之一。已知存在如下反应:
i.
ii.
iii.
……
iii为积炭反应,利用 和 计算 时,还需要利用___________反应的 。
【答案】(1)NO (g)+CO(g)=CO (g)+NO(g) ∆H=-234kJ/mol
2 2
(2)C(s)+H O(g)=H (g)+CO(g) ∆H=+131.5kJ•mol-1
2 2
(3)N (g)+3H(g)=2NH (g) ∆H=-90.0kJ•mol-1
2 2 3
(4)C(s)+H O(g)=CO(g)+H (g)或C(s)+CO(g)=2CO(g)
2 2 2
【解析】(1)根据图像可知1 mol NO 和1mol CO反应生成CO 和NO的焓变ΔH=(E-
2 2 1
E)kJ/mol=134kJ/mol-368kJ/mol=-234kJ/mol,故1molNO 和1molCO反应生成CO 和NO的热化学方程式
2 2 2
为:NO (g)+CO(g)=CO (g)+NO(g) ∆H=-234kJ/mol,故答案为:NO (g)+CO(g)=CO (g)+NO(g) ∆H=-234k
2 2 2 2
J/mol;
(2)已知:
①C(s) + O(g)=CO(g) ΔH=-437.3 kJ•mol-1
2 2
②H(g) +1/2O(g)=HO(g) ΔH=-285.8 kJ•mol-1
2 2 2
③CO(g) +1/2O (g)=CO(g) ΔH=-283.0 kJ•mol-1
2 2
根据盖斯定律可知①-②-③即得到碳单质与水蒸气反应生成一氧化碳和氢气的热化学方程式为C(s)
+H O(g)=H (g)+CO(g) ∆H=+131.5kJ•mol-1,故答案为:C(s)+HO(g)=H (g)+CO(g) ∆H=+131.5kJ•mol-1;
2 2 2 2
(3)氮气、氢气合成氨的反应为N(g)+3H(g)=2NH (g),焓变等于反应物的总键能减去生成物的总键能,故
2 2 3
∆H =436×3kJ/mol+948kJ/mol-391×6kJ/mol=-90.0kJ/mol,故氮气与氢气合成氨气的热化学方程式为:N
2
(g)
+3H (g)=2NH (g) ∆H=-90.0kJ•mol-1,故答案为:N(g)+3H(g)=2NH (g) ∆H=-90.0kJ•mol-1;
2 3 2 2 3(4)比较反应i、ii和iii的化学方程式,可发现反应i和反应ii中没有出现碳单质,故应缺少单质参加的反应,
碳单质可以与水蒸气或二氧化碳反应,故还需要利用反应C(s)+HO(g)=CO(g)+H (g)或C(s)+CO(g)=2CO(g)
2 2 2
的焓变,故答案为:C(s)+HO(g)=CO(g)+H (g)或C(s)+CO(g)=2CO(g)。
2 2 2
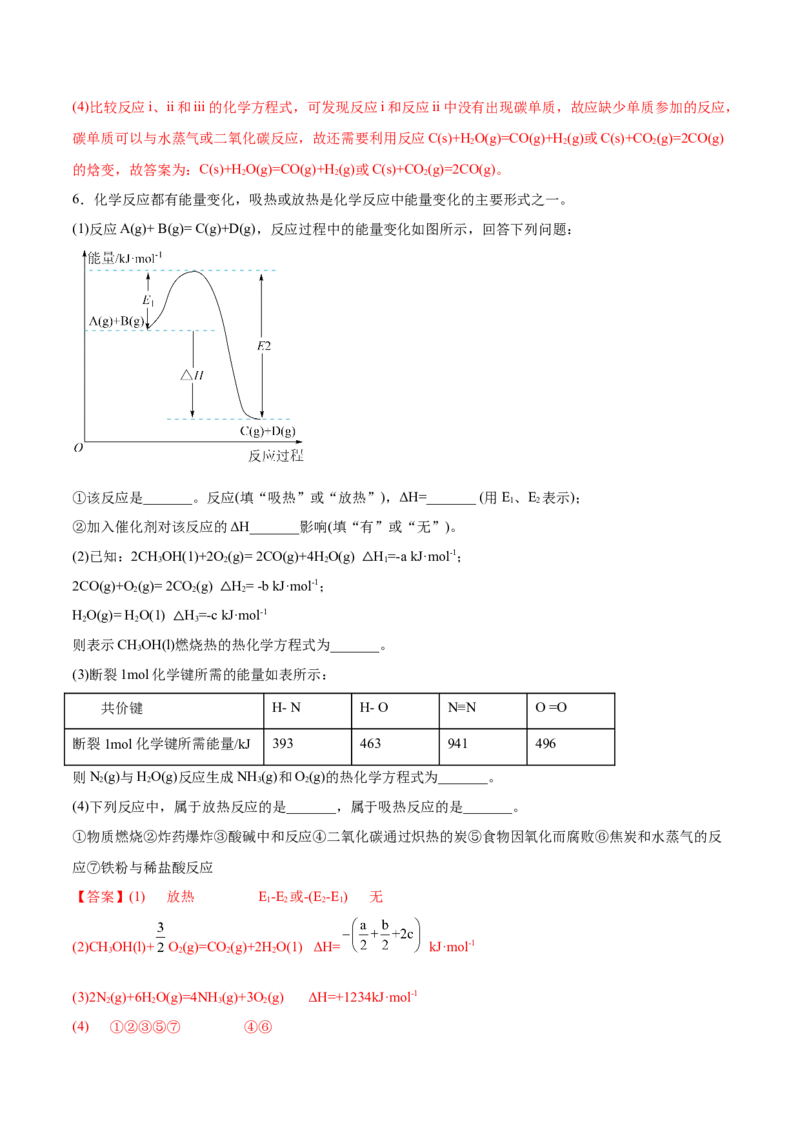
6.化学反应都有能量变化,吸热或放热是化学反应中能量变化的主要形式之一。
(1)反应A(g)+ B(g)= C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题:
①该反应是_______。反应(填“吸热”或“放热”),ΔH=_______ (用E、E 表示);
1 2
②加入催化剂对该反应的ΔH_______影响(填“有”或“无”)。
(2)已知:2CHOH(1)+2O (g)= 2CO(g)+4H O(g) H=-a kJ·mol-1;
3 2 2 1
2CO(g)+O 2 (g)= 2CO 2 (g) H 2 = -b kJ·mol-1; △
H
2
O(g)= H
2
O(1) H
3
=-c △kJ·mol-1
则表示CH
3
OH(l)△燃烧热的热化学方程式为_______。
(3)断裂1mol化学键所需的能量如表所示:
共价键 H- N H- O N≡N O =O
断裂1mol化学键所需能量/kJ 393 463 941 496
则N(g)与HO(g)反应生成NH (g)和O(g)的热化学方程式为_______。
2 2 3 2
(4)下列反应中,属于放热反应的是_______,属于吸热反应的是_______。
①物质燃烧②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的炭⑤食物因氧化而腐败⑥焦炭和水蒸气的反
应⑦铁粉与稀盐酸反应
【答案】(1) 放热 E-E 或-(E -E ) 无
1 2 2 1
(2)CH OH(l)+ O(g)=CO (g)+2HO(1) ΔH= kJ·mol-1
3 2 2 2
(3)2N (g)+6HO(g)=4NH (g)+3O(g) ΔH=+1234kJ·mol-1
2 2 3 2
(4) ①②③⑤⑦ ④⑥【解析】(1)①由题图可知,反应物的总能量高于生成物的总能量,故该反应为放热反应,AH=E -E 或-( E-
1 2 2
E);②使用催化剂只能改变反应的活化能,对反应的△H无影响;
1
(2)将已知中三个热化学方程式依次编号为①、②、③,根据盖斯定律: ×(①+②) +③×2得CHOH(l)+
3
O(g)=CO (g)+2HO(1) ΔH= kJ·mol-1;
2 2 2
(3)根据焓变和化学键键能之间的关系可知, =2E( ) +12E(H-O) -12E(N- H) -3E(
) =(2×941+12×463-12×393-3×496 ) kJ·mol-1 =+1234kJ·mol-1,故答案为2N(g)+6HO(g)=4NH (g)+3O(g)
2 2 3 2
ΔH=+1234kJ·mol-1;
(4)①物质燃烧属于放热反应;②炸药爆炸属于放热反应;③酸碱中和反应属于放热反应;④二氧化碳
通过炽热的炭属于化合反应,但为吸热反应;⑤食物因氧化而腐败属于放热反应;⑥焦炭和水蒸气的反应属
于吸热反应;⑦铁粉与稀盐酸反应属于放热反应;所以属于放热反应的有: ①②③⑤⑦,属于吸热反应的
④⑥;
题组三 反应热比较大小
1.标准状态下电极反应焓变可以分解为图所示的循环,下列关系正确的是
A. B.
C. D.
【答案】B
【答案】A.M(s)→M(g)需要吸收能量,即ΔH>0,M+(g)→M+(aq)需要放出能量,即ΔH<0,故A错误;
1 3
B.H+(aq)→H+(g)需要吸收能量,即ΔH>0,H(g)→ H(g),形成化学键放出热量,即ΔH<0,故B正确;
4 2 6C.ΔH+ΔH+ΔH 只是H+(aq)→ H(g)能量的变化,根据盖斯定律,ΔH=ΔH+ΔH+ΔH+ΔH+ΔH+ΔH,
4 5 6 2 1 2 3 4 5 6
故C错误;
D.ΔH+ΔH+ΔH 只是M(s)→M+(aq)能量的变化,故D错误;
1 2 3
答案为B。
2.(2021·辽宁·沈阳市第一二〇中学高一期中)在同温同压下,下列各组热化学方程式中, H> H 的
1 2
是 △ △
A.CHCOOH(aq)+NaOH(aq)=CH COONa(aq)+H O(l) H;HCl(aq)+NaOH(aq)=NaCl(aq)+H O(l) H
3 2 2 1 2 2
B.S(s)+O 2 (g)=SO 2 (l) H 1 ;S(s)+O 2 (g)=SO 2 (g) H 2 △ △
△ △
C.C(s)+O(g)=CO (g) H;C(s)+ O(g)=CO(g) H
2 2 1 2 2
△ △
D.H(g)+Cl (g)=2HCl(g) H; H(g)+ Cl(g)=HCl(g) H
2 2 1 2 2 2
△ △
【答案】A
【答案】A.CHCOOH(aq)+NaOH(aqg)=CH COONa(aq)+H O(l) H;HCl(aq)+NaOH(aq)=NaCl(aq)+H O(l)
3 2 2 1 2
H, △
2
△醋酸是弱酸,电离吸热,相同物质的量的醋酸和盐酸与氢氧化钠反应,醋酸放出的热量少,所以
△H> H,故选A;
1 2
B.S(s△)+O
2
(g)=SO
2
(l) H
1
;S(s)+O
2
(g)=SO
2
(g) H
2
气态SO
2
的能量大于液△态SO
2
,所以生成SO
2
(1)△放热多,△H
1
< H
2
,故不选B;
△
C.C(s)+O(g)=CO (g) H;C(s)+ O(g)=CO(g) H
2 2 1 2 2
△ △
碳完全燃烧比不完全燃烧放热多,所以生成二氧化碳放热多,△H< H,故不选C;
1 2
△
D.H(g)+Cl (g)=2HCl(g) H; H(g)+ Cl(g)=HCl(g) H,参加反应的氢气的物质的量越多,放热越
2 2 1 2 2 2
△ △
多,所以△H< H,故不选D。
1 2
选A。 △
3.CHCOOH和氨水反应的能量循环体系如图所示,下列说法正确的是
3A. H+ H+ H= H B. H+ H> H+ H
1 2 3 4 1 4 2 3
C.△H 4 <△H 1 -△H 2 △ D.△H 3 <△0 △ △
【答△案】C△ △ △
【答案】由图可知① ;②
;③ ;④
。
A.由以上得②+③+④=①,即△H+ H+ H= H,故A错误;
2 3 4 1
B.由△H
2
+ H
3
+ H
4
= H
1
得△H
1
+ △H
4
= △H
2
+ △H
3
+2 H
4
,中和反应是放热反应,故△H
4
<0,所以
H+ H< △H+ △H,△故B错误; △ △ △ △
1 4 2 3
△C.由△△H
2
+△ H
3
+△ H
4
= H
1
得△H
4
= H
1
- H
2
- H
3
<0,弱电解质的电离是吸热过程,所以△H
3
>0,所以
△H< H- △H,故△ C正△确; △ △ △
4 1 2
D.弱△电解质△的电离是吸热过程,所以△H
3
>0,故D错误;
故答案为:C。
4.相同温度和压强下,关于反应的 H,下列判断不正确的是
△
①CH(g)+CO (g) 2CO(g)+2H(g) H
4 2 2 1
△
②CH(g) C(s)+2H(g) H
4 2 2
△
③CO(g)+H(g) CO(g)+HO(g) H
2 2 2 3
△
④2CO(g) C(s)+CO(g) H
2 4
△
⑤CO(g)+H(g) C(s)+HO(g) H
2 2 5
△
A. H= H- H B. H>0, H>0
4 2 1 2 4
C.△H 5 =△H 2 +△H 3 - H 1 D.△H 3 >H 5 △
【答△案】B△ △ △ △
【答案】A.已知①CH(g)+CO (g) 2CO(g)+2H(g) H
4 2 2 1
△②CH(g) C(s)+2H(g) H
4 2 2
△
根据盖斯定律,将②-①,整理可得2CO(g) C(s)+CO(g) H= H- H= H,A正确;
2 2 1 4
△ △ △ △
B.②CH(g) C(s)+2H(g)的正反应为吸热反应, H>0,④2CO(g) C(s)+CO(g)的正反应为放
4 2 2 2
△
热反应, H<0,B错误;
4
△
C.已知①CH(g)+CO (g) 2CO(g)+2H(g) H
4 2 2 1
△
②CH(g) C(s)+2H(g) H
4 2 2
△
③CO(g)+H(g) CO(g)+HO(g) H
2 2 2 3
△
根据盖斯定律,将②+③-①,整理可得CO(g)+H(g) C(s)+HO(g) H = H+ H- H,即
2 2 2 3 1
△ △ △ △
H= H+ H- H,C正确;
5 2 3 1
△ △ △ △
D.③CO(g)+H(g) CO(g)+HO(g)的正反应是吸热反应, H>0,⑤CO(g)+H(g) C(s)+HO(g)
2 2 2 3 2 2
△
的正反应是吸热反应, H>0,③-⑤整理可得CO(g) CO(g)+C(s)为吸热反应, H- H>0,故
5 2 3 5
△ △ △
H>H,D正确;
3 5
△故合理选项是B。
5.(2022·山西·临汾第一中学校高二期末)已知: ;
;
;
;
下列关于上述反应焓变的判断正确的是
A. , B. ,C. D.
【答案】C
【答案】A.C(s)+O(g)=CO (g)和2CO(g)+O(g)=2CO (g)都是燃烧,都是放热反应,因此 ,
2 2 2 2
,故A错误;
B. CO(g)+C(s)=2CO(g)为吸热反应,则 ; 是放热反应,则 ,故
2
B错误;
C.①C(s)+O(g)=CO (g) ΔH ;②CO(g)+C(s)=2CO(g) ΔH ;③ 2CO(g)+O(g)=2CO (g) ΔH ,由盖斯定律
2 2 1 2 2 2 2 3
可知①=②+③,因此 ,故C正确;
D.③ 2CO(g)+O(g)=2CO (g) ΔH , 4Fe(s)+3O (g)=2Fe O(s) ΔH; 3CO(g)+Fe O(s)=3CO(g)+2Fe(s)
2 2 3 2 2 3 4 2 3 2
ΔH,由盖斯定律可知 ,因此 ,故D错误;
5
故答案选C。
6.相同温度和压强下,关于反应的ΔH,下列判断正确的是
ClO—(aq)+H+(aq) HClO(aq) ΔH
1
HO(l) H+(aq)+OH—(aq) ΔH
2 2
ClO— (aq)+H O(l) OH—(aq)+HClO(aq) ΔH
2 3
A.ΔH>0,ΔH>0 B.ΔH=ΔH+ΔH
1 2 3 1 2
C.ΔH>ΔH D.ΔH<0,ΔH>0
1 3 2 3
【答案】B
【答案】A.由分析可知,①为化学键形成的放热过程,焓变ΔH<0,故A错误;
1
B.由分析可知,①+②的反应③,则ΔH=ΔH+ΔH,故B正确;
3 1 2
C.由分析可知,①为化学键形成的放热过程,焓变ΔH<0,③为次氯酸根离子的水解反应,水解反应为
1
吸热反应,焓变ΔH>0,则焓变ΔH<ΔH,故C错误;
3 1 3
D.由分析可知,②为共价键断裂的吸热过程,焓变ΔH>0,故D错误;
2故选B。
7.(2022·湖南·雅礼中学高一期末)下列各组热化学方程式中,化学反应的 H前者大于后者的是
△
A.C(s)+O(g)=CO (g) H,C(s)+ O(g)=CO(g) H
2 2 1 2 2
△ △
B.S(s)+O (g)=SO(g) H,S(g)+O(g)=SO(g) H
2 2 3 2 2 4
△ △
C.2H(g)+O(g)=2HO(l) H;H(g)+ O(g)=HO(l) H
2 2 2 5 2 2 2 6
△ △
D.;CaO(s)+H O(l)=Ca(OH) (s) H CaCO (s)=CaO(s)+CO (g) H
2 2 8 3 2 7
【答案】B △ △
【答案】A.两个反应都为放热反应,ΔH<0,前者完全反应,放出的热量多,则ΔH<ΔH,故A错误;
1 2
B.两个反应都为放热反应,ΔH<0,前者S为固态,燃烧时放出的热量少,则ΔH>ΔH,故B正确;
3 4
C.两个反应都为放热反应,ΔH<0,前者反应物系数较大,则前者放出热量较多,则ΔH<ΔH,故C错
5 6
误;
D.前者为吸热反应,ΔH>0,后者为放热反应,ΔH<0,则ΔH>ΔH,故D错误;故选B。
7 8 7 8
8.(2022·河北·石家庄二中高一期中)MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A.△H(MgCO )> H(CaCO)>0
1 3 1 3
B.△H
2
(MgCO
3
)<△H
2
(CaCO
3
)>0
C.△H
1
(MgCO
3
)-△H
1
(CaCO
3
)= H
3
(CaO)- H
3
(MgO)
D.对于MgCO
3
和△CaCO
3
,△H△1 + H
2
> H△3
【答案】C △ △
【解析】A.ΔH 表示断裂 和M2+的离子键所吸收的能量,离子键强度越大,吸收的能量越大,因而
1
ΔH (MgCO )>ΔH (CaCO)>0,A项正确;
1 3 1 3
B.ΔH 表示断裂 中共价键形成O2-和CO 吸收的能量,与M2+无关,因而△H(MgCO )= H(CaCO)>
2 2 2 3 2 3
△
0,B项错误;
C.根据盖斯定律,ΔH(MgCO )-ΔH(CaCO)对应的化学反应为MgCO (s)+Ca2+(g)= CaCO(s)+Mg2+(g),
1 3 1 3 3 3ΔH(CaO)-ΔH(MgO)对应的化学反应为MgO(s)+Ca2+(g)= CaO(s)+Mg2+(g),所以ΔH(MgCO )-
3 3 1 3
ΔH(CaCO)≠ΔH(CaO)-ΔH(MgO),C项错误;
1 3 3 3
D.由上分析可知ΔH+ΔH>0,ΔH 对应的是M2+和O2-结合成MO放出的热量,所以ΔH<0,故
1 2 3 3
ΔH+ΔH>ΔH,D项正确;
1 2 3
答案选C。
9.回答下列关于焓变的问题:
(1)已知S(g)+O(g)=SO(g) ΔH<0; S(s)+O (g)=SO(g) ΔH<0。则ΔH_______ΔH 。
2 2 1 2 2 2 1 2
(2)已知2H(g)+O(g)=2HO(g) ΔH<0;2H(g)+O(g)=2HO(l) ΔH<0。则ΔH_____ΔH 。
2 2 2 1 2 2 2 2 1 2
(3)已知H(g)+1/2O (g)=HO(l) ΔH<0;2H(g)+O(g)=2HO(l) ΔH<0。则ΔH 和ΔH 的定量关系为_______。
2 2 2 1 2 2 2 2 1 2
(4)等物质的量的金属钾和金属钠与水的反应为:2K(s)+2H O(l)=2KOH(aq)+H (g) ΔH<0;2Na(s)
2 2 1
+2H O(l)=2NaOH(aq)+H (g) ΔH<0。则ΔH_______ΔH 。
2 2 2 1 2
(5)等物质的量碳分别发生如下反应:C(s)+O(g)=CO (g) ΔH<0;C(s)+1/2O (g)=CO(g) ΔH<0;则
2 2 1 2 2
ΔH_______ΔH 。
1 2
【答案】(1)ΔH <ΔH
1 2
(2)ΔH >ΔH
1 2
(3)2ΔH =ΔH
1 2
(4)ΔH <ΔH
1 2
(5)ΔH <ΔH
1 2
【解析】(1)S(s)转化为S(g)要吸收能量,因此S(g)燃烧放出的热量较多,则ΔH<ΔH 。
1 2
(2)HO(g)转化为HO(l)要放出能量,因此生成HO(g)放出的热量较少,则ΔH>ΔH 。
2 2 2 1 2
(3)方程式的化学计量数乘以n,焓变也变为n倍,因此2ΔH=ΔH 。
1 2
(4)K的活动性比Na强,与水反应更剧烈,因此等物质的量的金属钾和金属钠与水反应,K放出的热量
较多,则ΔH<ΔH 。
1 2
(5)两个反应都是放热反应,但第一个反应为碳完全燃烧,第二个反应为碳不完全燃烧,第一个反应程
度大,放热多,则ΔH<ΔH 。
1 2倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育