文档内容
第 02 讲 物质的转化
知识导航
知识精讲
一、酸、碱、盐的性质
1. 酸的通性(以盐酸为例)
(1)与指示剂反应:使紫色石蕊试剂变红,不能使酚酞试剂变色
(2)能与较活泼的金属发生置换反应,放出H: 6HCl + 2Al === 2AlCl + 3H ↑
2 3 2
(3)能与金属氧化物反应: 6HCl + Fe O === 2FeCl + 3H O
2 3 3 2
(4)能与碱反应生成盐和水(中和反应): HCl + NaOH === NaCl + H O
2
(5)能与某些盐反应: 2HCl + CaCO === CaCl + H O + CO ↑
3 2 2 2
2. 碱的通性(以烧碱为例)
(1)与指示剂作用:紫色石蕊变蓝,无色酚酞变红
(2)与非金属氧化物反应: 2NaOH+ CO === Na CO + H O(氢氧化钠必须密封保存)
2 2 3 2
(3)与酸发生中和反应: HCl + NaOH === NaCl + H O;
2
(4)能与某些盐反应: 2NaOH + MgCl === Mg(OH) ↓ + 2NaCl
2 2
3. 盐的通性
(1)盐 + 金属 → 新金属 + 新盐: CuSO + Zn ==== Cu + ZnSO
4
(2)盐 + 酸 → 新盐 + 新酸: CaCO +2HCl ==== CaCl + H O + CO ↑
3 2 2 2
(3)盐 + 碱 → 新碱 + 新盐: MgCl + 2NaOH ==== Mg(OH) ↓ + 2NaCl
2 2
(4)盐 + 盐 → 新盐 + 新盐: NaCl + AgNO ==== AgCl ↓+ NaNO
3 3二、化学反应类型
1. 按照生成物、反应物的种类和数目,化学反应可分为:_________________________________________
2. 按照物质是否得氧或失氧,化学反应可分为:____________________________________
【答案】化合反应 分解反应 置换反应 复分解反应
三、物质的转化关系
物质间的转化一般可以按照下列思路进行考虑:
(1)金属及其化合物的转化:金属单质→金属氧化物→碱→盐。
如:
写出各步的反应方程式,并标注其反应类型。
① ___________________________________________ ______________
② ___________________________________________ ______________
③ ___________________________________________ ______________
④ ___________________________________________ ______________
⑤ ___________________________________________ ______________
⑥ ___________________________________________ ______________
【答案】2Ca+O====2CaO 化合反应 CaO+HO====Ca(OH) 化合反应
2 2 2
CaO+CO====CaCO 化合反应 Ca(OH) +NaCO====CaCO ↓+2NaOH 复分解反应
2 3 2 2 3 3
Ca(OH) +2HCl====CaCl +2HO 复分解反应 CaCO +2HCl====CaCl +CO↑+HO 复分解反应
2 2 2 3 2 2 2
(2)非金属及其化合物的转化:非金属单质→非金属氧化物→酸→盐。
如:C→CO→HCO→NaCO
2 2 3 2 3
(3)按照各物质的通性进行转化
思考与交流:上述物质间的转化,你能各举出一个例子吗?四、物质转化的应用
根据物质的组成和性质,以及物质之间的转化关系,我们可以确定制备某种物质的可能方法。
例如,制备氢氧化钠,可采取以下方法:
(1)碱性氧化物与水反应:
(2)碱与盐反应:
【答案】NaO + HO === 2NaOH NaCO + Ca(OH) === CaCO↓ + 2NaOH
2 2 2 3 2 3
对点训练
题型一:酸、碱、盐的性质
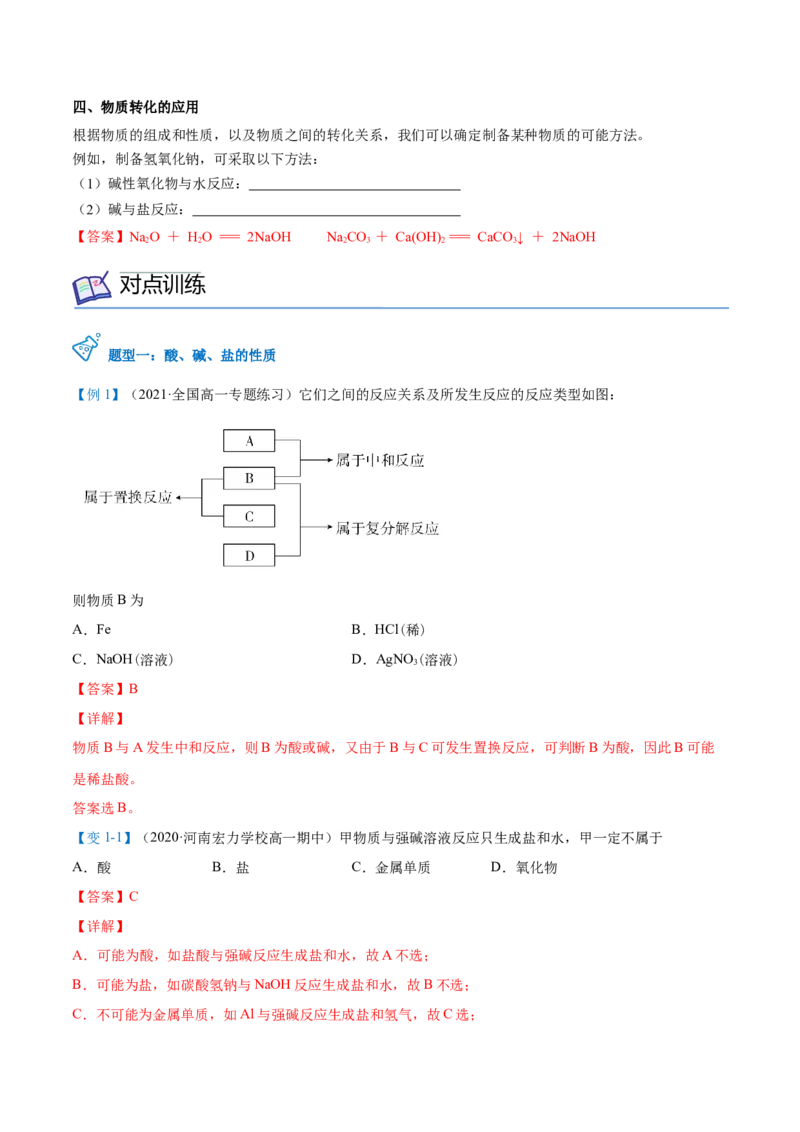
【例1】(2021·全国高一专题练习)它们之间的反应关系及所发生反应的反应类型如图:
则物质B为
A.Fe B.HCl(稀)
C.NaOH(溶液) D.AgNO(溶液)
3
【答案】B
【详解】
物质B与A发生中和反应,则B为酸或碱,又由于B与C可发生置换反应,可判断B为酸,因此B可能
是稀盐酸。
答案选B。
【变1-1】(2020·河南宏力学校高一期中)甲物质与强碱溶液反应只生成盐和水,甲一定不属于
A.酸 B.盐 C.金属单质 D.氧化物
【答案】C
【详解】
A.可能为酸,如盐酸与强碱反应生成盐和水,故A不选;
B.可能为盐,如碳酸氢钠与NaOH反应生成盐和水,故B不选;
C.不可能为金属单质,如Al与强碱反应生成盐和氢气,故C选;D.可能为氧化物,如二氧化碳与NaOH反应生成碳酸钠、水,故D不选;
故选C。
【变1-2】(2020·河南安阳市·五一中学高一期中)向下列物质中滴加稀硫酸或氯化镁溶液时,均有白色沉
淀生成的是
A.BaCl B.Ba(OH) C.NaCO D.KOH
2 2 2 3
【答案】B
【详解】
A.向BaCl 溶液中滴加氯化镁溶液不反应,没有沉淀生成,A错误;
2
B.向Ba(OH) 溶液中滴加稀硫酸生成硫酸钡白色沉淀,滴加氯化镁溶液生成氢氧化镁白色沉淀,B正确;
2
C.向NaCO 溶液中滴加稀硫酸生成硫酸钠.二氧化碳和水,没有沉淀生成,C错误;
2 3
D.向KOH溶液滴加稀硫酸生成硫酸钠和水,没有白色沉淀生成,D错误;
故选B。
【变1-3】(2020·华中师范大学潜江附属中学高一月考)有CuO、Fe、H、Ba(OH) 溶液、KCO 溶液、
2 2 2 3
NaOH溶液、稀硫酸七种物质,在常温下物质两两间能发生反应最多有 ( )
A.4个 B.5个 C.6个 D.7个
【答案】C
【详解】
由题目中的信息可以知道:两种物质之间分别验证,则CuO与H 反应需要加热,而题目要求“在常温
2
下”进行,故此反应不能进行;CuO与稀硫酸反应;Fe与稀硫酸反应;Ba(OH) 溶液和KCO 溶液反应生
2 2 3
成沉淀;Ba(OH) 溶液与稀硫酸反应生成沉淀;KCO 溶液与稀硫酸反应生成气体;NaOH溶液与稀硫酸
2 2 3
反应,生成盐和水;故共6个化学反应。C选项是正确的。
故选C。
【变1-4】(2020·全国高一课时练习)下列各组物质的溶液,不另加试剂无法一一鉴别的是( )
A.
B.
C.
D.
【答案】C
【详解】A.组内四种物质的溶液两两混合时,其中一种溶液与其他三种溶液混合时现象分别为出现白色沉淀、放
出气体、无明显现象,该溶液为 溶液;与 溶液混合产生气体的溶液为盐酸,产生白色沉
淀的为 溶液,与 溶液混合无明显现象的为 溶液,因此不加其他试剂可以鉴别,故
A不符合题意;
B. 溶液是蓝色的,首先鉴别出蓝色的 溶液,能与 溶液反应产生蓝色沉淀的是
溶液,能与 溶液反应产生白色沉淀的是 溶液,无明显变化的是盐酸,因此不加其
他试剂可以鉴别,故B不符合题意;
C. 溶液和 溶液混合后溶液变浑浊,但其余两两混合均没有明显现象,因此不加其他试剂无
法鉴别,故C符合题意;
D.组内四种物质的溶液两两混合时,其中一种溶液与其他三种溶液混合时现象分别为出现白色沉淀、放
出气体、无明显现象,该溶液为 溶液,与 溶液混合产生气体的溶液为 溶液,产生
白色沉淀的为 溶液,与 溶液混合无明显现象的为 溶液,因此不加其他试剂可以鉴别,
故D不符合题意。
综上所述,答案为C。
题型二:反应类型的判断
【例2】(2021·江苏南通市·高一月考)下列属于置换反应的是
A.Fe O+3CO 2Fe+3CO B.TiCl +4Na Ti+4NaCl
2 3 2 4
C.CH+HO 3H+CO D.4NH +5O 4NO+6HO
4 2 2 3 2 2
【答案】B
【分析】一种单质和一种化合物反应生成另一种单质和化合物的反应是置换反应,据此判断。
【详解】
A.Fe O+3CO 2Fe+3CO 不是置换反应,属于氧化还原反应,A不符合;
2 3 2
B.TiCl +4Na Ti+4NaCl属于置换反应,B符合;
4
C.CH+HO 3H+CO不是置换反应,属于氧化还原反应,C不符合;
4 2 2
D.4NH +5O 4NO+6HO不是置换反应,属于氧化还原反应,D不符合;
3 2 2
答案选B。
【变2-1】(2021·北京师范大学珠海分校附属外国语学校高一期中)碳及其化合物的转化关系:
,其中涉及的基本反应类型依次是
A.化合反应、置换反应、分解反应、复分解反应
B.置换反应、复分解反应、化合反应、分解反应
C.置换反应、化合反应、复分解反应、分解反应
D.置换反应、化合反应、分解反应、复分解反应
【答案】C
【详解】
C和CuO在高温条件下反应生成Cu和CO,属于置换反应;CO 和HO反应生成HCO,属于化合反应;
2 2 2 2 3
HCO 和Ca(OH) 反应生成CaCO 和HO,属于复分解反应;CaCO 在高温条件下生成CaO和CO,属于
2 3 2 3 2 3 2
分解反应;C项正确。
【变2-2】(2021·全国高一专题练习)下列关于化学反应类型的叙述正确的是
A.凡是生成盐和水的反应都是中和反应
B.复分解反应一定没有单质参加或生成
C.生成一种单质和一种化合物的反应一定是置换反应
D.分解反应的生成物中一定有单质
【答案】B
【详解】A.因为有盐和水生成的反应不一定是中和反应。例如二氧化碳和氢氧化钠反应就是生成盐碳酸钠和水的反
应,A不正确;
B.复分解反应一定没有单质参加,因为复分解反应中的物质都是化合物,B正确;
C.如一氧化碳还原氧化铜的反应,生成铜单质和二氧化碳的反应就不属于置换反应,C不正确;
D.如高温煅烧石灰石属于分解反应,但生成物为二氧化碳和氧化钙都是化合物,D不正确;
答案选B。
题型三:物质的转化
【例3】(2021·长治市第一中学校高一期末)物质之间的相互转化,可以直接实现,也可以间接实现,下
列转化可以一步实现的是
A. B.
C. D.
【答案】C
【详解】
A.碳在氧气中燃烧生成二氧化碳,二氧化碳通入石灰水中生成碳酸钙,C不能直接反应产生CaCO ,A
3
不符合题意;
B.CuO难溶于水,与水也不发生反应,氧化铜不能直接反应产生Cu(OH) ,B不符合题意;
2
C.Fe与CuSO 发生置换反应产生Cu和FeSO ,可以一步实现上述转化,C符合题意;
4 4
D.CaCO 高温煅烧反应产生CaO和CO,二氧化碳与碳高温下反应生成一氧化碳,碳酸钙不能直接反应
3 2
转化为CO,D不符合题意;
故合理选项是C。
【变3-1】(2021·全国高一专题练习)构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的
知识网络图:“﹣”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C
分别属于不同类别的化合物,则A、B、C可能是A.CuO、Ba(OH) 、CuSO
2 4
B.NaOH、HNO、KCO
3 2 3
C.KOH、FeCl 、NaCO
3 2 3
D.NaOH、Ba(NO )、HSO
3 2 2 4
【答案】B
【详解】
A.盐酸不与硫酸铜反应,盐酸不能转化为氢氧化钡,氢氧化钡不与氧化铜反应,故A不符合题意;
B.盐酸和氢氧化钠、碳酸钾都能反应,和硝酸银反应生成硝酸,硝酸和氢氧化钠、碳酸钾都能反应,故
B符合题意;
C.氯化铁和碳酸钠均为盐,属于相同类别的化合物,故C不符合题意;
D.盐酸不能转化为硝酸钡,盐酸不与硫酸反应,氢氧化钠与硝酸钡不反应,故D不符合题意;
故答案:B。
【变3-2】(2020·浙江宁波市·效实中学高一期中)分别能实现下列从左到右转化的单质是
金属单质 +O 碱性氧化物 +HO→ 碱 +酸或酸性氧化物→ 盐
2→ 2
非金属单质 +O 酸性氧化物 +HO→ 酸 +碱或碱性氧化物→ 盐
2→ 2
A.Ca和C B.Ca和Cl C.Cu和C D.Cu和Cl
【答案】A
【详解】
A.Ca与氧气反应生成CaO,CaO是碱性氧化物,CaO与水反应生成Ca(OH) ,Ca(OH) 是碱,Ca(OH) 与
2 2 2
盐酸反应生成盐CaCl ;C与氧气反应生成CO,CO 是酸性氧化物,CO 与水反应生成碳酸,碳酸与碱反
2 2 2 2
应生成碳酸盐,A符合题意;
B.Ca能完成题中的转化,但是Cl 与氧气不反应,不能实现题中的转化,B不合题意;
2
C.Cu与氧气反应生成CuO,CuO是碱性氧化物,但是CuO与水不反应,C不合题意;
D.Cu与氧气反应生成CuO,CuO是碱性氧化物,但是CuO与水不反应,D不合题意;
故答案为:A。【变3-3】(2021·福建泉州市·高一期末)如图,箭头方向表示在通常条件下能与某种常见试剂发生转化,
6步转化均能一步实现的一组物质是
物质
W X Y Z
选项
A Cu
B Na NaOH
C
D S
A.A B.B C.C D.D
【答案】C
【详解】
A.根据物质转化关系分析,铜不能直接转化为氢氧化铜,所以W不能发生图中转化为Z的反应,故A错
误;
B.根据物质转化关系分析,氢氧化钠不能直接转化为氧化钠,即Y不能发生图中转化为Z的反应,故B
错误;
C.氢氧化铝与硫酸反应生成硫酸铝,与盐酸反应生成氯化铝,与氢氧化钠溶液反应生成偏铝酸钠;硫酸
铝加入氯化钡溶液生成氯化铝和硫酸钡,氯化铝与足量的氢氧化钠溶液反应生成偏铝酸钠,偏铝酸钠溶液
与足量的硫酸反应生成硫酸铝,满足图中转化关系,故C可选;
D.硫不能直接转化为三氧化硫,即W不能发生图中生成Y的反应,故D错误;
故选C。
【变3-4】(2021·全国高一专题练习)A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如
图所示,其中所含的相同元素是( )A.铜 B.碳 C.铁 D.钙
【答案】D
【分析】
根据E高温会生成A,A和水反应生成的B和二氧化碳反应会生成A,可以猜测E是碳酸钙,A为氧化钙,B
为氢氧化钙,氢氧化钙和盐酸会生成氯化钙,所以C是氯化钙;氧化钙和硝酸会生成硝酸钙,氯化钙和硝
酸银会生成硝酸钙,所以D是硝酸钙,然后将推出的各种物质代入转化关系中验证即可。
【详解】
E高温会生成A,A和水反应生成的B和二氧化碳反应会生成A,可以猜测E是碳酸钙,A为氧化钙,B为氢
氧化钙,氢氧化钙和盐酸会生成氯化钙,所以C是氯化钙;氧化钙和硝酸会生成硝酸钙,氯化钙和硝酸银
会生成硝酸钙,所以D是硝酸钙;碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水反应生成氢
氧化钙,氧化钙和硝酸反应生成硝酸钙和水,氢氧化钙和盐酸反应生成氯化钙和水,氯化钙和硝酸银反应
生成硝酸钙和氯化银沉淀,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氯化钙和碳酸钠反应会生成碳
酸钙沉淀和氯化钠,硝酸钙和碳酸钠反应生成碳酸钙沉淀和硝酸钠,推出的各种物质均满足题中的转化关
系,所以A是氧化钙,B是氢氧化钙,C是氯化钙,D是硝酸钙,E是碳酸钙,其中所含的相同元素是:钙
元素;
综上所述,本题选D。
题型四:物质的分类与转化
【例4】同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰
(CaO)。
(1)生石灰属于________(填字母,下同)。
A.酸 B.碱 C.盐 D.纯净物 E.化合物 F.金属氧化物 G.非金属氧化物 H.碱性氧化物
I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、生石灰等物质划分为一类。该同学的分类依据为________。
A.酸类 B.碱类
C.氧化物 D.干燥剂
(3)生石灰可作干燥剂的理由是____________________________________(用化学方程式表示)。
(4)生石灰还可以跟哪些类别的物质发生化学反应?
请列举两例并填表。物质类别 化学方程式
(5)小纸袋中的物质能否长期持续地作干燥剂?________。
【答案】(1)DEFH (2)D
(3)CaO+HO====Ca(OH)
2 2
(4)酸 CaO+2HCl====CaCl +HO 酸性氧化物 CaO+CO====CaCO
2 2 2 3
(5)不能
【例5】(2020·云南民族大学附属中学高一月考)2020年9月20日是第32个“全国爱牙日”。为了防止龋
齿,正确的刷牙方式和选用适宜的牙膏很重要。对牙膏中的物质的探究要用到许多化学知识。
下表列出了三种牙膏中的摩擦剂:
牙膏 ×××牙膏 ×××牙膏 ××牙膏
摩擦剂 氢氧化铝 碳酸钙 二氧化硅
(1)三种牙膏的摩擦剂中,氢氧化铝是碱,碳酸钙和二氧化硅分别是___________、___________(填“酸”“碱”
“盐”或“氧化物”)。
(2)根据你的推测,牙膏摩擦剂的溶解性___________(填“易溶”和“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某同学设计了一种实验室制备碳酸钙的实验方案,其流程
图为:
请写出上述方案中反应③的化学方程式:___________。
(4)请你仍用石灰石作为原料(其他试剂自选),设计实验室制备碳酸钙的另一种实验方案,依照(3)所示,将
你的实验方案用流程图表示出来:
→___________________
你设计的方案的优点为___________。
【答案】盐 氧化物 难溶 Ca(OH) +Na CO=CaCO ↓+2NaOH
2 2 3 3
不需要高温条件,条件温和、节
能;实验步骤少,操作简单。
【详解】(1)三种牙膏的摩擦剂中,氢氧化铝是碱;碳酸钙是由金属阳离子与酸根离子组成的化合物,属于盐;二氧
化硅是由氧与硅两种元素组成的化合物,属于氧化物;
(2)牙膏摩擦剂氢氧化铝、碳酸钙和二氧化硅都难溶于水,因此牙膏摩擦剂属于难溶性物质;
(3)石灰水主要成分是Ca(OH) ,Ca(OH) 与NaCO 发生复分解反应产生CaCO 沉淀和NaOH,所以反应③
2 2 2 3 3
的化学方程式为:Ca(OH) +Na CO=CaCO ↓+2NaOH;
2 2 3 3
(4)另一种以石灰石为原料制备CaCO 的方案是:CaCO 与HCl发生复分解反应产生CaCl 、HO、CO,反
3 3 2 2 2
应产生的CaCl 与NaCO 在溶液中反应产生CaCO 沉淀和NaCl。反应方程式为:
2 2 3 3
CaCO +2HCl=CaCl +CO ↑+H O;CaCl +Na CO=CaCO ↓+2NaCl,实验方案用流程图表示出来为:
3 2 2 2 2 2 3 3
该方案与第一种实验方案比较优点是:不需要高温条件,条件温和、节能;实验步骤少,操作简单。
【例6】(2020·山西太原市·太原十二中高一月考)单质、氧化物、酸、碱和盐的相互关系,可以用图简单
表示。限选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定
序号的转变用化学方程式表示(所写化学方程式不得重复)。
① ;
②____________________________________________________________;
③_____________________________________________________________;
④_____________________________________________________________;
⑤______________________________________________________________;
⑥______________________________________________________________;
⑦_____________________________________________________________。
【答案】CO+H O=HCO CO+Ca(OH) =CaCO ↓+H O Fe+2HCl=FeCl +H ↑
2 2 2 3 2 2 3 2 2 2
CaO+2HCl=CaCl +H O Ca(OH) +2HCl=CaCl +2H O CaO+H O=Ca(OH)
2 2 2 2 2 2 2【分析】
属于同一类的物质必定符合同一标准,就会有某一共同的性质,利用一类物质和另一类物质之间的关系,
就可以找出物质之间转化的方法:非金属 酸性氧化物 ;金属 碱性氧化物
,该题对各类物质之间的转化限定了8种物质,从这8种物质中选出符合条件的物质进行各类物
质间的转化。
【详解】
②酸性氧化物+水→酸,CO 属于酸性氧化物,该反应为: CO +H O=HCO;
2 2 2 2 3
③酸性氧化物+碱→盐和水,CO 属于酸性氧化物,Ca(OH) 属于碱,该反应为:
2 2
CO+Ca(OH) =CaCO ↓+H O;
2 2 3 2
④金属+酸→盐+H ↑,Fe属于金属,HCl属于酸,该反应为:Fe+2HCl=FeCl +H ↑;
2 2 2
⑤碱性氧化物+酸→盐+水,CaO属于碱性氧化物,HCl属于酸,该反应为:CaO+2HCl=CaCl +H O;
2 2
⑥碱+酸→盐+水,Ca(OH) 属于碱,HCl属于酸,该反应为:Ca(OH) +2HCl=CaCl +2H O;
2 2 2 2
⑦碱性氧化物+水→碱,CaO属于碱性氧化物,该反应为:CaO+H O=Ca(OH) 。
2 2
【点睛】
复分解反应是四大基本反应类型之一,考生一定要掌握复分解反应的基本规律及反应发生的条件。
【例7】(2020·全国高一课时练习)下图表示的是物质A—H相互间的关系(“→”表示物质间的转化关系,
“——”表示两端的物质能发生化学反应)。A、G都是常见单质,气体C常用于灭火,D是纯碱,E是熟石
灰,F是一种蓝色溶液,可用于配制农药波尔多液。请你回答:
(1)C的化学式__________,H可能是 __________。
(2)写出标号①、②、③、④的化学方程式:①_____________;②___________ ;
③______________;④__________。
【答案】CO HCl 2C+O 2CO 2NaOH+CO =Na CO+H O
2 2 2 2 3 2
NaCO+Ca(OH) =CaCO ↓+2NaOH Fe+CuSO=Cu+FeSO
2 3 2 3 4 4
【分析】
C常用来灭火,可知C为二氧化碳,A和B在一定条件下都能生成C,可以知道B为一氧化碳,而A为氧
气或是碳单质;D是纯碱,E是熟石灰,F是一种蓝色溶液,可用于配制农药波尔多液,则F为硫酸铜;G
是常见单质,能够与硫酸铜反应,则G是比铜活泼的金属,如铁等;H能够与碳酸钠反应,也能与活泼金
属反应,则H可能为酸,据此分析解答。
【详解】
(1)根据C常用来灭火,可知C为二氧化碳;D是纯碱,F为硫酸铜;G是常见单质,能够与硫酸铜反应,
则G是比铜活泼的金属,如铁等;H能够与碳酸钠反应,也能与活泼金属反应,则H可能为酸,如稀硫酸
或盐酸,故答案为CO;HCl(或HSO );
2 2 4
(2)根据上述分析,C为二氧化碳,可以知道A为氧气或是碳单质,B为一氧化碳,D是纯碱,E是熟石灰,
F为硫酸铜,H为盐酸或硫酸, G是活泼的金属,如铁等;因此反应①:2C+O 2CO;反应②:
2
2NaOH+CO =Na CO+H O;反应③:NaCO+Ca(OH) =CaCO ↓+2NaOH;反应④:Fe+CuSO=Cu+FeSO ,
2 2 3 2 2 3 2 3 4 4
故答案为2C+O 2CO;2NaOH+CO =Na CO+H O;NaCO+Ca(OH) =CaCO ↓+2NaOH;
2 2 2 3 2 2 3 2 3
Fe+CuSO=Cu+FeSO 。
4 4
提分特训
【题1】(2021·吉林延边朝鲜族自治州·高一期末)下列有关分类的叙述合理的是
A.物质分为混合物、纯净物、化合物
B.化学基本反应类型有化合反应、分解反应、置换反应、氧化还原反应
C.物质的分类方法只有交叉分类法和树状分类法
D.单质分为金属单质、非金属单质、稀有气体
【答案】D
【详解】A.根据构成物质微粒种类的多少,将物质分为纯净物和混合物,仅有一种微粒构成的物质属于纯净物,
由两种或两种以上的微粒构成的物质属于混合物,化合物属于纯净物,A错误;
B.化学基本反应类型有化合反应、分解反应、置换反应、复分解反应,B错误;
C.物质的分类方法除有交叉分类法和树状分类法外,还有其它分类方法,如单一分类法等,因此不是仅
有交叉分类法和树状分类法,C错误;
D.元素周期表的元素有金属元素、非金属元素和稀有气体元素,因此由这些元素组成的单质有金属单质、
非金属单质、稀有气体,D正确;
故合理选项是D。
【题2】(2020·南京市第十三中学高一月考)下列性质中,不属于碱的通性的是
A.能与酸反应生成盐和水 B.能与酸性氧化物反应生成盐和水
C.能与某些盐反应生成新碱和新盐 D.能与金属反应放出氢气
【答案】D
【详解】
A.能与酸反应生成盐和水,属于碱的通性,故A不符合;
B.能与酸性氧化物反应生成盐和水,属于碱的通性,故B不符合;
C.能与某些盐反应生成新碱和新盐,属于碱的通性,故C不符合;
D.能与金属反应放出氢气,不属于碱的通性,故D符合;
答案选D。
【题3】(2020·沙坪坝区·重庆八中)下列物质转化不能通过一步反应实现的是
A.CaO→CaCl B.CuO→Cu(OH)
2 2
C.CaO→Ca(OH) D.Mg(OH) →MgCl
2 2 2
【答案】B
【详解】
A.CaO与HCl反应生成CaCl 和水,可以通过一步反应实现,故A不选;
2
B.CuO与水不反应,CuO→Cu(OH) 转化不能通过一步反应实现,故B选;
2
C.CaO与水反应生成Ca(OH) ,可以通过一步反应实现,故C不选;
2
D.Mg(OH) 与HCl反应生成MgCl 和水,可以通过一步反应实现,故D不选;
2 2
答案选B。
【题4】(2020·全国高一)铜器久置于空气中会和空气中的水蒸气、二氧化碳、氧气作用产生“绿锈”,该
“绿锈”俗称“铜绿”,又称“孔雀石”(碱式碳酸铜),“铜绿”能跟酸反应生成铜盐、二氧化碳和水。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。铜 铜绿 甲 Cu(OH) 乙 Cu,下列说法不
正确的是
A.铜绿属于碱 B.乙为氧化铜 C.④为分解反应 D.⑤为置换反应
【答案】A
【详解】
A. 铜绿(碱式碳酸铜)属于盐而不是碱,A错误;
B.反应④为Cu(OH) CuO+HO,则乙为氧化铜,B正确;
2 2
C.反应④为Cu(OH) CuO+HO,④为分解反应,C正确;
2 2
D.反应⑤为CuO+H Cu+HO,⑤为置换反应,D正确;
2 2
答案选A。
【题5】(2020·全国高一课时练习)下列各组物质中,满足图所示物质一步转化关系的是( )
选项 X Y Z
A CO CO HCO
2 2 3
B Cu CuO Cu(OH)
2
C CaO Ca(OH) CaCO
2 3
D CuSO Cu(OH) CuCl
4 2 2
A.A B.B C.C D.D
【答案】C
【详解】
A.CO燃烧产生CO,CO 与HO反应产生HCO,但HCO 不能通过一步反应生成CO,A错误;
2 2 2 2 3 2 3
B.Cu与O 加热反应产生CuO,CuO难溶于水,不能通过一步反应生成Cu(OH) ,Cu(OH) 也不能通过一
2 2 2
步反应转化为Cu,B错误;
C.CaO与HO反应产生Ca(OH) ,Ca(OH) 与CO 反应产生CaCO ,CaCO 高温分解产生CaO,可以实现
2 2 2 2 3 3
物质之间的转化关系,C正确;
D.CuSO 与NaOH反应产生Cu(OH) 沉淀,Cu(OH) 与HCl反应产生CuCl ,但CuCl 不能通过一步反应
4 2 2 2 2转化为CuSO ,D错误;
4
故答案为C。
【题6】(2020·全国高一课时练习)已知X和Y能发生如下反应:X+Y HO+盐,下列有关X和Y所属
2
种类的说法中一定不正确的是 ( )
A B C D
X 酸性氧化物 碱性氧化物 盐 酸性氧化物
Y 碱 酸 碱 碱性氧化物
A.A B.B C.C D.D
【答案】D
【详解】
A、X是酸性氧化物 +Y是碱 HO+盐
2
B、x是碱性氧化物+ Y是酸 HO+盐
2
C、X是盐+ Y是碱可能生成HO和盐,如NaHSO+NaOH=Na SO +HO;
2 4 2 4 2
D、X是酸性氧化物+ Y是碱性氧化物 盐
选D。
【题7】(2020·湖北荆州市·沙市中学高一期中)碱溶液中都含有OH-,因此不同的碱表现出一些共同的性
质。下列关于Ba(OH) 性质的描述中不属于碱的共同性质的是
2
A.能使紫色石蕊试液变蓝色 B.能与盐酸反应生成水
C.能与NaS0 溶液反应生成BaS0 沉淀 D.能与CO 反应生成水
2 4 4 2
【答案】C
【详解】
碱的通性有使紫色的石蕊试液显蓝色,无色的酚酞试液显红色;和酸发生中和反应;和酸性氧化物反应生
成盐和水;和某些盐发生复分解反应等。因此选项A、B、D都是碱的通性。但并非所有的碱和盐反应都
反应,且生成物也不一定都是沉淀,所以选项C不是碱的通性,答案选C。
【点睛】
所谓通性是指所有的物质都具备的,对于碱来讲,就是所有的碱都具备的,显然并不是所有的碱和硫酸钠
都反应。
【题8】(2020·景谷傣族彝族自治县第一中学高一月考)常温下,向稀盐酸中逐渐加入试剂X后,溶液的
pH变化如图所示。试剂X是下列物质中的( )A. B. C. D.
【答案】A
【详解】
A.氢氧化钠溶液显碱性,氢氧化钠和稀盐酸发生中和反应,溶液的酸性逐渐减弱,当恰好完全反应时溶
液的pH为7,继续加入氢氧化钠则溶液呈碱性,pH大于7,图像与之相符,故A正确;
B.加水稀释盐酸,溶液的酸性变弱,溶液的pH增大,但溶液始终呈酸性,即溶液的pH不会大于7,图
像与之不相符,故B错误;
C. 能与稀盐酸反应生成氯化亚铁和氢气,稀盐酸被消耗,溶液的pH增大,最终得到FeCl 溶液,pH
2
不会大于7,图像与之不相符,故C错误;
D.碳酸钙能与稀盐酸反应,稀盐酸被消耗,溶液的pH增大,但不会大于7,图像与之不相符,故D错误。
综上所述,答案为A。
【题9】(2020·全国高一课时练习)将稀硫酸、硫酸铜溶液、氯化镁溶液、氢氧化钡溶液两两混合,最多
能发生的反应个数及生成沉淀的种类数分别为( )
A.2、2 B.2、3 C.3、3 D.3、2
【答案】C
【详解】
稀硫酸与氢氧化钡溶液反应可生成硫酸钡沉淀;硫酸铜溶液与氢氧化钡溶液反应可生成氢氧化铜沉淀和硫
酸钡沉淀;氯化镁溶液与氢氧化钡溶液反应可生成氢氧化镁沉淀,故这四种溶液两两混合最多能发生3个
反应,并生成3种沉淀,答案为C。
【题10】(2020·全国高一课时练习)向滴有石蕊试液的稀盐酸中,慢慢滴入过量氢氧化钠溶液,石蕊颜
色变化的过程是
A.红→蓝→紫 B.紫→蓝→红 C.蓝→紫→红 D.红→紫→蓝
【答案】D
【详解】
紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,稀盐酸显酸性,滴有石蕊试液的稀盐酸,显红色;慢慢
滴入过量氢氧化钠溶液,至恰好完全反应时,显中性,溶液颜色变为紫色;继续滴加氢氧化钠溶液,溶液
显碱性,颜色变为蓝色。故石蕊颜色变化的过程是红→紫→蓝,故选D。【点睛】
解答本题要注意石蕊试液的本来颜色——紫色,在中性溶液中,石蕊试液不变色,显示紫色。
【题11】(2020·云南红河哈尼族彝族自治州·弥勒市一中)下表所列各组物质,物质之间按箭头方向不能
通过一步反应实现如图所示转化的是( )
A.A B.B C.C D.D
【答案】C
【详解】
A. 该组物质均可以一步反应:甲→乙: ,乙→丙:CO+2NaOH=Na CO+H O,甲
2 2 3 2
→丙: ,A错误;
B. 该组物质均可以一步反应:甲→乙: ,乙→丙: ,甲→丙:
,B错误;
C. 该组物质中,仅CaCO →Ca(OH) 不能一步反应得到,甲→乙: ,乙→丙:
3 2
CaO+H O=Ca(OH) ,C正确;
2 2
D. 该组物质均可以一步反应:甲→乙:HSO +2NaOH=Na SO +H O,乙→丙: ,
2 4 2 4 2
甲→丙:HSO +Zn=ZnSO+H ↑,D错误;
2 4 4 2故合理选项为C。
【题12】(2020·全国高一课时练习)下表中有三组物质,每组均有甲、乙、丙三种物质。
第Ⅰ组 第Ⅱ组 第Ⅲ组
甲 BaCl 溶液 盐酸 Cu(NO) 溶液
2 3 2
乙 FeCO KSO 溶液 HSO 溶液
3 2 4 2 4
丙 Fe NaOH溶液 MgCl 溶液
2
请回答下列问题:
(1)第Ⅲ组中有一种物质能与第______________组中的所有物质反应,这种物质是______________。
(2)第Ⅱ组物质中,与第Ⅰ组中的所有物质都不能发生反应的是______________,该物质能与第Ⅲ组中的所
有物质发生反应,其化学方程式分别为_____________、________、____________。
【答案】I HSO 溶液 NaOH溶液 Cu(NO )+2NaOH=2NaNO +Cu(OH) ↓
2 4 3 2 3 2
HSO +2NaOH=Na SO +2H O 2NaOH+MgCl =Mg(OH) ↓+2NaCl
2 4 2 4 2 2 2
【详解】
(1)第III组中的HSO 溶液可以与第I组中的氯化钡反应生成硫酸钡沉淀,与碳酸亚铁反应生成二氧化碳、
2 4
水和硫酸亚铁,与铁反应生成硫酸亚铁和氢气,可与所有物质发生反应。
(2)第Ⅱ组中的NaOH溶液与第I组中的所有物质都不能反应,但可以与第Ⅲ组中的硝酸铜反应生成氢氧化
铜沉淀和硝酸钠,与硫酸发生中和反应,与氯化镁反应生成氢氧化镁沉淀和氯化钠,与所有物质均能反应。
提分作业
【练1】下列关于物质的分类及反应均正确的是( )
A. 碳酸钙属于盐,可用于实验室制CO:CaCO +HSO ==== CaSO + H O + CO ↑
2 3 2 4 4 2 2
B. 铁属于较活泼金属,可用于实验室制H:6HCl + 2Fe === 2FeCl + 3H ↑
2 3 2
C. 纯碱属于碱,可与稀盐酸发生反应:2HCl + Na CO === 2NaCl + H O + CO ↑
2 3 2 2
D. 烧碱属于碱,可与稀硫酸反应:HSO + 2NaOH === Na SO + 2H O;
2 4 2 4 2
【答案】A
【练2】(2020·江西南昌市·高一期中)完成下列变化,不能通过一步化学反应实现的是
A.HC1→HNO B.CaO→CaCO C.CuO→CuSO D.CO→Na CO
3 3 4 2 3
【答案】D
【详解】
A. HC1与AgNO 反应生成氯化银和HNO,能一步实现,故A不符合;
3 3
B. CaO与二氧化碳在高温下可反应生成CaCO ,能一步实现,故B不符合;
3C. CuO与稀硫酸反应生成CuSO ,能一步实现,故C不符合;
4
D. CO需先与氧气反应生成二氧化碳,二氧化碳再与氢氧化钠溶液反应生成NaCO,不能一步实现,故D
2 3
符合;
故选D。
【练3】(2020·利辛县阚疃金石中学)下列关系式错误的是( )
A.酸性氧化物+碱性氧化物→盐
B.酸+碱性氧化物→盐+H
2
C.酸+碱→盐+水
D.难溶性碱→水+碱性氧化物
【答案】B
【详解】
A. 酸性氧化物与碱性氧化物反应生成盐,如二氧化碳与氧化钙反应生成碳酸钙,故A正确;
B. 酸与碱性氧化物反应生成盐和水,如盐酸与氧化钙反应生成氯化钙和水,故B错误;
C. 酸与碱反应生成盐和水,如盐酸与氢氧化钠反应生成氯化钠和水,故C正确;
D. 难溶性碱加热分解生成水和碱性氧化物,如氢氧化铁加热反应生成氧化铁和水,故D正确;
答案选B。
【练4】在Zn、ZnO、ZnCO 、盐酸和NaCl溶液中,每两种物质发生反应能生成ZnCl 的组合有(
3 2
)
A.2种 B.3种 C.4种 D.5种
【答案】B
【练5】(2020·全国高一课时练习)实现下列物质的转化时,只有加入酸才能通过一步反应实现的是
A.Fe O→Fe (SO ) B.Zn→ZnCl
2 3 2 4 3 2
C.NaOH→NaCl D.BaCl →BaSO
2 4
【答案】A
【详解】
A.Fe O 是难溶性碱性氧化物,只有与酸反应才能转化为盐,A符合题意;
2 3
B.活泼金属Zn可以与盐酸或CuCl 等比Zn活动性弱的金属的盐溶液通过置换反应得到ZnCl,B与题意
2 2
不符;
C.NaOH与盐酸或CuCl 等盐溶液反应都可得到NaCl,C与题意不符;
2
D.BaCl 与HSO 或可溶性硫酸盐反应都可得到BaSO,D与题意不符。
2 2 4 4
答案为A。
【练6】(2020·全国高一单元测试)构建知识网络,厘清物质间的相互转化关系是化学学习中的一种重要方法。如图中线段两端的物质在一定条件下可以发生反应。下列符合图示要求的是
A.①NaHCO ②CO ③BaCl
3 2 2
B.①NaCO ②Fe ③KCO
2 3 2 3
C.①Fe O ②CO ③Ba(NO )
2 3 3 2
D.①Ca(HCO ) ②SO ③NaCO
3 2 2 2 3
【答案】D
【详解】
A.NaHCO 和HCl,NaHCO 和Ca(OH) 、CO 和Ca(OH) 都能发生相应反应,BaCl 和Ca(OH) 不能发生
3 3 2 2 2 2 2
反应,A不符合题意;
B.NaCO 和HCl,NaCO 和Ca(OH) 、KCO 和Ca(OH) 都能发生相应反应,Fe不能和Ca(OH) 反应,B
2 3 2 3 2 2 3 2 2
不符合题意;
C.Fe O 能和HCl反应,不能和Ca(OH) 反应,CO,Ba(NO ) 均不能和Ca(OH) 反应,C不符合题意;
2 3 2 3 2 2
D.Ca(HCO ) 和HCl、Ca(HCO ) 和Ca(OH) 、SO 和Ca(OH) ,NaCO 和Ca(OH) 都能发生相应反应,D
3 2 3 2 2 2 2 2 3 2
符合题意。
答案为D。
【练7】(2020·全国高一)下图中,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁
在一定条件下通过置换反应可以转化为乙。下列四组选项中,符合图示要求的是
选项 甲 乙 丙 丁
A HSO NaSO NaOH NaCl
2 4 2 4
B BaCl KCO HCl KOH
2 2 3
C O CO CuO C
2
D Fe CuCl Zn HCl
2
A.A B.B C.C D.D
【答案】C【详解】
A.硫酸与氯化钠不能反应,氯化钠钠与氢氧化钠也不反应,氢氧化钠与硫酸钠也不反应,故A错误;
B.氯化钡和氢氧化钾不能反应,氢氧化钾也不能通过置换反应生成碳酸钾,故B错误;
C.氧气与CO反应生成二氧化碳,CO与氧化铜反应生成铜和二氧化碳,氧化铜与C反应生成二氧化碳和
铜,过量氧气与C反应生成二氧化碳,少量氧气与C反应生成CO,故C正确;
D.盐酸不能与铜发生置换反应生成氯化铜和氢气,故D错误;
故选:C。
【练8】(2021·哈尔滨市第三十二中学校高一期末)铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中
常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分①、②、③、④表示物质间的反应,其
中对应的四种反应类型正确的是
A.复分解反应、复分解反应、化合反应、置换反应
B.复分解反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
【答案】C
【详解】
本题图形中物质间的反应分别为① (复分解反应);
② (复分解反应);
③ (置换反应);
④ (置换反应)。
故答案选:C。
【练9】(2020·重庆市云阳高级中学校高一月考)不用其他试剂,用最简单的方法鉴别下列物质:
①NaOH溶液,②Mg(NO) 溶液,③CuSO 溶液,④KCl溶液,正确的鉴别顺序是
3 2 4A.①②③④ B.③④②① C.④①②③ D.③①②④
【答案】D
【分析】
不用其他试剂进行鉴别,通常观察颜色、闻气味,再用已经鉴别的物质鉴别其它物质。
【详解】
观察题中待鉴别的物质,溶液呈蓝色的是③CuSO 溶液,其余为无色溶液。各取少量三种无色溶液于试管
4
中,分别滴加CuSO 溶液,生成蓝色沉淀的是①NaOH溶液,另两溶液无明显变化。又分别取少量无明显
4
变化的溶液于试管中,滴加NaOH溶液,有白色沉淀的为②Mg(NO) 溶液,余下的为④KCl溶液。
3 2
本题选D。
【点睛】
若待鉴别的一组物质均无色无味,则可分别取少量进行两两混合,列表记录实验现象,再据现象进行推断,
从而确定待鉴别物质。
【练10】(2021·河北区·天津二中高一开学考试)各物质间有着一定的转化关系,下列各组物质间可以按
下图所示直接转化的是
A.Fe→Fe O→FeSO →Fe B.CO→CO →HCO→CO
2 3 4 2 2 3
C.NaOH→NaCl→Na CO→NaOH D.HCl→CuCl →BaCl →HCl
2 3 2 2
【答案】D
【详解】
A、Fe O→FeSO 不能一步实现转化,故A错误;
2 3 4
B、HCO→CO不能一步实现转化,故B错误;
2 3
C、NaCl→Na CO 不能一步实现转化,故C错误;
2 3
D、HCl能够与Cu(OH) 反应生成CuCl ;Ba(OH) 与CuCl 反应生成BaCl ;HSO 和BaCl 反应生成HCl,
2 2 2 2 2 2 4 2
能一步实现转化,故D正确;
故选D。
【点睛】
本题的易错点为A,要注意氧化铁与硫酸反应生成硫酸铁,不是硫酸亚铁。
【练11】有物质①O ②Fe ③HSO ④NaOH ⑤CuCl ,请回答:
2 2 4 2
(1)写出一个上述物质发生化合反应的化学方程式_______________________________________________;
(2)写出两个上述物质发生复分解反应的化学方程式_____________________________________________;
(3)写出两个上述物质发生置换反应的化学方程式_______________________________________________。【答案】(1)2O +3FeFe O
2 3 4
(2)H SO +2NaOH====Na SO +2HO CuCl +2NaOH====Cu(OH) ↓+2NaCl
2 4 2 4 2 2 2
(3)Fe+HSO ====FeSO+H↑ Fe+CuCl ====Cu+FeCl
2 4 4 2 2 2
【练12】(2020·平潭县新世纪学校高一月考)铜器久置于空气中会和空气中的 、 、 作用产
生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为 ],“铜绿”能跟酸反应生成铜
盐、 和 。某同学利用如图所示的一系列反应实现了“铜→铜绿→……→铜”的转化。
铜 铜绿 CuCl Cu(OH) CuO Cu
2 2
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?__________。
(2)请写出反应②的化学方程式:________。
(3)上述转化过程中属于化合反应的是________(填序号)。
(4)写出反应⑤的化学方程式和反应类型___________、____________。
【答案】铜盐、碳酸盐、碱式盐、含氧酸盐(任选三个即可)
① CuO+H Cu+H O 置换反应
2 2
【分析】
铜与 、 、 发生化合反应生成铜绿 , 与盐酸反应生成氯化铜,
氯化铜与碱反应生成氢氧化铜,氢氧化铜受热分解生成氧化铜,氢气还原氧化铜得到铜单质,据此分析解
答。
【详解】
(1)铜绿是 ,根据盐的分类,它可以是铜盐、碳酸盐、碱式盐、含氧酸盐等;
(2)由题给信息可知,反应②的化学方程式是 ;
(3)反应①是化合反应。
(4)由题给信息,反应⑤的化学方程式是 ,属于置换反应。