文档内容
第 04 讲 离子反应与离子方程式
知识导航
课前引入
三国时期,诸葛亮在七擒孟获的过程中,
蜀军由于误饮哑泉水、个个不能言语,生命危
在旦夕。幸得巧遇老叟,指点迷津——饮用万
安溪安乐泉水可解毒。终于转危为安,渡过难
关。
哑泉水为何能致哑,万安溪安乐泉水又是
什么灵丹妙药呢?
原来哑泉水中含有较多的硫酸铜,人喝了
含铜盐较多的水就会中毒。而万安溪安乐泉水
中含有较多的碱,铜离子遇氢氧根离子发生离
子反应生成沉淀而失去了毒性。
思考与交流:什么叫离子反应?离子反应要发生具备什么条件呢?实验探究
实验 现象 是否发生化学反应 判断的依据
向盛有2 mL的CuSO 溶液的试
4
管中加入2 mL的NaCl溶液
向盛有2 mL的CuSO 溶液的试
4
管中加入2 mL的BaCl 溶液
2
CuSO 溶液与BaCl 溶液反应的深入分析:
4 2
CuSO 与BaCl 的电离方程式
4 2
混合前溶液中所含离子
混合后溶液中剩余离子
Ba2+与SO2-发生反应,生成难溶性沉淀:Ba2++SO2- ===BaSO ↓;
该反应的本质 4 4 4
而Cu2+ 与Cl- 没有发生化学反应。
思考与交流:请写出下列几个反应,对比反应前后溶液中的离子,思考这些反应的实质是什么。
(1)NaCO + Ca(OH)
2 3 2
(2)NaCO + HCl(过量)
2 3
(3)Ca(OH) +HCl
2
知识精讲
一、离子反应
1. 概念:电解质在溶液中的反应实质上是离子之间的反应,有离子参加的化学反应称为离子反应。
2. 本质:离子反应总是向着某种离子浓度减小的方向进行。
3. 离子反应的发生条件:
生成难溶物(沉淀)、气体或难电离物(弱酸、弱碱、水),只要具备上述条件之一,反应就能发生。
二、离子方程式
1.定义:用实际参加反应的离子符号表示离子反应的式子,叫做离子方程式。
2.书写步骤:
①写:写出正确的化学反应方程式
②拆:把易溶于水、易电离的物质(如强酸、强碱、可溶性盐)写成离子的形式
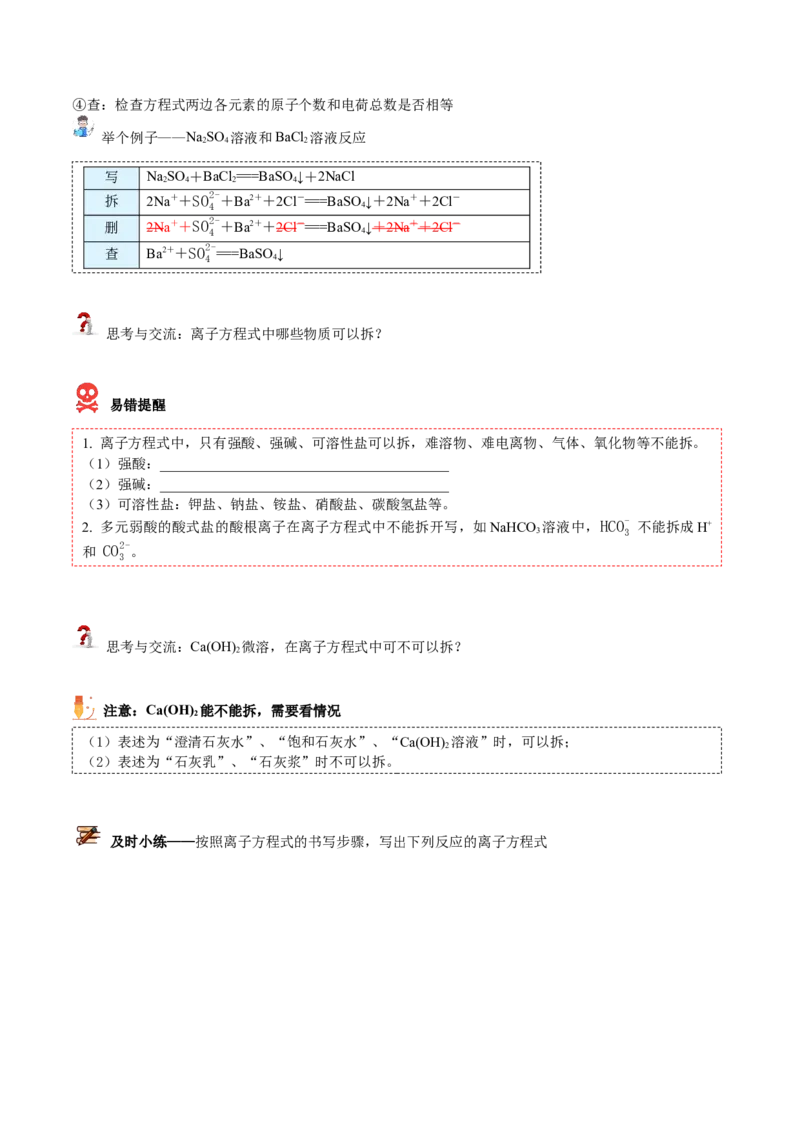
③删:并将把不参加反应的离子从方程式两端等量删去,并将化学计量数化成最简整数比④查:检查方程式两边各元素的原子个数和电荷总数是否相等
举个例子——NaSO 溶液和BaCl 溶液反应
2 4 2
写 NaSO +BaCl ===BaSO ↓+2NaCl
2 4 2 4
拆 2Na++SO2-+Ba2++2Cl-===BaSO ↓+2Na++2Cl-
4 4
删 2Na++SO2-+Ba2++2Cl-===BaSO ↓+2Na++2Cl-
4 4
查
Ba2++SO2-
===BaSO ↓
4 4
思考与交流:离子方程式中哪些物质可以拆?
易错提醒
1. 离子方程式中,只有强酸、强碱、可溶性盐可以拆,难溶物、难电离物、气体、氧化物等不能拆。
(1)强酸:_________________________________________
(2)强碱:_________________________________________
(3)可溶性盐:钾盐、钠盐、铵盐、硝酸盐、碳酸氢盐等。
2. 多元弱酸的酸式盐的酸根离子在离子方程式中不能拆开写,如NaHCO 溶液中,HCO- 不能拆成H+
3 3
和
CO2-
。
3
思考与交流:Ca(OH) 微溶,在离子方程式中可不可以拆?
2
注意:Ca(OH) 能不能拆,需要看情况
2
(1)表述为“澄清石灰水”、“饱和石灰水”、“Ca(OH) 溶液”时,可以拆;
2
(2)表述为“石灰乳”、“石灰浆”时不可以拆。
及时小练——按照离子方程式的书写步骤,写出下列反应的离子方程式(1)铁和稀硫酸反应
(2)向澄清石灰水中通入少量二氧化碳
(3)氧化铜溶于稀盐酸
(4)稀盐酸和氢氧化镁反应
(5)烧碱和醋酸反应
思考与交流
(1)下表都是酸和碱的中和反应,请书写对应的化学方程式与离子方程式。
反应物 化学方程式 离子方程式
HCl+NaOH
HSO + KOH
2 4
HNO + Ba(OH)
3 2
HClO+KOH
4
HSO +
2 4
Ba(OH)
2
(2)观察上述方程式,思考两种方程式在表示酸碱中和反应时,其含义有什么不同?
三、离子方程式的意义
离子方程式不仅可以表示某一个具体的化学反应,还可以表示同一类型的离子反应。
及时小练——把下列离子方程式改写成化学方程式。(1)Ba2+ + SO2- ====== BaSO↓
4 4
(2)2H+ + CO2- === CO↑+ HO
3 2 2
思考与交流:判断下列离子方程式书写是否正确。
(1)2Fe + 6H+ === 2Fe3+ + 3H↑ ( )
2
(2)Cu + 2H+ === Cu2+ + H↑ ( )
2
(3)氧化铜与盐酸反应:O2- + 2H+ === HO ( )
2
(4)CaCO 溶于醋酸溶液:CaCO + 2H+ === Ca2+ + HO + CO ↑( )
3 3 2 2
(5)Fe3+ + Cu === Cu2+ + Fe2+ ( )
(6)Fe2++Cl === Fe3++2Cl- ( )
2
(7)HSO 和Ba(OH) 溶液反应:H++SO2- +OH- +Ba2+===BaSO ↓+H O ( )
2 4 2 4 4 2
四、离子方程式的正误判断
(1)物质间反应是否符合反应的客观事实;
(2)物质拆写是否正确;
(3)是否符合原子守恒和电荷守恒;
(4)方程式整体的阴、阳离子配比是否正确。
经典例题
题型一:离子反应的概念与判断
【例1】(2020·江西高一上学期期末)根据化学反应前后是否有离子参加或离子生成,可以将化学反应分
为离子反应和非离子反应。下列化学反应中不属于置换反应但属于离子反应的是( )
A.CO + CuO ===== Cu + CO B.2Na + 2HO === 2NaOH + H ↑
2 2 2
C.Fe + CuSO === FeSO + Cu D.2FeCl + Cu === 2FeCl + CuCl
4 4 3 2 2
【变1】(2020·黄石市育英高中有限公司)下列对于离子反应的表述正确的是( )
A.离子反应中一定有沉淀生成
B.反应中有气体生成的反应一定是离子反应
C.复分解离子反应发生的条件之一是有难电离物质生成D.非电解质二氧化碳与足量烧碱溶液的反应不属于离子反应
题型二:离子方程式的书写
【例2】离子反应方程式书写:(注意写化学方程式不给分)
(1)用盐酸中和烧碱,请写出其反应的离子方程式: 。
(2)用稀硫酸清洗铁锈(Fe O),请写出其反应的离子方程式: 。
2 3
(3)用足量的澄清石灰水检验二氧化碳,请写出其反应的离子方程式: 。
(4)用铝片与硝酸汞溶液反应,请写出其反应的离子方程式: 。
(5)用醋酸可以溶解碳酸钙,请写出其反应的离子方程式: 。
【变2】写出下列离子方程式:
(1)HSO + NaOH:___________________________________________________________;
2 4
(2)HSO +Ba(OH) :___________________________________________________________。
2 4 2
(3)Mg + HSO :______________________________________________________________;
2 4
(4)MgO + HCl:____________________________________________________________。
(5)NaOH + CHCOOH:___________________________________________________________;
3
(6)Ca(OH) (澄清石灰水) + CO(少量):____________________________________________。
2 2
题型三:离子方程式的正误判断
【例3】判断下列反应的离子方程式是否正确,在括号中打“√”或“×”。
(1)盐酸与碳酸钡反应:CO2- + 2H+ === CO↑ + H O( )
3 2 2
(2)铝与盐酸反应:Al + 6H+ === Al3+ +3H↑( )
2
(3)硝酸银溶液中加入铜粉:Ag+ + Cu === Cu2+ + Ag( )
(4)Mg与醋酸溶液反应:Mg + 2H+ === Mg2+ + H ↑( )
2
(5)碳酸氢钙溶液与盐酸反应:Ca(HCO ) + 2H+ === Ca2+ + 2H O + 2CO ↑( )
3 2 2 2
(6)澄清石灰水与盐酸反应:Ca(OH) + 2H+ === 2HO + Ca2+( )
2 2
(7)碳酸钠与氯化钙混合:CO2- + Ca2+ === CaCO ↓( )
3 3
(8)稀硫酸与氢氧化钡溶液混合:H+ + SO2- + Ba2+ + OH- === HO + BaSO↓( )
4 2 4
(9)氧化铁与稀盐酸混合: Fe O + 6H+ === 2Fe3+ + 3H O( )
2 3 2
【变3】(2021·眉山冠城七中实验学校高一期末)下列离子方程式正确的是
A.用醋酸除去水垢:2H++CaCO =Ca2++CO ↑+H O
3 2 2
B.氯化亚铁溶液中通入氯气:Fe2++Cl=Fe3++2Cl-
2
C.石灰乳与稀盐酸反应:Ca(OH) +2H+=Ca2++2H O
2 2D.CO 通入氯化钙溶液:Ca2++H O+CO=CaCO ↓+2H+
2 2 2 3
题型四:离子反应的意义
【例4】(2020·安徽省肥东县第二中学高一月考)能用离子方程式 H++OH-=H O 表示的化学反应是
2
A.Cu(OH) (s)和 HSO (aq)的反应 B.澄清石灰水和 HCl(aq)的反应
2 2 4
C.KOH(aq)和 CHCOOH 的反应 D.Ba(OH) (aq)和 HSO (aq)的反应
3 2 2 4
【变4-1】(2021·内蒙古杭锦后旗奋斗中学高一期中)下列各组的两种物质在溶液中的反应,可用同一离
子方程式表示的是
A.氢氧化钠与盐酸;氢氧化钠与碳酸
B.BaCl 溶液与NaSO 溶液;Ba(OH) 溶液与HSO 溶液
2 2 4 2 2 4
C.NaCO 溶液与硝酸溶液,BaCO 溶液与硝酸溶液
2 3 3
D.石灰石与硝酸反应;石灰石与盐酸
【变4-2】下列离子方程式中,只能表示一个化学反应的是
①Fe+Cu2+=Fe2++Cu ②Ba2++2OH-+2H++ =BaSO ↓+2H O
4 2
③Cl+H O=H++Cl-+HClO ④ +2H+=CO ↑+H O
2 2 2 2
⑤Ag++Cl-=AgCl↓
A.只有③ B.②③ C.③⑤ D.①④
【例5】(2020·安徽省肥东县第二中学高一月考)(1)书写下列反应的离子方程式。
①NaCl 溶液和 AgNO 溶液_____
3
②Ba(OH) 溶液和 HSO 溶液_____
2 2 4
③MgO 与稀盐酸反应_____
④NaHSO 与 NaHCO 溶液_____
4 3
(2)写出一个下列离子方程式表示的化学方程式。
①CO +2H+=CO ↑+HO:_____
2 2
②Ag++Cl-=AgCl↓:_____
③Cu2++2OH-=Cu(OH) ↓:_____
2④SO +2OH-=SO +HO:_____
2 2
提分特训
【题1】下列反应能够发生且属于离子反应的是( )
A.KMnO 加热分解制取O B.氢氧化铜和硫酸镁反应
4 2
C.用稀硫酸清洗铁锈 D.NH 遇HCl气体生成白烟
3
【题2】(2021·南宁市英华学校高一期中)下列化学反应的离子方程式正确的是
A.碳酸钙与盐酸溶液反应:
B.铁钉放入稀硫酸中:
C.碳酸氢钠与稀盐酸反应:
D.氢氧化钡溶液与稀硫酸反应:
【题3】(2021·南宁市英华学校高一期中)下列物质中,不能发生反应的是
A. 和 B. 和
C. 和KOH D. 和HCl
【题4】(2019·全国高一课时练习)下列各组反应中,不能用同一个离子方程式表示的是( )
A.盐酸分别与氢氧化钠溶液、澄清石灰水反应
B.硫酸分别与氢氧化钠溶液、氢氧化钡溶液反应
C.硝酸分别与碳酸钠溶液、碳酸钾溶液反应
D.锌分别与稀盐酸、稀硫酸反应
【题5】(2022·全国高三专题练习)下列离子方程式正确的是
A.Mg溶于稀HSO 中;Mg+2H++SO =MgSO ↓+H ↑
2 4 4 2
B.MgO溶于稀HNO 中,MgO+2H+=Mg2++H O
3 2C.Mg(OH) 与稀盐酸反应:H++OH-=H O
2 2
D.MgSO 溶液与Ba(OH) 溶液混合:Mg2++2OH-=Mg(OH) ↓
4 2 2
【题6】离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在________ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)现有铜、氯化铁溶液、盐酸、硝酸银溶液、氧化铝、二氧化碳、氧气七种物质,两两能发生反应的
反应中,属于离子反应的有 种,属于置换反应的有 种。
【题7】写出下列反应的离子方程式
(1)硫酸铜和氯化钡:_____________________________________________________;
(2)锌和硫酸铜溶液反应:_________________________________________________;
(3)碳酸钙和稀盐酸反应:_________________________________________________;
(4)氢氧化钠与氯化镁反应:_______________________________________________;
(5)氢氧化铜与硫酸反应:_________________________________________________;
(6)醋酸与碳酸钙反应:___________________________________________________。
【题8】(2020·安徽省肥东县第二中学高一月考)A、B、C、D 四种可溶性盐,其阳离子分别是 Na+、
Ba2+、Cu2+、Ag+中的某一种,阴离子分别是 Cl-、SO 、CO 、NO 中的某一种。现做以下实验:①将
四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试
管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无
明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为:A___________B___________; C___________;
D___________。
(2)写出下列反应的离子方程式:
①B+D→:_____
②C+HCl→气体:_____
提分作业
【练1】(2020·伊美区第二中学高一月考)对于离子反应的表述正确的是( )
A.离子反应中一定有沉淀生成B.反应中有气体生成的反应一定是离子反应
C.复分解型离子反应是一定有沉淀、气体和水生成的反应
D.Fe O 与稀硫酸的反应一定属于离子反应
2 3
【练2】(2020·全国高一课时练习)下列反应的离子方程式书写正确的是
A.碳酸钙与盐酸反应:CO +2H+=H O+CO↑
2 2
B.稀HSO 与铁粉反应:2Fe+6H+=2Fe3++3H ↑
2 4 2
C.氢氧化钡溶液与稀HSO 反应:Ba2++ =BaSO ↓
2 4 4
D.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
【练3】(2019·全国)下列化学方程式不能用Ba2++SO ═BaSO
4
↓来表示的是( )
A.Ba(NO )+H SO ═BaSO ↓+2HNO
3 2 2 4 4 3
B.BaCO +H SO ═BaSO ↓+CO ↑+H O
3 2 4 4 2 2
C.NaSO +BaCl ═BaSO ↓+2NaCl
2 4 2 4
D.BaCl +H SO ═BaSO ↓+2HCl
2 2 4 4
【练4】(双选)(2020·安徽省肥东县第二中学高一月考)下列离子方程式改写成化学方程式正确的是
A.Cu2++2OH﹣=Cu(OH) ↓ CuSO +2NaOH=Cu(OH) ↓+Na SO
2 4 2 2 4
B. +2H+=CO ↑+H O BaCO +2HCl=BaCl +CO ↑+H O
2 2 3 2 2 2
C.Ca2++ =CaCO ↓ Ca(NO ) +Na CO =CaCO ↓+2NaNO
3 3 2 2 3 3 3
D.H++OH﹣=H O Ba(OH) +H SO =BaSO +2H O
2 2 2 4 4 2
【练5】(2021·内蒙古杭锦后旗奋斗中学高一期中)下表中对离子方程式的评价合理的是
选项 化学反应及其离子方程式 评价
A HSO 溶液与Ba(OH) 溶液反应:H++ SO +Ba2++OH-=BaSO↓+HO 正确
2 4 2 4 2
错误,碳酸镁不应写成离
B 向碳酸镁浊液中加入足量稀盐酸:CO +2H+=CO↑+HO
2 2 子形式
C 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3HO= 正确
2Fe(OH)↓+3H+
3
D 向NaOH溶液中加入 CuCl 溶液:OH−+ Cu2+ = Cu(OH)↓ 正确
2 2
A.A B.B C.C D.D
【练6】下列离子方程式中,正确的是( )
A.氢氧化钡溶液和稀硫酸反应:Ba2+ + OH- + H+ + SO2- === BaSO↓+ HO
4 4 2
B.大理石和硝酸反应:CO2- + 2H+ === HO + CO↑
3 2 2
C.氯化铵晶体和石灰粉共热产生氨气:NH+ + OH- ===== NH ↑+ HO
4 3 2
D.醋酸溶液与氨水反应:CHCOOH + NH ·HO === NH+ + CHCOO- + HO
3 3 2 4 3 2
【练7】(2018·河北省隆化存瑞中学高一月考)按要求填空:
(1)Fe(SO)(写出电离方程式)_____________________________。
2 4 3
(2)氢氧化钡溶液和稀硫酸反应(写出离子方程式)_______________________。
(3)碳酸钙和盐酸反应(写出离子方程式)_______________________________。
(4)碳酸氢钠和氢氧化钠反应(写出离子方程式)__________________________________。
【练8】写出下列反应的离子或化学方程式
(1)写出氢氧化铜与稀硫酸反应的离子方程式:_______________________。
(2)写出碳酸氢钠与稀盐酸反应的离子方程式:_______________________。
(3)写出离子方程式H++OH-=H O相对应的一个化学方式:________________________。
2
(4)写出铁与硫酸铜溶液反应的离子方程式:____________________________。
(5)写出离子方程式Ag++Cl-=AgCl↓相对应的一个化学方程式:___________________________。