文档内容
第 01 讲 硫、二氧化硫
知识导航
课前引入
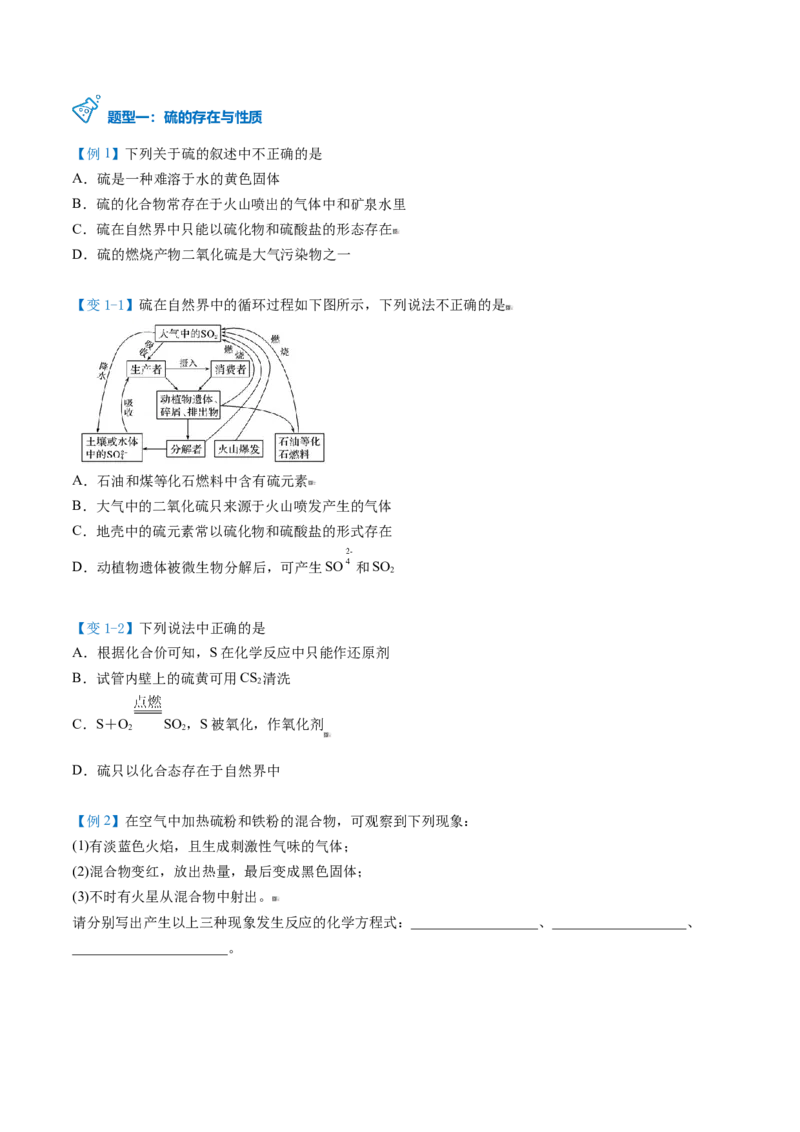
在印度尼西亚东部有一座著名的活火山——卡哇伊真火山,火山口以富含硫磺而著称,为著名的旅游
胜地,每年都吸引大量游客慕名前来参观。
然而,这些硫磺被称为“恶魔的黄金”。
这个火山矿每天生产14吨硫磺,当地很多青壮年男子冒险去火山口采硫磺矿谋生。
要采硫磺,要先用金属杆攻击大的硫磺,令其破碎成小块,然后用漏斗装着大概150磅-200磅的硫磺
返回,这一趟大概收入只有5美元。
硫燃烧产生毒烟,这些毒烟甚至能够融化人类的牙齿。而这些采硫人只有少数人有防毒面具,更多人
依靠湿巾或抹布覆盖他们的嘴巴,以阻止喉咙和肺部吸入腐蚀性气体。
近40年来,已经有超过200名矿工死于硫磺矿内所产生的有毒气体,可是为了生活,他们只能继续这
样坚持到底。而因为硫磺燃烧气体的有毒性,多数矿工的寿命都不超过50岁。模块一 硫
知识精讲
一、硫元素的“位——构——性”
元素位置 原子结构 元素性质
第____周期 容易得到2个电子,非金属性:S ___ Cl
第______族 主要化合价:_______________________
二、硫元素的存在形式
三、硫单质的物理性质
俗名 颜色状态 溶解性
硫黄 ____色晶体,易研成粉末 不溶于水,微溶于酒精,易溶于______
资料卡片——二硫化碳
二硫化碳是一种无机物,化学式为 CS₂,常见溶剂,无色液体,可溶解硫单质。二硫化碳用于制
造人造丝、杀虫剂、促进剂等,也用作溶剂。
四、硫的化学性质(1)当银饰所处的环境空气质量不佳(含有一些酸性气体如硫化氢)或使用硫磺皂时,银会和空气中的
硫元素(或硫单质)发生化学反应,产生硫化银,也就是我们常说的银垢。
(2)汞有毒,实验室里不慎洒落汞(或打破水银温度计),可撒上硫粉进行处理。
(3)FeS、Cu S均为不溶于水的黑色固体。
2
思考与交流
(1)从氧化还原角度分析,硫与金属单质,非金属单质反应时分别体现什么性质?
(2)对比金属单质与氯气,硫反应的产物,可以得出什么结论?
(3)类比Cl 与NaOH溶液的反应,试着写出S与NaOH溶液加热时的反应。
2
(4)从氧化还原的角度,试着写出S和浓硫酸在加热时的反应。
五、硫的用途
用于制造硫酸和硫磺、硫化天然橡胶,还被用来杀真菌,用做化肥,也可用于制药和黑火药。
资料卡片——黑火药
黑火药的成分为“一硫二硝三木炭”(S + 2KNO + 3C === KS + N↑ + 3CO↑)
3 2 2 2
明辨是非
(1)在自然界中有游离态的硫存在( )
(2)试管内壁的硫粉可以用热碱液或CS 除去( )
2
(3)硫与金属反应,生成金属的低价态化合物( )
(4)硫的氧化性比氯气强( )
(5)硫是一种黄色的能溶于水的晶体( )
(6)硫的化合物常存在于火山喷出的气体中和矿泉水里( )
(7)硫在空气中燃烧的产物是二氧化硫,硫在纯氧中燃烧的产物是三氧化硫( )
(8)我国古代四大发明之一的黑火药是以硫黄等为原料配制而成的( )
对点训练题型一:硫的存在与性质
【例1】下列关于硫的叙述中不正确的是
A.硫是一种难溶于水的黄色固体
B.硫的化合物常存在于火山喷出的气体中和矿泉水里
C.硫在自然界中只能以硫化物和硫酸盐的形态存在
D.硫的燃烧产物二氧化硫是大气污染物之一
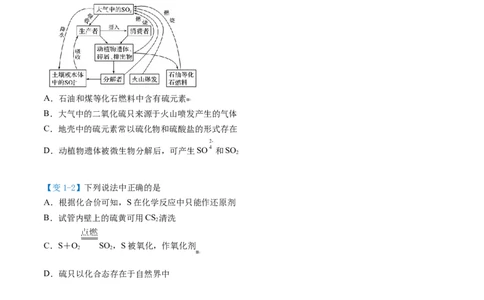
【变1-1】硫在自然界中的循环过程如下图所示,下列说法不正确的是
A.石油和煤等化石燃料中含有硫元素
B.大气中的二氧化硫只来源于火山喷发产生的气体
C.地壳中的硫元素常以硫化物和硫酸盐的形式存在
D.动植物遗体被微生物分解后,可产生SO 和SO
2
【变1-2】下列说法中正确的是
A.根据化合价可知,S在化学反应中只能作还原剂
B.试管内壁上的硫黄可用CS 清洗
2
C.S+O SO ,S被氧化,作氧化剂
2 2
D.硫只以化合态存在于自然界中
【例2】在空气中加热硫粉和铁粉的混合物,可观察到下列现象:
(1)有淡蓝色火焰,且生成刺激性气味的气体;
(2)混合物变红,放出热量,最后变成黑色固体;
(3)不时有火星从混合物中射出。
请分别写出产生以上三种现象发生反应的化学方程式:__________________、___________________、
______________________。【变2】黑火药爆炸时发生的反应是S+2KNO+3C KS+3CO↑+N↑,反应中的氧化剂是__________,每
3 2 2 2
生成1mol CO 转移____mol电子。分离黑火药中三种成分的方法是将黑火药溶于水,过滤,蒸发滤液得
2
________________;将滤纸上的物质溶于__________,过滤,滤纸上留下的物质是_________。
【例3】下列化合物能用相应的单质直接化合得到的是____________
①CuS ②FeS ③HCl ④SO ⑤SO ⑥FeCl ⑦CuCl
2 3 2 2
模块二 二氧化硫
知识精讲
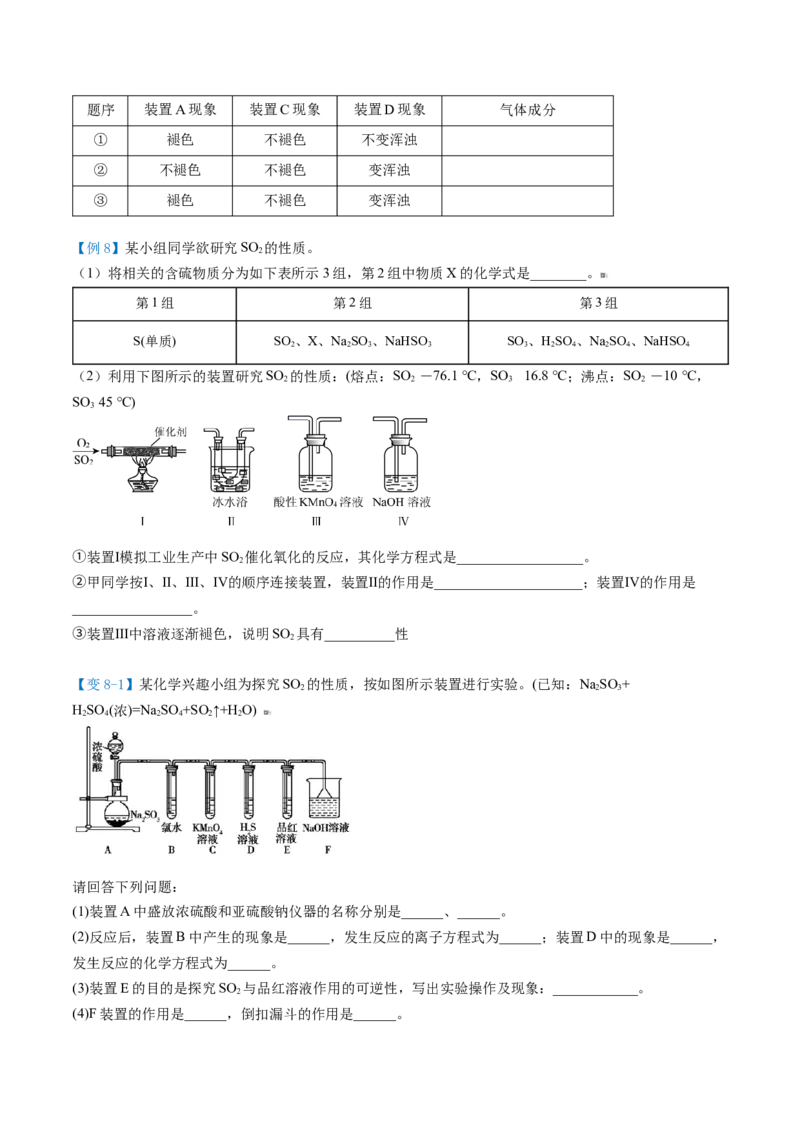
实验探究——SO 溶于水
2
实验操作 把充满SO 、塞有橡胶塞的试管倒立在水中,在水面下打开橡胶塞。
2
实验现象 试管内_________________
实验结论 _______________________
一、二氧化硫的物理性质
颜色 气味 状态 密度 溶解性 沸点
无色 刺激性 气体 比空气大 易溶于水,1体积水能溶解40体积SO 较低,易液化
2
资料卡片——可逆反应
1.定义:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
2.表示:书写可逆反应的方程式不用“===”,而用“ ”连接。
3.特点:(1)双向性:正反应和逆反应;
(2)双同性:同一条件,同时进行;
(3)共存性:反应物与生成物共存。
二、二氧化硫的化学性质
1.具有酸性氧化物的通性(与CO 类似)
2
(1)与水反应(可逆反应):________________________________________________
(2)与碱性氧化物反应(如CaO):__________________________________________
思考与交流(1)CO 通入澄清石灰水,现象是?如果通入过量CO 呢?
2 2
(2)SO 通入澄清石灰水至过量,现象是?
2
(3)与碱反应:a. 少量SO + 澄清石灰水:_________________________________(现象:________)
2
b. 过量SO + 澄清石灰水:_________________________________(现象:________)
2
2.SO 的还原性(强)与氧化性(弱)
2
实验探究——SO 的漂白性
2
实验操作 实验现象 实验结论
用试管取2 mL SO 的水溶液,向
2
其中滴入1~2滴品红溶液,振
荡,观察溶液的颜色变化。
然后加热试管,注意通风,再观
察溶液的变化。
3.SO 的漂白性
2
(1)SO 具有漂白作用,能使品红溶液褪色,但不能使酸碱指示剂褪色。
2
(2)漂白原理:SO 与有色物质结合生成了不稳定的无色物质,加热(或见光、长久放置)后,不稳定的
2
无色物质又会发生分解,恢复到原来的颜色。
我们学过的,有漂白性的还有哪些物质?归纳总结——常见物质的漂白原理
漂白类型 实例 漂白原理 特点
HClO、NaClO、
氧化型 将有色物质氧化使其失去原有的颜色 不可逆
NaO、HO
2 2 2 2
SO 使品红溶液 与有色物质结合,生成不稳定的无色
加合型 2 可逆
褪色 物质
活 性 炭 、
疏松多孔,表面积较大,可以吸附一 物理变化,部分吸附剂可重复使
吸附型 Al(OH) 、
3
些有色物质 用
Fe(OH) 胶体
3
三、二氧化硫的用途
1. 工业上常用SO 来漂白纸浆、毛、丝等;
2
2. SO 可用于杀菌消毒,还是一种食品添加剂。
2
资料卡片——食品添加剂SO
2
SO 作为食品添加剂有多种用途,如在食糖制备过程中作漂白剂,葡萄酒、干果制作中添加适量 SO 作
2 2
防腐剂、抗氧化剂,但SO 作为食品添加剂应严格控制用量。
2
归纳总结——SO 的性质
2
思考与交流(1)如何鉴别SO 与CO?
2 2
(2)SO 通入BaCl 溶液,能否产生白色沉淀?为什么?
2 2
(3)若想在(2)中产生白色沉淀,可以如何操作?
对点训练
题型二:二氧化硫的漂白性
【例4】下列物质能使品红溶液褪色,且褪色原理基本相同的是( )
①活性炭 ②新制氯水③二氧化硫 ④臭氧 ⑤过氧化钠 ⑥双氧水
A.①②④ B.②③⑤ C.②④⑤⑥ D.③④⑥
【变4-1】下列有色溶液褪色原理相同的是
① 使品红溶液褪色 ② 使品红溶液褪色 ③将 加入含酚酞的水溶液中,溶液先变红后褪色
④ 使酸性 溶液褪色
A.④② B.②④ C.②③ D.①④
【变4-2】Cl 和SO 都具有漂白作用,能使品红溶液褪色。若将等物质的量的Cl、SO 混合后再通入品红
2 2 2 2
与BaCl 的混合溶液,能观察到的现象是( )
2
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①② B.①③ C.②③ D.②④
题型三:二氧化硫的沉淀问题
【例5】将SO 气体通入BaCl 溶液至饱和,未见有沉淀生成,继续通入另一种气体仍无沉淀产生,则通入
2 2
的气体可能是
① O ②Cl ③NH ④HS ⑤CO
2 2 3 2 2
A.②③④ B.⑤ C.①⑤ D.①②⑤
【变5】将SO 气体通入BaCl 溶液至饱和,未见有沉淀生成,继续通入或加入另一种物质仍无沉淀产生,
2 2
则通入或加入的物质不可能是
A.氨水 B.CO C.过氧化氢溶液 D.SO
2 3题型四:二氧化硫的性质综合
【例6】下列有关SO 的说法错误的是
2
A.SO 能与NaOH溶液反应,说明SO 是酸性氧化物
2 2
B.SO 通入溴水,溴水褪色,说明SO 有还原性
2 2
C.SO 通入HS溶液中有浅黄色沉淀生成,说明SO 有氧化性
2 2 2
D.SO 气体能使酸性高锰酸钾溶液褪色,说明SO 有漂白性
2 2
【变6-1】下列离子方程式正确的是( )
A.向NaOH溶液中通入少量的SO:SO+OH-===
2 2
B.向新制氯水中通入少量的SO:Cl+SO+2HO===4H++2Cl-+
2 2 2 2
C.将SO 通入饱和NaHCO 溶液:2H++ ===HO+CO↑
2 3 2 2
D.将SO 通入BaCl 溶液:SO+HO+Ba2+===BaSO↓+2H+
2 2 2 2 3
【变6-2】少量的SO 通入下列物质中,能发生反应,但无沉淀产生的是( )
2
①溴水 ②Ba(OH) 溶液 ③澄清石灰水 ④NaCO 溶液 ⑤稀硫酸 ⑥HS溶液 ⑦NaSO 溶液
2 2 3 2 2 3
A.仅① B.仅①④⑤
C.仅④⑥⑦ D.仅①④⑦
【例7】除去二氧化碳中混有的少量二氧化硫气体,不可选用的试剂是( )
A.饱和碳酸钠溶液 B.高锰酸钾溶液
C.溴水 D.饱和碳酸氢钠溶液
【变7】已知混合气体中可能含有SO 或CO 中的一种或两种,设计成以下装置进行鉴别:
2 2
(1)B中应该装下列________(填编号)试剂。
A.NaCl溶液 B.酸性KMnO 溶液 C.盐酸 D.澄清石灰水
4
(2)A中品红溶液的作用是:______________________________________________;
C中品红溶液的作用是:______________________________________________。
(3)D中澄清石灰水的作用是:____________________________________________。
(4)根据实验现象,判断气体成分:题序 装置A现象 装置C现象 装置D现象 气体成分
① 褪色 不褪色 不变浑浊
② 不褪色 不褪色 变浑浊
③ 褪色 不褪色 变浑浊
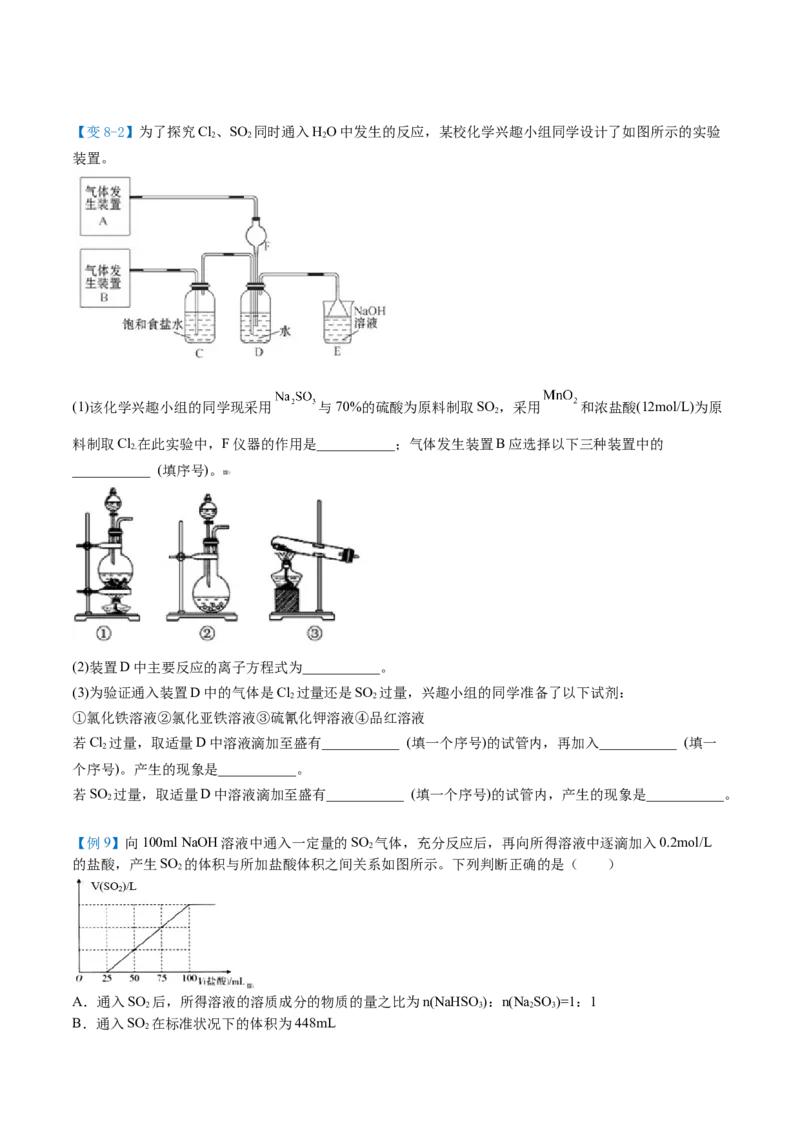
【例8】某小组同学欲研究SO 的性质。
2
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是________。
第1组 第2组 第3组
S(单质) SO、X、NaSO、NaHSO SO、HSO、NaSO、NaHSO
2 2 3 3 3 2 4 2 4 4
(2)利用下图所示的装置研究SO 的性质:(熔点:SO -76.1℃,SO 16.8 ℃;沸点:SO -10℃,
2 2 3 2
SO 45℃)
3
①装置Ⅰ模拟工业生产中SO 催化氧化的反应,其化学方程式是__________________。
2
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是_____________________;装置Ⅳ的作用是
_________________。
③装置Ⅲ中溶液逐渐褪色,说明SO 具有__________性
2
【变8-1】某化学兴趣小组为探究SO 的性质,按如图所示装置进行实验。(已知:NaSO +
2 2 3
HSO (浓)=Na SO +SO↑+H O)
2 4 2 4 2 2
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠仪器的名称分别是______、______。
(2)反应后,装置B中产生的现象是______,发生反应的离子方程式为______;装置D中的现象是______,
发生反应的化学方程式为______。
(3)装置E的目的是探究SO 与品红溶液作用的可逆性,写出实验操作及现象:____________。
2
(4)F装置的作用是______,倒扣漏斗的作用是______。【变8-2】为了探究Cl、SO 同时通入HO中发生的反应,某校化学兴趣小组同学设计了如图所示的实验
2 2 2
装置。
(1)该化学兴趣小组的同学现采用 与70%的硫酸为原料制取SO ,采用 和浓盐酸(12mol/L)为原
2
料制取Cl 在此实验中,F仪器的作用是___________;气体发生装置B应选择以下三种装置中的
2.
___________ (填序号)。
(2)装置D中主要反应的离子方程式为___________。
(3)为验证通入装置D中的气体是Cl 过量还是SO 过量,兴趣小组的同学准备了以下试剂:
2 2
①氯化铁溶液②氯化亚铁溶液③硫氰化钾溶液④品红溶液
若Cl 过量,取适量D中溶液滴加至盛有___________ (填一个序号)的试管内,再加入___________ (填一
2
个序号)。产生的现象是___________。
若SO 过量,取适量D中溶液滴加至盛有___________ (填一个序号)的试管内,产生的现象是___________。
2
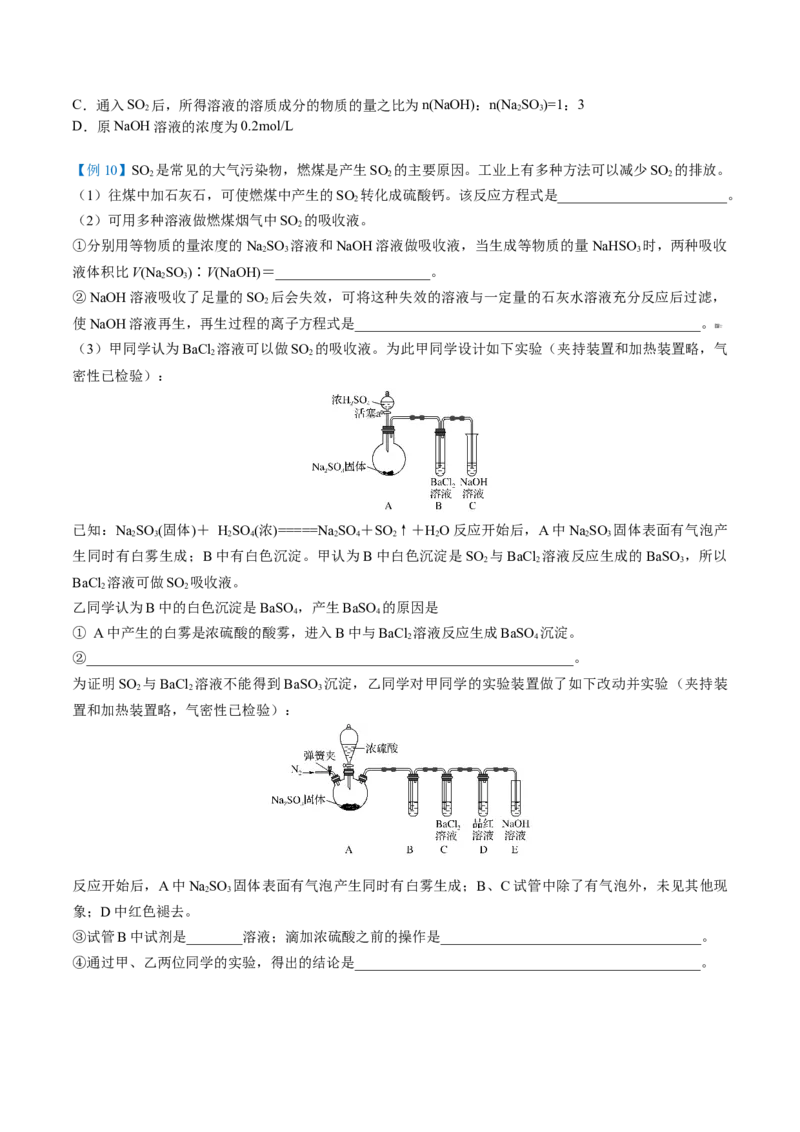
【例9】向100ml NaOH溶液中通入一定量的SO 气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L
2
的盐酸,产生SO 的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )
2
A.通入SO 后,所得溶液的溶质成分的物质的量之比为n(NaHSO):n(Na SO )=1:1
2 3 2 3
B.通入SO 在标准状况下的体积为448mL
2C.通入SO 后,所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na SO )=1:3
2 2 3
D.原NaOH溶液的浓度为0.2mol/L
【例10】SO 是常见的大气污染物,燃煤是产生SO 的主要原因。工业上有多种方法可以减少SO 的排放。
2 2 2
(1)往煤中加石灰石,可使燃煤中产生的SO 转化成硫酸钙。该反应方程式是________________________。
2
(2)可用多种溶液做燃煤烟气中SO 的吸收液。
2
①分别用等物质的量浓度的NaSO 溶液和NaOH溶液做吸收液,当生成等物质的量NaHSO 时,两种吸收
2 3 3
液体积比V(Na SO )∶V(NaOH)=______________________。
2 3
②NaOH溶液吸收了足量的SO 后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,
2
使NaOH溶液再生,再生过程的离子方程式是_________________________________________________。
(3)甲同学认为BaCl 溶液可以做SO 的吸收液。为此甲同学设计如下实验(夹持装置和加热装置略,气
2 2
密性已检验):
已知:NaSO (固体)+ HSO (浓)=====NaSO +SO ↑+HO反应开始后,A中NaSO 固体表面有气泡产
2 3 2 4 2 4 2 2 2 3
生同时有白雾生成;B中有白色沉淀。甲认为B中白色沉淀是SO 与BaCl 溶液反应生成的BaSO ,所以
2 2 3
BaCl 溶液可做SO 吸收液。
2 2
乙同学认为B中的白色沉淀是BaSO,产生BaSO 的原因是
4 4
① A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl 溶液反应生成BaSO 沉淀。
2 4
②_____________________________________________________________________。
为证明SO 与BaCl 溶液不能得到BaSO 沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装
2 2 3
置和加热装置略,气密性已检验):
反应开始后,A中NaSO 固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现
2 3
象;D中红色褪去。
③试管B中试剂是________溶液;滴加浓硫酸之前的操作是_____________________________________。
④通过甲、乙两位同学的实验,得出的结论是_________________________________________________。提分作业
【练1】下列说法正确的是
A.硫质脆,微溶于酒精和二硫化碳
B.硫与氢气反应,体现了硫的还原性
C.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物
D.从硫的化合价角度分析,硫单质既可作氧化剂又可作还原剂
【练2】下列关于硫的说法不正确的是
A.试管内壁附着的硫可用二硫化碳溶解除去
B.游离态的硫存在于火山喷口附近或地壳的岩层里
C.单质硫既有氧化性,又有还原性
D.硫在空气中的燃烧产物是二氧化硫,在纯氧气中的燃烧产物是三氧化硫
【练3】下列四种有色溶液与SO 作用,均能褪色,其实质相同的是( )
2
①品红溶液 ②酸性KMnO 溶液 ③溴水 ④滴有酚酞的NaOH溶液
4
A.①④ B.②③ C.②③④ D.①②③
【练4】下列物质中,不能由单质直接化合生成的是
①CuS ②FeS ③SO ④HS ⑤FeCl
3 2 2
A.①③⑤ B.①②③⑤ C.①②④⑤ D.全部
【练5】下列关于二氧化硫的说法不正确的是( )
A.能使某些有色物质褪色 B.无色、有刺激性气味、无毒
C.既有氧化性、又有还原性 D.既可溶于水、又可与水反应
【练6】如图装置可用于收集SO 并验证其某些化学性质,下列说法正确的是
2
选项 试剂 现象 结论
A 酸性KMnO 溶液 溶液褪色 SO 有氧化性
4 2
B 品红溶液 溶液褪色 SO 有漂白性
2
C NaOH溶液 无明显现象 SO 与NaOH溶液不反应
2D 硫化氢水溶液 溶液变浑浊 SO 有还原性
2
A.A B.B C.C D.D
【练7】下列关于SO 性质的说法正确的是( )
2
A.二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加
B.氯气和二氧化硫都有漂白性,若将等物质的量的这两种气体同时作用于潮湿的有色布条,可以观察到
有色布条先褪色,后复原
C.将少量SO 气体通入BaCl 和FeCl 的混合溶液中,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产
2 2 3
生,该白色沉淀是BaSO
3
D.向SO 水溶液中通入HS气体,有淡黄色沉淀产生,说明SO 水溶液具有还原性
2 2 2
【练8】能正确表示下列反应的离子方程式的是( )
A.向澄清石灰水中通入少量SO 气体:Ca2++SO =CaSO ↓
2 2 3
B.过量SO 气体通入氢氧化钠溶液中:SO +OH-=
2 2
C.SO 气体通入溴水中:SO +Br +HO=2H++2Br-+
2 2 2 2
D.向氢硫酸中通入氯气:S2-+Cl=S↓+2Cl-
2
【练9】如图是实验室制备SO 并验证SO 某些性质的装置图。试回答:
2 2
(1)写出仪器A的名称___________,写出此实验中制备SO 化学方程式___________________。
2
(2)C中的现象是___________________,此实验证明SO 是___气体。
2
(3)D中的反应现象证明SO 有___性;F中的现象是_________________________,G中SO 与碘水反应
2 2
的方程式:_______。
(4)H中的试剂是氢氧化钠溶液,用于吸收多余的二氧化硫气体,防止污染空气;反应的离子方程式为
___。
【练10】某化学兴趣小组为探究SO 的性质,按如图所示装置进行实验。(已知:NaSO +
2 2 3
HSO (浓)=Na SO +SO↑+H O)
2 4 2 4 2 2请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠仪器的名称分别是______、______。
(2)反应后,装置B中产生的现象是______,发生反应的离子方程式为______;装置D中的现象是 ______,
发生反应的化学方程式为______。
(3)装置E的目的是探究SO 与品红溶液作用的可逆性,写出实验操作及现象:____________。
2
(4)F装置的作用是______,倒扣漏斗的作用是______。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育