文档内容
第 01 讲 硫、二氧化硫、三氧化硫
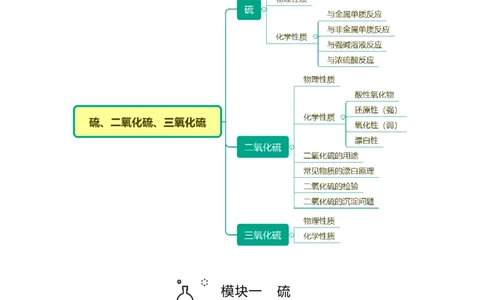
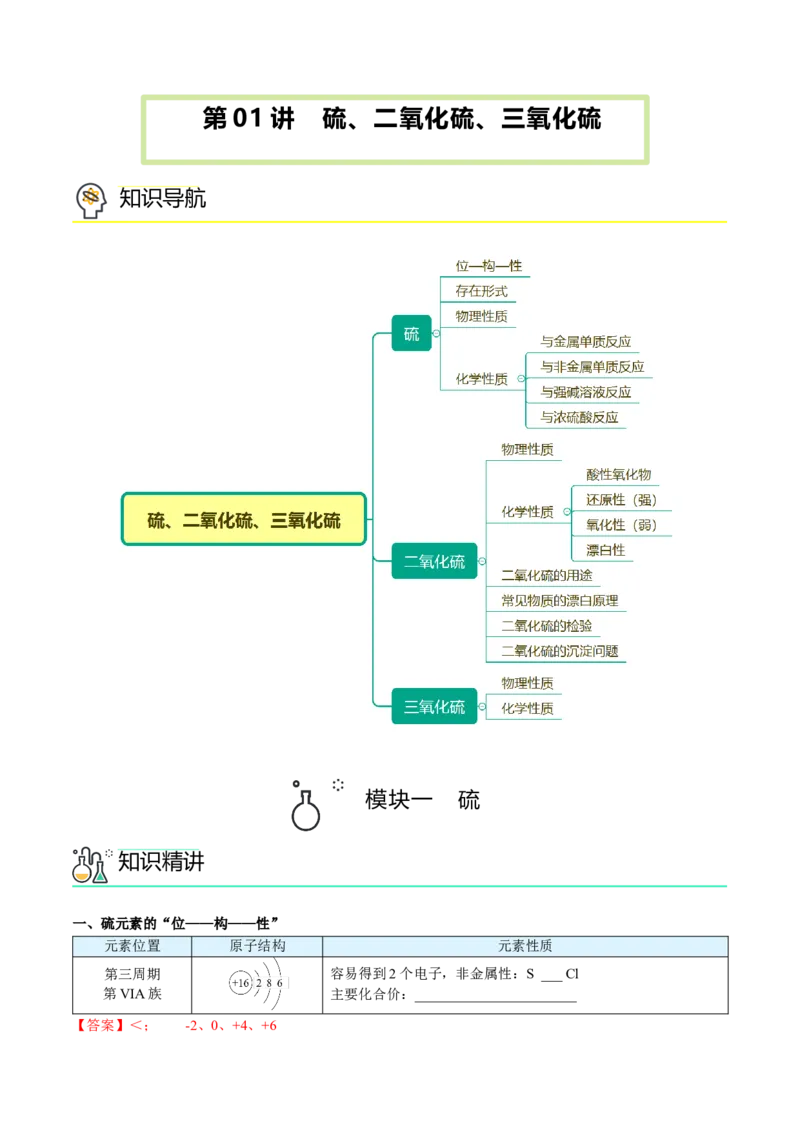
知识导航
模块一 硫
知识精讲
一、硫元素的“位——构——性”
元素位置 原子结构 元素性质
第三周期 容易得到2个电子,非金属性:S ___ Cl
第VIA族 主要化合价:_______________________
【答案】<; -2、0、+4、+6二、硫元素的存在形式
三、硫单质的物理性质
俗名 颜色状态 溶解性
硫黄 ____色晶体,易研成粉末 不溶于水,微溶于酒精,易溶于______
【答案】黄,CS
2
资料卡片——二硫化碳
二硫化碳是一种无机物,化学式为CS₂,常见溶剂,无色液体,可溶解硫单质。二硫化碳用于制造人
造丝、杀虫剂、促进剂等,也用作溶剂。
四、硫的化学性质
【答案】Fe + S ===== FeS ; 2Cu + S ===== Cu S ; > S + O =====SO
2 2 2
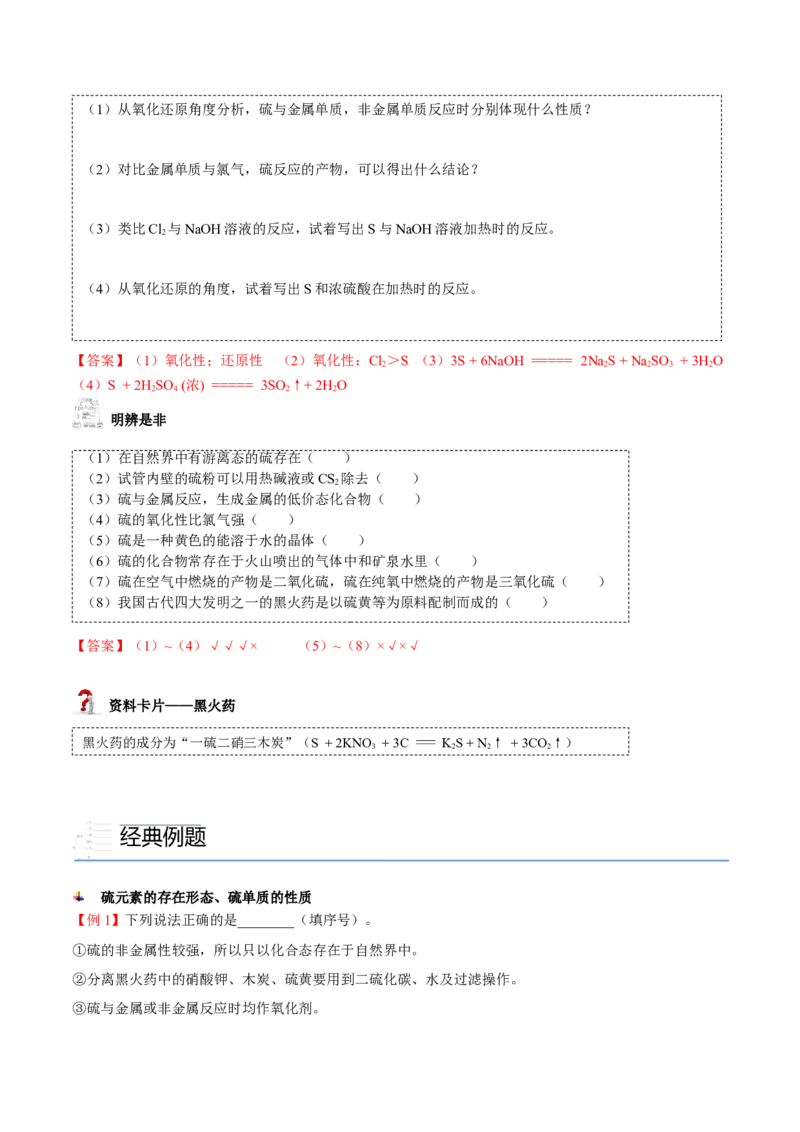
思考与交流(1)从氧化还原角度分析,硫与金属单质,非金属单质反应时分别体现什么性质?
(2)对比金属单质与氯气,硫反应的产物,可以得出什么结论?
(3)类比Cl 与NaOH溶液的反应,试着写出S与NaOH溶液加热时的反应。
2
(4)从氧化还原的角度,试着写出S和浓硫酸在加热时的反应。
【答案】(1)氧化性;还原性 (2)氧化性:Cl>S (3)3S + 6NaOH ===== 2NaS + NaSO + 3H O
2 2 2 3 2
(4)S + 2H SO (浓) ===== 3SO ↑+ 2H O
2 4 2 2
明辨是非
(1)在自然界中有游离态的硫存在( )
(2)试管内壁的硫粉可以用热碱液或CS 除去( )
2
(3)硫与金属反应,生成金属的低价态化合物( )
(4)硫的氧化性比氯气强( )
(5)硫是一种黄色的能溶于水的晶体( )
(6)硫的化合物常存在于火山喷出的气体中和矿泉水里( )
(7)硫在空气中燃烧的产物是二氧化硫,硫在纯氧中燃烧的产物是三氧化硫( )
(8)我国古代四大发明之一的黑火药是以硫黄等为原料配制而成的( )
【答案】(1)~(4)√√√× (5)~(8)×√×√
资料卡片——黑火药
黑火药的成分为“一硫二硝三木炭”(S + 2KNO + 3C === KS + N↑ + 3CO↑)
3 2 2 2
经典例题
硫元素的存在形态、硫单质的性质
【例1】下列说法正确的是________(填序号)。
①硫的非金属性较强,所以只以化合态存在于自然界中。
②分离黑火药中的硝酸钾、木炭、硫黄要用到二硫化碳、水及过滤操作。
③硫与金属或非金属反应时均作氧化剂。④硫在空气中燃烧产物只是SO 。
2
⑤不能由单质直接化合而制得CuS、CuCl 、Fe S、FeCl 。
2 2 3 2
⑥用蒸馏水清洗试管内壁残留的硫。
【答案】②④
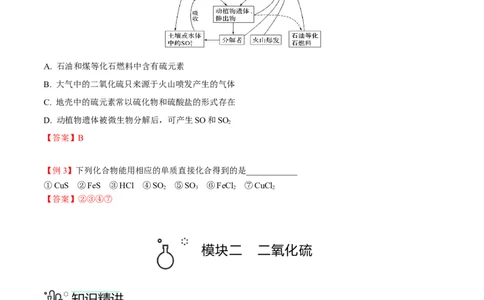
【例2】硫在自然界中的循环过程如下图所示,下列说法不正确的是( )
A. 石油和煤等化石燃料中含有硫元素
B. 大气中的二氧化硫只来源于火山喷发产生的气体
C. 地壳中的硫元素常以硫化物和硫酸盐的形式存在
D. 动植物遗体被微生物分解后,可产生SO和SO
2
【答案】B
【例3】下列化合物能用相应的单质直接化合得到的是____________
①CuS ②FeS ③HCl ④SO ⑤SO ⑥FeCl ⑦CuCl
2 3 2 2
【答案】②③④⑦
模块二 二氧化硫
知识精讲
一、二氧化硫的物理性质
颜色 气味 状态 密度 溶解性 沸点
无色 刺激性 气体 比空气大 易溶于水,1体积水能溶解40体积SO 较低,易液化
2
二、二氧化硫的化学性质
1.SO 具有酸性氧化物的通性(类比CO)
2 2
(1)与水反应(可逆反应):________________________________________________(2)与碱性氧化物反应(如CaO):__________________________________________
思考与交流
(1)CO 通入澄清石灰水,现象是?如果通入过量CO 呢?
2 2
(2)SO 通入澄清石灰水至过量,现象是?
2
(3)与碱反应:a. 少量SO + 澄清石灰水:_________________________________(现象:________)
2
b. 过量SO + 澄清石灰水:_________________________________(现象:________)
2
【答案】(1)SO + H O HSO ;(2)SO + CaO === CaSO (3)Ca(OH) + SO === CaSO↓ +
2 2 2 3 2 3 2 2 3
HO;变浑浊;Ca(OH) + 2SO === Ca(HSO );先浑浊,后澄清
2 2 2 3 2
思考与交流:将少量/过量的二氧化硫气体通入碳酸氢钠溶液中,方程式分别如何书写?
【答案】少量:SO + 2NaHCO === Na SO + 2CO + H O
2 3 2 3 2 2
过量:SO + NaHCO === NaHSO + CO
2 3 3 2
2.SO 的还原性与氧化性
2
【答案】2SO + O 2SO
2 2 3
SO + H O === HSO
2 2 2 2 4
5SO + 2 + 2HO === 5 + 2Mn2+ + 4H+
2 MnO- 2 SO2-
4 4
X + SO + 2H O === 4H+ + 2X- +
2 2 2 SO2-
4
2Fe3+ + SO + 2H O === 4H+ + 2Fe2+ +
2 2 SO2-
4SO + 2H S === 3S↓+ 2H O
2 2 2
3.SO 的漂白性
2
(1)SO 具有漂白作用,能使品红溶液褪色,但不能使酸碱指示剂褪色。
2
(2)漂白原理:SO 与有色物质结合生成了不稳定的无色物质,加热(或见光、长久放置)后,不稳定的
2
无色物质又会发生分解,恢复到原来的颜色。
我们学过的,有漂白性的还有哪些物质?
归纳总结——常见物质的漂白原理
漂白类型 实例 漂白原理 特点
HClO、NaClO、
氧化型 将有色物质氧化使其失去原有的颜色 不可逆
NaO、HO
2 2 2 2
SO 使品红溶液 与有色物质结合,生成不稳定的无色
加合型 2 可逆
褪色 物质
活 性 炭 、
疏松多孔,表面积较大,可以吸附一 物理变化,部分吸附剂可重复使
吸附型 Al(OH) 、
3 些有色物质 用
Fe(OH) 胶体
3
4.SO 的用途
2
(1)工业上常用SO 来漂白纸浆、毛、丝等;
2
(2)SO 可用于杀菌消毒,还是一种食品添加剂。
2
资料卡片——食品添加剂SO
2
SO 作为食品添加剂有多种用途,如在食糖制备过程中作漂白剂,葡萄酒、干果制作中添加适量 SO 作
2 2
防腐剂、抗氧化剂,但SO 作为食品添加剂应严格控制用量。
2
归纳总结——SO 的性质
2品红褪色
______性
______性 ______性
S SO SO、SO2-
H 2 S 2 + Fe3+、X 2 、KMnO 4 、O 2 、H 2 O 2 3 4
______性
HSO、SO2-
2 3 3
【答案】漂白,还原,酸,氧化
思考与交流
(1)如何鉴别SO 与CO?
2 2
(2)SO 通入BaCl 溶液,能否产生白色沉淀?为什么?
2 2
(3)若想在(2)中产生白色沉淀,可以如何操作?
【答案】(1)利用SO 的漂白性/还原性,可通入品红/酸性高锰酸钾/溴水等溶液。
2
(2)不能,弱酸不能制强酸
(3)加入碱性物质如NH/NH·HO,可产生BaSO 沉淀;或强氧化性物质如Cl/酸性KMnO 等,可产生
3 4 2 3 2 4
BaSO 沉淀。
4
经典例题
SO 的漂白性
2
【例4】下列物质能使品红溶液褪色,且褪色原理基本相同的是( )
①活性炭 ②氯水 ③二氧化硫 ④臭氧 ⑤过氧化钠 ⑥双氧水
A.①②④⑥ B.①②③⑤ C.②④⑤⑥ D.③④⑤⑥
【答案】C
【变4】氯水和SO 都具有漂白作用,能使品红溶液褪色。若将等物质的量的 Cl 、SO 混合后再通入品红
2 2 2
与BaCl 的混合溶液,能观察到的现象是( )
2
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①② B.①③ C.②③ D.②④
【答案】CSO 的沉淀问题
2
【例5】含有FeCl 和BaCl 的强酸性溶液中通入足量的SO 有白色沉淀生成。由此得出的结论正确的是
3 2 2
__________。
①白色沉淀是BaSO ②白色沉淀是BaSO
4 3
③白色沉淀是BaSO 和BaSO 的混合物 ④FeCl 被SO 还原为FeCl
3 4 3 2 2
【答案】 ①④
【变5-1】将SO 通入BaCl 溶液至饱和,未见沉淀生成,继续通入另一种气体(或物质),仍无沉淀,则
2 2
通入的气体(或物质)可能是( )
A.CO B.NH C.FeCl D.Cl
2 3 3 2
【答案】A
【变5-2】将SO 分别通入下列溶液中,能出现白色沉淀且不溶解的是___________,所生成的白色沉淀分
2
别是____________。
①Ca(OH) ②Ba(NO ) ③Ca(ClO) ④BaCl ⑤酸性高锰酸钾溶液
2 3 2 2 2
【答案】 ②③; BaSO、CaSO
4 4
SO 与CO 的鉴别
2 2
【例6】已知混合气体中可能含有SO 或CO 中的一种或两种,设计成以下装置进行鉴别:
2 2
(1)B中应该装下列________(填编号)试剂。
A.NaCl溶液 B.酸性KMnO 溶液 C.盐酸 D.澄清石灰水
4
(2)A中品红溶液的作用是:______________________________________________;
C中品红溶液的作用是:______________________________________________。
(3)D中澄清石灰水的作用是:____________________________________________。
(4)根据实验现象,判断气体成分:
题序 装置A现象 装置C现象 装置D现象 气体成分
① 褪色 不褪色 不变浑浊
② 不褪色 不褪色 变浑浊
③ 褪色 不褪色 变浑浊
【答案】(1)B; (2)验证混合气体中是否含有SO ;验证SO 是否已经完全除去;
2 2
(3)验证混合气体中是否含有CO;(4)①只有SO ;②只有CO;③CO 和SO 的混合气体
2 2 2 2 2SO 的性质综合
2
【例7】判断下列说法是否正确。
(1)SO 使KMnO 溶液褪色,说明SO 具有漂白性( )
2 4 2
(2)在NaOH和酚酞的混合液中通入SO ,溶液褪色是因为SO 的漂白作用( )
2 2
(3)紫色石蕊试液中通入二氧化硫,溶液先变红后褪色( )
(4)氯气与二氧化硫1:1混合使用,漂白效果更佳( )
(5)SO 是酸性氧化物,溶于水得稳定的亚硫酸( )
2
(6)SO 气体通入HS溶液中,生成淡黄色沉淀,体现了SO 的还原性( )
2 2 2
(7)过量SO 气体通入NaOH溶液得到NaSO ( )
2 2 3
(8)将1.12 L的SO 气体通入100 mL 1 mol/L的FeCl 溶液中,恰好完全反应( )
2 3
(9)SO 可以作食品漂白剂和制冷剂( )
2
(10)在葡萄酒中添加微量二氧化硫作抗氧化剂,使酒保持良好品质( )
【答案】××××× ; ××××√
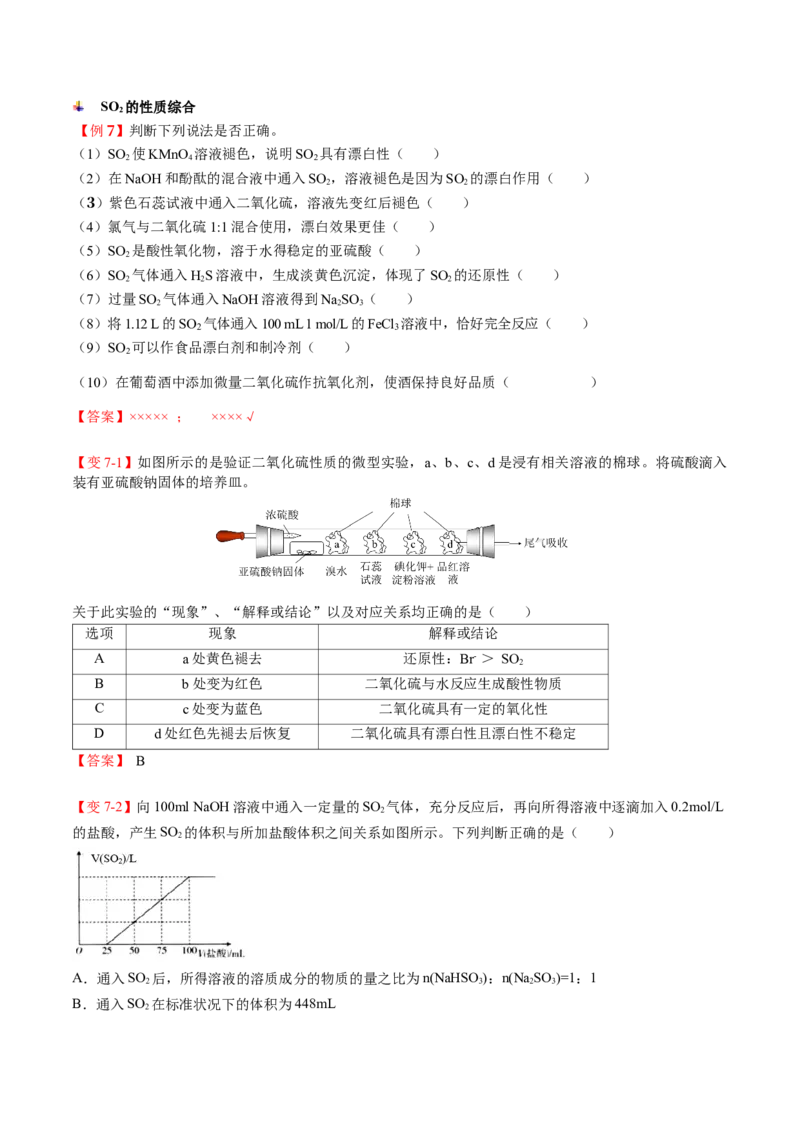
【变7-1】如图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将硫酸滴入
装有亚硫酸钠固体的培养皿。
关于此实验的“现象”、“解释或结论”以及对应关系均正确的是( )
选项 现象 解释或结论
A a处黄色褪去 还原性:Br- > SO
2
B b处变为红色 二氧化硫与水反应生成酸性物质
C c处变为蓝色 二氧化硫具有一定的氧化性
D d处红色先褪去后恢复 二氧化硫具有漂白性且漂白性不稳定
【答案】 B
【变7-2】向100ml NaOH溶液中通入一定量的SO 气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L
2
的盐酸,产生SO 的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )
2
A.通入SO 后,所得溶液的溶质成分的物质的量之比为n(NaHSO):n(Na SO )=1:1
2 3 2 3
B.通入SO 在标准状况下的体积为448mL
2C.通入SO 后,所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na SO )=1:3
2 2 3
D.原NaOH溶液的浓度为0.2mol/L
【答案】D
【分析】
假设NaOH与SO 气体反应所得溶液中只有NaSO ,则开始阶段发生反应:NaSO +HCl=NaHSO +NaCl,
2 2 3 2 3 3
生成SO 发生的反应为:NaHSO+HCl=NaCl+SO ↑+H O,由方程式可知,前后两个阶段消耗盐酸的体积应
2 3 2 2
相等,而实际生成SO 消耗的盐酸体积多,故NaOH与SO 气体反应所得溶液中溶质为NaSO 、NaHSO,
2 2 2 3 3
0~25mL时,无气体生成,发生反应为NaSO +HCl═NaHSO +NaCl,加盐酸的体积为25mL~100 mL时,
2 3 3
产生气体,发生的反应为NaHSO+HCl═SO ↑+NaCl+HO,据此分析解答。
3 2 2
【详解】
A.根据图象可知,加盐酸的体积0~25mL时,无气体生成,发生反应为NaSO +HCl═NaHSO +NaCl,消
2 3 3
耗盐酸的物质的量为0.2mol/L×0.025L=0.005mol,所以n(Na SO )=0.005mol;加入盐酸100mL时恰好完全
2 3
反应,此时溶质只有氯化钠,n(Na+)=n(Cl-)=0.2mol/L×0.1L=0.02mol,则
n(NaHSO)=0.02mol-0.005mol×2=0.01mol,通入SO 后,所得溶液的溶质成分的物质的量之比为
3 2
n(NaHSO):n(Na SO )=2:1,故A错误;
3 2 3
B.加盐酸的体积为25mL~100 mL时,产生气体,发生的反应为NaHSO+HCl═SO ↑+NaCl+HO,此反应
3 2 2
消耗盐酸的物质的量是0.2mol/L×0.075L=0.015mol,放出SO 在标准状况下的体积为0.015mol×22.4L/
2
mol=0.336L=336mL,所以氢氧化钠溶液通入SO 在标准状况下的体积为336mL,故B错误;
2
C.假设NaOH与SO 气体反应所得溶液中只有NaSO ,则开始阶段发生反应:
2 2 3
NaSO +HCl=NaHSO +NaCl,由方程式可知,前后两个阶段消耗盐酸的体积应相等,而实际生成二氧化碳
2 3 3
消耗的盐酸体积多,故NaOH与SO 气体反应所得溶液中溶质为NaSO 、NaHSO,没有氢氧化钠,故C
2 2 3 3
错误;
D.加入100mL盐酸时SO 的体积达最大,此时溶液为NaCl溶液,根据元素守恒,所以
2
n(NaOH)=n(NaCl)=n(HCl)=0.1L×0.2mol/L=0.02mol,所以c(NaOH)= =0.2mol/L,故D正确;
故选D。
【变7-3】SO 是常见的大气污染物,燃煤是产生SO 的主要原因。工业上有多种方法可以减少SO 的排放。
2 2 2
(1)往煤中加石灰石,可使燃煤中产生的SO 转化成硫酸钙。该反应方程式是________________________。
2
(2)可用多种溶液做燃煤烟气中SO 的吸收液。
2
①分别用等物质的量浓度的NaSO 溶液和NaOH溶液做吸收液,当生成等物质的量NaHSO 时,两种吸收
2 3 3
液体积比V(Na SO )∶V(NaOH)=______________________。
2 3
②NaOH溶液吸收了足量的SO 后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,
2
使NaOH溶液再生,再生过程的离子方程式是_________________________________________________。
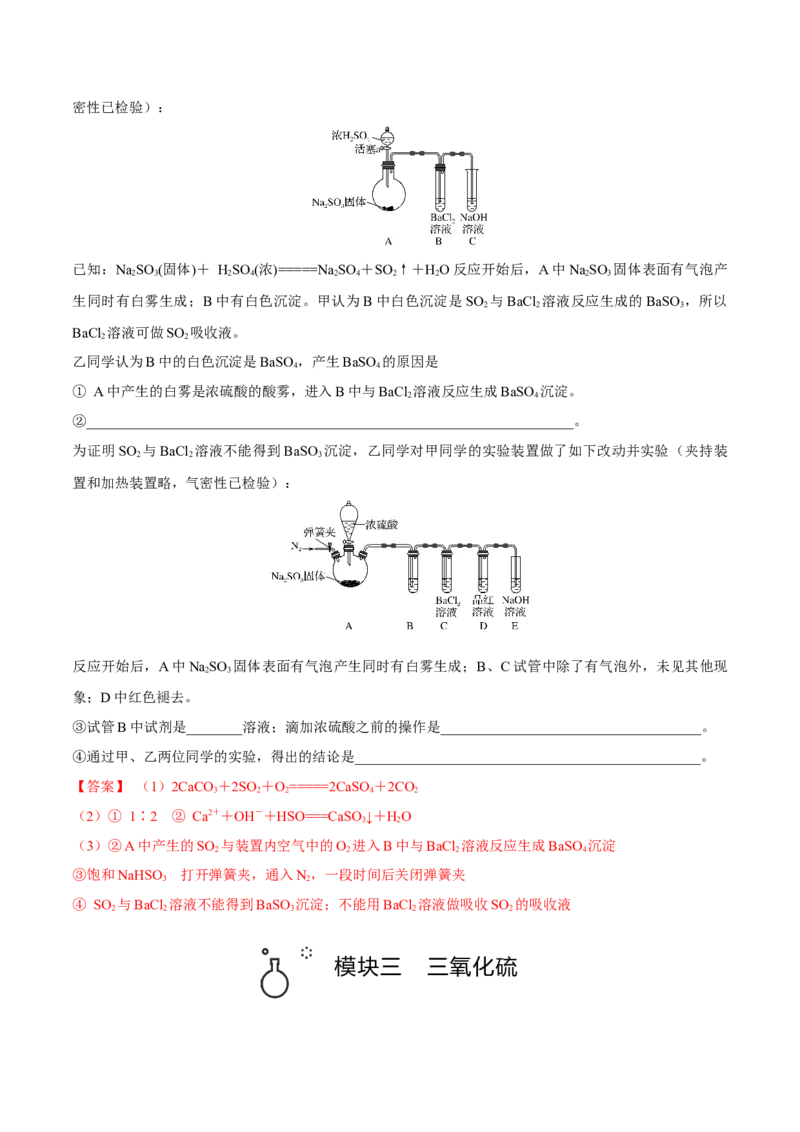
(3)甲同学认为BaCl 溶液可以做SO 的吸收液。为此甲同学设计如下实验(夹持装置和加热装置略,气
2 2密性已检验):
已知:NaSO (固体)+ HSO (浓)=====NaSO +SO ↑+HO反应开始后,A中NaSO 固体表面有气泡产
2 3 2 4 2 4 2 2 2 3
生同时有白雾生成;B中有白色沉淀。甲认为B中白色沉淀是SO 与BaCl 溶液反应生成的BaSO ,所以
2 2 3
BaCl 溶液可做SO 吸收液。
2 2
乙同学认为B中的白色沉淀是BaSO,产生BaSO 的原因是
4 4
① A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl 溶液反应生成BaSO 沉淀。
2 4
②_____________________________________________________________________。
为证明SO 与BaCl 溶液不能得到BaSO 沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装
2 2 3
置和加热装置略,气密性已检验):
反应开始后,A中NaSO 固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现
2 3
象;D中红色褪去。
③试管B中试剂是________溶液;滴加浓硫酸之前的操作是_____________________________________。
④通过甲、乙两位同学的实验,得出的结论是_________________________________________________。
【答案】 (1)2CaCO +2SO +O=====2CaSO+2CO
3 2 2 4 2
(2)① 1∶2 ② Ca2++OH-+HSO===CaSO ↓+HO
3 2
(3)②A中产生的SO 与装置内空气中的O 进入B中与BaCl 溶液反应生成BaSO 沉淀
2 2 2 4
③饱和NaHSO 打开弹簧夹,通入N,一段时间后关闭弹簧夹
3 2
④ SO 与BaCl 溶液不能得到BaSO 沉淀;不能用BaCl 溶液做吸收SO 的吸收液
2 2 3 2 2
模块三 三氧化硫知识精讲
一、SO 的物理性质
3
颜色 状态 水溶性
无色 固体(标况下) 易溶于水
二、SO 的化学性质
3
SO 是酸性氧化物,具有酸性氧化物的通性:
3
1.与水反应:__________________________________________________________
2.SO 与碱反应(如Ca(OH) ):__________________________________________
3 2
3.SO 与碱性氧化物反应(如CaO):______________________________________
3
【答案】SO + H O === HSO SO + Ca(OH) === CaSO + H O SO + CaO === CaSO
3 2 2 4 3 2 4 2 3 4
经典例题
SO 的性质
3
【例8】已知SO 的熔点为16.8℃,沸点为44.8℃,下列关于SO 性质的描述不正确的是( )
3 3
A.是酸性氧化物,可与氢氧化钠溶液反应
B.标况下,1mol SO 的体积约为22.4 L
3
C.是工业制取硫酸的原料
D.可以与氯化钡溶液反应生成白色沉淀
【答案】B
【例9】将SO 和SO 两种气体的混合物通入BaCl 溶液中,其结果是( )
2 3 2
A.两种气体都被吸收,并有BaSO 沉淀生成
4
B.只有 BaSO 沉淀,SO 通入溶液中无沉淀生成
3 3
C.生成 BaSO 和BaSO 两种沉淀
3 4
D.只生成BaSO 沉淀,SO 从溶液中逸出
4 2
【答案】D
提分作业
【练1】下列反应中气体只作还原剂的是( )
A.Cl 通入水中 B.Cl 通入水NaSO 溶液中
2 2 2 3
C.SO 通入氯水中 D.SO 通入氢硫酸中
2 2
【答案】C
【练2】早在古代,我国人民就积累了不少对化学物质变化的认识。例如,晋代炼丹家、医学家葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银,积变又还成丹砂”。这句话中的丹砂指的是HgS,下列有关
说法正确的是( )
A.这个过程只涉及物理变化
B.“积变又还成丹砂”过程中发生反应:HgS Hg+S
C.实验室中不慎洒落的水银可用硫黄处理
D.“丹砂烧之成水银”过程中还可能产生SO
3
【答案】C
【练3】下列溶液能够区别SO 和CO 气体的是( )
2 2
①澄清的石灰水 ②HS溶液 ③酸性KMnO 溶液 ④氯水 ⑤品红溶液
2 4
A.①②③ B.②③④ C.除①以外 D.全部
【答案】 C
【练4】下列说法中不正确的是( )
A.SO 、HO 均能使品红溶液褪色,但其漂白原理不相同
2 2 2
B.加热可判断品红溶液褪色是由于通入SO 还是加入HO 引起的
2 2 2
C.SO 、活性炭使品红溶液褪色均发生了化学反应
2
D.向通入过量SO 的品红溶液中通入Cl 气体,溶液由无色变为红色
2 2
【答案】 C
【练5】下列实验用来证明气体SO 的存在,其中正确的是( )
2
①能使品红溶液褪色
②能使湿润的蓝色石蕊试纸变红
③能使澄清的石灰水变浑浊
④通入足量的NaOH溶液中,再滴入BaCl 溶液,有白色沉淀生成,该沉淀溶于盐酸
2
⑤通入到溴水中使其褪色,再滴入Ba(NO ) 溶液,有白色沉淀生成
3 2
A.①②④⑤ B.都不能证明 C.①⑤能证明 D.只有⑤能证明
【答案】 D
【练6】如图所示是一种综合处理SO 废气的工艺流程,若每步都完全反应。下列说法正确的是( )
2
A. 溶液B中发生的反应为2SO +O===2SO
2 2 3
B. 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
C. 由以上流程可推知氧化性:Fe3+>O>SO
2
D. 此工艺的优点之一是物质能循环利用【答案】D
【练7】下列说法正确的是( )
A.因为SO 具有漂白性,所以它能使品红溶液、溴水、KMnO 溶液、石蕊试液褪色
2 4
B.能使品红褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同
2 2 2
D.SO 和Cl 等物质的量混合后同时通入装有湿润的有色布条的集气瓶中,漂白效果更好
2 2
【答案】B
【练8】下列情况会对人体健康造成较大危害的是( )
A.自来水中通入少量O 进行消毒杀菌 B.用SO 漂白食品
3 2
C.用食醋清洗热水瓶胆内壁附着的水垢 D.用小苏打发酵面团制作馒头
【答案】B
【练9】下列说法不正确的是( )
A. SO 和CO 均有毒
2 2
B. SO 和CO 均能与澄清石灰水反应,并有白色沉淀生成
2 2
C. SO 具有漂白性,但通入石蕊溶液中却不能使之褪色
2
D. SO 和Cl 均能使品红溶液褪色
2 2
【答案】A
【练10】某工厂的一个生产工艺流程如图所示,下列叙述正确的是( )
A. 该工艺流程是用来制备Fe (SO ) 的
2 4 3
B. 气体M是SO
3
C. 气体M参加的反应是化合反应
D. SO 参加反应时氧化剂和还原剂的物质的量之比是1∶1
2
【答案】D
【练11】已知X、Y为有刺激性气味的气体,有以下转化关系,部分产物未标出。试回答:
(1)写出下列物质的化学式:
X___________、Y_____________、A____________、B__________、C__________。
(2)反应①的化学方程式为___________________________________________________,
反应②的离子方程式为___________________________________________________。
【答案】 (1)Cl;SO ;HCl;HSO ;FeCl ;
2 2 2 4 3
(2)Cl + SO + 2H O === 2HCl + H SO ;2Fe3+ + SO + 2H O === 2Fe2++ + 4H+
2 2 2 2 4 2 2 SO2-
4
【练12】二氧化硫为无色气体,有强烈刺激性气味,是大气主要污染物之一。某化学兴趣小组欲制备并探
究SO 的某些性质。
2
SO 的制备:用亚硫酸钠与较浓的硫酸反应制备SO 的装置图如图1(夹持仪器省略)。
2 2
(1)图中的装置错误的是________________________________________;B中发生反应的化学方程式为
___________________________________________;D的作用是____________________________________。
SO 的性质:探究SO 气体性质的装置如图2所示。
2 2
(2)装置Ⅰ中的现象是_____________________________;说明SO 具有_______(填“氧化”或“还
2
原 ” ) 性 。 写 出 装 置 Ⅰ 中 通 入 足 量 SO 的 离 子 方 程 式 :
2
__________________________________________________。
(3)在上述装置中通入过量的SO ,为了验证Ⅱ中发生了氧化还原反应,取Ⅱ中溶液并分成两等份,设计
2
了如下实验:
方案一:往第一份试液中加入少量酸性KMnO 溶液,紫红色褪去;
4
方案二:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的方案是_____________,原因是________________________________________________,
写出解释该原因的离子方程式:________________________________________________________________。
(4)SO 可以用来制备硫代硫酸钠,硫代硫酸钠可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。
2
实验室可通过NaS、NaCO 和SO 共同反应来制取NaSO 。写出如图3所示装置的三颈瓶中制取NaSO
2 2 3 2 2 2 3 2 2 3
的化学方程式:______________________________________________。
【答案】 (1)集气瓶C中导管长短反了;NaSO + HSO === NaSO + HO + SO ↑;吸收尾气中的
2 3 2 4 2 4 2 2
SO ,防止污染环境
2(2)有浅黄色沉淀生成,氧化,2S2- + 5SO + 2HO === 3S↓+ 4
2 2 HSO-
3
(3)方案一;过量的二氧化硫能溶于水,也能使高锰酸钾褪色;
5SO + 2 + 2HO === 5 + 2Mn2+ + 4H+
2 MnO- 2 SO2-
4 4
(4)2NaS + NaCO + 4SO === 3NaSO + CO
2 2 3 2 2 2 3 2