文档内容
第 03 讲 氮气、一氧化氮、二氧化氮
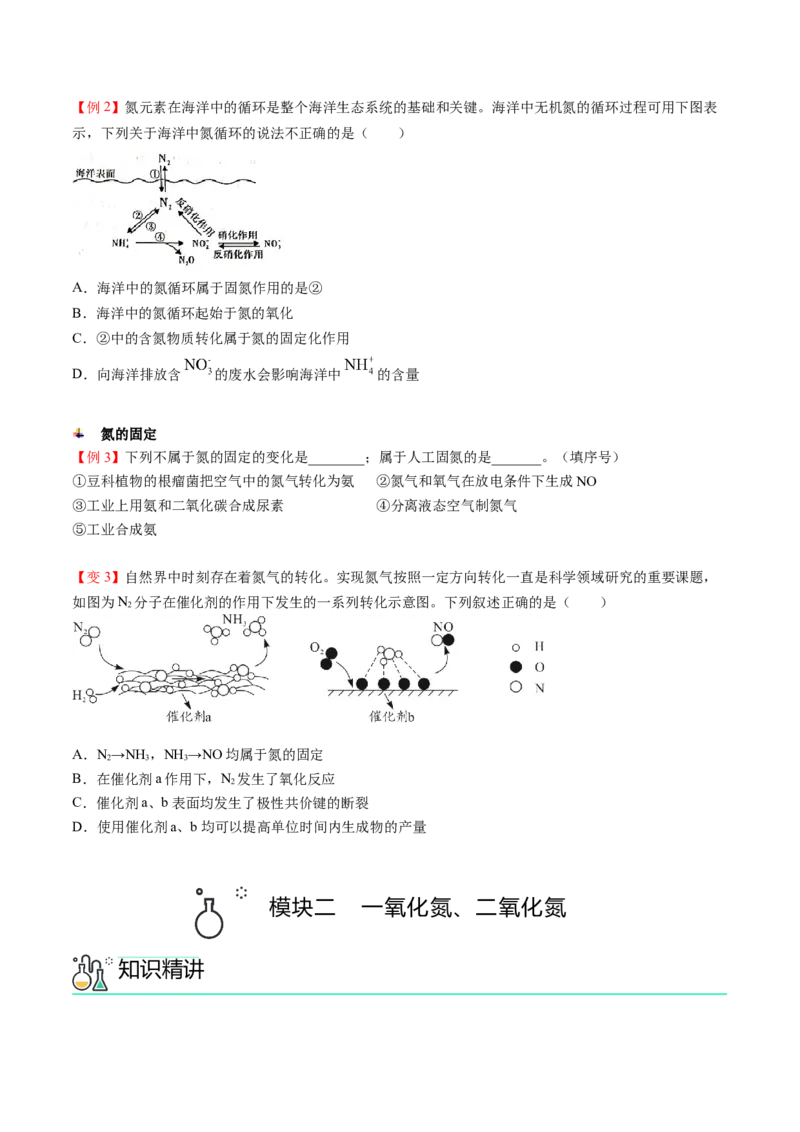
知识导航
模块一 氮气
知识精讲
一、氮元素的“位——构——性”
元素位置 原子结构 元素性质
第三周期 不容易得失电子,一般通过共用电子对与其他原子结合
第VA族 主要化合价:_______________________
二、氮元素的存在形式
三、自然界中氮的循环四、氮气的物理性质和化学性质
物理性质 氮气是一种无色无味的气体,难溶于水,密度与空气相近。
化学性质
思考与交流:镁条在空气中燃烧,固体产物有几种?
五、氮的固定
1.概念:把空气中游离态的氮转变为氮的化合物的过程。
2.分类:
(1)自然固氮:大自然通过闪电释放的能量将空气中的氮气转化为含氮的化合物,或豆科植物根瘤菌将
氮气转化为氨。
(2)人工固氮:如工业合成氨。
经典例题
氮气的性质
【例1】下列关于氮气的叙述,正确的是( )
A.氮气性质稳定,即使在高温下也很难跟其他物质发生反应
B.氮气比空气轻,且不溶于水
C.氮气无氧化性,也无还原性,不跟其他物质反应
D.氮气可与许多物质发生化学反应,所以氮气的化学性质活泼
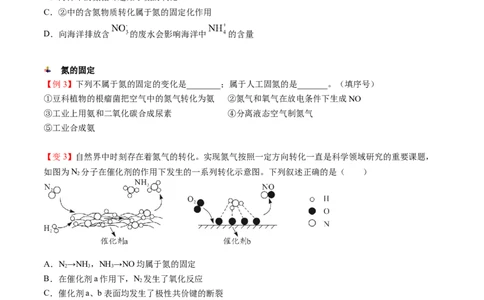
氮的循环【例2】氮元素在海洋中的循环是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表
示,下列关于海洋中氮循环的说法不正确的是( )
A.海洋中的氮循环属于固氮作用的是②
B.海洋中的氮循环起始于氮的氧化
C.②中的含氮物质转化属于氮的固定化作用
D.向海洋排放含 的废水会影响海洋中 的含量
氮的固定
【例3】下列不属于氮的固定的变化是________;属于人工固氮的是_______。(填序号)
①豆科植物的根瘤菌把空气中的氮气转化为氨 ②氮气和氧气在放电条件下生成NO
③工业上用氨和二氧化碳合成尿素 ④分离液态空气制氮气
⑤工业合成氨
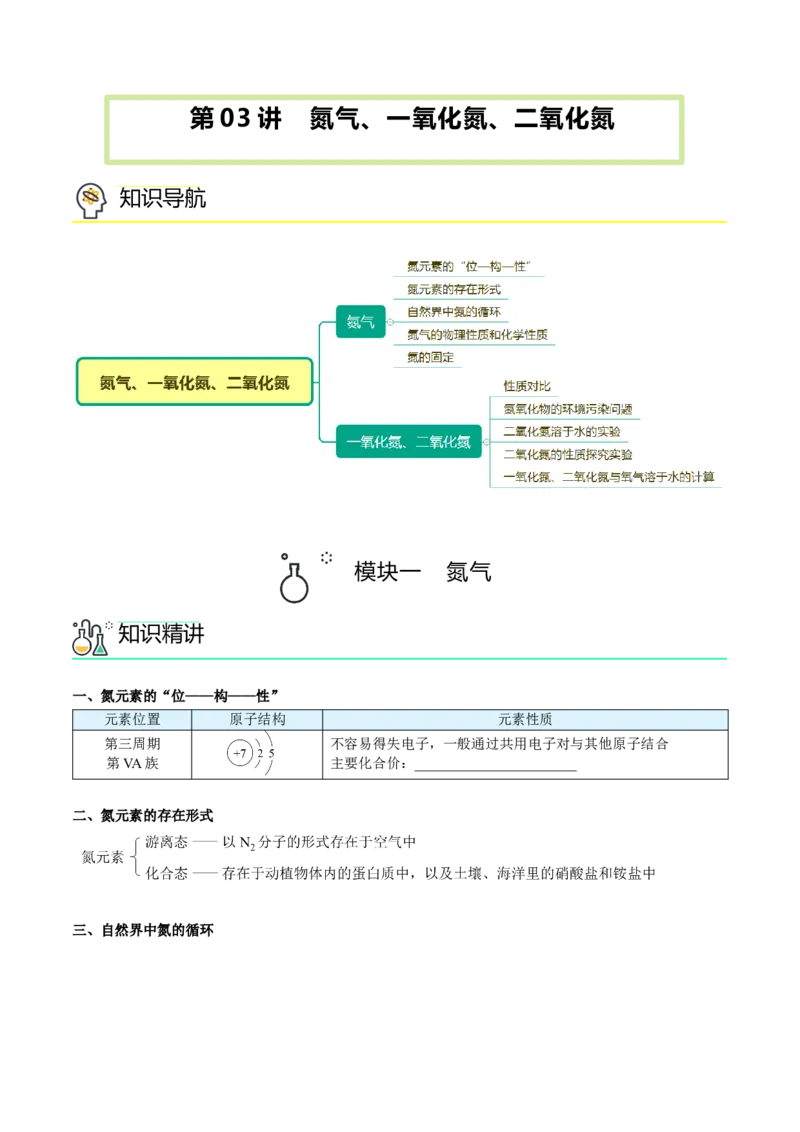
【变3】自然界中时刻存在着氮气的转化。实现氮气按照一定方向转化一直是科学领域研究的重要课题,
如图为N 分子在催化剂的作用下发生的一系列转化示意图。下列叙述正确的是( )
2
A.N→NH ,NH →NO均属于氮的固定
2 3 3
B.在催化剂a作用下,N 发生了氧化反应
2
C.催化剂a、b表面均发生了极性共价键的断裂
D.使用催化剂a、b均可以提高单位时间内生成物的产量
模块二 一氧化氮、二氧化氮
知识精讲一、NO、NO 的性质
2
NO NO
2
物理性质 无色、有毒气体、不溶于水 ________色、有刺激性气味、有毒气体、易溶于水
常温下易与O 反应: ①与水反应,制硝酸:_____________________________
化学性质 2
_________________________ ②自身化合:2NO NO
2 2 4
思考与交流
(1)NO、NO 是酸性氧化物吗?
2
(2)如何收集NO、NO 气体?
2
(3)氮氧化物可造成什么环境污染问题?
资料卡片——光化学烟雾
汽车、工厂等污染源排入大气的氮氧化物与碳氢化合物(一次污染物),经紫外线照射发生光化学反
应生成以臭氧为主的二次污染物,参与光化学反应过程的一次污染物和二次污染物的混合物,称为光
化学烟雾。光化学烟雾危害人体健康和植物生长。
资料卡片——NO、NO 的氧化性
2
NO氧化性较弱:6NO + 4NH ======= 5N + 6H O 、2NO + 2CO ====== N + 2CO (汽车尾气处
3 2 2 2 2
理)
NO 氧化性较强:NO + SO === NO + SO
2 2 2 3
实验探究——NO 溶于水
2实验操作 实验现象 实验结论
在一支50 mL的注射器里充入20
mL NO,然后吸入5mL水,用乳胶
管和弹簧夹封住管口,振荡注射器 无明显现象 NO不溶于水
打开弹簧夹,快速吸入10 mL空气 无色气体变为红棕色,注 NO与O 反应生成红棕色的
2
后夹上弹簧夹 射器活塞向左移动 NO
2
红棕色气体变为无色,注
振荡注射器 NO 溶于水生成无色的NO
射器活塞继续向左移动 2
思考与交流
(1)将充满NO 的试管倒置在装满水的水槽里,会有什么现象?最终试管里剩余气体占试管体积的几
2
分之几?
(2)将一充满 NO 的试管倒置于水槽中,同时不断地缓慢通入O ,最终液体充满整个试管,该过程
2 2
的总反应式可表示为:_________________________________。
(3)将一充满 NO 气体的试管倒置于水槽中,同时不断地缓慢通入O ,最终液体充满整个试管,该
2
过程的总反应式可表示为:_________________________________。
(4)有一个倒置于水槽且装满水的容器,依次通入一定体积的NO、NO、O,充分反应后容器中仍
2 2
充满溶液,若NO与O 的物质的量之比为2:3,求NO 与NO的物质的量之比。
2 2
经典例题
一氧化氮和二氧化氮的性质
【例4】某无色混合气体中可能含有Cl 、O 、SO 、NO、NO 中的两种或多种气体。现将此混合气体通过
2 2 2 2
品红溶液后,品红溶液褪色,向剩余气体中通入空气,很快变为红棕色。下列对于原混合气体成分的判断
中正确的是( )
A.肯定有SO 、O 和NO B.肯定没有Cl、O 和NO
2 2 2 2 2
C.可能有Cl 和O D.肯定只有NO
2 2
【变4-1】无色的混合气体甲,可能含NO、CO、NO 、N 中的几种,将一定量的甲气体经过如图实验的
2 2 2
处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )A.NO 、N B.NO、CO
2 2 2
C.NO 、CO D.NO、CO、N
2 2 2 2
【变4-2】把少量NO 体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,
2
最后收集到的气体是( )
A.氧气 B.二氧化氮 C.二氧化氮和氧气 D.二氧化氮和一氧化氮
二氧化氮的性质探究实验
【例5】某化学学习小组为探究NO 和SO 的反应,特进行如下实验(如下图所示)。
2 2
图1 图2 图3
(1)图1两集气瓶中________(填“上”或“下”)瓶颜色深。
(2)图2中反应的现象是_______________________________。
(3)图3中“有红棕色气体产生”说明NO 和SO 反应的产物中有____,NO 在该反应中显_______性。
2 2 2
(4)由图2和图3中的现象写出NO 和SO 反应的化学方程式:__________。
2 2
【例6】某课外活动小组欲探究镁与NO 的反应。已知镁与CO 的反应为2Mg+CO 2MgO+C
2 2 2
(1)该小组类比Mg与CO 的反应对Mg与NO 的反应进行猜测,写出Mg与NO 反应的化学方程式:
2 2 2
____________________________。
(2)该小组设计如下实验验证上述猜测,实验装置(用于连接玻璃管的乳胶管均内衬锡纸)如图所示。
资料信息:2NO +2NaOH===NaNO +NaNO +H O
2 2 3 2
①装置A中的试剂是____________。
②干燥管和装置B的作用分别是___________________、_________________。
③正确的实验操作步骤是______ 。
a.通入NO b.打开弹簧夹
2
c.点燃酒精灯 d.当硬质玻璃管充满红棕色气体后,关闭弹簧夹二氧化氮与水的反应
【例7】四支试管中分别充满NO、SO 、NO 、Cl 中的一种,把它们分别倒立于盛有水的水槽中,充分放
2 2 2
置后的现象如图所示。其中原试管充满NO 的是( )
2
A B C D
【变7-1】如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管
内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复
后,试管内完全被水充满,原来试管中盛装的不可能是( )
A.NO与NO 的混合气体 B.O 与NO 的混合气体
2 2 2
C.N 与NO 的混合气体 D.NO 一种气体
2 2 2
【变7-2】相同条件下,两个容积相同的试管分别装满NO 和NO气体,分别倒置于水槽中,然后通过导管
2
缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内充满液体。假设试管内的溶质不向水槽中扩散,则
两个试管内溶质物质的量浓度之比为( )
A.1∶1 B.5∶7 C.7∶5 D.4∶3
【例8】如图所示:在B水槽中装有500 mL水,容积为a mL的试管A充满了NO 和NO的混合气体(标准
2
状况),将试管A倒插入B水槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL。
(1)将A倒插入B槽中发生反应的化学方程式为_______________________________________,该反应中
氧化剂与还原剂的质量比为________,原混合气体中NO 和NO的物质的量之比为________。
2
(2)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是
_____________________________________________________________________。
(3)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为
________ mol·L−1(设溶液的体积仍为500 mL)。【变8-1】有一充有20 mL NO 和O 混合气体的试管,倒置于盛有水的水槽中,充分反应后,仍有10 mL
2 2
无色气体,则原混合气体中NO 与O 体积比为(气体体积均在相同状况下测得)( )
2 2
A.2∶3 B.3∶2 C.3∶1 D.2∶5
【变8-2】有一个倒置于水槽且装满水的容器,依次通入一定体积的NO 、NO、O ,充分反应后容器中仍
2 2
充满溶液,则通入的NO 、NO、O 的体积比可能是____________。
2 2
①1:1:1 ②4:3:2 ③4:16:13 ④4:3:4
【变8-3】将V mL NO和NO 的混合气体通过水吸收后,得到无色气体A。将此无色气体A与等体积的O
2 2
通入水中充分吸收后,得到5 mL无色气体B,下列说法不正确的是( )
A.A气体是NO,B气体是O
2
B.A气体的体积是20 mL
C.V的取值范围是20 mL<V<60 mL
D.将盛有体积比为4:1 NO 和O 的混合气体的烧瓶倒立于水槽中充分反应后,烧瓶中所得溶液的物质的
2 2
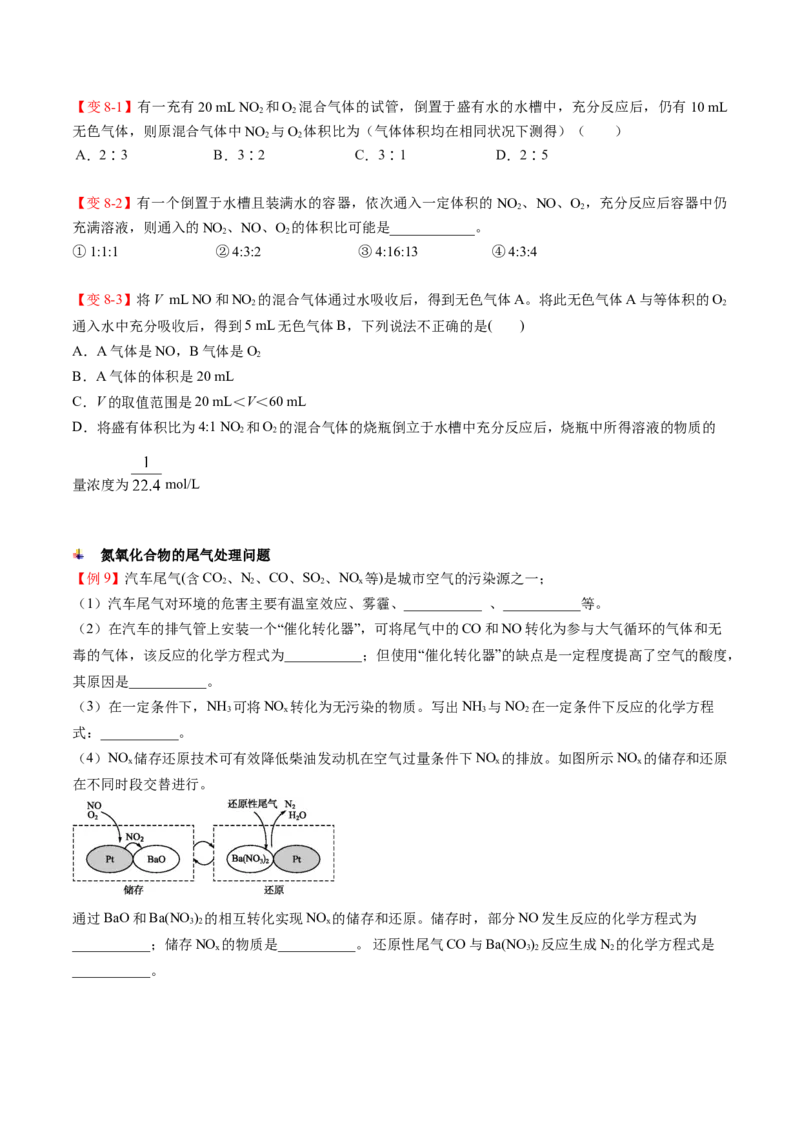
量浓度为 mol/L
氮氧化合物的尾气处理问题
【例9】汽车尾气(含CO、N、CO、SO 、NO 等)是城市空气的污染源之一;
2 2 2 x
(1)汽车尾气对环境的危害主要有温室效应、雾霾、___________ 、___________等。
(2)在汽车的排气管上安装一个“催化转化器”,可将尾气中的CO和NO转化为参与大气循环的气体和无
毒的气体,该反应的化学方程式为___________;但使用“催化转化器”的缺点是一定程度提高了空气的酸度,
其原因是___________。
(3)在一定条件下,NH 可将NO 转化为无污染的物质。写出NH 与NO 在一定条件下反应的化学方程
3 x 3 2
式:___________。
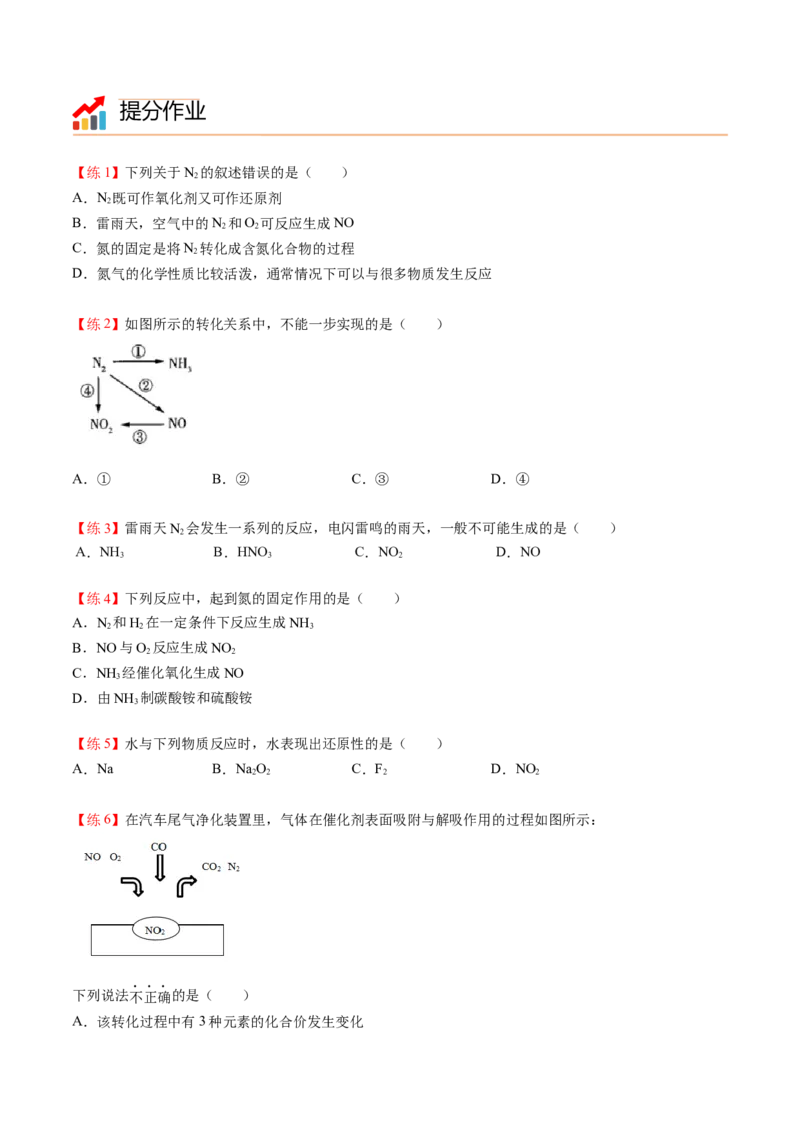
(4)NO 储存还原技术可有效降低柴油发动机在空气过量条件下NO 的排放。如图所示NO 的储存和还原
x x x
在不同时段交替进行。
通过BaO和Ba(NO ) 的相互转化实现NO 的储存和还原。储存时,部分NO发生反应的化学方程式为
3 2 x
___________;储存NO 的物质是___________。 还原性尾气CO与Ba(NO ) 反应生成N 的化学方程式是
x 3 2 2
___________。提分作业
【练1】下列关于N 的叙述错误的是( )
2
A.N 既可作氧化剂又可作还原剂
2
B.雷雨天,空气中的N 和O 可反应生成NO
2 2
C.氮的固定是将N 转化成含氮化合物的过程
2
D.氮气的化学性质比较活泼,通常情况下可以与很多物质发生反应
【练2】如图所示的转化关系中,不能一步实现的是( )
A.① B.② C.③ D.④
【练3】雷雨天N 会发生一系列的反应,电闪雷鸣的雨天,一般不可能生成的是( )
2
A.NH B.HNO C.NO D.NO
3 3 2
【练4】下列反应中,起到氮的固定作用的是( )
A.N 和H 在一定条件下反应生成NH
2 2 3
B.NO与O 反应生成NO
2 2
C.NH 经催化氧化生成NO
3
D.由NH 制碳酸铵和硫酸铵
3
【练5】水与下列物质反应时,水表现出还原性的是( )
A.Na B.NaO C.F D.NO
2 2 2 2
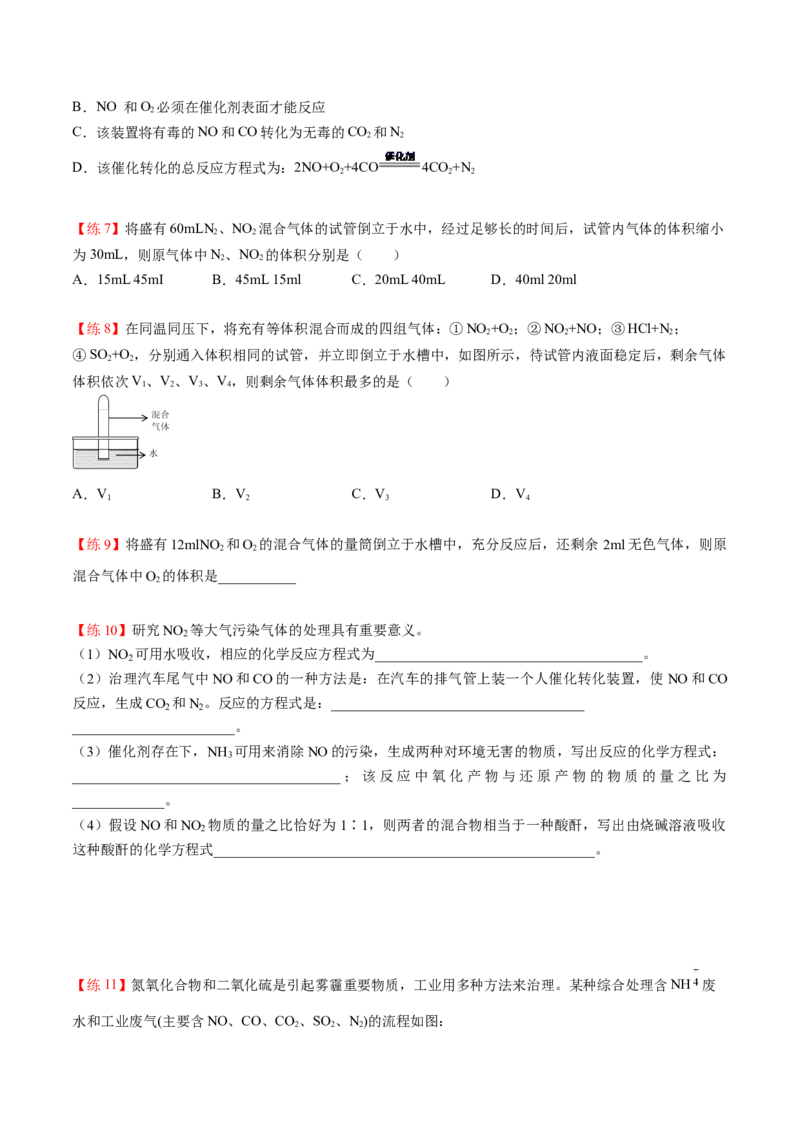
【练6】在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示:
下列说法不正确的是( )
A.该转化过程中有3种元素的化合价发生变化B.NO 和O 必须在催化剂表面才能反应
2
C.该装置将有毒的NO和CO转化为无毒的CO 和N
2 2
D.该催化转化的总反应方程式为:2NO+O +4CO 4CO+N
2 2 2
【练7】将盛有60mLN 、NO 混合气体的试管倒立于水中,经过足够长的时间后,试管内气体的体积缩小
2 2
为30mL,则原气体中N、NO 的体积分别是( )
2 2
A.15mL 45mI B.45mL 15ml C.20mL 40mL D.40ml 20ml
【练8】在同温同压下,将充有等体积混合而成的四组气体:①NO +O ;②NO +NO;③HCl+N ;
2 2 2 2
④SO +O ,分别通入体积相同的试管,并立即倒立于水槽中,如图所示,待试管内液面稳定后,剩余气体
2 2
体积依次V、V、V、V,则剩余气体体积最多的是( )
1 2 3 4
A.V B.V C.V D.V
1 2 3 4
【练9】将盛有12mlNO 和O 的混合气体的量筒倒立于水槽中,充分反应后,还剩余 2ml无色气体,则原
2 2
混合气体中O 的体积是___________
2
【练10】研究NO 等大气污染气体的处理具有重要意义。
2
(1)NO 可用水吸收,相应的化学反应方程式为______________________________________。
2
(2)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装一个人催化转化装置,使 NO和CO
反应,生成CO 和N 。反应的方程式是:____________________________________
2 2
_______________________。
(3)催化剂存在下,NH 可用来消除NO的污染,生成两种对环境无害的物质,写出反应的化学方程式:
3
______________________________________;该反应中氧化产物与还原产物的物质的量之比为
_____________。
(4)假设NO和NO 物质的量之比恰好为1∶1,则两者的混合物相当于一种酸酐,写出由烧碱溶液吸收
2
这种酸酐的化学方程式______________________________________________________。
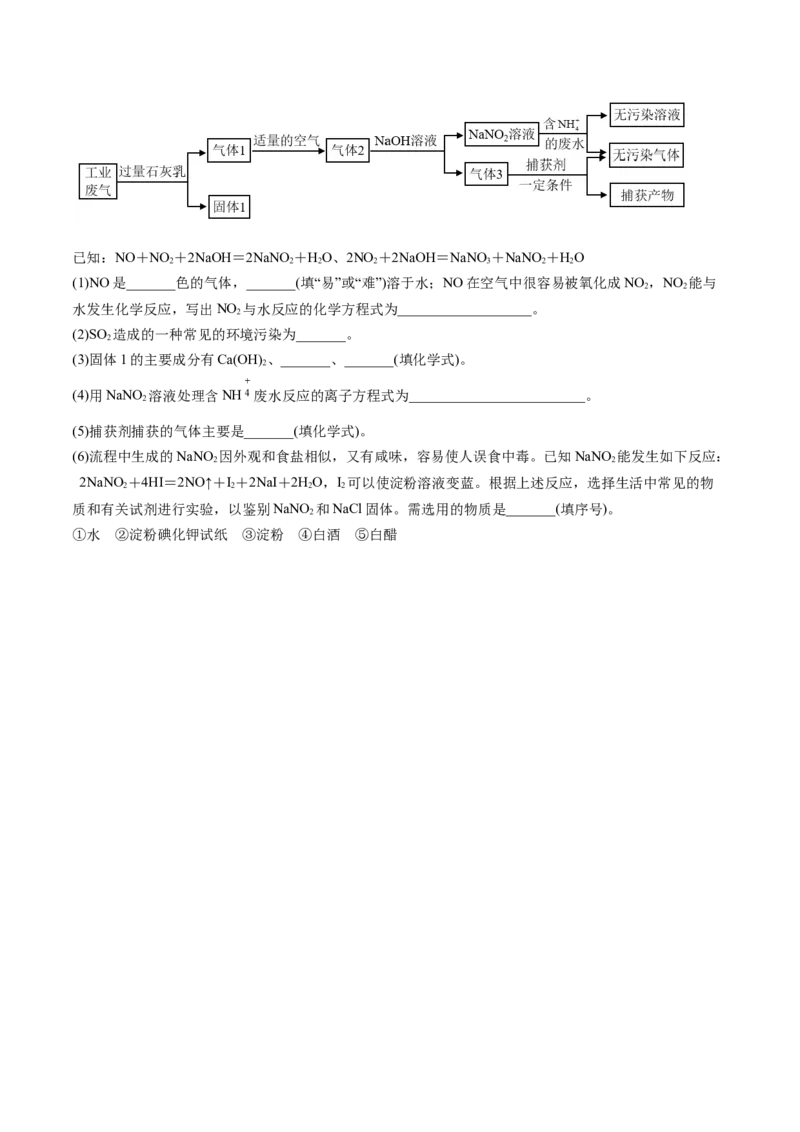
【练11】氮氧化合物和二氧化硫是引起雾霾重要物质,工业用多种方法来治理。某种综合处理含NH 废
水和工业废气(主要含NO、CO、CO、SO 、N)的流程如图:
2 2 2已知:NO+NO +2NaOH=2NaNO +HO、2NO +2NaOH=NaNO +NaNO +HO
2 2 2 2 3 2 2
(1)NO是_______色的气体,_______(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO ,NO 能与
2 2
水发生化学反应,写出NO 与水反应的化学方程式为___________________。
2
(2)SO 造成的一种常见的环境污染为_______。
2
(3)固体1的主要成分有Ca(OH) 、_______、_______(填化学式)。
2
(4)用NaNO 溶液处理含NH 废水反应的离子方程式为_________________________。
2
(5)捕获剂捕获的气体主要是_______(填化学式)。
(6)流程中生成的NaNO 因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO 能发生如下反应:
2 2
2NaNO +4HI=2NO↑+I+2NaI+2HO,I 可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物
2 2 2 2
质和有关试剂进行实验,以鉴别NaNO 和NaCl固体。需选用的物质是_______(填序号)。
2
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋