文档内容
第 04 讲 元素周期律
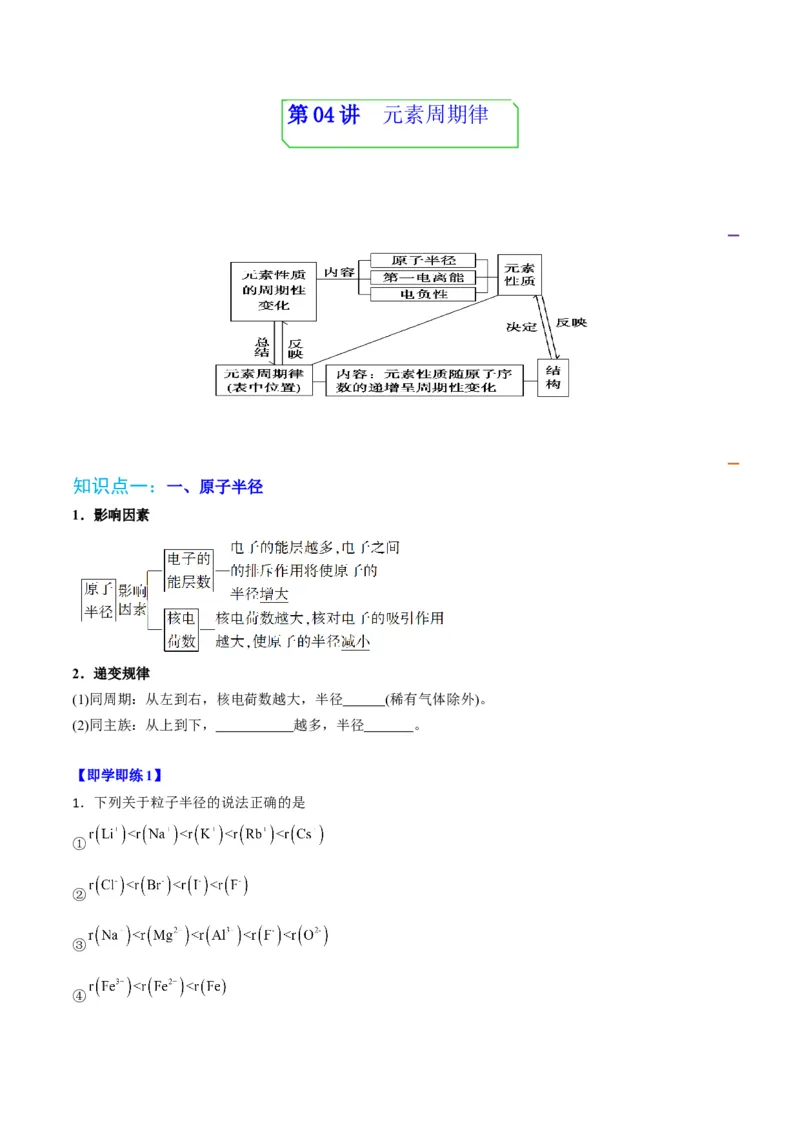
考点导航
知识精讲
知识点一:一、原子半径
1.影响因素
2.递变规律
(1)同周期:从左到右,核电荷数越大,半径 (稀有气体除外)。
(2)同主族:从上到下, 越多,半径 。
【即学即练1】
1.下列关于粒子半径的说法正确的是
①
②
③
④A.①②④ B.①③ C.③④ D.①④
2.下列元素的原子半径最小的是
A.Na B.Mg C.Al D.Cl
3.下列微粒半径的大小顺序不正确的是
A.F->O2->Na+>Mg2+ B.Fe>Fe2+>Fe3+
C.S2->Cl->K+>Ca2+ D.S>O>F
知识点二: 二、电离能
1.电离能的概念
失去一个电子转化为 所需要的 能量叫做第一电离能。
2.元素的第一电离能变化规律
(1)对同一周期的元素而言, 元素的第一电离能最小, 元素的第一
电离能最大;从左到右,元素的第一电离能在总体上呈现从 到 的变化趋势,表示元素原子越来越
难失去电子。
(2)同族元素,自上而下第一电离能 ,表明自上而下原子越来越 失去电子。
3.电离能的应用
可以衡量元素的原子失去一个电子的难易程度。第一电离能数值越 ,原子越容易失去一个电子,元
素金属性越 。
【即学即练2】
1.下列关于元素第一电离能的说法不正确的是
A.因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大
B.对于同一元素而言,原子的电离能I Na>K> Rb B.电负性: P>N>O>C
C.第一电离能: Na①>②
B.原子半径:③>②>①
C.第一电离能:③>①>②
D.电负性:③>②>①
知识点三:
三、电负性1.键合电子和电负性的含义
(1)键合电子:元素相互化合时,原子中用于形成化学键的电子。
(2)电负性:用来描述不同元素的原子对键合电子吸引力的大小。电负性越大的原子,对键合电子的吸引力
越大。
2.衡量标准
以氟的电负性为4.0 和锂的电负性为1.0 作为相对标准,得出各元素的电负性(稀有气体未计)。
3.递变规律(一般情况)
(1)同周期,自左到右,元素的电负性逐渐变大。
(2)同主族,自上到下,元素的电负性逐渐变小。
4.应用:判断金属性、非金属性强弱
【即学即练3】
1.下列有关电负性的说法中正确的是
A.主族金属元素的电负性比过渡金属元素的电负性更小
B.主族元素原子的电负性越大,其第一电离能也越大
C.在元素周期表中,同一周期主族元素电负性从左到右递增
D.形成化合物时,元素的电负性越大,吸引电子的能力越强,越容易显示正价
2.处于同一周期的A、B、C、D四种短周期元素,其气态原子获得一个电子所放出的能量A>B>C>D.
则下列说法正确的是
A.元素的非金属性:A<B<C<D
B.元素的电负性:A<B<C<D
C.元素的第一电离能:A<B<C<D
D.最高价氧化物对应水化物的酸性:A>B>C>D
3.下列各组元素的电负性大小顺序正确的是
A. B. C. D.
易错精析1.分析粒子半径大小比较的关键是什么?
【细剖精析】
2.第ⅡA族和ⅤA族元素的第一电离能比同周期的相邻元素都高,解释原因。
【细剖精析】
3.根据Na、Mg、Al的电离能数据,回答:
①为什么同一元素的电离能逐级增大?
②为什么Na、Mg、Al的化合价分别为+1、+2、+3?
【细剖精析】
4.根据化合物SiC、CCl 判断,Si、C、Cl的电负性由大到小的顺序是什么?
4
【细剖精析】
5.根据铝元素和氯元素的电负性差值判断,AlCl 是离子化合物还是共价化合物?为什么?
3
【细剖精析】
能力拓展
电负性的应用
1.判断元素的金属性和非金属性
(1)金属元素的电负性一般小于1.8,非金属元素的电负性一般大于1.8,而位于金属、非金属界线两侧的元
素的电负性则在1.8左右,它们既有金属性,又有非金属性。
(2)金属元素的电负性越小,金属元素越活泼;非金属元素的电负性越大,非金属元素越活泼。
2.判断元素的化合价
(1)电负性数值小的元素在化合物中吸引电子的能力弱,元素的化合价为正值。
(2)电负性数值大的元素在化合物中吸引电子的能力强,元素的化合价为负值。
3.判断化学键的类型
一般认为:
(1)如果两个成键元素原子间的电负性差值大于1.7,它们之间通常形成离子键。
(2)如果两个成键元素原子间的电负性差值小于1.7,它们之间通常形成共价键。
4.解释元素“对角线”规则
在元素周期表中,某些主族元素与其右下方的主族元素(如图所示)的有些性质是相似的,被称为“对角线
规则”。
这可以由元素的电负性得到解释:Li、Mg的电负性分别为1.0、1.2;Be、Al的电负性分别为1.5、1.5;
B、Si的电负性分别为2.0、1.8。它们的电负性接近,说明它们对键合电子的吸引力相当,它们表现出的性
质相似,如Li、Mg在空气中燃烧的产物分别为LiO和MgO;Be(OH) 、Al(OH) 均属于难溶的两性氢氧化
2 2 3
物;B、Si的含氧酸都是弱酸等。电负性是不同元素的原子对键合电子吸引力大小的量度,电负性越大,非金属性越强。电负性的大小能用
来判断元素之间的成键类型,也可以用来判断元素化合价的正负。电负性相同或差值小的非金属元素的原
子之间形成的化学键主要是共价键,当电负性差值为零时通常形成非极性共价键;差值不为零时,形成极
性共价键;而且差值越小,形成的共价键极性越弱。
分层提分
题组A 基础过关练
1.关于氟、氯的性质递变规律,描述不正确的是
A.原子半径:F<Cl B.原子得电子能力:F<Cl
C.单质氧化性:F >Cl D.热稳定性:HF>HCl
2 2
2.下列叙述中正确的是
A.同一周期中,ⅦA族元素的原子半径最大
B.ⅥA族元素的原子,其半径越大,越难失去电子
C.室温时,0族元素的单质都是气体
D.同一周期中,碱金属元素的第一电离能最大
3.下列曲线表示卤族元素或其单质性质随核电荷数的变化趋势,正确的是
A. B. C. D.
4.下列变化规律不正确的是
A.硬度:Al>Mg>Na B.沸点:HI>HBr>HCl>HF
C.酸性:HClO >H SO >H PO D.原子半径:O>F>H
4 2 4 3 4
5.下列说法中,正确的是
A.原子序数为38的元素处于周期表的第四周期ⅡA族
B.第一电离能的大小可以作为判断金属性强弱的依据
C.共价化合物中,电负性大的成键元素通常表现为负价
D.第四周期的金属元素从左到右,元素的金属性依次减弱
6. 为两种元素的原子, 的阴离子与 的阳离子具有相同的电子层结构,则
A.原子半径: B.电负性:C.离子半径: D.第一电离:
7.下表列出了某短周期元素R的各级电离能数据(用 、 ……表示,单位为 )。
…
…
R 740 1500 7700 10500
下列关于元素R的判断正确的是A.R的最高正价为 价 B.R元素位于元素周期表中第
Ⅱ族
C.R元素第一电离能大于同周期相邻元素 D.R元素基态原子的电子排布式为
8.短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是
Y Z W
元素最高价氧化物的水化
X
物
分子式 H ZO
3 4
0.1 mol·L-1溶液对应的pH 1.00 13.00 1.57 0.70
A.元素电负性: ZZ
题组B 能力提升练
1.处于同一周期的A、B、C、D四种短周期元素,其气态原子获得一个电子所放出的能量A>B>C>D.
则下列说法正确的是
A.元素的非金属性:A<B<C<D
B.元素的电负性:A<B<C<D
C.元素的第一电离能:A<B<C<D
D.最高价氧化物对应水化物的酸性:A>B>C>D
2.现有四种元素的基态原子的电子排布式如下:
① ;② ;③ ;④则下列有关比较中正确的是
A.最高正化合价:④>③=②>① B.电负性:④>③>②>①
C.原子半径:④>③>②>① D.第一电离能:④>③>②>①
3.下列叙述中正确的是
A.同周期元素中,ⅦA族元素的原子半径最大
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.同一元素的电离能I > I > I > I …
1 2 3 4
D.同一周期中,碱金属元素的第一电离能最小
4.下列各组比较正确的是
A.第一电离能:B>Al>Ga B.电负性:F>N>O
C.离子半径:K+>Cl->S2- D.原子半径:P>O>N
5.下列叙述正确的是
A.同周期元素(稀有气体元素除外)中,第ⅦA族元素的原子半径最大
B.第ⅥA族元素的原子,半径越大,越容易得到电子
C.电负性的大小可以作为判断元素金属性和非金属性强弱程度
D.同周期中(稀有气体除外),碱金属元素的第一电离能最大
6.工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
7.现有4种元素的基态原子的电子排布式如下:① ;② ;③ ;④ 。
下列比较中,正确的是
A.非金属性:④>②>③>① B.简单离子半径:①>③>②>④
C.原子半径:①>④>③>② D.元素的电负性:④>③>①>②
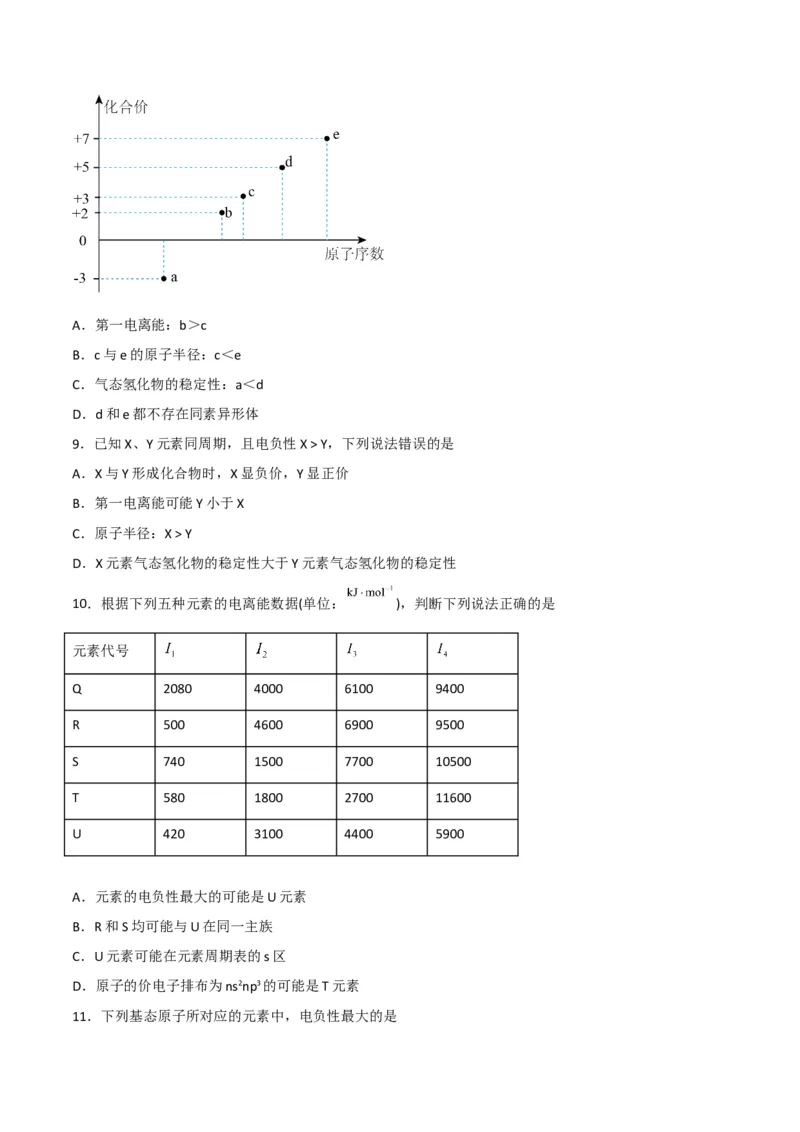
8.a~e为短周期元素,其原子序数与其某种化合价的关系如图所示。下列说法正确的是A.第一电离能:b>c
B.c与e的原子半径:c<e
C.气态氢化物的稳定性:a<d
D.d和e都不存在同素异形体
9.已知X、Y元素同周期,且电负性X > Y,下列说法错误的是
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能可能Y小于X
C.原子半径:X > Y
D.X元素气态氢化物的稳定性大于Y元素气态氢化物的稳定性
10.根据下列五种元素的电离能数据(单位: ),判断下列说法正确的是
元素代号
Q 2080 4000 6100 9400
R 500 4600 6900 9500
S 740 1500 7700 10500
T 580 1800 2700 11600
U 420 3100 4400 5900
A.元素的电负性最大的可能是U元素
B.R和S均可能与U在同一主族
C.U元素可能在元素周期表的s区
D.原子的价电子排布为ns2np3的可能是T元素
11.下列基态原子所对应的元素中,电负性最大的是A.电子排布式:1s22s22p63s2 B.外围电子排布式:4s24p3
C.电子排布式:[Ne]3s23p1 D.电子排布式:1s22s22p63s23p5倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育