文档内容
1.2 反应热的计算(精练)
题组一 盖斯定律
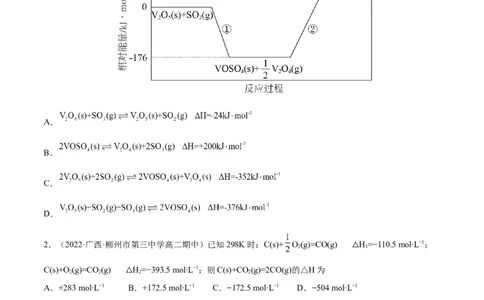
1.(2022·河南南阳·高二期末)硫酸工业中的钒催化剂参与反应的相对能量变化如图所示,下列热化学方
程式错误的是
A.
B.
C.
D.
2.(2022·广西·柳州市第三中学高二期中)已知298K时:C(s)+ O(g)=CO(g) H=−110.5 mol∙L−1;
2 1
△
C(s)+O(g)=CO (g) H=−393.5 mol∙L−1;则C(s)+CO(g)=2CO(g)的△H为
2 2 2 2
A.+283 mol∙L−1 △B.+172.5 mol∙L−1 C.−172.5 mol∙L−1 D.−504 mol∙L−1
3.已知下列热化学方程式:
HO(g)=H O(l) H=QkJ·mol-1;
2 2 1
C
2
H
5
OH(g)=C
2
H△5 OH(l) H=Q
2
kJ·mol-1;
C
2
H
5
OH(g)+3O
2
(g)=2CO△2 (g)+3H
2
O(g) H=Q
3
kJ·mol-1
。
若46g液体酒精完全燃烧,最后恢复到△室温,放出的热量为(单位:kJ)
A.3Q+Q +Q B.-(3Q +Q +Q ) C.-3Q +Q -Q D.3Q-Q +Q
1 2 3 1 2 3 1 2 3 1 2 3
4.已知下列热化学方程式:①
②
③
④
现有由2mol上述四种烃中的两种组成的气体混合物,经充分燃烧后放出2988kJ热量,则下列组合中不可
能的是
A. 和 B. 和 C. 和 D. 和
5.(2022·云南保山·高二期中)完成下列问题。
(1)常温下,0.1molCl 与焦炭、TiO 完全反应,生成一种还原性气体和一种易水解成TiO·xH O的液态化合
2 2 2 2
物,放热4.28kJ,该反应的热化学方程式为_______。
(2)联氨(又称肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。已知:
2 4
①2O(g)+N(g)=NO(1) H
2 2 2 4 1
②N
2
(g)+2H
2
(g)=N
2
H
4
(1) △H
2
③O
2
(g)+2H
2
(g)=2H
2
O(g) △H
3
④2N
2
H
4
(l)+N
2
O
4
(l)=3N
2
(g)△+4H
2
O(g) H
4
=-1048.9kJ/mol
上述反应热效应之间的关系式为△H
4
=△_______,联氨和N
2
O
4
可作为火箭推进剂的主要原因为_______。
(3)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
①与汽油相比,氢气作为燃料的优点是_______(至少答出两点)。
②利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
6.氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH(g)+HO(g)=CO(g)+3H (g) ΔH=206.2 kJ·mol-1①
4 2 2
CH(g)+CO (g)=2CO(g)+2H(g) ΔH=247.4 kJ·mol-1②
4 2 2
又知CH 的燃烧热为890.3 kJ·mol-1。
4
(1)利用上述已知条件写出表示CH 燃烧热的热化学方程式:_______。
4
(2)以甲烷为原料制取氢气是工业上常用的制氢方法。CH(g)与HO(g)反应生成CO(g)和H(g)的热化学方
4 2 2 2
程式为_______。
(3)若在相同温度下,1 mol H O按下列两种途径转化为氢原子与氧原子。
2则ΔH、ΔH、ΔH 三者之间的关系是_______。
1 2 3
题组二 反应热的计算
1.回答下列问题
(1)甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水放出热量222.5kJ,则甲烷燃烧的热化
学方程式为___________。
(2)已知:2SO (g)+O(g)=2SO(g) ΔH=-xkJ·mol-1
2 2 3
2NO(g)+O(g)=2NO (g) ΔH=-ykJ·mol-1
2 2
则反应NO (g)+SO (g)=SO(g)+NO(g)的ΔH=___________kJ·mol-1。
2 2 3
(3)已知:2H(g)+O(g)=2HO(g) ΔH=-483.6kJ·mol-1,
2 2 2
查阅文献资料,化学键的键能如下表:
化学键 H—H键 N≡N键 N—H键
E/(kJ·mol-1) 436 946 391
①氨分解反应NH (g)= N(g)+ H(g)的活化能E =300kJ·mol-1,则合成氨反应 N(g)+ H(g)=NH (g)的
3 2 2 al 2 2 3
活化能E =___________kJ·mol-1。
a2
②氨气完全燃烧生成N(g)和气态水的热化学方程式为___________。
2
(4)研究氮氧化物与悬浮的大气中海盐粒子的相互作用时,涉及如下反应:
Ⅰ.2NO(g)+NaCl(s)=NaNO (s)+ClNO(g) ΔH<0
2 3 1
Ⅱ.2NO(g)+Cl(g)=2ClNO(g) ΔH<0
2 2
则反应4NO (g)+2NaCl(s)=2NaNO (s)+2NO(g)+Cl(g)的ΔH=___________(用ΔH、ΔH 表示);
2 3 2 1 2
2.回答下列问题:
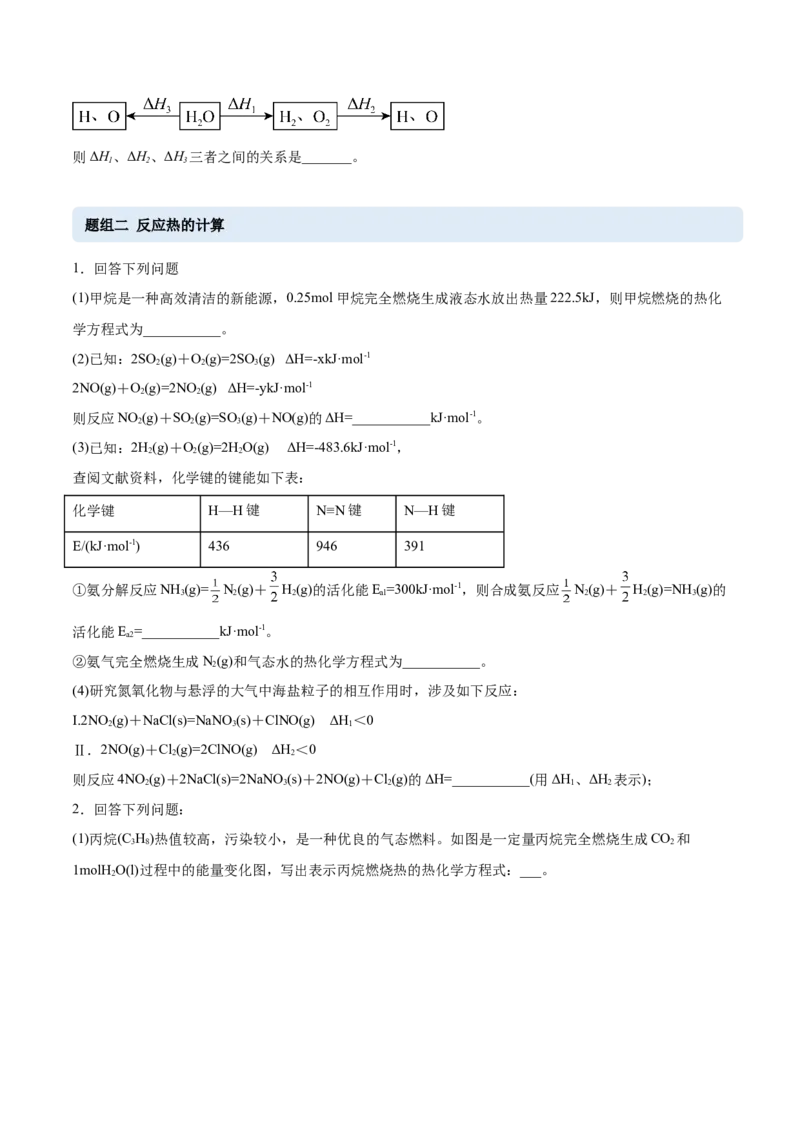
(1)丙烷(C H)热值较高,污染较小,是一种优良的气态燃料。如图是一定量丙烷完全燃烧生成CO 和
3 8 2
1molH O(l)过程中的能量变化图,写出表示丙烷燃烧热的热化学方程式:___。
2(2)已知:C(s,石墨)+O (g)=CO (g) H=-393kJ·mol-1
2 2 1
2H
2
(g)+O
2
(g)=2H
2
O(l) H
2
=-572kJ·m△ol-1
2C
2
H
2
(g)+5O
2
(g)=4CO
2
(△g)+2H
2
O(l) H
3
=-2598kJ·mol-1
根据盖斯定律,计算298K时由C(s△,石墨)和H
2
(g)生成1molC
2
H
2
(g)反应的焓变: H=__。
(3)已知25℃、101kpa时,一些物质的燃烧热为: △
化学式 CO(g) H(g) CHOH(l)
2 3
H/(kJ/mol) -283.0 -285.8 -726.5
△完成CO和H 生成CHOH的热化学方程式_ _。
2 3
(4)已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,放出xkJ热量。已知单质碳的燃烧热为ykJ/mol,则
1molC与O 反应生成CO的反应热 H为__kJ•mol-1。
2
3.回答下列问题: △
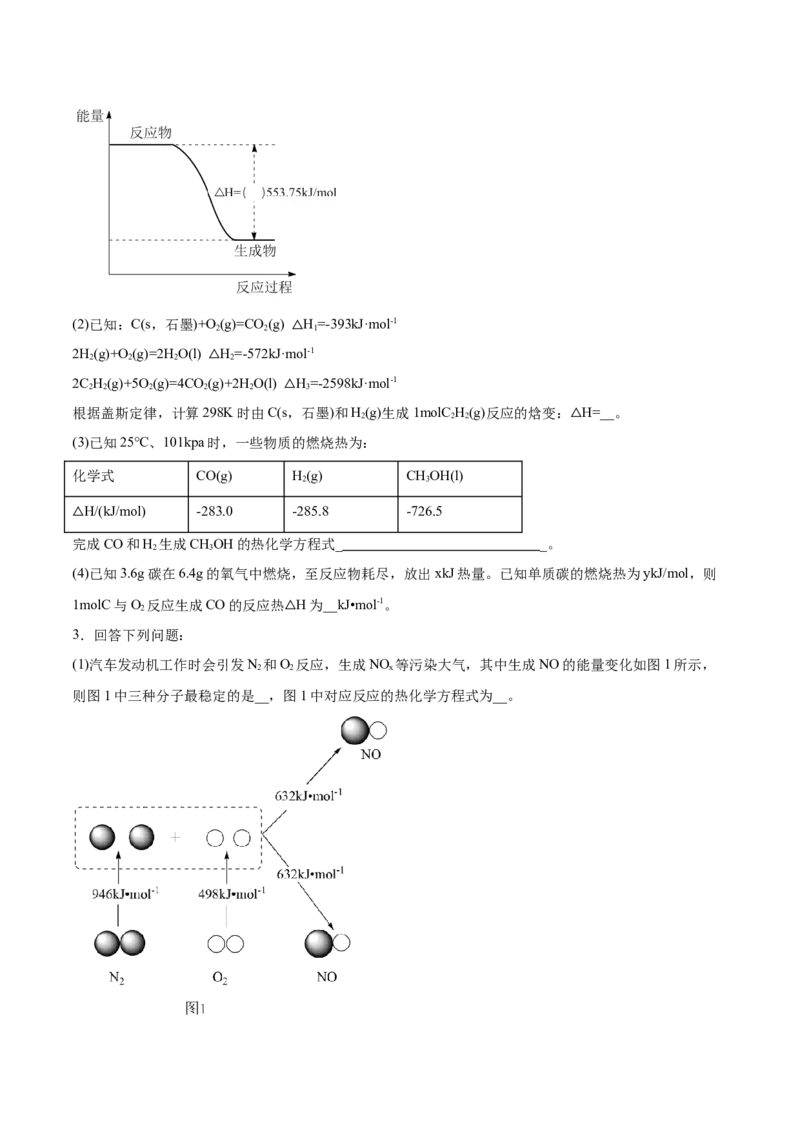
(1)汽车发动机工作时会引发N 和O 反应,生成NO 等污染大气,其中生成NO的能量变化如图1所示,
2 2 x
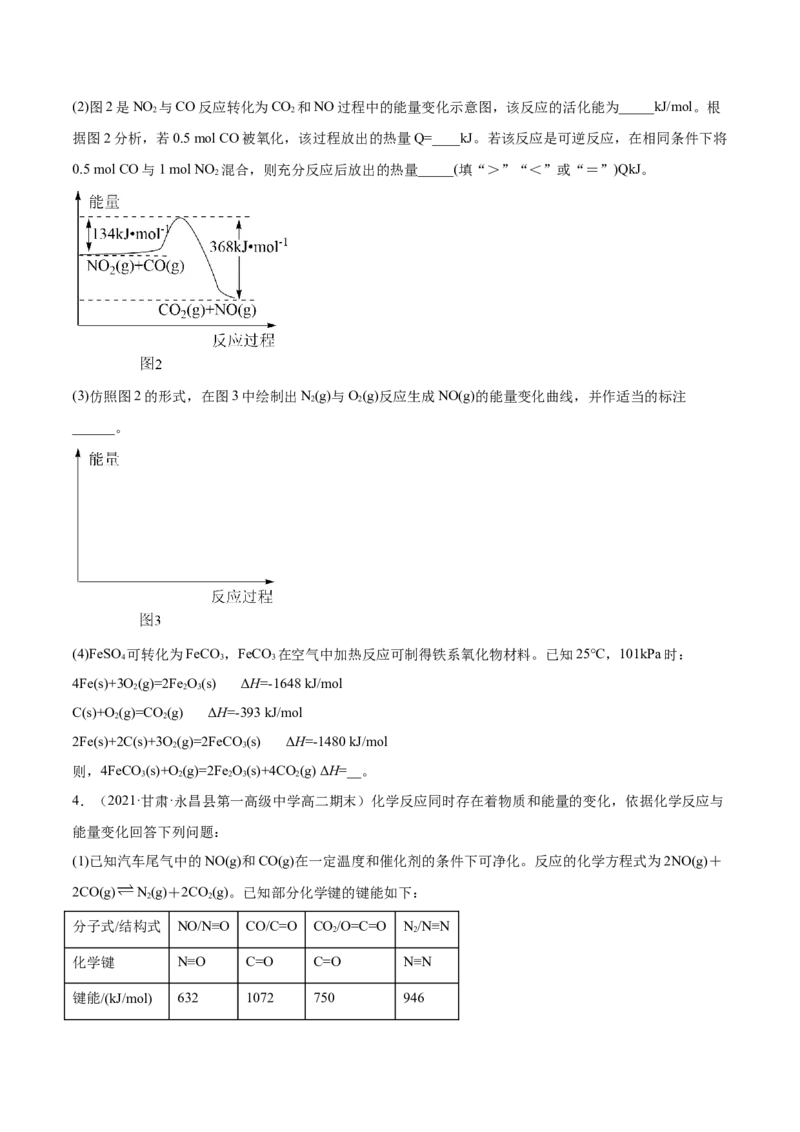
则图1中三种分子最稳定的是__,图1中对应反应的热化学方程式为__。(2)图2是NO 与CO反应转化为CO 和NO过程中的能量变化示意图,该反应的活化能为_____kJ/mol。根
2 2
据图2分析,若0.5 mol CO被氧化,该过程放出的热量Q=____kJ。若该反应是可逆反应,在相同条件下将
0.5 mol CO与1 mol NO 混合,则充分反应后放出的热量_____(填“>”“<”或“=”)QkJ。
2
(3)仿照图2的形式,在图3中绘制出N(g)与O(g)反应生成NO(g)的能量变化曲线,并作适当的标注
2 2
______。
(4)FeSO 可转化为FeCO,FeCO 在空气中加热反应可制得铁系氧化物材料。已知25℃,101kPa时:
4 3 3
4Fe(s)+3O (g)=2Fe O(s) ΔH=-1648 kJ/mol
2 2 3
C(s)+O(g)=CO (g) ΔH=-393 kJ/mol
2 2
2Fe(s)+2C(s)+3O (g)=2FeCO (s) ΔH=-1480 kJ/mol
2 3
则,4FeCO(s)+O(g)=2Fe O(s)+4CO(g) ΔH=__。
3 2 2 3 2
4.(2021·甘肃·永昌县第一高级中学高二期末)化学反应同时存在着物质和能量的变化,依据化学反应与
能量变化回答下列问题:
(1)已知汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。反应的化学方程式为2NO(g)+
2CO(g) N(g)+2CO(g)。已知部分化学键的键能如下:
2 2
分子式/结构式 NO/N≡O CO/C=O CO/O=C=O N/N≡N
2 2
化学键 N≡O C=O C=O N≡N
键能/(kJ/mol) 632 1072 750 946请计算上述反应的ΔH=_____kJ/mol。
(2)1gH 气体完全燃烧生成液态水放出143kJ热量,其热化学方程式为:_____。
2
(3)已知①2O(g)+N(g)=NO(l)ΔH;
2 2 2 4 1
②N(g)+2H(g)=NH(l)ΔH;
2 2 2 4 2
③O(g)+2H(g)=2HO(g)ΔH
2 2 2 3
④2NH(l)+N O(l)=3N (g)+4HO(g)ΔH =-1048.9kJ·mol-1
2 4 2 4 2 2 4
上述反应热效应之间的关系式为ΔH=_____。
4
(4)已知稀溶液中,H+(aq)+OH-(aq)=H O(l)ΔH=-57.3kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol水
2
时放出的热量比57.3kJ_____(填“大”“小”)。
(5)将1molCH 与Cl 发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗Cl 的物
4 2 2
质的量为_____。
5.(2021·北京市第三中学高二期中)书写下列化学方程式
(1)下图是1 mol NO 和1mol CO反应生成CO 和NO过程中能量变化示意图,请写出NO 和CO反应的热
2 2 2
化学方程式___________。
(2)已知:C(s) + O(g) = CO (g) ΔH=-437.3 kJ•mol-1
2 2
H(g) +1/2O(g) = HO(g) ΔH=-285.8 kJ•mol-1
2 2 2
CO(g) +1/2O (g) = CO (g) ΔH=-283.0 kJ•mol-1
2 2
则固态碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是___________。
(3)已知拆开1mol H-H键、1molN≡N和1mol N—H键分别需要的能量是436kJ、948kJ、391 kJ。则N、H
2 2
合成NH 的热化学方程式为:___________。
3
(4)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢
的方法之一。已知存在如下反应:
i.ii.
iii.
……
iii为积炭反应,利用 和 计算 时,还需要利用___________反应的 。
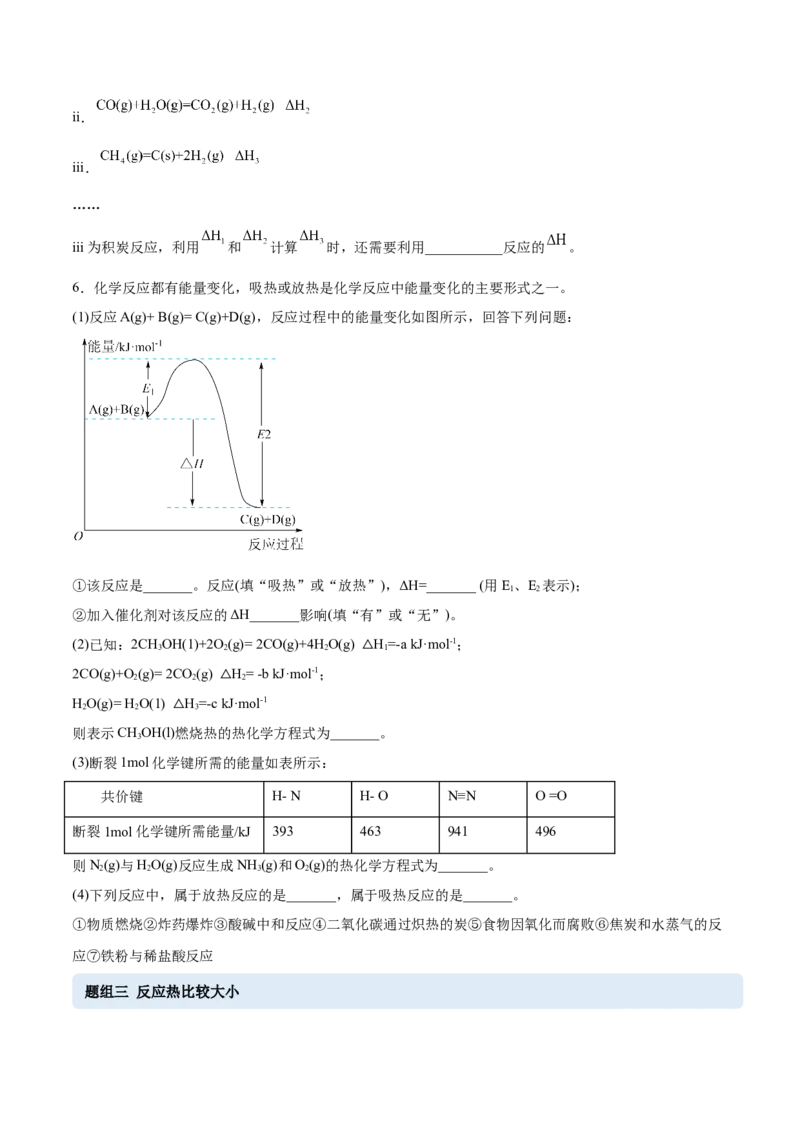
6.化学反应都有能量变化,吸热或放热是化学反应中能量变化的主要形式之一。
(1)反应A(g)+ B(g)= C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题:
①该反应是_______。反应(填“吸热”或“放热”),ΔH=_______ (用E、E 表示);
1 2
②加入催化剂对该反应的ΔH_______影响(填“有”或“无”)。
(2)已知:2CHOH(1)+2O (g)= 2CO(g)+4H O(g) H=-a kJ·mol-1;
3 2 2 1
2CO(g)+O 2 (g)= 2CO 2 (g) H 2 = -b kJ·mol-1; △
H
2
O(g)= H
2
O(1) H
3
=-c △kJ·mol-1
则表示CH
3
OH(l)△燃烧热的热化学方程式为_______。
(3)断裂1mol化学键所需的能量如表所示:
共价键 H- N H- O N≡N O =O
断裂1mol化学键所需能量/kJ 393 463 941 496
则N(g)与HO(g)反应生成NH (g)和O(g)的热化学方程式为_______。
2 2 3 2
(4)下列反应中,属于放热反应的是_______,属于吸热反应的是_______。
①物质燃烧②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的炭⑤食物因氧化而腐败⑥焦炭和水蒸气的反
应⑦铁粉与稀盐酸反应
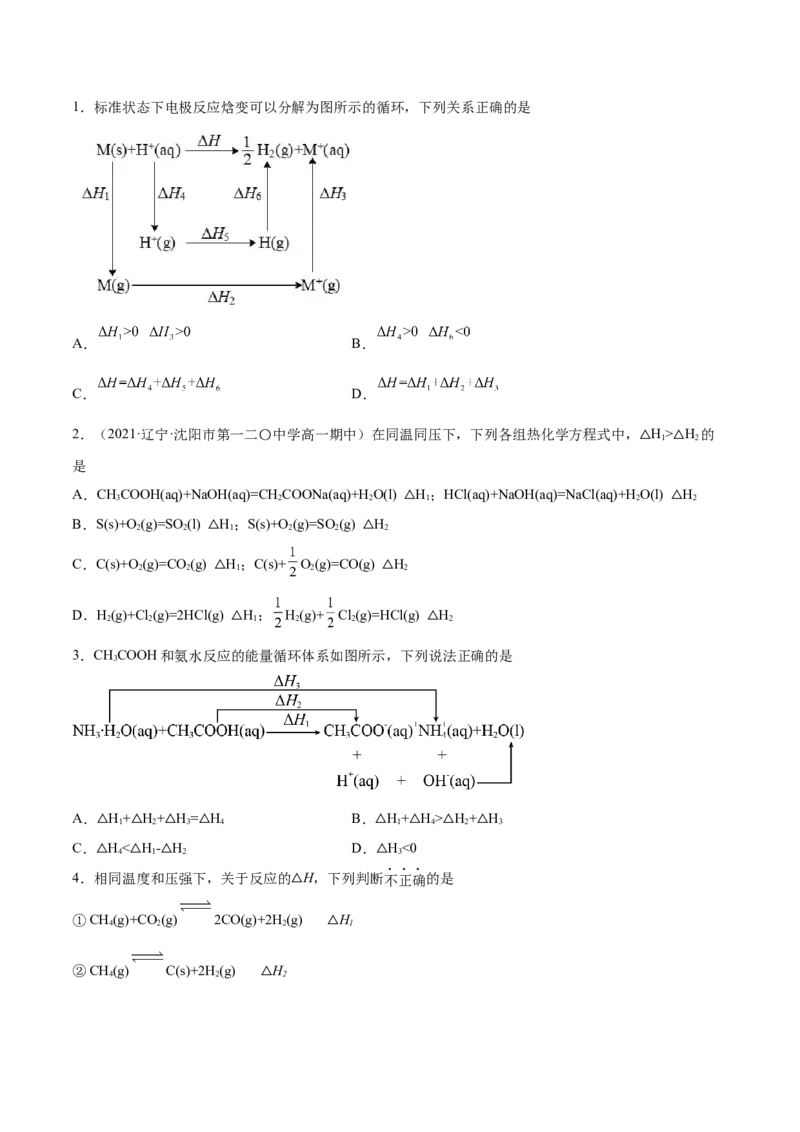
题组三 反应热比较大小1.标准状态下电极反应焓变可以分解为图所示的循环,下列关系正确的是
A. B.
C. D.
2.(2021·辽宁·沈阳市第一二〇中学高一期中)在同温同压下,下列各组热化学方程式中, H> H 的
1 2
是 △ △
A.CHCOOH(aq)+NaOH(aq)=CH COONa(aq)+H O(l) H;HCl(aq)+NaOH(aq)=NaCl(aq)+H O(l) H
3 2 2 1 2 2
B.S(s)+O 2 (g)=SO 2 (l) H 1 ;S(s)+O 2 (g)=SO 2 (g) H 2 △ △
△ △
C.C(s)+O(g)=CO (g) H;C(s)+ O(g)=CO(g) H
2 2 1 2 2
△ △
D.H(g)+Cl (g)=2HCl(g) H; H(g)+ Cl(g)=HCl(g) H
2 2 1 2 2 2
△ △
3.CHCOOH和氨水反应的能量循环体系如图所示,下列说法正确的是
3
A. H+ H+ H= H B. H+ H> H+ H
1 2 3 4 1 4 2 3
C.△H 4 <△H 1 -△H 2 △ D.△H 3 <△0 △ △
4.相△同温△度和△压强下,关于反应的 H,下列判断△不正确的是
△
①CH(g)+CO (g) 2CO(g)+2H(g) H
4 2 2 1
△
②CH(g) C(s)+2H(g) H
4 2 2
△③CO(g)+H(g) CO(g)+HO(g) H
2 2 2 3
△
④2CO(g) C(s)+CO(g) H
2 4
△
⑤CO(g)+H(g) C(s)+HO(g) H
2 2 5
△
A. H= H- H B. H>0, H>0
4 2 1 2 4
C.△H 5 =△H 2 +△H 3 - H 1 D.△H 3 >H 5 △
△ △ △ △ △
5.(2022·山西·临汾第一中学校高二期末)已知: ;
;
;
;
下列关于上述反应焓变的判断正确的是
A. , B. ,
C. D.
6.相同温度和压强下,关于反应的ΔH,下列判断正确的是
ClO—(aq)+H+(aq) HClO(aq) ΔH
1
HO(l) H+(aq)+OH—(aq) ΔH
2 2
ClO— (aq)+H O(l) OH—(aq)+HClO(aq) ΔH
2 3
A.ΔH>0,ΔH>0 B.ΔH=ΔH+ΔH
1 2 3 1 2
C.ΔH>ΔH D.ΔH<0,ΔH>0
1 3 2 3
7.(2022·湖南·雅礼中学高一期末)下列各组热化学方程式中,化学反应的 H前者大于后者的是
△
A.C(s)+O(g)=CO (g) H,C(s)+ O(g)=CO(g) H
2 2 1 2 2
△ △
B.S(s)+O (g)=SO(g) H,S(g)+O(g)=SO(g) H
2 2 3 2 2 4
△ △C.2H(g)+O(g)=2HO(l) H;H(g)+ O(g)=HO(l) H
2 2 2 5 2 2 2 6
△ △
D.;CaO(s)+H O(l)=Ca(OH) (s) H CaCO (s)=CaO(s)+CO (g) H
2 2 8 3 2 7
△ △
8.(2022·河北·石家庄二中高一期中)MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A.△H(MgCO )> H(CaCO)>0
1 3 1 3
B.△H
2
(MgCO
3
)<△H
2
(CaCO
3
)>0
C.△H
1
(MgCO
3
)-△H
1
(CaCO
3
)= H
3
(CaO)- H
3
(MgO)
D.对于MgCO
3
和△CaCO
3
,△H△1 + H
2
> H△3
9.回答下列关于焓变的问题: △ △
(1)已知S(g)+O(g)=SO(g) ΔH<0; S(s)+O (g)=SO(g) ΔH<0。则ΔH_______ΔH 。
2 2 1 2 2 2 1 2
(2)已知2H(g)+O(g)=2HO(g) ΔH<0;2H(g)+O(g)=2HO(l) ΔH<0。则ΔH_____ΔH 。
2 2 2 1 2 2 2 2 1 2
(3)已知H(g)+1/2O (g)=HO(l) ΔH<0;2H(g)+O(g)=2HO(l) ΔH<0。则ΔH 和ΔH 的定量关系为_______。
2 2 2 1 2 2 2 2 1 2
(4)等物质的量的金属钾和金属钠与水的反应为:2K(s)+2H O(l)=2KOH(aq)+H (g) ΔH<0;2Na(s)
2 2 1
+2H O(l)=2NaOH(aq)+H (g) ΔH<0。则ΔH_______ΔH 。
2 2 2 1 2
(5)等物质的量碳分别发生如下反应:C(s)+O(g)=CO (g) ΔH<0;C(s)+1/2O (g)=CO(g) ΔH<0;则
2 2 1 2 2
ΔH_______ΔH 。
1 2倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育