文档内容
第五章 化学生产中的重要非金属元素
第二节 氮及其化合物
第二课时 氨和铵盐
【学习目标】1.通过实验探究、讨论交流,从氨、铵盐的类别及氮元素价态的角度,了解氨与水、酸
或氧气的反应,知道氨的催化氧化反应是工业上制取硝酸的基础,知道铵盐是重要的氮肥。
2.通过对铵盐性质的学习,了解氨的实验室制取原理、装置、收集、检验等,知道铵盐(NH)的检验
方法,培养学以致用的理念。
【学习重点】氨和铵盐的性质、氨的制备和铵根离子的检验
【学习难点】氨的实验室制取实验设计
【课前预习】
旧知回顾:1.从元素化合价角度分析氮元素常见氧化物有哪些?
2.解答氮的氧化物(NO、NO )溶于水的计算问题应明确原理是什么?
2
新知预习:1.氨(NH )的主要性质特点及规律是什么?
3
2.氨的实验室制法原理、干燥及验满方法分别是什么?
①反应原理:
②干燥方法:
③验满方法:
【课中探究】情景导入:合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足
而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。(见PPT视频“天使与恶魔的化身”)
一、氨
活动一、氨的物理性质
任务一、阅毒教材P13页相关内容,观察氨或浓氨水样品,并打开闻其气味,回答氨具有哪些重要的
物理性质,并填写下表内容。
颜色 气味 密度 溶解性 沸点
【注意】
任务二、实验探究:观察教材P13页【实验5-6】:在干燥的圆底烧瓶中充满氨气,用带有玻璃管和
滴管(滴管里预先吸入水)的塞子塞紧瓶口,倒置烧瓶,使玻璃管插入盛有水(含酚酞)的烧杯中,轻轻挤压滴
管的胶头,使少量水进入烧瓶,装置如图。观察有何现象?可得出什么结论?
任务三、问题探究:(1)该喷泉实验中,引发喷泉的实验操作是什么?实验成功的关键是什么?
(2)形成喷泉的原理及条件是什么?请举例什么?
①喷泉产生的本质原因:
②类型:
③常见组合:
CO、Cl、HS、
2 2 2
气体 HCl NH NO +O
3 2 2
SO
2
吸收剂
④常见装置:【注意】
【对应训练】1.有关氨气的实验较多,下面对这些实验原理的分析中,正确的是( )
A.氨气极易溶于水,可以用来做喷泉实验
B.氨气的还原性可以解释氨气与氯化氢的反应实验
C.NH ·H O不稳定,实验室可用NH Cl和石灰水制取氨气
3 2 4
D.NH 液化时放出大量的热,因而,不能用氨作制冷剂
3
2.右图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )
A.该实验说明氨气极易溶于水
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水呈碱性
C.氨水很稳定,将烧瓶内的红色溶液加热颜色不会发生变化
D.形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压
活动二、氨的化学性质
任务一、讨论交流:【实验5-6】中,打开止水夹,挤压滴管的胶头,烧杯中的溶液由玻璃管进入烧
瓶后,烧瓶内液体为什么呈红色?你知道液氨和氨水有什么区别吗?
①溶解度:
②氨溶于水并与水反应反应:
③液氨与氨水的有何区别:
液氨 氨水
物质成分
粒子种类
主要性质
存在条件
【注意】
任务二、观察教材P14页图5-12(或观察视频实验),将分别蘸有浓氨水、浓盐酸的两支玻璃棒渐渐
靠近,观察现象,分析原因是什么?【注意】
任务三、阅读教材P14页相关内容,根据氧化还原反应原理,从元素化合价视角分析NH 还可能具有
3
哪些的化学性质?并举例说明。
【对应训练】1.关于氨的下列叙述中,不正确的是( )
A.氨极易溶于水,其水溶液能使湿润的蓝色石蕊试纸变红
B.氨具有还原性,可以被氧化为
C.液氨可用来作制冷剂
D.氨遇氯化氢气体产生白烟
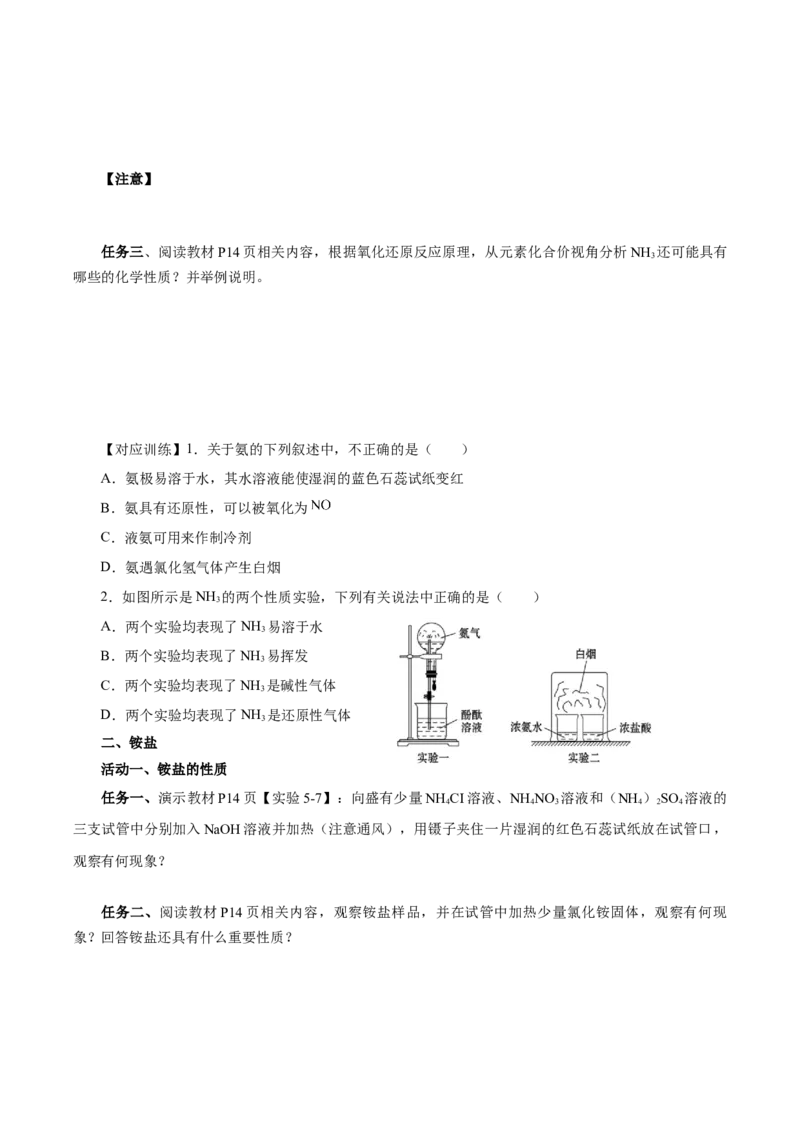
2.如图所示是NH 的两个性质实验,下列有关说法中正确的是( )
3
A.两个实验均表现了NH 易溶于水
3
B.两个实验均表现了NH 易挥发
3
C.两个实验均表现了NH 是碱性气体
3
D.两个实验均表现了NH 是还原性气体
3
二、铵盐
活动一、铵盐的性质
任务一、演示教材P14页【实验5-7】:向盛有少量NH CI溶液、NH NO 溶液和(NH ) SO 溶液的
4 4 3 4 2 4
三支试管中分别加入NaOH溶液并加热(注意通风),用镊子夹住一片湿润的红色石蕊试纸放在试管口,
观察有何现象?
任务二、阅读教材P14页相关内容,观察铵盐样品,并在试管中加热少量氯化铵固体,观察有何现
象?回答铵盐还具有什么重要性质?【对应训练】1.关于铵盐的叙述:①绝大多数铵盐易溶于水;②铵盐中氮元素均为-3价;③铵盐受
热易分解;④铵盐都只能跟碱反应,不能跟酸反应;⑤铵态氮肥不宜跟碱性物质如草木灰混合施用。其中
正确的是
A.①②③④⑤ B.③④⑤
C.①③⑤ D.①②④
2.下列描述正确的是( )
A.氯化铵和氯化钠的固体混合物可用升华法分离
B.将少量硫酸铵和熟石灰混合在研钵中进行研磨,可以闻到刺激性气味
C.检验某白色固体是铵盐的方法是:加氢氧化钠溶液,加热,用湿润蓝色石蕊试纸在试管口检验,
观察试纸是否变红
D.所有铵盐都易溶于水,铵盐中的氮元素均为-3价
活动二、氨的实验室制法
任务一、讨论交流:结合教材P15页“思考与讨论”栏目,思考实验室如何制备NH ?填写表格内容,
3
并注明其原因。
制备装置
制备原理
净化
装置
收集
装置
验满
方法
尾气
处理【注意】
任务二、问题探究:(1)根据下面甲、乙两个实验装置,你认为实验室制备氨还有哪些方法?
(2)实验中选择氨的干燥剂原则是什么?实验中氨不能直接排入空气中,如何进行尾气处理?
【对应训练】1.下列说法中正确的是( )
A.所有铵盐受热均可以分解,产物均有NH
3
B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C.NH Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH+OH-=====NH ↑+HO
4 3 2
D.NH Cl和NaCl的固体混合物可用升华法分离
4
2.下列叙述错误的是( )
A.利用如图装置可制取NH
3
B.将干燥的红色石蕊试纸接近图中a处,可观察到试纸变蓝
C.图中收集完NH 后,取下试管,在导管口b处堵上浸有稀硫酸的棉花可防止NH 污染空气
3 3D.进行图示实验时,可观察到液体迅速充满试管并变为红色,说明 极易溶于水,其水溶液显碱
性
【课后巩固】1.(易)教材作业:P18-19页练习1、2、3、4
2.(易)下列关于氨气的说法中正确的是( )
A.NH 转化为NH NO 属于氮的固定
3 4 3
B.氨水能导电,所以NH 是电解质
3
C.蘸有浓盐酸、浓硫酸的玻璃棒分别与蘸有浓氨水的玻璃棒相互靠近,都有白烟
D.气体能使湿润的红色石蕊试纸变蓝
3.(易)喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是( )
选项 气体 溶液 装置
A HS 稀盐酸
2
B HCl 稀氨水
C NO 稀HSO
2 4
D CO 饱和NaHCO 溶液
2 3
4.(中)下列由相关实验现象所推出的结论正确的是( )
A.NH 遇到浓盐酸产生白烟NH Cl,该反应不是氧化还原反应
3 4
B.向溶液中滴加HCl酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定有SO
3 2
C.NH Cl受热能分解生成NH ,可以用加热NH Cl的方法实验室制氨气
4 3 4
D.NH 通入水中,水溶液可以导电,NH 为电解质
3 3
5.(中)下列实验操作及实验现象均正确的是( )
实验目的 实验操作及实验现象
A.检验某溶液中含K+ 用铂丝蘸取某溶液,在酒精灯火焰上灼烧,观察到火焰呈紫色
B.检验加碘盐中的碘元素 取少量加碘盐于试管中,加水溶解,滴加几滴淀粉溶液,溶液变蓝
C.检验钠与水反应生成碱 向一只盛有水的小烧杯中滴加几滴酚酞溶液,然后投入一小块金属
性物质 钠,溶液变红
取少量样品于试管中,滴加NaOH溶液,加热试管,将湿润的蓝色
D.检验某溶液中含NH
石蕊试纸靠近试管口,试纸变红
6.(中)实验室用下图装置(夹持装置已略去)制备NH ,并研究其性质。其中,a、b为湿润的红色石
3
蕊试纸,下列关于NH 性质实验的说法中,不正确的是( )
3A.装置乙中,b先变蓝,a后变蓝
B.装置丙中,产生大量白烟
C.装置丁中,试剂可以是水
D.装置丁具有防止倒吸的作用
7.(难)氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备
和性质,设计了如图所示装置。下列说法错误的是( )
A.甲装置中的固体可以是NaOH或CaO
B.乙装置中的干燥剂可以是碱石灰
C.丙中发生的反应是4NH +5O=====4NO+6HO
3 2 2
D.若戊中观察到紫色溶液变红,则说明已制得HNO
3
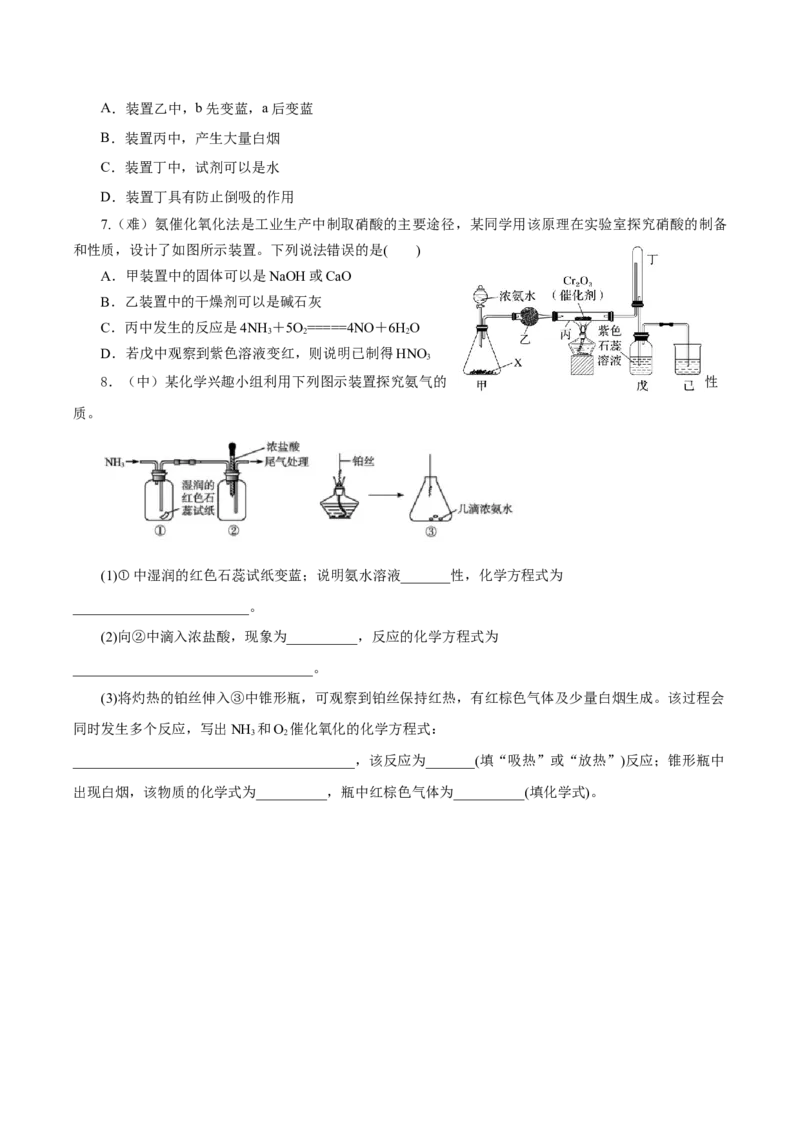
8.(中)某化学兴趣小组利用下列图示装置探究氨气的 性
质。
(1)①中湿润的红色石蕊试纸变蓝;说明氨水溶液_______性,化学方程式为
_________________________。
(2)向②中滴入浓盐酸,现象为__________,反应的化学方程式为
__________________________________。
(3)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会
同时发生多个反应,写出NH 和O 催化氧化的化学方程式:
3 2
________________________________________,该反应为_______(填“吸热”或“放热”)反应;锥形瓶中
出现白烟,该物质的化学式为__________,瓶中红棕色气体为__________(填化学式)。