文档内容
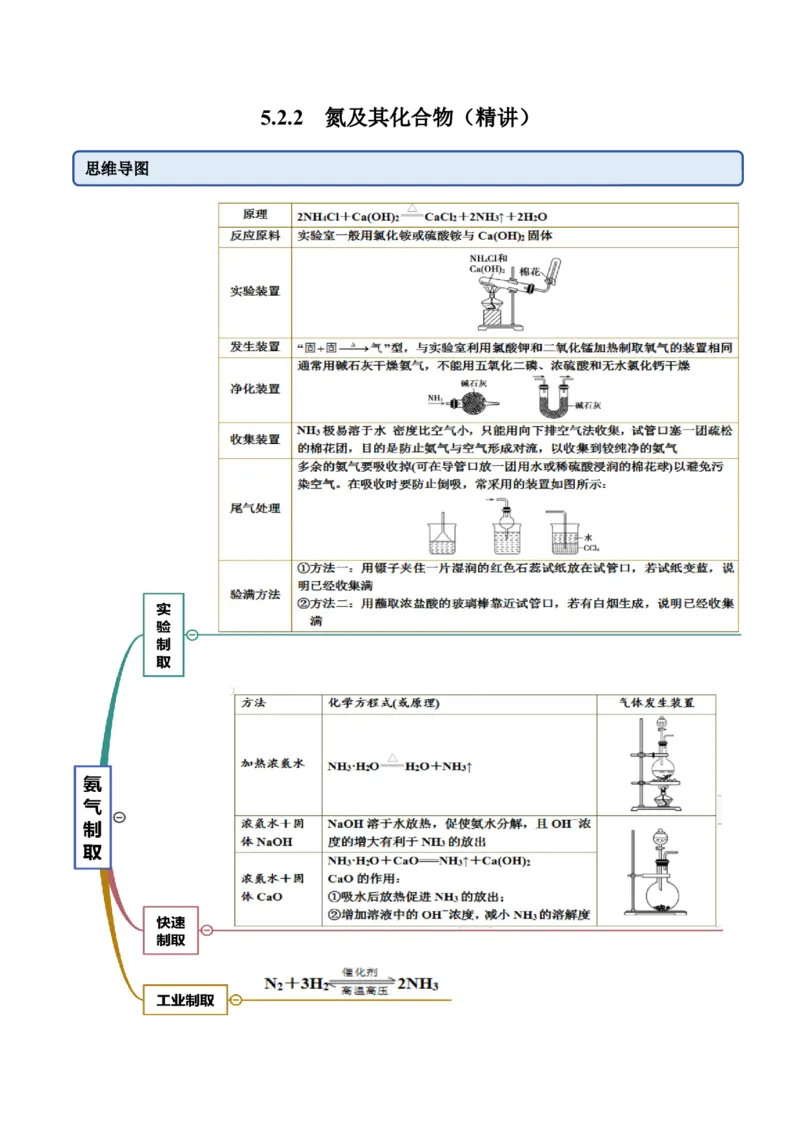
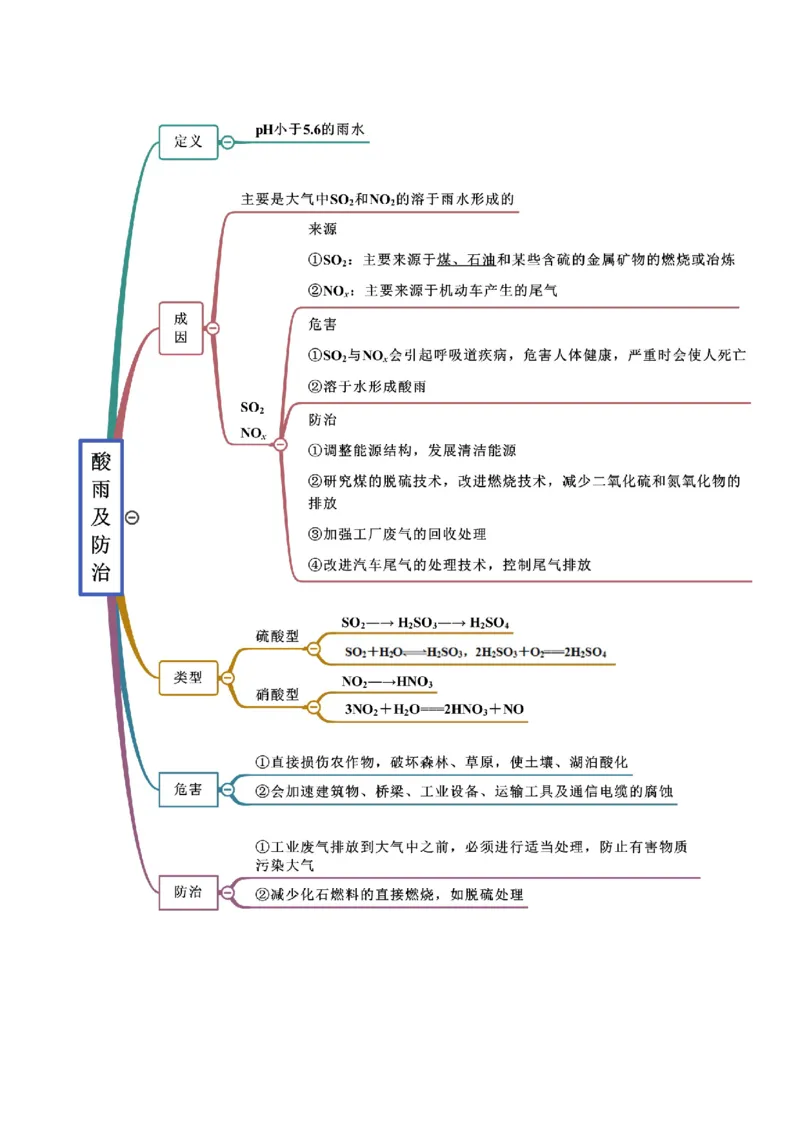
5.2.2 氮及其化合物(精讲)
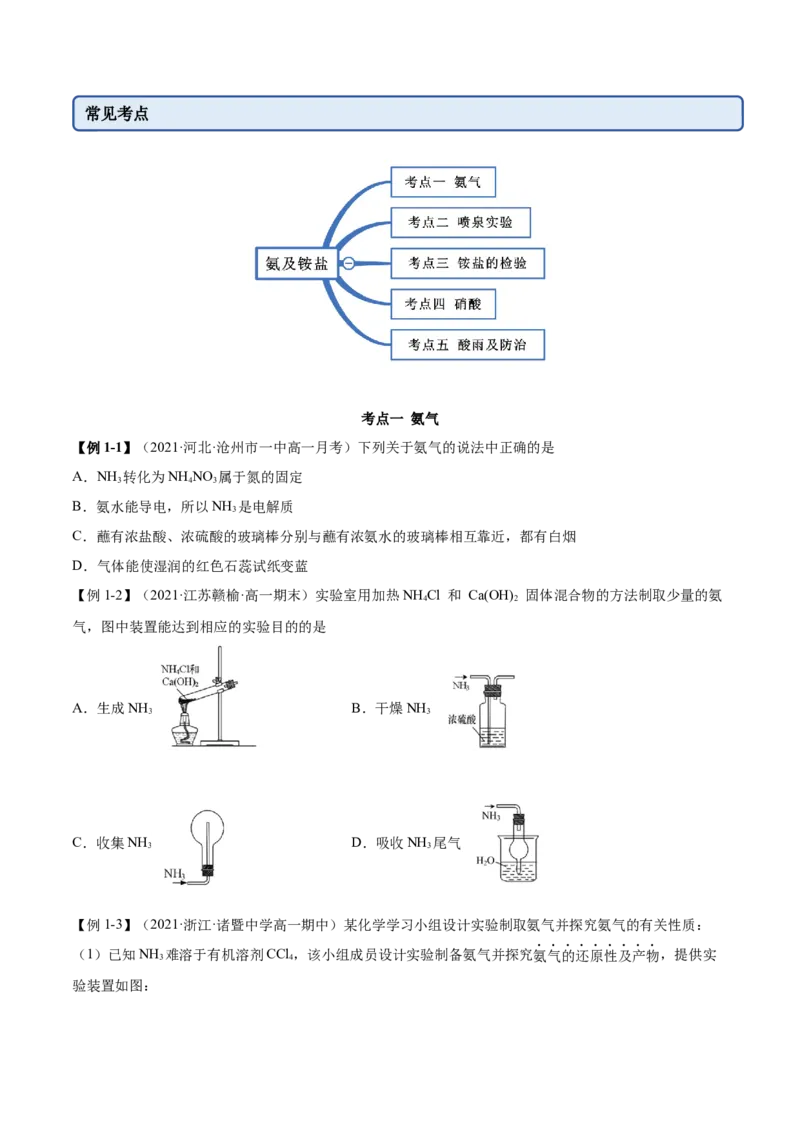
思维导图常见考点
考点一 氨气
【例1-1】(2021·河北·沧州市一中高一月考)下列关于氨气的说法中正确的是
A.NH 转化为NH NO 属于氮的固定
3 4 3
B.氨水能导电,所以NH 是电解质
3
C.蘸有浓盐酸、浓硫酸的玻璃棒分别与蘸有浓氨水的玻璃棒相互靠近,都有白烟
D.气体能使湿润的红色石蕊试纸变蓝
【例1-2】(2021·江苏赣榆·高一期末)实验室用加热NH Cl 和 Ca(OH) 固体混合物的方法制取少量的氨
4 2
气,图中装置能达到相应的实验目的的是
A.生成NH B.干燥NH
3 3
C.收集NH D.吸收NH 尾气
3 3
【例1-3】(2021·浙江·诸暨中学高一期中)某化学学习小组设计实验制取氨气并探究氨气的有关性质:
(1)已知NH 难溶于有机溶剂CCl ,该小组成员设计实验制备氨气并探究氨气的还原性及产物,提供实
3 4
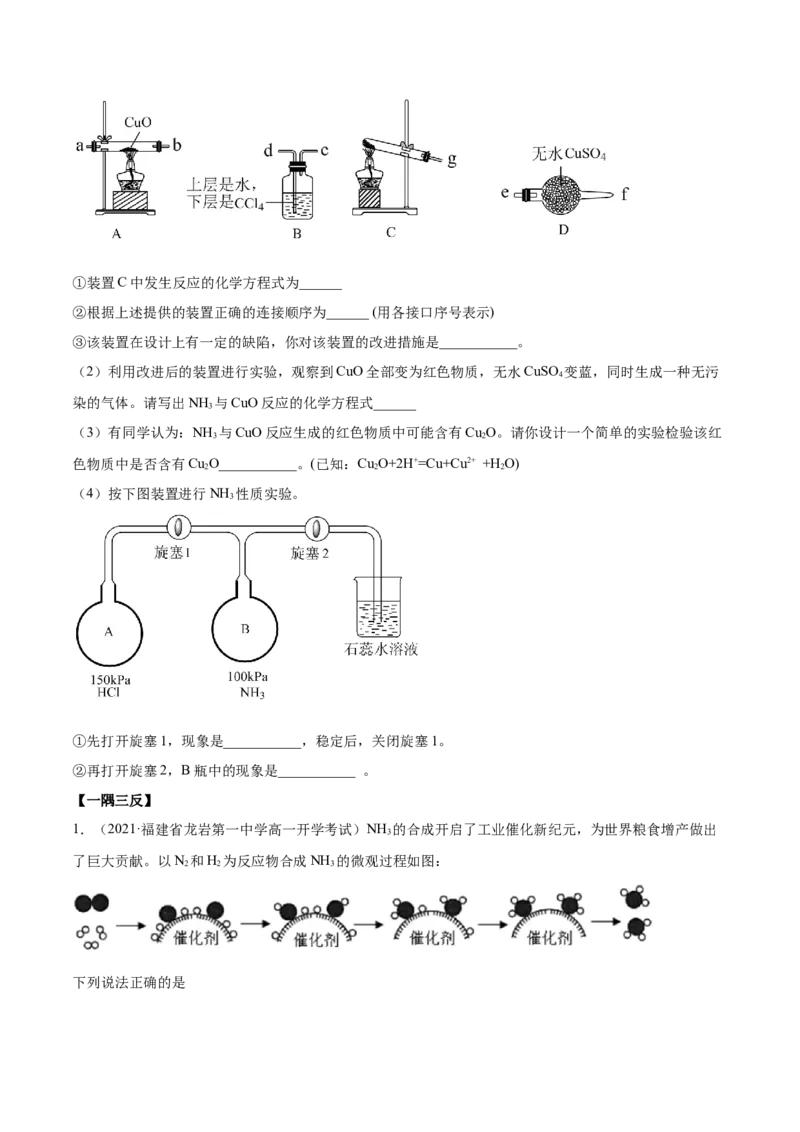
验装置如图:①装置C中发生反应的化学方程式为______
②根据上述提供的装置正确的连接顺序为______ (用各接口序号表示)
③该装置在设计上有一定的缺陷,你对该装置的改进措施是___________。
(2)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO 变蓝,同时生成一种无污
4
染的气体。请写出NH 与CuO反应的化学方程式______
3
(3)有同学认为:NH 与CuO反应生成的红色物质中可能含有Cu O。请你设计一个简单的实验检验该红
3 2
色物质中是否含有Cu O___________。(已知:Cu O+2H+=Cu+Cu2+ +H O)
2 2 2
(4)按下图装置进行NH 性质实验。
3
①先打开旋塞1,现象是___________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是___________ 。
【一隅三反】
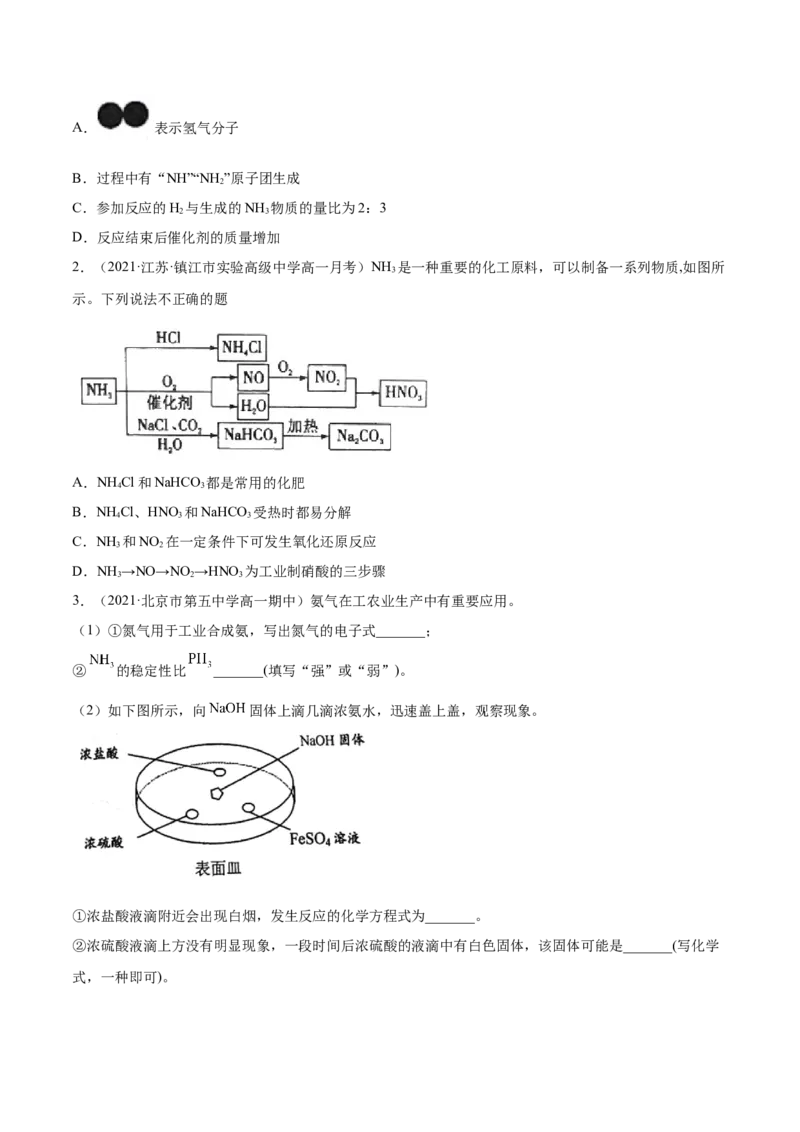
1.(2021·福建省龙岩第一中学高一开学考试)NH 的合成开启了工业催化新纪元,为世界粮食增产做出
3
了巨大贡献。以N 和H 为反应物合成NH 的微观过程如图:
2 2 3
下列说法正确的是A. 表示氢气分子
B.过程中有“NH”“NH ”原子团生成
2
C.参加反应的H 与生成的NH 物质的量比为2:3
2 3
D.反应结束后催化剂的质量增加
2.(2021·江苏·镇江市实验高级中学高一月考)NH 是一种重要的化工原料,可以制备一系列物质,如图所
3
示。下列说法不正确的题
A.NH Cl和NaHCO 都是常用的化肥
4 3
B.NH Cl、HNO 和NaHCO 受热时都易分解
4 3 3
C.NH 和NO 在一定条件下可发生氧化还原反应
3 2
D.NH →NO→NO →HNO 为工业制硝酸的三步骤
3 2 3
3.(2021·北京市第五中学高一期中)氨气在工农业生产中有重要应用。
(1)①氮气用于工业合成氨,写出氮气的电子式_______;
② 的稳定性比 _______(填写“强”或“弱”)。
(2)如下图所示,向 固体上滴几滴浓氨水,迅速盖上盖,观察现象。
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是_______(写化学
式,一种即可)。③ 液滴中先出现白色沉淀,写出离子反应方程式_______。白色沉淀迅速变成灰绿色沉淀,过一段时
间后变成红褐色,写出化学反应方程式_______。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO),反应的化学方程
2
式为_______。若反应中有 电子发生转移时,生成亚硝酸的质量为_______g(小数点后保留两位有效
数字)。
(4) 可以转化为其他含氮物质,下图为 转化为 的流程。
①写出 与 反应转化为 的化学方程式_______。
② 转化为 的整个过程中,为提高氮原子的利用率,可采取的措施是_______。
4.(2021·北京·中国农业大学附属中学高一期末)地球上的氮元素对动植物有重要作用,其中氨的合成与
应用是当前的研究热点。
(1)人工固氮最主要的方法是Haber-Bosch法。通常用以铁为主的催化剂在400~500℃和10~30MPa的条
件下,由氮气和氢气直接合成氨。写出反应的化学方程式___。
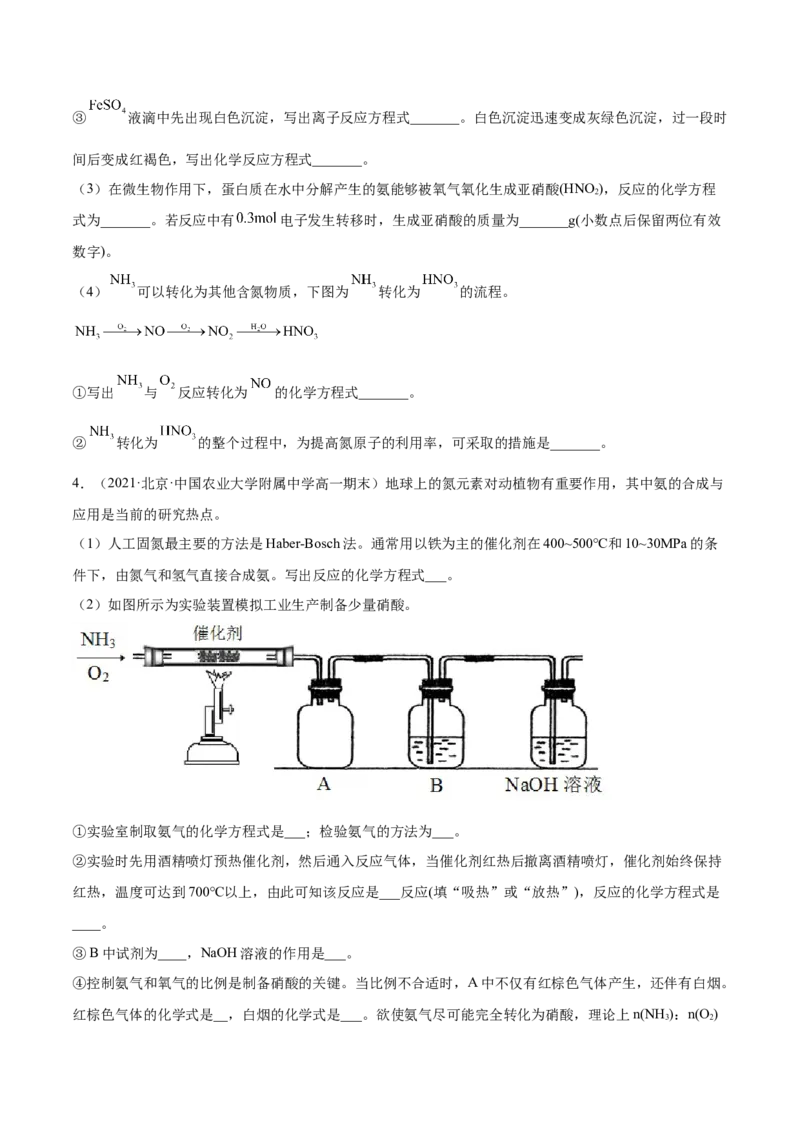
(2)如图所示为实验装置模拟工业生产制备少量硝酸。
①实验室制取氨气的化学方程式是___;检验氨气的方法为___。
②实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持
红热,温度可达到700℃以上,由此可知该反应是___反应(填“吸热”或“放热”),反应的化学方程式是
____。
③B中试剂为____,NaOH溶液的作用是___。
④控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。
红棕色气体的化学式是__,白烟的化学式是___。欲使氨气尽可能完全转化为硝酸,理论上n(NH ):n(O )
3 2的最佳比例为___。
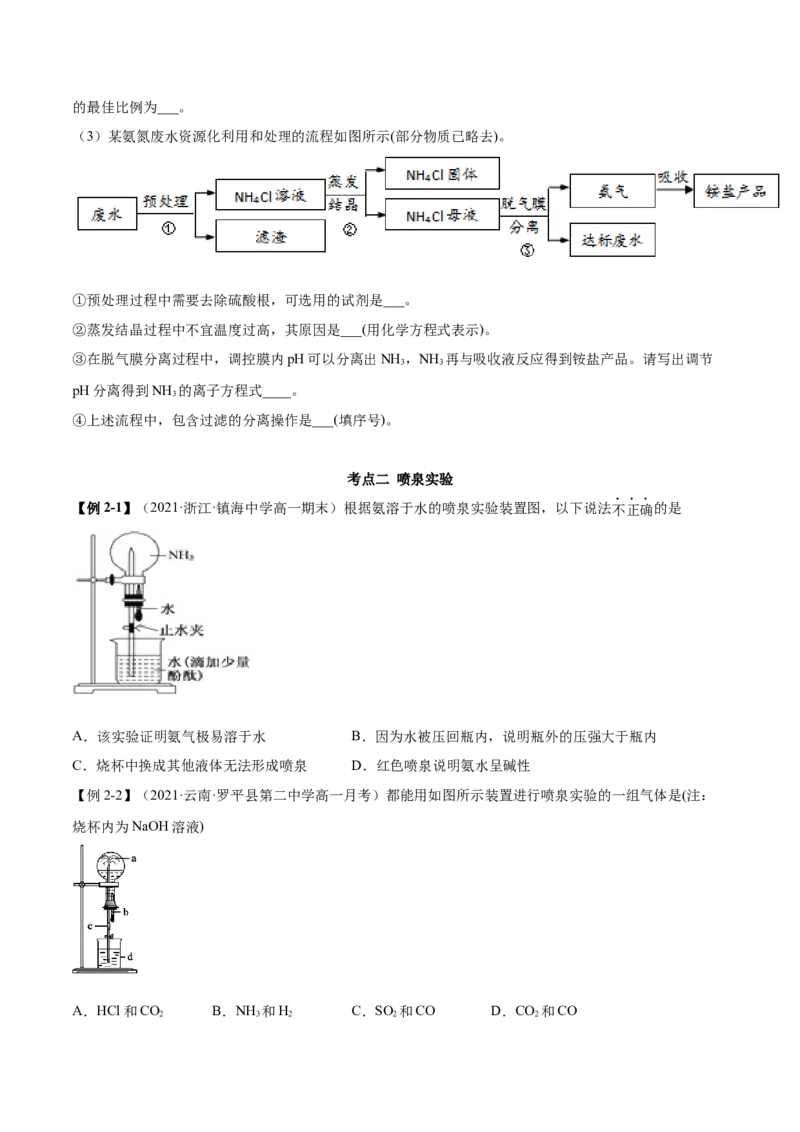
(3)某氨氮废水资源化利用和处理的流程如图所示(部分物质已略去)。
①预处理过程中需要去除硫酸根,可选用的试剂是___。
②蒸发结晶过程中不宜温度过高,其原因是___(用化学方程式表示)。
③在脱气膜分离过程中,调控膜内pH可以分离出NH ,NH 再与吸收液反应得到铵盐产品。请写出调节
3 3
pH分离得到NH 的离子方程式____。
3
④上述流程中,包含过滤的分离操作是___(填序号)。
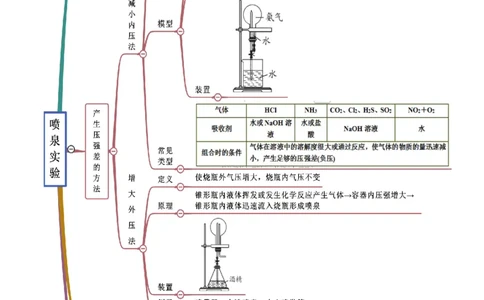
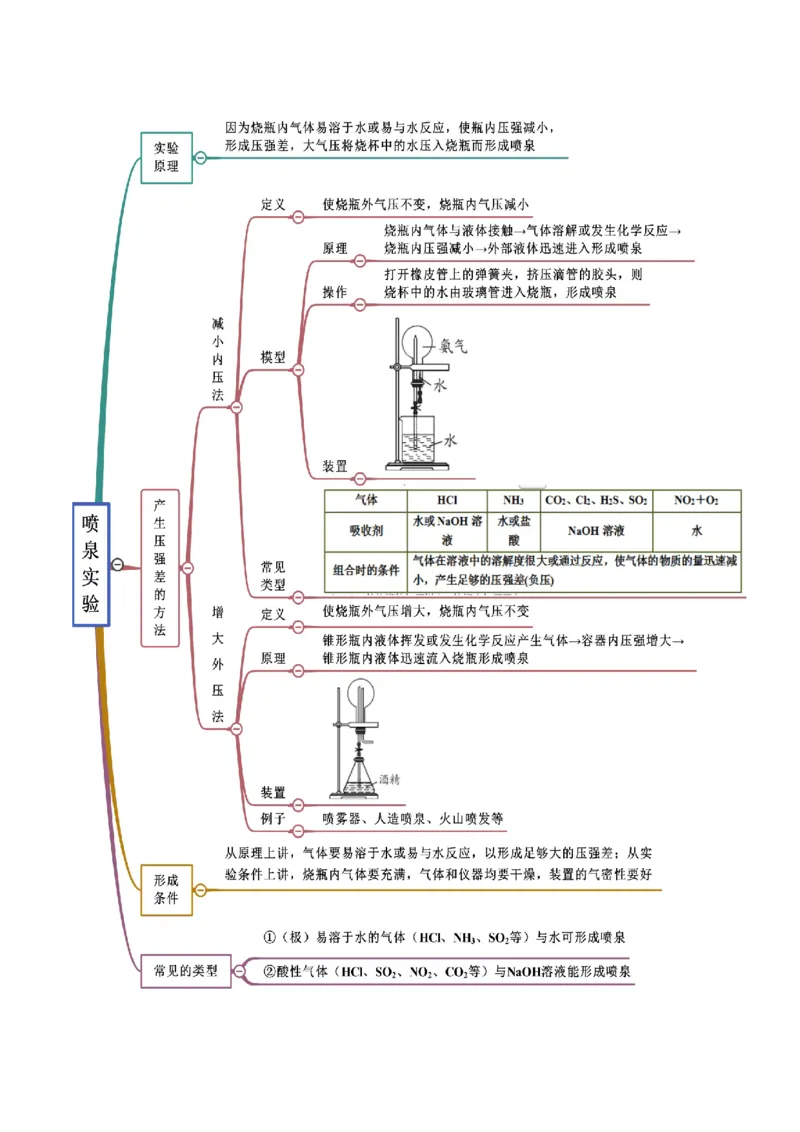
考点二 喷泉实验
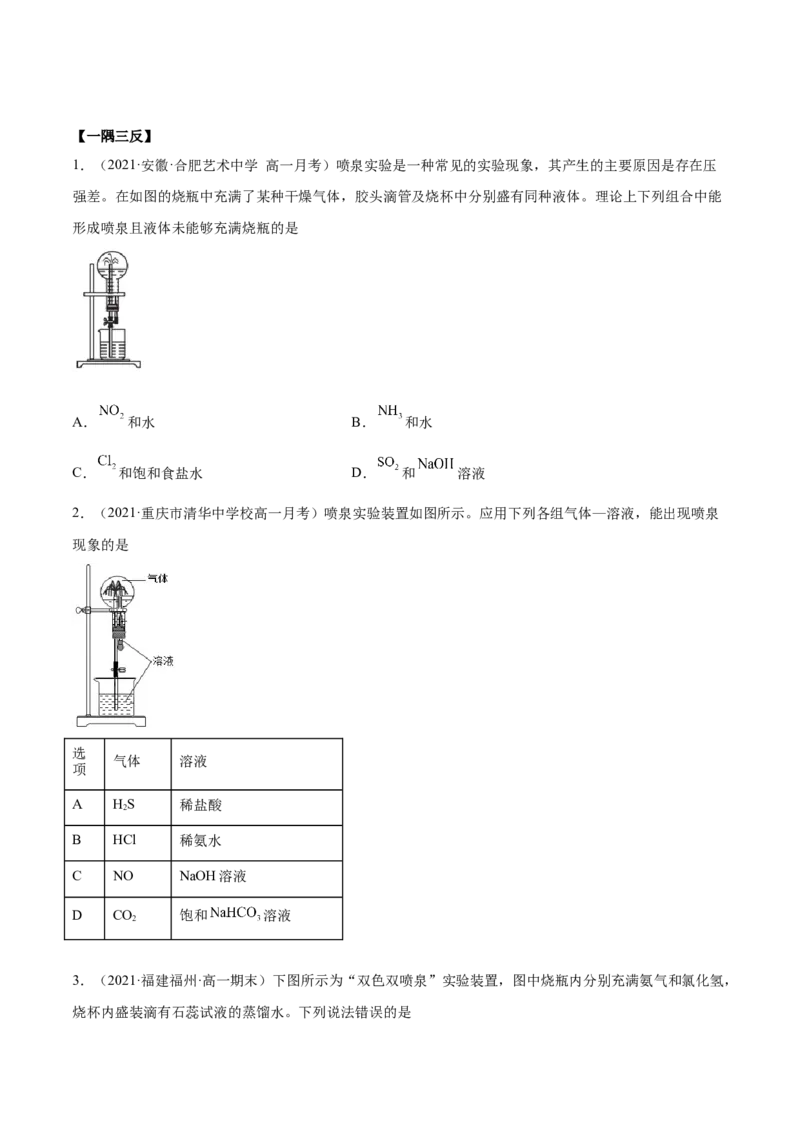
【例2-1】(2021·浙江·镇海中学高一期末)根据氨溶于水的喷泉实验装置图,以下说法不正确的是
A.该实验证明氨气极易溶于水 B.因为水被压回瓶内,说明瓶外的压强大于瓶内
C.烧杯中换成其他液体无法形成喷泉 D.红色喷泉说明氨水呈碱性
【例2-2】(2021·云南·罗平县第二中学高一月考)都能用如图所示装置进行喷泉实验的一组气体是(注:
烧杯内为NaOH溶液)
A.HCl和CO B.NH 和H C.SO 和CO D.CO 和CO
2 3 2 2 2【一隅三反】
1.(2021·安徽·合肥艺术中学 高一月考)喷泉实验是一种常见的实验现象,其产生的主要原因是存在压
强差。在如图的烧瓶中充满了某种干燥气体,胶头滴管及烧杯中分别盛有同种液体。理论上下列组合中能
形成喷泉且液体未能够充满烧瓶的是
A. 和水 B. 和水
C. 和饱和食盐水 D. 和 溶液
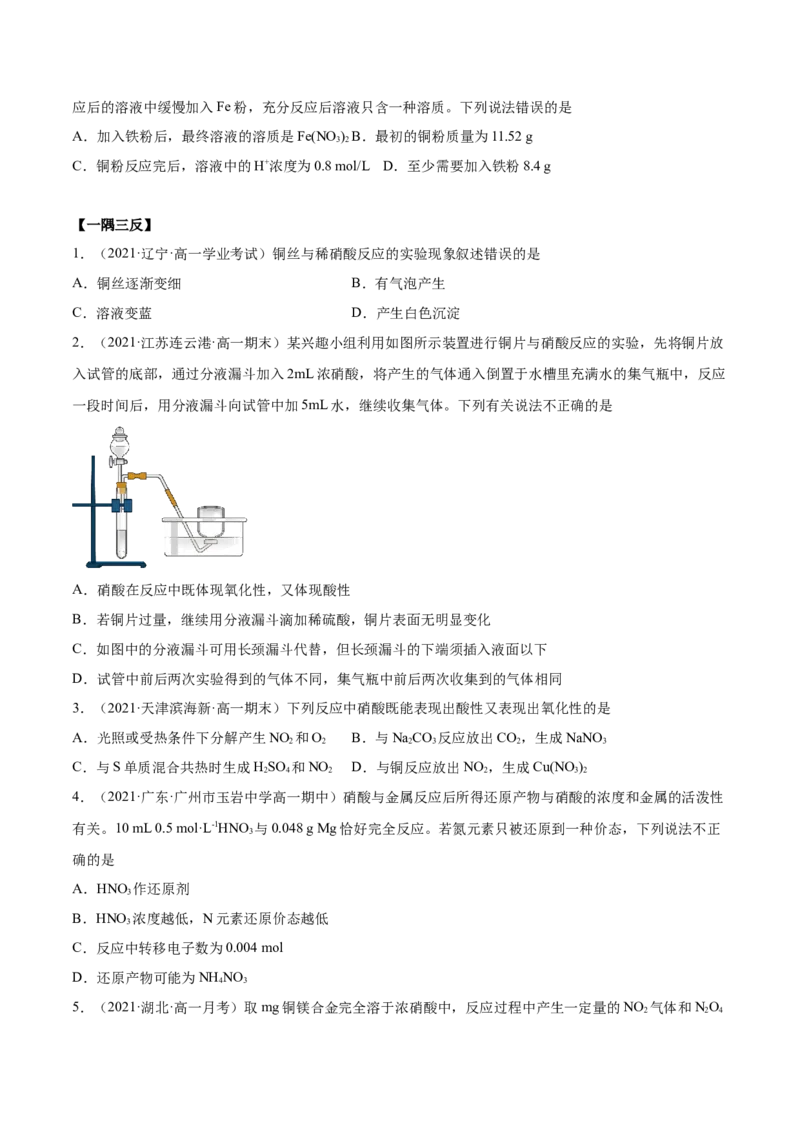
2.(2021·重庆市清华中学校高一月考)喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉
现象的是
选
气体 溶液
项
A HS 稀盐酸
2
B HCl 稀氨水
C NO NaOH溶液
D CO 饱和 溶液
2
3.(2021·福建福州·高一期末)下图所示为“双色双喷泉”实验装置,图中烧瓶内分别充满氨气和氯化氢,
烧杯内盛装滴有石蕊试液的蒸馏水。下列说法错误的是A.在实验室中,可用浓氨水和生石灰制备氨气,用浓盐酸和浓硫酸制备氯化氢
B.在实验室中制备干燥的氨气时可以选用碱石灰做干燥剂
C.实验中同时打开止水夹a、c、d,即可分别形成蓝色和红色喷泉
D.喷泉结束后,将烧瓶内溶液混合后蒸干,可得氯化铵固体
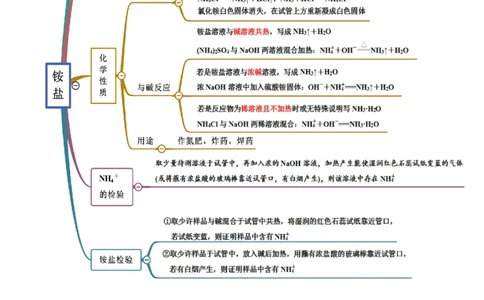
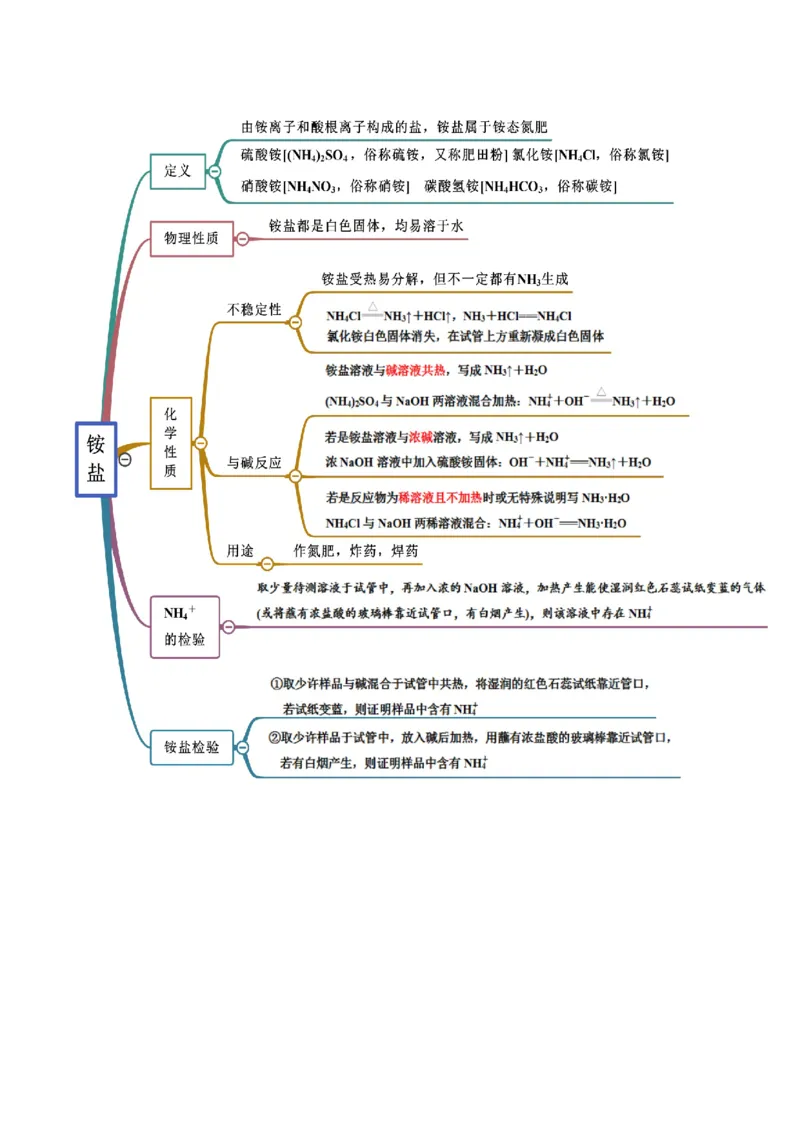
考点三 铵盐的检验
【例3-1】(2021·甘肃·金昌市第一中学高一期中)关于铵盐的叙述中正确的是
①所有铵盐中,氮元素化合价都是-3价 ②所有铵盐都溶于水 ③铵态氮肥不宜跟草木灰混合使用 ④铵
盐都是离子化合物 ⑤铵盐都能与碱反应,不能与酸反应
A.①③④ B.②③④ C.①②③④ D.①②③④⑤
【例3-2】(2021·河北·雄县第一高级中学高一月考)现有 、 、 、 四种溶液,
某化学兴趣小组设计如下实验可将其鉴别出来。实验步骤如下:
①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的
溶液、加热、将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
②向①中反应后的四支试管中,分别依次加入足量 溶液,观察到盛装B、C溶液的试管内产生白色
沉淀。
根据所学知识,按要求回答下列问题:
(1)溶液A、B、C、D中的溶质依次为___________、___________、___________、___________。(填化
学式)
(2)溶液B与 溶液共热时发生反应的化学方程式为___________。
(3)步骤②试管中产生的白色沉淀的化学式为___________。
(4)检验溶液D中溶质的阴离子的具体实验操作为___________,现象为___________,发生反应的化学
方程式为___________。
【一隅三反】1.(2021·河北·张家口市宣化第一中学高一期中)对于铵盐的描述都正确的是
①都溶于水 ②都是白色晶体 ③都有刺激性气味 ④加热后都有 放出 ⑤与碱混合后加热都
有 放出 ⑥都能使红色石蕊试纸变蓝
A.全部 B.①②⑤⑥ C.①②⑤ D.③④⑤
2.(2021·山西·浑源县第七中学校高一月考)检验铵盐的方法是将待检物取出少量放入试管中,然后
A.加热,用湿润的红色石蕊试纸放在试管口检验
B.加水溶解,用红色石蕊试纸检验溶液的酸碱性
C.加入碱溶液,加热,再滴入酚酞试液
D.加入苛性钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验
3.(2021·上海市长征中学高一期中)以下不是所有铵盐的通性的是
A.均为固体、能溶于水 B.都可分解放出氨气
C.都能与碱反应,且均放出氨气 D.都是离子化合物
4.(2021·吉林·通化县综合高级中学高一期中)下列实验能证明某溶液中不含有铵根离子的是
A.向溶液中加入石蕊溶液后,溶液呈红色
B.向溶液中加入酚酞溶液后,溶液呈红色
C.将溶液在试管中加热至沸腾,试管口放置的红色石蕊试纸不变色
D.将溶液中加入过量烧碱溶液加热至沸腾,试管口放置的红色石蕊试纸不变色
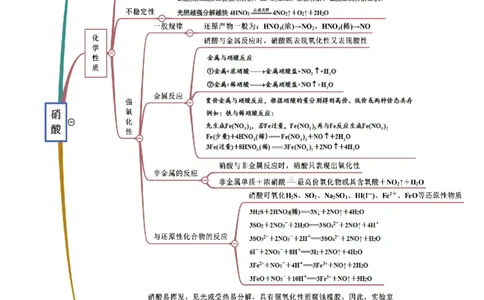
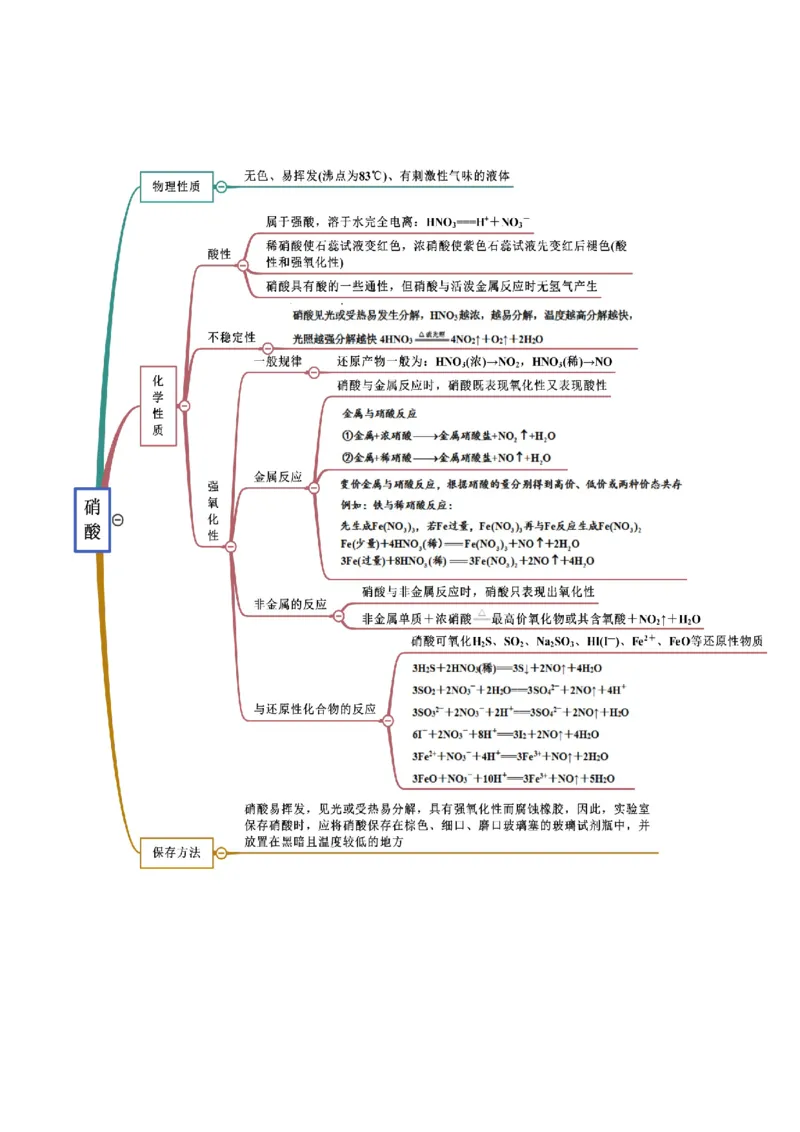
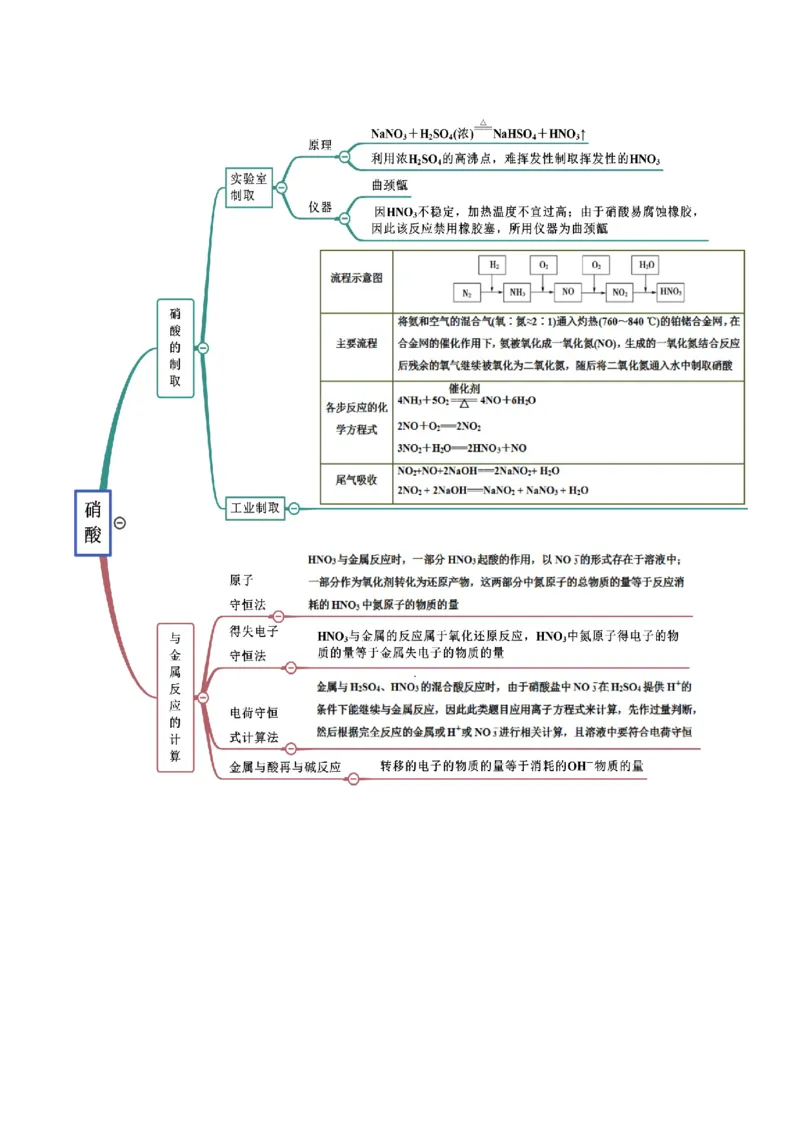
考点四 硝酸
【例4-1】(2021·辽宁·高一学业考试)下列事实与硝酸性质的对应关系错误的是
A.打开浓硝酸的试剂瓶,瓶口有白雾——挥发性
B.用棕色试剂瓶保存浓硝酸——不稳定性
C.稀硝酸使紫色石蕊试液变红——酸性
D.稀硝酸使黑色氧化铜固体溶解——强氧化性
【例4-2】(2021·辽宁·高一学业考试)下列关于硝酸的用途叙述正确的是
A.做防腐剂 B.用于环境消毒
C.制氮肥 D.工业合成氨气
【例4-3】(2021·四川绵阳·高一期末)将一定质量的Cu粉投入到400 mL 2 mol/L的稀硝酸中,待Cu粉完
全溶解时,收集到标准状况下的NO气体2.688 L(假设硝酸的还原产物只有NO且气体全部逸出),再向反应后的溶液中缓慢加入Fe粉,充分反应后溶液只含一种溶质。下列说法错误的是
A.加入铁粉后,最终溶液的溶质是Fe(NO ) B.最初的铜粉质量为11.52 g
3 2
C.铜粉反应完后,溶液中的H+浓度为0.8 mol/L D.至少需要加入铁粉8.4 g
【一隅三反】
1.(2021·辽宁·高一学业考试)铜丝与稀硝酸反应的实验现象叙述错误的是
A.铜丝逐渐变细 B.有气泡产生
C.溶液变蓝 D.产生白色沉淀
2.(2021·江苏连云港·高一期末)某兴趣小组利用如图所示装置进行铜片与硝酸反应的实验,先将铜片放
入试管的底部,通过分液漏斗加入2mL浓硝酸,将产生的气体通入倒置于水槽里充满水的集气瓶中,反应
一段时间后,用分液漏斗向试管中加5mL水,继续收集气体。下列有关说法不正确的是
A.硝酸在反应中既体现氧化性,又体现酸性
B.若铜片过量,继续用分液漏斗滴加稀硫酸,铜片表面无明显变化
C.如图中的分液漏斗可用长颈漏斗代替,但长颈漏斗的下端须插入液面以下
D.试管中前后两次实验得到的气体不同,集气瓶中前后两次收集到的气体相同
3.(2021·天津滨海新·高一期末)下列反应中硝酸既能表现出酸性又表现出氧化性的是
A.光照或受热条件下分解产生NO 和O B.与NaCO 反应放出CO,生成NaNO
2 2 2 3 2 3
C.与S单质混合共热时生成HSO 和NO D.与铜反应放出NO ,生成Cu(NO )
2 4 2 2 3 2
4.(2021·广东·广州市玉岩中学高一期中)硝酸与金属反应后所得还原产物与硝酸的浓度和金属的活泼性
有关。10 mL 0.5 mol·L-1HNO 与0.048 g Mg恰好完全反应。若氮元素只被还原到一种价态,下列说法不正
3
确的是
A.HNO 作还原剂
3
B.HNO 浓度越低,N元素还原价态越低
3
C.反应中转移电子数为0.004 mol
D.还原产物可能为NH NO
4 3
5.(2021·湖北·高一月考)取mg铜镁合金完全溶于浓硝酸中,反应过程中产生一定量的NO 气体和NO
2 2 4气体,将反应产生的气体与2.24L的O(已折算到标准状况)一起通入水中,恰好完全反应生成硝酸;在合
2
金与硝酸反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀的质量为10.2g.则m等于
A.3.4 B.6.8 C.10.0 D.10.2
考点五 酸雨及防治
【例5-1】(2021·吉林·延边二中高一期末)自然界中“酸雨”形成的原因主要是
A.未经处理的工业废水的任意排放
B.大气中二氧化碳含量增多
C.工业上大量燃烧含硫的燃料和金属矿石的冶炼
D.燃料不完全燃烧产生的气体
【例5-2】(2021·浙江·镇海中学高一期末)为减少酸雨的产生可采取的措施有
①用煤作燃料②在已酸化的土壤中加石灰③化石燃料脱硫④把工厂烟囱造高⑤开发新能源
A.①②③ B.②③④⑤ C.③⑤ D.②③⑤
【一隅三反】
1.(2020·福建·莆田二中高一期末)下列说法正确的是
A.在已酸化的土壤中加石灰可以减少酸雨的产生
B.CO 会引起温室效应,因此其含量会对空气质量指标产生影响
2
C.工业废水任意排放是造成酸雨的主要原因
D.为了减少酸雨的形成,必须减少SO 的排放量,对燃料脱硫处理
2
2.(2019·新疆·莎车县第一中学高一期中)酸雨的危害极大,下列有关酸雨的描述不正确的是
A.酸雨的pH小于4.6 B.酸雨的形成源于人们过多使用含硫燃料
C.酸雨中的酸性物质主要是硫酸 D.南疆地区不具备酸雨形成的条件
3.(2021·辽宁·大连市第一中学高一期中)酸雨有很大危害,能直接破坏农作物。下列物质中可以形成酸
雨的是
A.N B.SO C.O D.CO
2 2 2 2
4.(2021·黑龙江·哈师大附中高一期末)下列叙述不正确的是
A.pH小于7的雨水就是酸雨
B.酸雨能损伤农作物,破坏森林和草原
C.酸雨能使土壤、湖泊酸化
D.二氧化硫和氮氧化物都是形成酸雨的主要物质倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育