文档内容
1.1 反应热(精练)
题组一 反应热与焓
1.下列过程中,一定存在ΔH<0的是
A.化合反应 B.分解反应 C.分子拆成原子 D.原子组成分子
2(2022·广西桂林·高二期末)下列各组涉及的变化属于吸热反应的是
A. 溶于水 B. 晶体与 混合研磨
C.Na投入到水中 D.Zn和稀硫酸反应
3.(2022·上海中学东校高二期末)下列反应属于放热反应的是
A.煅烧石灰石 B.电解水 C.甲烷燃烧 D.小苏打受热分解
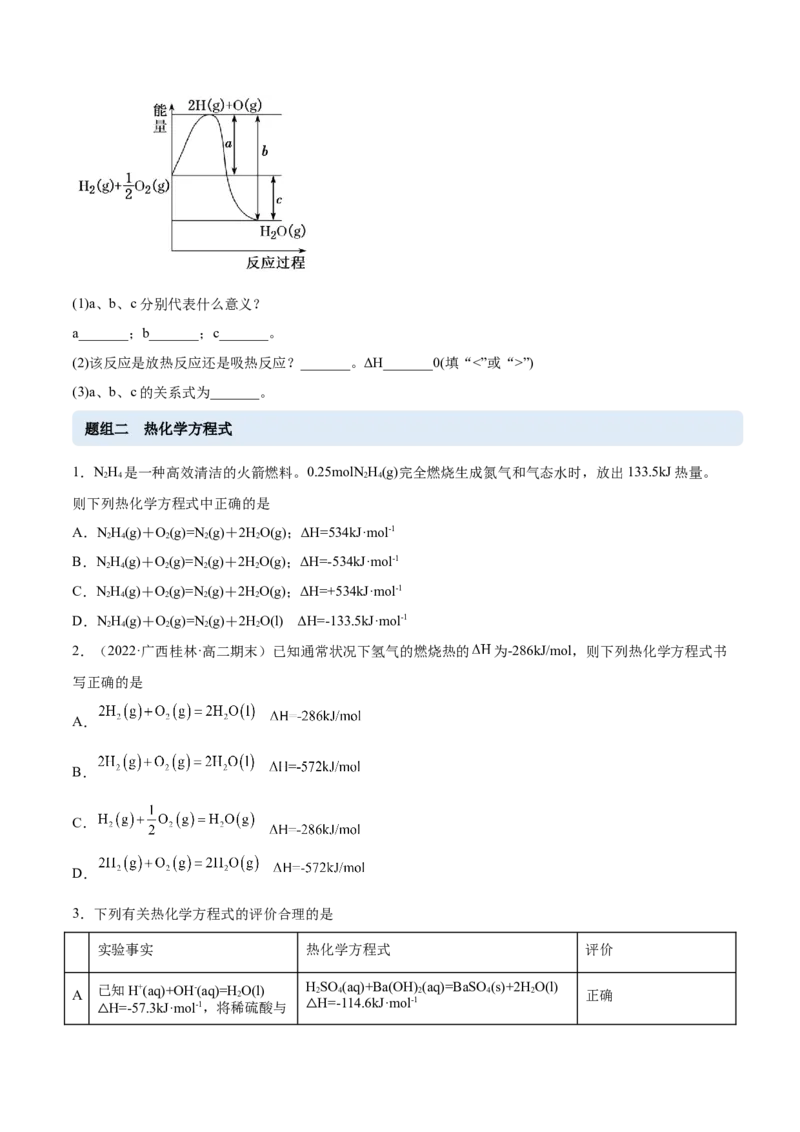
4.(2022·四川成都·高二期末)下列反应属于非氧化还原反应,且能量变化与图示能量相符合的是
A. 与稀 反应 B.氢气与氮气的化合反应
C.灼热的炭与 反应 D. 晶体与 晶体反应
5.下列反应既属于氧化还原反应,又属于吸热反应的是
A.灼热的碳与CO 的反应 B.锌与稀硫酸反应
2
C.Ba(OH) •8H O与NH Cl的反应 D.铝热反应
2 2 4
6.(2021·云南文山·高二期末)中国研究人员研制一种新型复合光催化剂,利用太阳光在催化剂表面实现
高效分解水,主要过程如图所示。下列说法不正确的是A.整个过程实现了光能向化学能的转化 B.过程Ⅱ放出能量并生成了O-O键
C.总反应为 D.过程Ⅲ中有一种反应物含有离子键
7.下列物质间的能量变化与如图所示图像相符的是
A.稀释浓硫酸 B.过氧化氢的分解反应
C.氮气和氧气生成一氧化氮的反应 D.铁和稀盐酸的反应
8.(2021·福建省福州华侨中学高二期中)下列反应属于放热反应的是
A. B.浓硫酸溶于水
C.铝热反应 D.石灰石分解制备氧化钙
9.如下图所示,在101 kPa时,ΔH=-393.5 kJ·mol-1,ΔH=-395.4 kJ·mol-1。下列说法中正确的是
1 2
A.断裂金刚石和石墨中的化学键要放出能量
B.石墨转化成金刚石需要吸收能量,是物理变化
C.石墨比金刚石稳定
D.1 mol金刚石与1 mol O 的总能量低于1 mol CO 的总能量
2 2
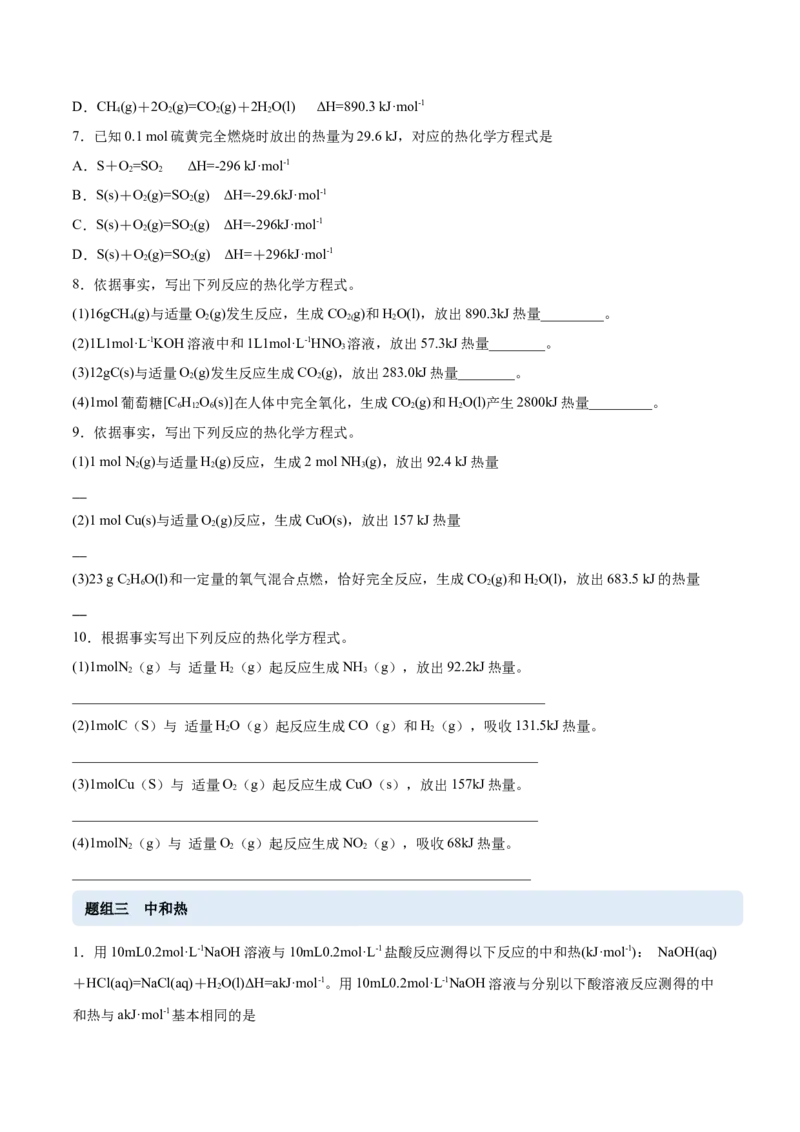
10.已知:H(g)+ O(g)=HO(g),反应过程中能量变化如图,问:
2 2 2(1)a、b、c分别代表什么意义?
a_______;b_______;c_______。
(2)该反应是放热反应还是吸热反应?_______。ΔH_______0(填“<”或“>”)
(3)a、b、c的关系式为_______。
题组二 热化学方程式
1.NH 是一种高效清洁的火箭燃料。0.25molNH(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量。
2 4 2 4
则下列热化学方程式中正确的是
A.NH(g)+O(g)=N(g)+2HO(g);ΔH=534kJ·mol-1
2 4 2 2 2
B.NH(g)+O(g)=N(g)+2HO(g);ΔH=-534kJ·mol-1
2 4 2 2 2
C.NH(g)+O(g)=N(g)+2HO(g);ΔH=+534kJ·mol-1
2 4 2 2 2
D.NH(g)+O(g)=N(g)+2HO(l) ΔH=-133.5kJ·mol-1
2 4 2 2 2
2.(2022·广西桂林·高二期末)已知通常状况下氢气的燃烧热的 为-286kJ/mol,则下列热化学方程式书
写正确的是
A.
B.
C.
D.
3.下列有关热化学方程式的评价合理的是
实验事实 热化学方程式 评价
A 已知H+(aq)+OH-(aq)=H 2 O(l) H 2 SO 4 (aq)+Ba(OH) 2 (aq)=BaSO 4 (s)+2H 2 O(l) 正确
H=-57.3kJ·mol-1,将稀硫酸与
H=-114.6kJ·mol-1
△
△稀氢氧化钡溶液混合
醋酸溶液与稀氢氧化钠溶液混 CHCOOH(l)+NaOH(aq)=CH COONa(aq)
B 3 3 正确
合 +H O(l) H=-57.3kJ·mol-1
2
160gSO 气体与适量水恰好完 △
3 SO (g)+HO(l)=HSO (aq) 不正确;因为反应热为
C 全反应生成HSO ,放出热量 3 2 2 4
2 4 H=-130.3kJ·mol-1 H=-260.6kJ·mol-1
260.6kJ
△ △
已知25℃、101kPa下,120g石 不正确;同素异形体要
D C(s)+O(g)=CO (g) H=-393.51kJ·mol-1
墨完全燃烧放出热量3935.1kJ 2 2 注名称:C(石墨)
△
4.向50mL 溶液中加入足量稀硫酸充分反应后,放出2.56kJ的热量。向50mL
稀盐酸溶液中加入足量 充分反应后,放出1.1kJ的热量,则硫酸钠溶液与氯化钡溶液反
应的热化学方程式为
A.
B.
C.
D.
5.下列热化学方程式书写正确的是
A.2SO +O 2SO ;△H=-196.6kJ•mol-1
2 2 3
B.2H(g)+O(g)=2HO(l);△H=+571.6kJ•mol-1
2 2 2
C.H(g)+ O(g)=HO(l);△H=-285.8kJ•mol-1
2 2 2
D.C(s)+O(g) CO(g);△H=-393.5kJ
2 2
6.实验测得:101 kPa时,1 mol H 完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH 完全燃烧生成
2 4
液态水和CO,放出890.3 kJ的热量。下列热化学方程式书写正确的是
2
A.2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
B.CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890.3 kJ
4 2 2 2
C.CH(g)+2O(g)=CO (g)+2HO(g) ΔH=-890.3 kJ·mol-1
4 2 2 2D.CH(g)+2O(g)=CO (g)+2HO(l) ΔH=890.3 kJ·mol-1
4 2 2 2
7.已知0.1 mol硫黄完全燃烧时放出的热量为29.6 kJ,对应的热化学方程式是
A.S+O=SO ΔH=-296 kJ·mol-1
2 2
B.S(s)+O(g)=SO(g) ΔH=-29.6kJ·mol-1
2 2
C.S(s)+O(g)=SO(g) ΔH=-296kJ·mol-1
2 2
D.S(s)+O(g)=SO(g) ΔH=+296kJ·mol-1
2 2
8.依据事实,写出下列反应的热化学方程式。
(1)16gCH (g)与适量O(g)发生反应,生成CO g)和HO(l),放出890.3kJ热量_________。
4 2 2( 2
(2)1L1mol·L-1KOH溶液中和1L1mol·L-1HNO 溶液,放出57.3kJ热量________。
3
(3)12gC(s)与适量O(g)发生反应生成CO(g),放出283.0kJ热量________。
2 2
(4)1mol葡萄糖[C H O(s)]在人体中完全氧化,生成CO(g)和HO(l)产生2800kJ热量_________。
6 12 6 2 2
9.依据事实,写出下列反应的热化学方程式。
(1)1 mol N (g)与适量H(g)反应,生成2 mol NH (g),放出92.4 kJ热量
2 2 3
(2)1 mol Cu(s)与适量O(g)反应,生成CuO(s),放出157 kJ热量
2
(3)23 g C HO(l)和一定量的氧气混合点燃,恰好完全反应,生成CO(g)和HO(l),放出683.5 kJ的热量
2 6 2 2
10.根据事实写出下列反应的热化学方程式。
(1)1molN (g)与 适量H(g)起反应生成NH (g),放出92.2kJ热量。
2 2 3
___________________________________________________________________
(2)1molC(S)与 适量HO(g)起反应生成CO(g)和H(g),吸收131.5kJ热量。
2 2
__________________________________________________________________
(3)1molCu(S)与 适量O(g)起反应生成CuO(s),放出157kJ热量。
2
__________________________________________________________________
(4)1molN (g)与 适量O(g)起反应生成NO (g),吸收68kJ热量。
2 2 2
_________________________________________________________________
题组三 中和热
1.用10mL0.2mol·L-1NaOH溶液与10mL0.2mol·L-1盐酸反应测得以下反应的中和热(kJ·mol-1): NaOH(aq)
+HCl(aq)=NaCl(aq)+HO(l)ΔH=akJ·mol-1。用10mL0.2mol·L-1NaOH溶液与分别以下酸溶液反应测得的中
2
和热与akJ·mol-1基本相同的是A.20mL0.5mol·L-1硝酸溶液 B.10mL0.2mol·L-1醋酸溶液
C.10mL0.2mol·L-1氢氟酸 D.2mL18.4mol·L-1浓硫酸
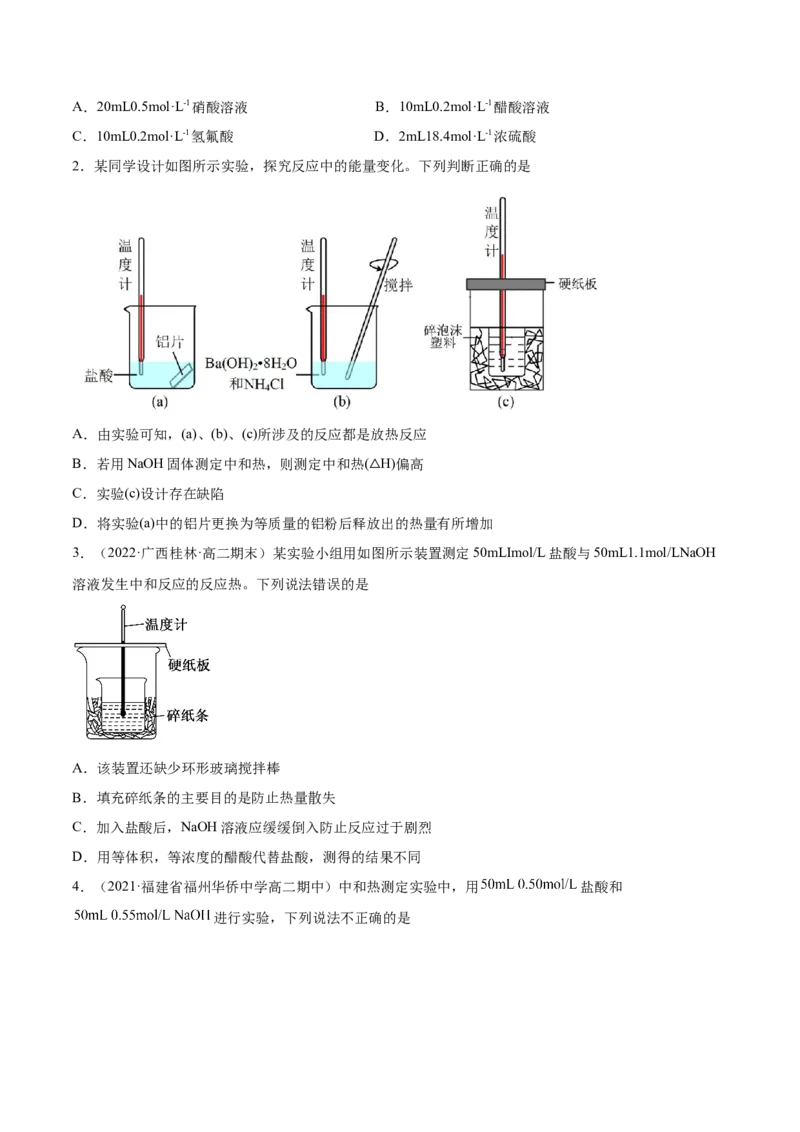
2.某同学设计如图所示实验,探究反应中的能量变化。下列判断正确的是
A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B.若用NaOH固体测定中和热,则测定中和热( H)偏高
C.实验(c)设计存在缺陷 △
D.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
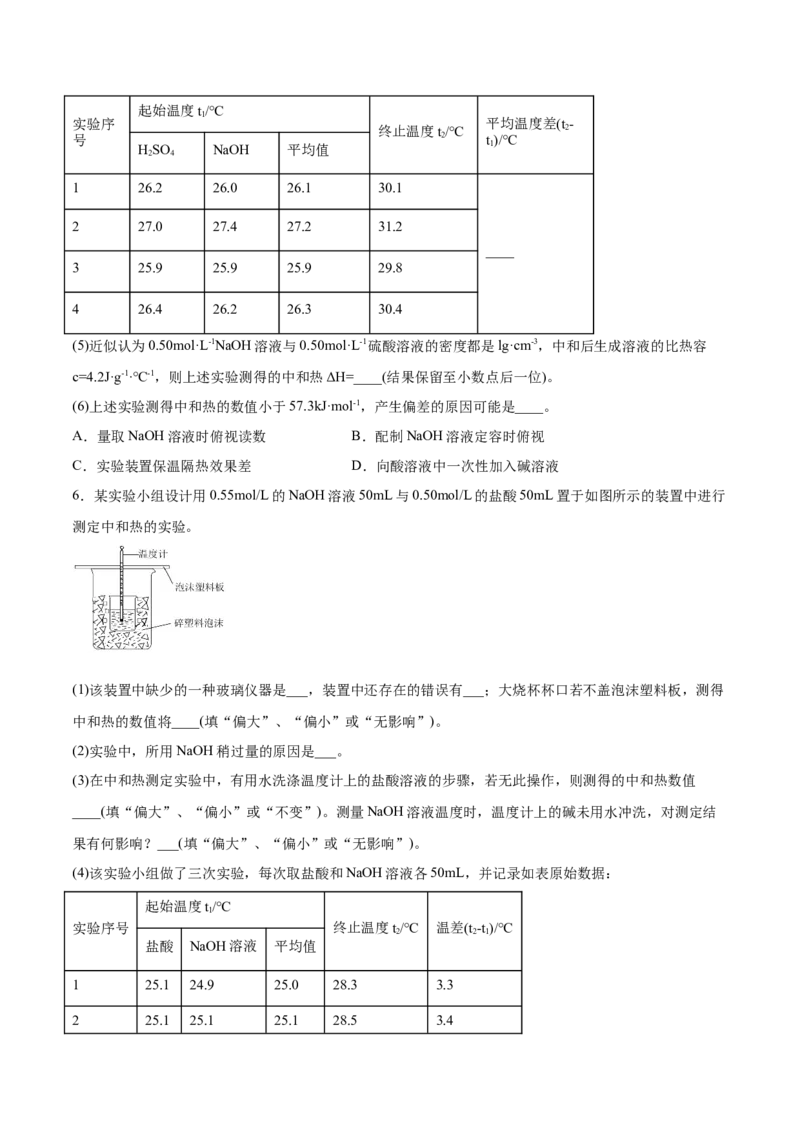
3.(2022·广西桂林·高二期末)某实验小组用如图所示装置测定50mLImol/L盐酸与50mL1.1mol/LNaOH
溶液发生中和反应的反应热。下列说法错误的是
A.该装置还缺少环形玻璃搅拌棒
B.填充碎纸条的主要目的是防止热量散失
C.加入盐酸后,NaOH溶液应缓缓倒入防止反应过于剧烈
D.用等体积,等浓度的醋酸代替盐酸,测得的结果不同
4.(2021·福建省福州华侨中学高二期中)中和热测定实验中,用 盐酸和
进行实验,下列说法不正确的是A.改用 盐酸跟 溶液进行反应,求出的中和热数值和原来相同,放
热不同
B.所加 溶液过量,目的是保证盐酸完全被中和
C.酸碱混合时,量筒中 溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌
D.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热、减少热量损失
5.在测定中和热的实验中,下列说法正确的是
A.用0.55mol·L1NaOH溶液分别与0.5mol·L1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得
的中和热数值相同
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计
D.使用环形玻璃搅拌棒是为了使反应物混合均匀,加快反应速率,减小实验误差
6.(2022·浙江丽水·高二开学考试)某实验小组用100mL0.50mol·L-1NaOH溶液与60mL0.50mo·L-1硫酸溶
液进行中和热的测定,装置如图所示。回答下列问题:
(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体____g。
(2)图中玻璃搅拌棒“环形”的目的是____。
(3)测量终止温度的方法是____。
(4)请填写表中的平均温度差:起始温度t/℃
1
实验序 平均温度差(t -
终止温度t/℃ 2
号 2 t)/℃
HSO NaOH 平均值 1
2 4
1 26.2 26.0 26.1 30.1
2 27.0 27.4 27.2 31.2
____
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
(5)近似认为0.50mol·L-1NaOH溶液与0.50mol·L-1硫酸溶液的密度都是lg·cm-3,中和后生成溶液的比热容
c=4.2J·g-1·℃-1,则上述实验测得的中和热ΔH=____(结果保留至小数点后一位)。
(6)上述实验测得中和热的数值小于57.3kJ·mol-1,产生偏差的原因可能是____。
A.量取NaOH溶液时俯视读数 B.配制NaOH溶液定容时俯视
C.实验装置保温隔热效果差 D.向酸溶液中一次性加入碱溶液
6.某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行
测定中和热的实验。
(1)该装置中缺少的一种玻璃仪器是___,装置中还存在的错误有___;大烧杯杯口若不盖泡沫塑料板,测得
中和热的数值将____(填“偏大”、“偏小”或“无影响”)。
(2)实验中,所用NaOH稍过量的原因是___。
(3)在中和热测定实验中,有用水洗涤温度计上的盐酸溶液的步骤,若无此操作,则测得的中和热数值
____(填“偏大”、“偏小”或“不变”)。测量NaOH溶液温度时,温度计上的碱未用水冲洗,对测定结
果有何影响?___(填“偏大”、“偏小”或“无影响”)。
(4)该实验小组做了三次实验,每次取盐酸和NaOH溶液各50mL,并记录如表原始数据:
起始温度t/℃
1
实验序号 终止温度t/℃ 温差(t -t )/℃
2 2 1
盐酸 NaOH溶液 平均值
1 25.1 24.9 25.0 28.3 3.3
2 25.1 25.1 25.1 28.5 3.43 25.1 25.1 25.1 28.6 3.5
已知盐酸、NaOH溶液密度均近似为1.00g/cm3,中和后混合液的比热容c=4.18×10-3kJ/(g·℃),则该反应的
中和热ΔH=___。(保留到小数点后1位)
7.(2021·福建·漳州市正兴学校高二期中)反应热的测定具有重要的意义。利用如图所示装置测定中和热
的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)所用NaOH溶液要稍过量的原因是___________。
(2)倒入NaOH溶液的正确操作是___________ (填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入
C.一次迅速倒入 D.加水稀释后再倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是___________ (填序号)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,
其反应热分别为ΔH、ΔH、ΔH,则ΔH、ΔH、ΔH 的大小关系为___________。
1 2 3 1 2 3
(5)测定中和热时,不可用Ba(OH) 溶液和硫酸代替NaOH溶液和盐酸,理由是___________。
2
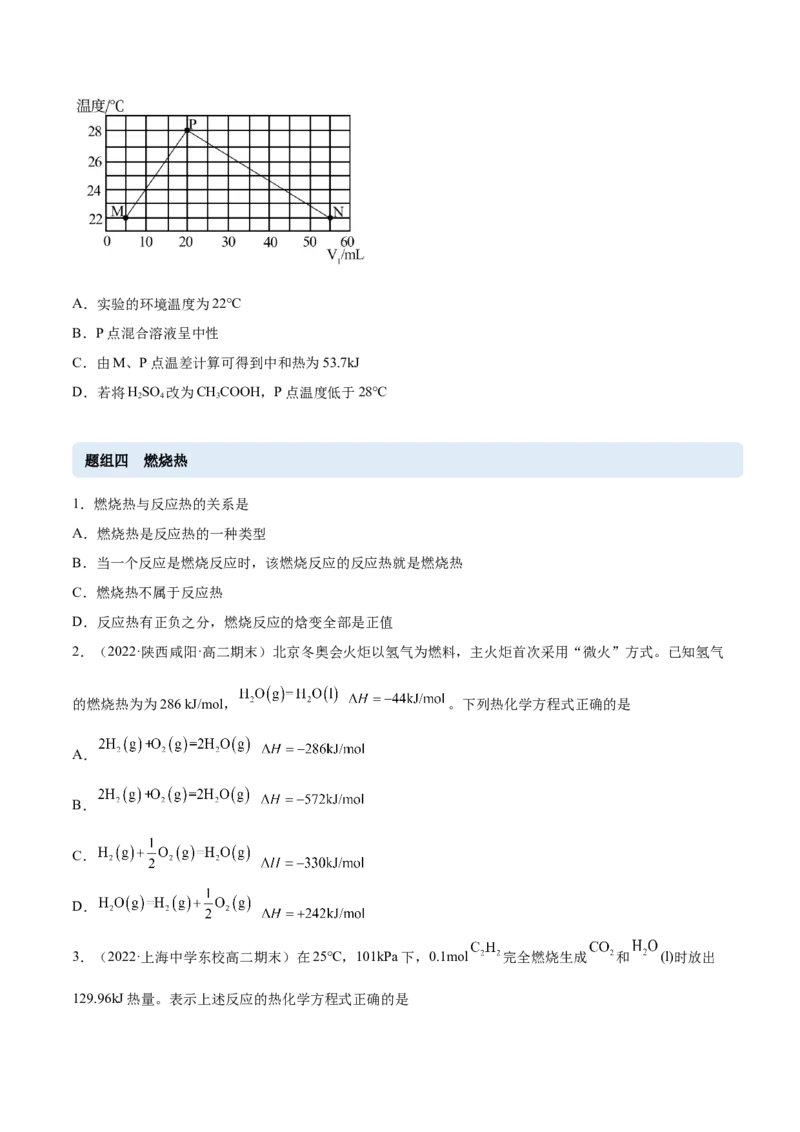
(6)现将浓度相等、体积分别为V、V 的HSO 、NaOH溶液混合,测量混合液温度,结果如图(已知:
1 2 2 4
V+V =60mL)。下列叙述正确的是___________。
1 2A.实验的环境温度为22℃
B.P点混合溶液呈中性
C.由M、P点温差计算可得到中和热为53.7kJ
D.若将HSO 改为CHCOOH,P点温度低于28℃
2 4 3
题组四 燃烧热
1.燃烧热与反应热的关系是
A.燃烧热是反应热的一种类型
B.当一个反应是燃烧反应时,该燃烧反应的反应热就是燃烧热
C.燃烧热不属于反应热
D.反应热有正负之分,燃烧反应的焓变全部是正值
2.(2022·陕西咸阳·高二期末)北京冬奥会火炬以氢气为燃料,主火炬首次采用“微火”方式。已知氢气
的燃烧热为为286 kJ/mol, 。下列热化学方程式正确的是
A.
B.
C.
D.
3.(2022·上海中学东校高二期末)在25℃,101kPa下,0.1mol 完全燃烧生成 和 (l)时放出
129.96kJ热量。表示上述反应的热化学方程式正确的是A.
B.
C.
D.
4.(2022·湖南·长沙市南雅中学高二阶段练习)俄乌冲突爆发以来,许多西方国家宣布制裁俄罗斯,制裁
范围涵盖俄罗斯的猫、树以及该国的文艺作品等,但俄罗斯的石油和天然气目前并不在制裁之列。天然气
的主要成分是甲烷,下列能正确表示甲烷燃烧热的热化学方程式是
A.
B.
C.
D.
5.按照下列要求书写热化学方程式
(1)1 mol C(石墨,s)与适量HO(g)反应生成CO(g)和H(g),吸收131.3 kJ热量:
2 2
_________________________________________。
(2)实验测得25℃、101kPa时1mol H 完全燃烧放出285.8 kJ的热量,写出H 燃烧热的热化学方程式:
2 2
________________________________。
(3)卫星发射时可用肼(N H)作燃料,1molN H(l)在O 中燃烧,生成N(g)和HO(l),放出5518KJ热量,写出
2 4 2 4 2 2 2
NH 燃烧的热化学方程式_________________________________________________。
2 4
题组五 反应热的综合运用
1.(1)已知乙醇的燃烧热为-1366.8kJ/mol,写出相应的热化学方程式_ _。
(2)已知强酸强碱的中和热为-57.3kJ/mol,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式:
_ _ 。
(3)已知16g硫固体完全燃烧时放出148.4kJ的热量,则硫的燃烧热的热化学方程式:_
_。
(4)已知:101kPa时,2C(s)+O(g)=2CO(g)ΔH=-221kJ/mol,则碳的燃烧热数值___110.5kJ/mol(填>,<,
2=)。
(5)已知:稀溶液中,H+(aq)+OH-(aq)=H O(l)ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1mol
2
水,放出的热量___57.3kJ(填>,<,=)。
(6)已知一定条件下合成氨反应:N(g)+3H(g) 2NH (g)ΔH=-92.0kJ·mol-1,相同条件下将1molN
2 2 3 2
和3molH 放在一密闭容器中充分反应,测得反应放出的热量___(假定热量无损失)92.0kJ(填>,<,=)。
2
(7)相同条件下2mol氢原子所具有的能量___1mol氢分子所具有的能量(填>,<,=)
2.按要求填空
(1) 是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态 。已知室温下
自燃放出热量 。写出室温下 自燃的热化学方程式___ ___。
(2)在 时, 在 中完全燃烧生成 液态水,放出 的热量, 的燃烧热为_____,
表示 燃烧热的热化学方程式为__ ___。
(3)在 、 下,一定质量的无水乙醇完全燃烧时放出热量 ,燃烧生成的 用过量饱和石灰
水吸收可得 沉淀,则在此条件下, 乙醇完全燃烧的 ____ 。
(4) 与 反应生成 和一种黑色固体。在 、 下,已知该反应每转移 ,放
热 ,该反应的热化学方程式___ __。
3.依据事实写出下列反应的热化学方程式。
(1)含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应的中和热的热化学方程
式为__ _。
(2)CH OH是优质液体燃料。在25℃、101kPa下,每充分燃烧1g CH OH并恢复到原状态,会释放22.68kJ
3 3
的热量。请写出表示CHOH燃烧热的热化学反应方程式:__ _。
3
(3)如图是1molNO 和1molCO反应生成CO 和NO过程中能量变化示意图,请写出NO 和CO反应的热化
2 2 2
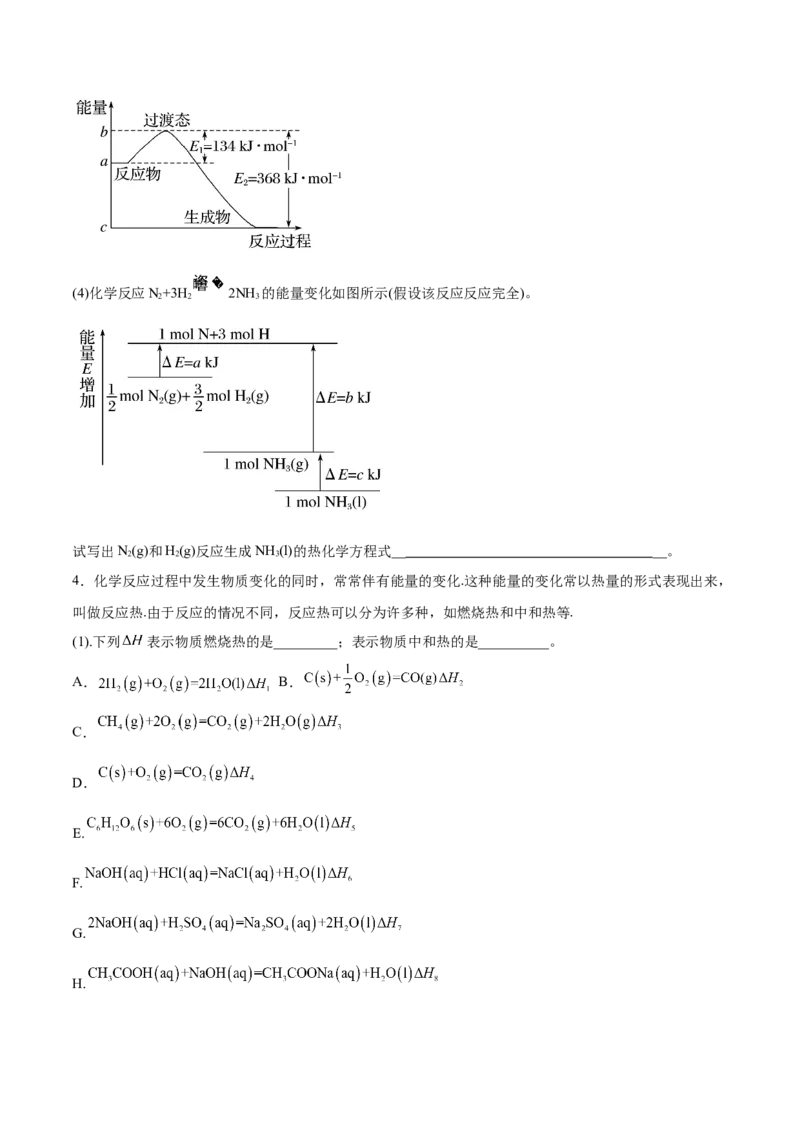
学方程式:__ _。(4)化学反应N+3H 2NH 的能量变化如图所示(假设该反应反应完全)。
2 2 3
试写出N(g)和H(g)反应生成NH (l)的热化学方程式__ __。
2 2 3
4.化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热量的形式表现出来,
叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
(1).下列 表示物质燃烧热的是_________;表示物质中和热的是__________。
A. B.
C.
D.
E.
F.
G.
H.(2)2.00g 气体完全燃烧生成液态水和 气体,放出99.6kJ的热量,写出该反应的热化学方程式
_______________________________________________。
(3)充分燃烧一定量的丁烷放出的热量大小为 ,生成的 恰好与100mL浓度为5 的KOH溶液完
全反应,则燃烧1mol丁烷放出的热量为________________。
5.奥运会火炬常用的燃料为丙烷、丁烷等。
已知:丙烷的燃烧热 H=-2220 kJ/mol;正丁烷的燃烧热 H= -2878 kJ/mol,异丁烷的燃烧热 H=-2869.6
1 2 3
kJ/mol。 △ △ △
(1)写出丙烷燃烧的热化学方程式__ ___。
(2)下列有关说法不正确的是_____(填序号)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
(3)已知A气体的燃烧热为300 kJ/mol,B气体的燃烧热为500 kJ/mol。现有6 mol由A和B组成的混合气体,
完全燃烧放出的热量是2000 kJ,则该混合气体中气体A和气体B的物质的量之比是______。
(4)1 molH 完全燃烧生成液态水放出286 kJ热量。已知单位质量的燃料完全燃烧时所放出的热量称为该燃
2
料的热值,则氢气的热值是______kJ/g。
6.Ⅰ.用如图所示的装置测定中和反应反应热。
实验药品:100mL 0.50 盐酸、 溶液、 氨水。
实验步骤:略。
已知弱碱电离时吸热。
回答下列问题。
(1)从实验装置上看,还缺少___________,其能否用铜质材料替代?___________(填“能”或“不能”),
理由是___________。(2)装置中隔热层的作用是___________。
(3)将浓度为 的酸溶液和 的碱溶液各50mL混合(溶液密度均为 ),生成的溶
液的比热容 ,测得温度如下:
反应物 起始温度 最高温度
甲组(HCl+NaOH) 15.0 18.3
乙组 15.0 18.1
①两组实验结果存在差异的原因是___________。
② 的 =___________(保留一位小数)。
③某同学利用上述装置重新做甲组实验,测得反应热 偏大,则可能的原因是___________(填序号)。
A.测完盐酸的温度直接测NaOH溶液温度
B.做该实验时室温较高
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
II.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(4)如图是 和 反应生成 过程中能量的变化示意图,请写出1mol 和 反
应的热化学方程式:___________。
(5)用 催化还原NO,还可以消除氮氧化物的污染。已知:
①
②若1mol 还原NO至 ,则该反应过程中的反应热 =___________ (用含a、b的式子表示)。
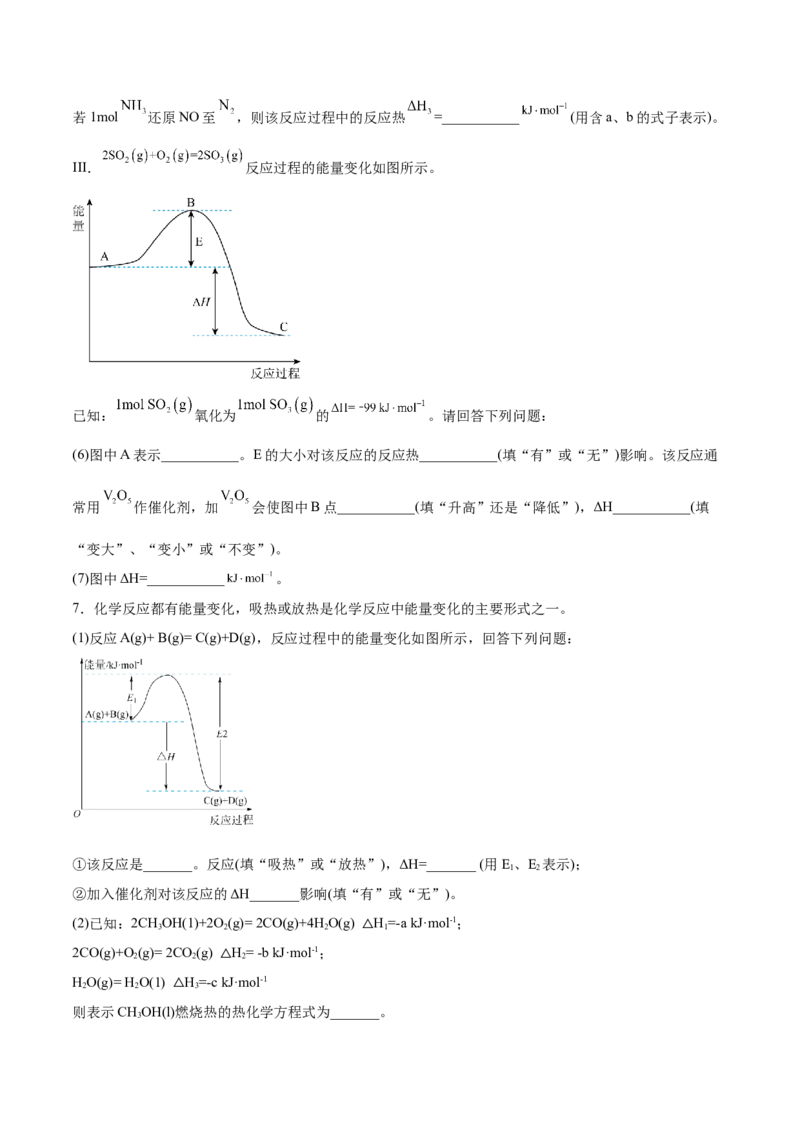
III. 反应过程的能量变化如图所示。
已知: 氧化为 的 。请回答下列问题:
(6)图中A表示___________。E的大小对该反应的反应热___________(填“有”或“无”)影响。该反应通
常用 作催化剂,加 会使图中B点___________(填“升高”还是“降低”),ΔH___________(填
“变大”、“变小”或“不变”)。
(7)图中ΔH=___________ 。
7.化学反应都有能量变化,吸热或放热是化学反应中能量变化的主要形式之一。
(1)反应A(g)+ B(g)= C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题:
①该反应是_______。反应(填“吸热”或“放热”),ΔH=_______ (用E、E 表示);
1 2
②加入催化剂对该反应的ΔH_______影响(填“有”或“无”)。
(2)已知:2CHOH(1)+2O (g)= 2CO(g)+4H O(g) H=-a kJ·mol-1;
3 2 2 1
2CO(g)+O 2 (g)= 2CO 2 (g) H 2 = -b kJ·mol-1; △
H
2
O(g)= H
2
O(1) H
3
=-c △kJ·mol-1
则表示CH
3
OH(l)△燃烧热的热化学方程式为_______。(3)断裂1mol化学键所需的能量如表所示:
共价键 H- N H- O N≡N O =O
断裂1mol化学键所需能量/kJ 393 463 941 496
则N(g)与HO(g)反应生成NH (g)和O(g)的热化学方程式为_______。
2 2 3 2
(4)下列反应中,属于放热反应的是_______,属于吸热反应的是_______。
①物质燃烧②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的炭⑤食物因氧化而腐败⑥焦炭和水蒸气的反
应⑦铁粉与稀盐酸反应倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育