文档内容
第五章 化学生产中的重要非金属元素
第二节 氮及其化合物 课时作业
第一课时 氮气与氮的固定 一氧化氮和二氧化氮
基础达标
1.通常状况下,氮气的性质不活泼的原因是( )
A.氮分子中有三个共价键,键能很大 B.氮元素非金属性很弱
C.氮分子中氮元素化合价为零 D.固态氮属于分子晶体
2.下列关于氮的循环,叙述错误的是( )
A.氮气转化为氮的化合物的过程叫做氮的固定
B.氮的固定可以通过自然固氮和人工固氮的方式实现
C.人类的生产活动参与了氮的循环过程
D.氮的循环过程中只有氮元素被氧化的过程
3.N 是空气的重要组成部分,因此有科学家根据蒸汽机的原理,设计制造出液氮蒸
2
汽机,即利用液态氮的蒸发来驱动机车,从而达到环境保护的目的。其主要依据是
( )
A.液态氮的沸点为-195.8 ℃,远低于常温 B.N 在空气中燃烧放热
2
C.N 与H 反应放热 D.N 在空气中约占78%(体积分数)
2 2 2
4.氮是植物生长必需的元素,在大气中主要以分子形式存在在放电条件下,与O 可
2
发生反应: 。20世纪初,德国化学家哈伯等首次合成了氨气,化学方程式
为: ,生成的NH 与HCl反应合成氮肥。固氮可分为人工固氮
3
和自然固氮。下列可实现自然固氮的是( )
A.N→NO B.N→NH C.NH →NO D.NO→NO
2 2 3 3 2
5.下列关于氮的氧化物的说法中,正确的是( )
A.氮的氧化物都是酸性氧化物
B.氮的氧化物都既有氧化性,又有还原性
C.NO 与 HO 反应生成 HNO,所以 NO 是酸性氧化物
2 2 3 2D.NO 和 NO 均有毒
2
6.下列关于氮及其化合物的说法正确的是( )
A.N 的化学性质稳定,但在一定条件下,可与O、H 等发生反应
2 2 2
B.NO、NO 均为大气污染气体,在大气中可稳定存在
2
C.NO、NO 均易溶于水
2
D.NO、NO 均能与水发生反应
2
7.德国滤清专家曼胡默尔推出一项新技术,用于降低污染严重地区的二氧化氮(NO )
2
浓度。下列关于氮的氧化物的说法中正确的是( )
A.氮的氧化物都是酸性氧化物,都是大气污染物
B.氮的氧化物都既有氧化性,又有还原性
C.NO 与HO反应生成HNO,所以NO 是酸性氧化物
2 2 3 2
D.可以用排空气法收集NO
2
8.在汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。下列
说法不正确的是( )
A.该转化过程中有3种元素的化合价发生变化
B.NO和O 必须在催化剂表面才能反应
2
C.该装置将有毒的NO和CO转化为无毒的CO 和N
2 2
D.该催化转化的总反应的化学方程式为2NO+O+4CO=====4CO+N
2 2 2
9.众所周知,一氧化氮是一种大气污染物,是吸烟、汽车尾气及垃圾燃烧等释放出的
有害气体,但是这种最常见、最简单的气体小分子在生物体内却是一种重要的信使分子,
具有保护心血管、降低血压以及提升记忆力的作用。下列关于NO的说法正确的是 ( )
A.NO是无色气体,易溶于水,是酸性氧化物
B.NO在人体内可作“信使分子”,能扩张血管,提高免疫力等,因此大气中的 NO
对人体无害
C.NO在空气中可以转为NO ,二者都是大气污染物
2
D.NO在化学反应中,只能作还原剂,不能作氧化剂
10.在一定条件下,将m体积NO和n体积O 同时通入倒立于水中且盛满水的容器
2
内,充分反应后,容器内残留体积的气体,该气体与空气接触后变为红棕色,则 m与n的
比值为( )
A.3∶2 B.2∶3 C.8∶3 D.3∶8
能力提升
11.诺贝尔化学奖曾授予德国化学家Gerhard Ertl,以表彰他对固体表面化学研究过程
中的重大发现。使CO、NO 等在铂表面发生化学反应转变成无毒气体,以减少汽车尾气中
x有毒气体的排放,正是此项研究的重要应用之一。下列有关说法不正确的是 ( )
A.CO在铂表面被氧化生成CO,铂起催化作用
2
B.汽车尾气中的NO 在铂表面发生反应的产物是N
x 2
C.CO在铂表面可能和O、NO 反应
2 x
D.NO、CO、CO 均能与人体中的血红蛋白结合
x 2
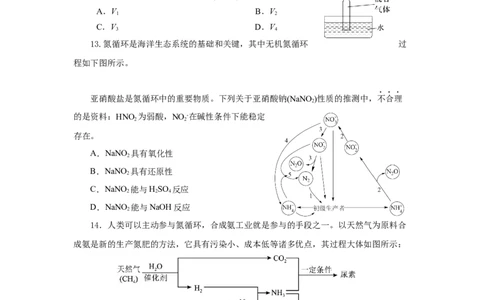
12.在同温同压下,将等体积混合而成的四组气体:
①NO +O 、②NO +NO、③HCl+N 、④SO +O ,分别通入体积相同的试管,并
2 2 2 2 2 2
立即倒立于水槽中,如图所示。待试管内液面稳定后,剩余气体的体积依次为 V 、V 、
1 2
V、V,则剩余气体的体积最小的是 ( )
3 4
A.V B.V
1 2
C.V D.V
3 4
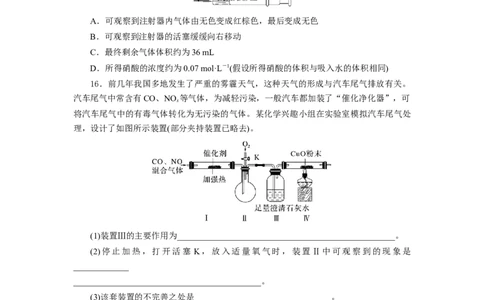
13.氮循环是海洋生态系统的基础和关键,其中无机氮循环 过
程如下图所示。
亚硝酸盐是氮循环中的重要物质。下列关于亚硝酸钠(NaNO )性质的推测中,不合理
2
的是资料:HNO 为弱酸,NO -在碱性条件下能稳定
2 2
存在。
A.NaNO 具有氧化性
2
B.NaNO 具有还原性
2
C.NaNO 能与HSO 反应
2 2 4
D.NaNO 能与NaOH反应
2
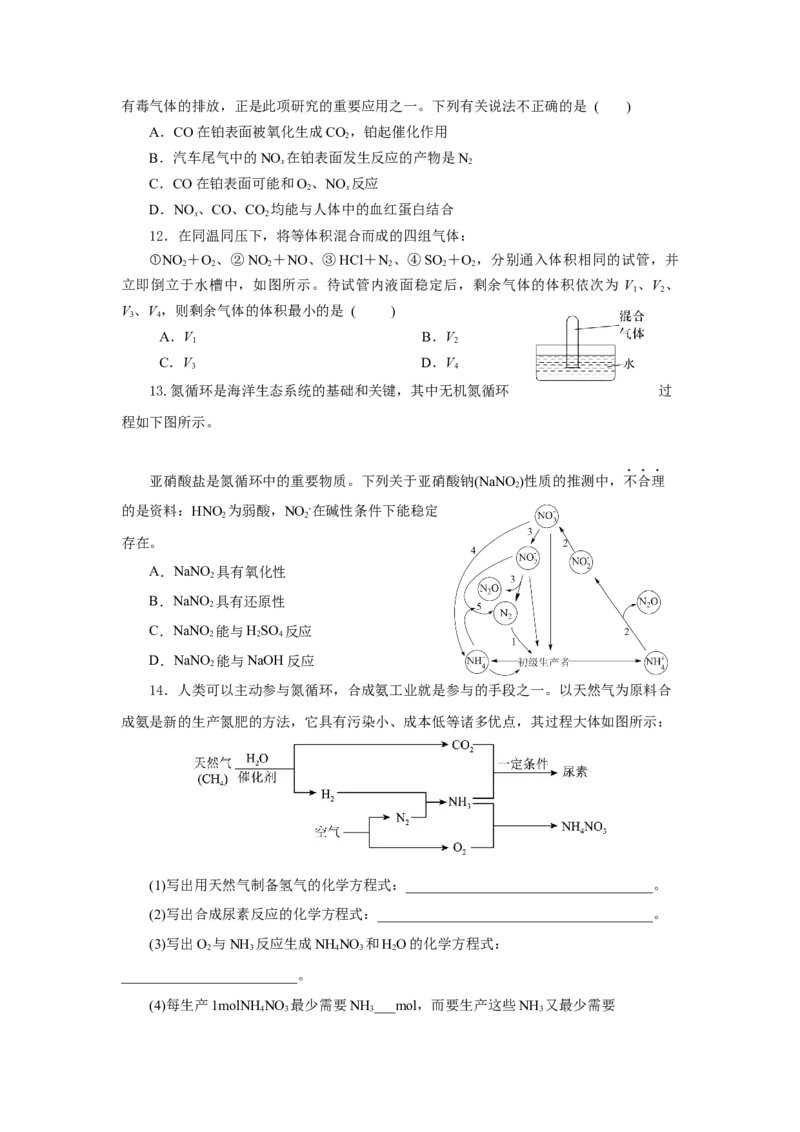
14.人类可以主动参与氮循环,合成氨工业就是参与的手段之一。以天然气为原料合
成氨是新的生产氮肥的方法,它具有污染小、成本低等诸多优点,其过程大体如图所示:
(1)写出用天然气制备氢气的化学方程式:___________________________________。
(2)写出合成尿素反应的化学方程式:_______________________________________。
(3)写出O 与NH 反应生成NH NO 和HO的化学方程式:
2 3 4 3 2
_________________________。
(4)每生产1molNH NO 最少需要NH ___mol,而要生产这些NH 又最少需要
4 3 3 3CH___mol。
4
直击高考
15.如图所示,在注射器里吸入20 mL NO(标准状况下),然后吸入5 mL水。若再吸
入30 mL空气(标准状况,按O 占空气总体积计算),夹住弹簧夹,让内外大气压相同,观
2
察现象。下列叙述不正确的是( )
A.可观察到注射器内气体由无色变成红棕色,最后变成无色
B.可观察到注射器的活塞缓缓向右移动
C.最终剩余气体体积约为36 mL
D.所得硝酸的浓度约为0.07 mol·L-1(假设所得硝酸的体积与吸入水的体积相同)
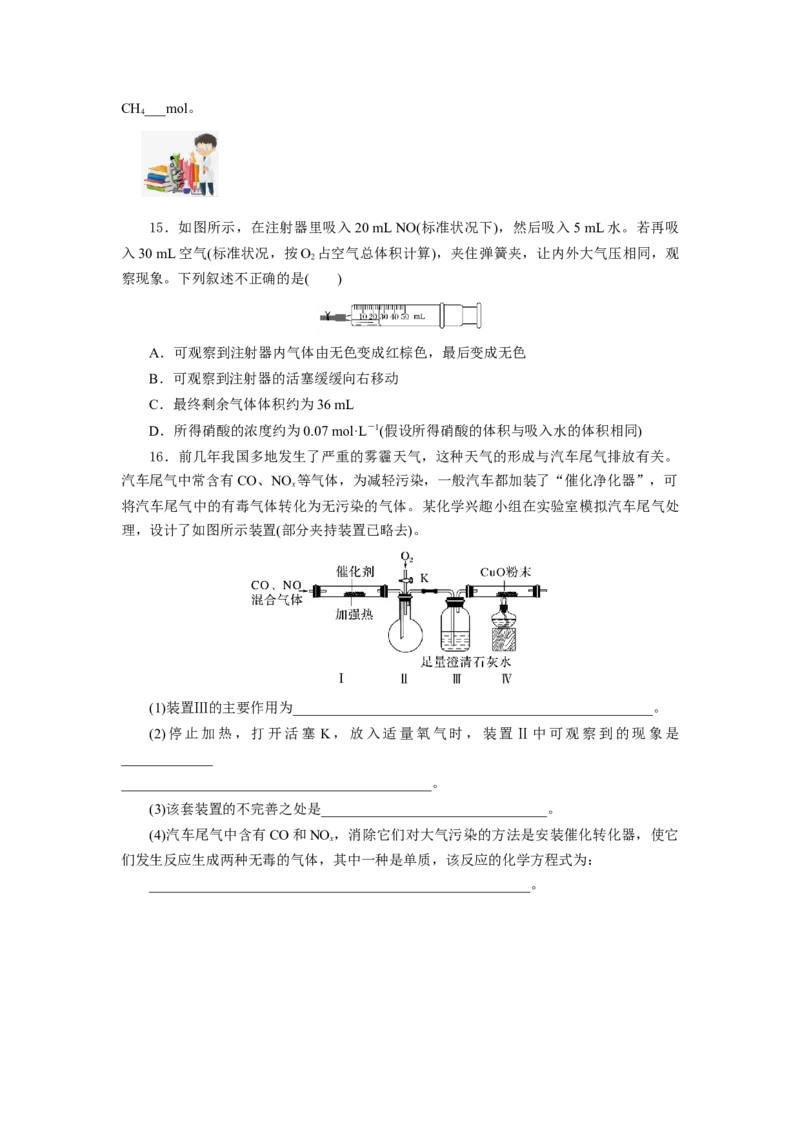
16.前几年我国多地发生了严重的雾霾天气,这种天气的形成与汽车尾气排放有关。
汽车尾气中常含有CO、NO 等气体,为减轻污染,一般汽车都加装了“催化净化器”,可
x
将汽车尾气中的有毒气体转化为无污染的气体。某化学兴趣小组在实验室模拟汽车尾气处
理,设计了如图所示装置(部分夹持装置已略去)。
(1)装置Ⅲ的主要作用为___________________________________________________。
(2)停止加热,打开活塞 K,放入适量氧气时,装置Ⅱ中可观察到的现象是
_____________
____________________________________________。
(3)该套装置的不完善之处是________________________________。
(4)汽车尾气中含有CO和NO,消除它们对大气污染的方法是安装催化转化器,使它
x
们发生反应生成两种无毒的气体,其中一种是单质,该反应的化学方程式为:
______________________________________________________。