文档内容
第 05 讲 氨
知识导航
知识精讲
一、氨的物理性质
颜色 气味 状态 密度 溶解性 沸点
无色 刺激性 气体 比空气小 极易溶于水(约1:700) -33.5℃,易液化
二、氨的化学性质
1.氨与水的反应
(1)氨气易溶于水,也易与水反应,化学方程式为:_________________________________。
(2)氨水中含有的粒子:_________________________________________________________。
△
(3)NH
3
·H
2
O受热易分解:NH
3
·H
2
O NH
3
↑+ H
2
O。
实验探究——喷泉实验
实验装置 操作及现象 结论
操作:打开弹簧夹,挤压胶头滴管,让水进入烧
瓶 氨气极易溶于水,水溶液呈
现象:烧杯中的酚酞溶液由玻璃管进入烧瓶,形 碱性。
成红色喷泉。
(4)常见的能形成喷泉的组合气体 HCl NH CO、Cl、HS、SO NO
3 2 2 2 2 2
溶液 水或碱 水或酸 碱 水或碱
实验探究——NH 与HCl 反应
3
实验操作 现象
用两根玻璃棒分别在浓氨水和浓盐酸里蘸一
下,然后使这两根玻璃棒接近。观察发生的现 两根玻璃棒接近时______________
象。
2.氨与酸的反应
氨几乎能与所有的酸(难溶性酸如HSiO 除外)反应生成盐,如:
2 3
NH + HCl === NH Cl NH + HNO === NH NO 2NH + H SO === (NH )SO
3 4 3 3 4 3 3 2 4 4 2 4
3.氨的催化氧化
化学方程式:________________________________________。
思考与交流:如何检验氨气?
三、氨的用途
1.氨易液化,当液氨汽化时要吸收大量的热,使周围温度急剧降低,因此液氨常用作__________。
2.氨是氮肥工业及制造硝酸、铵盐、纯碱等的重要原料。
3.氨是有机合成工业的常用原料(如制尿素、合成纤维、燃料等)。
对点训练
题型一:氨的性质
【例1】将导出的氨气接近下列物质时,不会产生白烟的是
A.氯气 B.浓 HSO C.浓 HCl D.浓 HNO
2 4 3
【例2】下列反应中,说明氨有还原性和碱性的是
A.2NH +3CuO 3Cu+N +3H O
3 2 2
B.
C.4NH +6NO 5N+6H O
3 2 2D.
【变3】下列关于氨气、氨水和铵盐的叙述正确的是
A.NH 易液化,液氨常用作制冷剂 B.实验室常用向上排空气法收集氨气
3
C.氨水中只含有NH 和HO两种分子 D.铵盐较稳定,不怕风吹雨打日晒,可露天贮存
3 2
【变4】下列NH 的干燥试剂和收集方法中,正确的是
3
选项 A B C D
干燥试剂 浓硫酸 浓硫酸 碱石灰 碱石灰
收集方法 向上排空气法 向下排空气法 向上排空气法 向下排空气法
A.A B.B C.C D.D
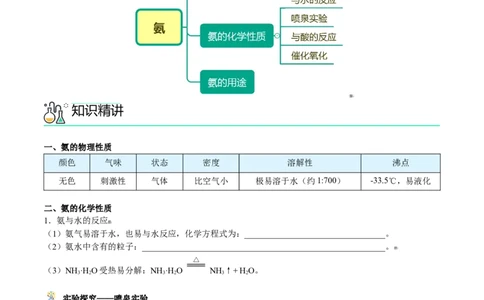
题型二:喷泉实验
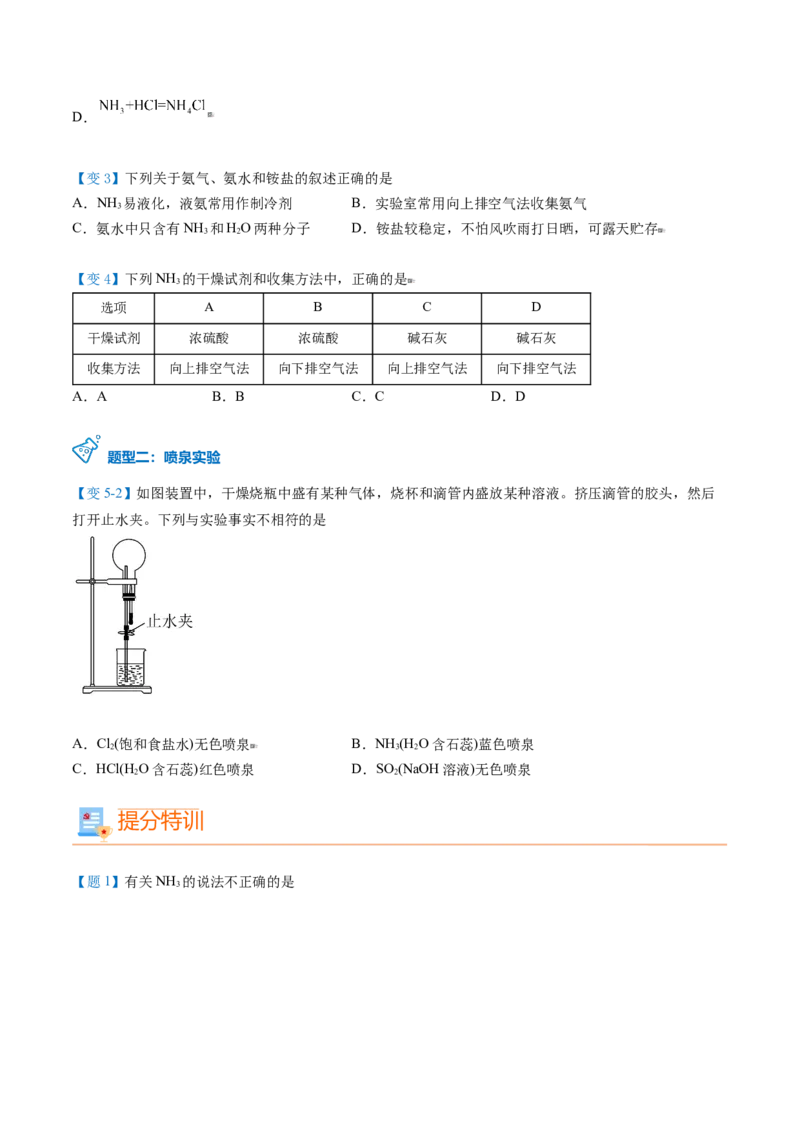
【变5-2】如图装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,然后
打开止水夹。下列与实验事实不相符的是
A.Cl(饱和食盐水)无色喷泉 B.NH (H O含石蕊)蓝色喷泉
2 3 2
C.HCl(HO含石蕊)红色喷泉 D.SO (NaOH溶液)无色喷泉
2 2
提分特训
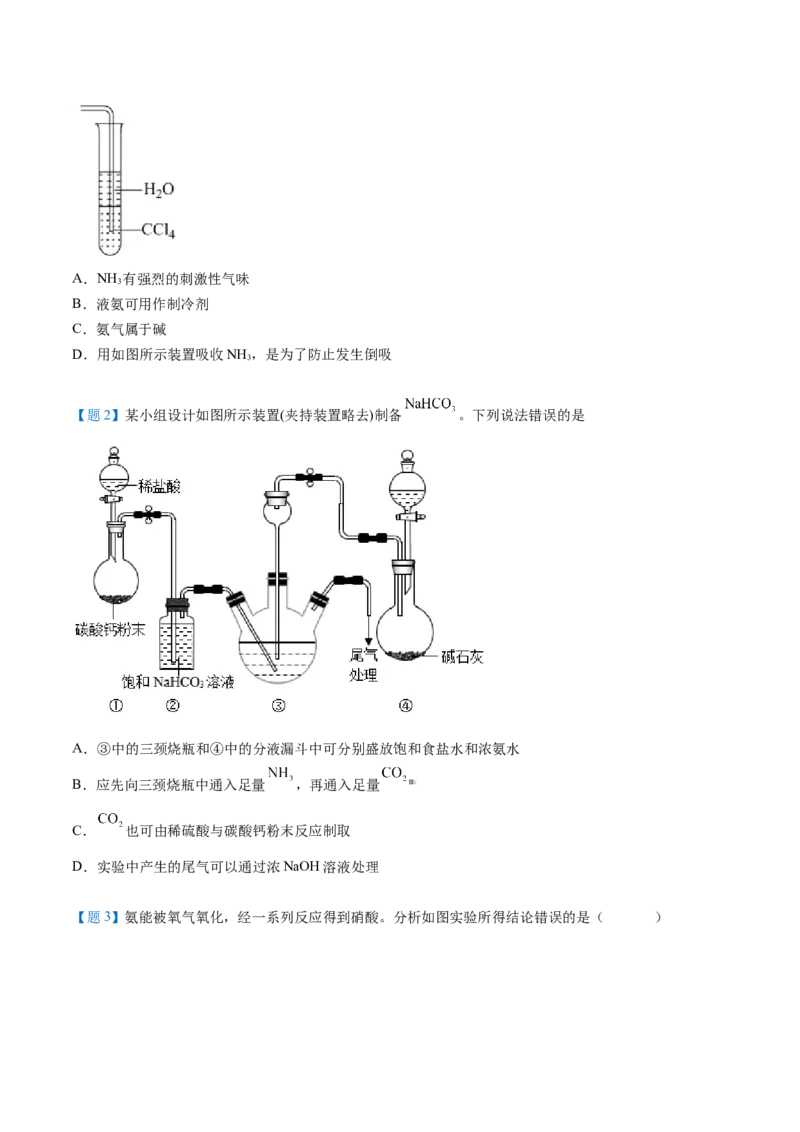
【题1】有关NH 的说法不正确的是
3A.NH 有强烈的刺激性气味
3
B.液氨可用作制冷剂
C.氨气属于碱
D.用如图所示装置吸收NH ,是为了防止发生倒吸
3
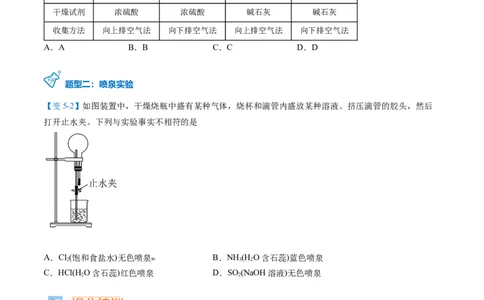
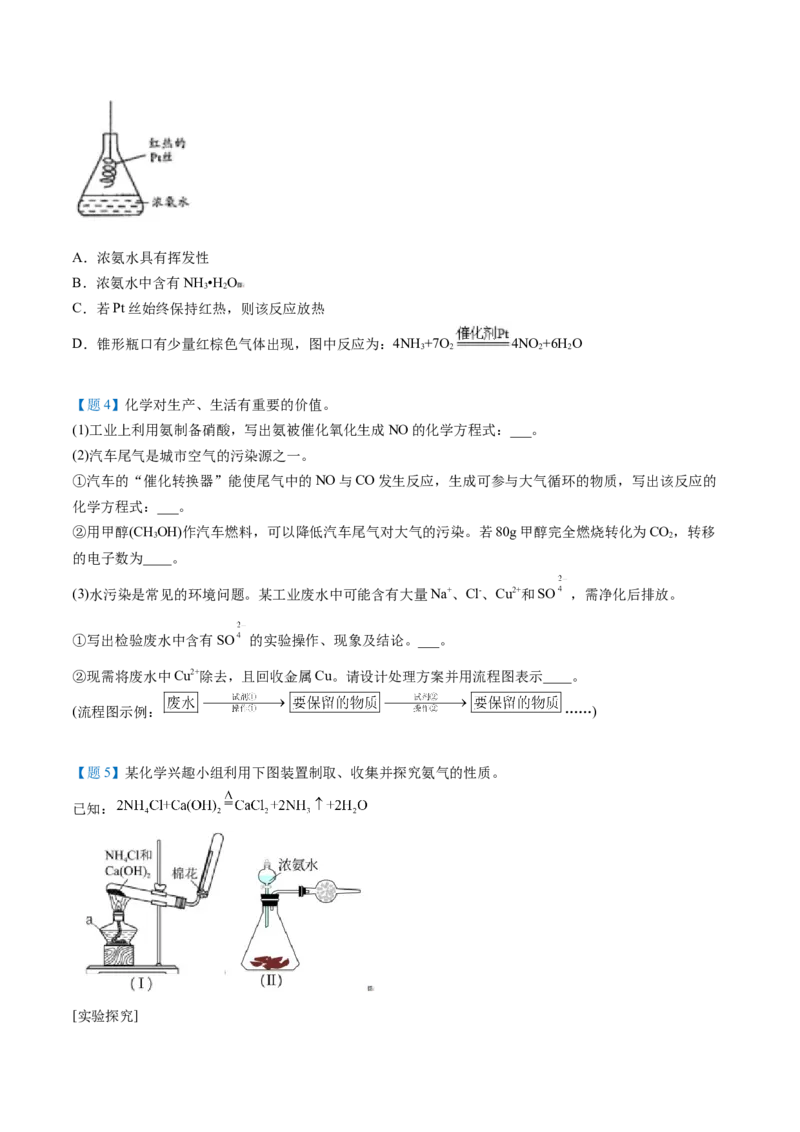
【题2】某小组设计如图所示装置(夹持装置略去)制备 。下列说法错误的是
A.③中的三颈烧瓶和④中的分液漏斗中可分别盛放饱和食盐水和浓氨水
B.应先向三颈烧瓶中通入足量 ,再通入足量
C. 也可由稀硫酸与碳酸钙粉末反应制取
D.实验中产生的尾气可以通过浓NaOH溶液处理
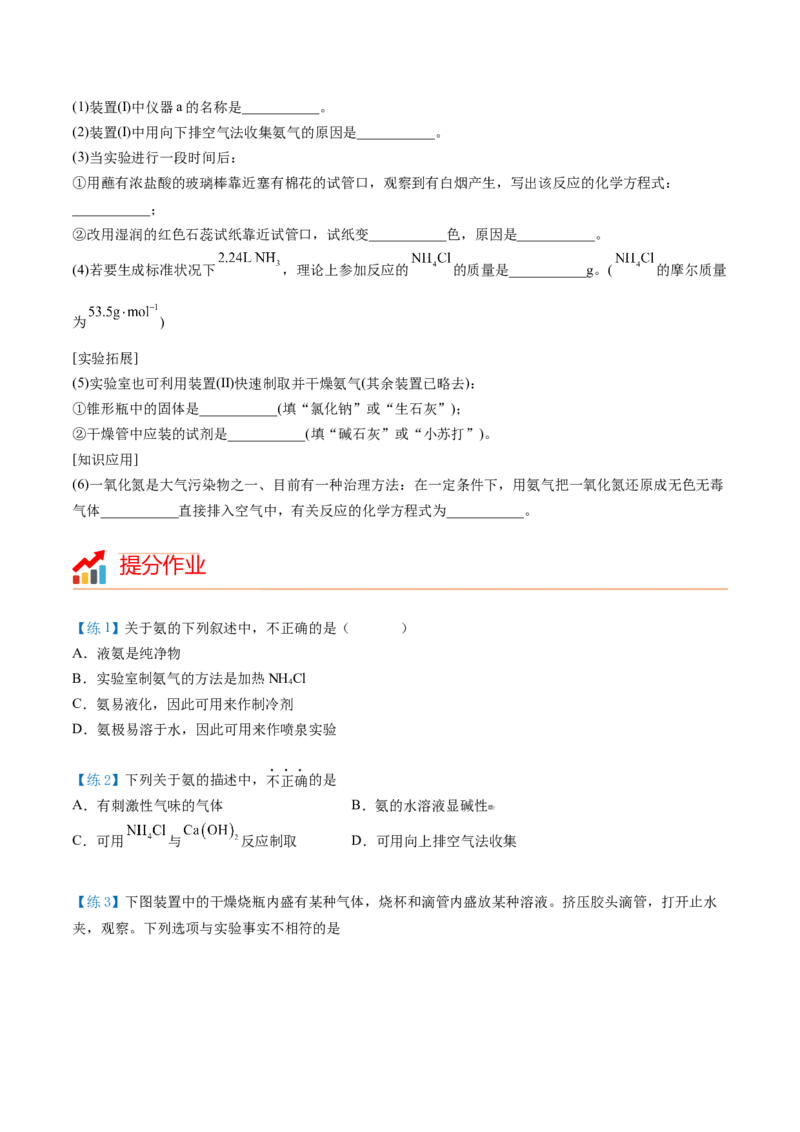
【题3】氨能被氧气氧化,经一系列反应得到硝酸。分析如图实验所得结论错误的是( )A.浓氨水具有挥发性
B.浓氨水中含有NH •H O
3 2
C.若Pt丝始终保持红热,则该反应放热
D.锥形瓶口有少量红棕色气体出现,图中反应为:4NH +7O 4NO +6H O
3 2 2 2
【题4】化学对生产、生活有重要的价值。
(1)工业上利用氨制备硝酸,写出氨被催化氧化生成NO的化学方程式:___。
(2)汽车尾气是城市空气的污染源之一。
①汽车的“催化转换器”能使尾气中的NO与CO发生反应,生成可参与大气循环的物质,写出该反应的
化学方程式:___。
②用甲醇(CHOH)作汽车燃料,可以降低汽车尾气对大气的污染。若80g甲醇完全燃烧转化为CO,转移
3 2
的电子数为____。
(3)水污染是常见的环境问题。某工业废水中可能含有大量Na+、Cl-、Cu2+和SO ,需净化后排放。
①写出检验废水中含有SO 的实验操作、现象及结论。___。
②现需将废水中Cu2+除去,且回收金属Cu。请设计处理方案并用流程图表示____。
(流程图示例: ……)
【题5】某化学兴趣小组利用下图装置制取、收集并探究氨气的性质。
已知:
[实验探究](1)装置(Ⅰ)中仪器a的名称是___________。
(2)装置(Ⅰ)中用向下排空气法收集氨气的原因是___________。
(3)当实验进行一段时间后:
①用蘸有浓盐酸的玻璃棒靠近塞有棉花的试管口,观察到有白烟产生,写出该反应的化学方程式:
___________;
②改用湿润的红色石蕊试纸靠近试管口,试纸变___________色,原因是___________。
(4)若要生成标准状况下 ,理论上参加反应的 的质量是___________g。( 的摩尔质量
为 )
[实验拓展]
(5)实验室也可利用装置(Ⅱ)快速制取并干燥氨气(其余装置已略去):
①锥形瓶中的固体是___________(填“氯化钠”或“生石灰”);
②干燥管中应装的试剂是___________(填“碱石灰”或“小苏打”)。
[知识应用]
(6)一氧化氮是大气污染物之一、目前有一种治理方法:在一定条件下,用氨气把一氧化氮还原成无色无毒
气体___________直接排入空气中,有关反应的化学方程式为___________。
提分作业
【练1】关于氨的下列叙述中,不正确的是( )
A.液氨是纯净物
B.实验室制氨气的方法是加热NH Cl
4
C.氨易液化,因此可用来作制冷剂
D.氨极易溶于水,因此可用来作喷泉实验
【练2】下列关于氨的描述中,不正确的是
A.有刺激性气味的气体 B.氨的水溶液显碱性
C.可用 与 反应制取 D.可用向上排空气法收集
【练3】下图装置中的干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液。挤压胶头滴管,打开止水
夹,观察。下列选项与实验事实不相符的是选项 气体 溶液 喷泉
A NH HO(含石蕊溶液) 蓝色喷泉
3 2
B HCl HO(含石蕊溶液) 红色喷泉
2
C Cl 饱和食盐水 无色喷泉
2
D. CO NaOH溶液 无色喷泉
2
A.A B.B C.C D.D
【练4】氨水中存在的微粒有
①NH ②NH ·H O ③HO ④OH- ⑤NH + ⑥H+
3 3 2 2 4
A.只有①②③④ B.只有②④⑤⑥ C.只有①②③④⑤ D.全部
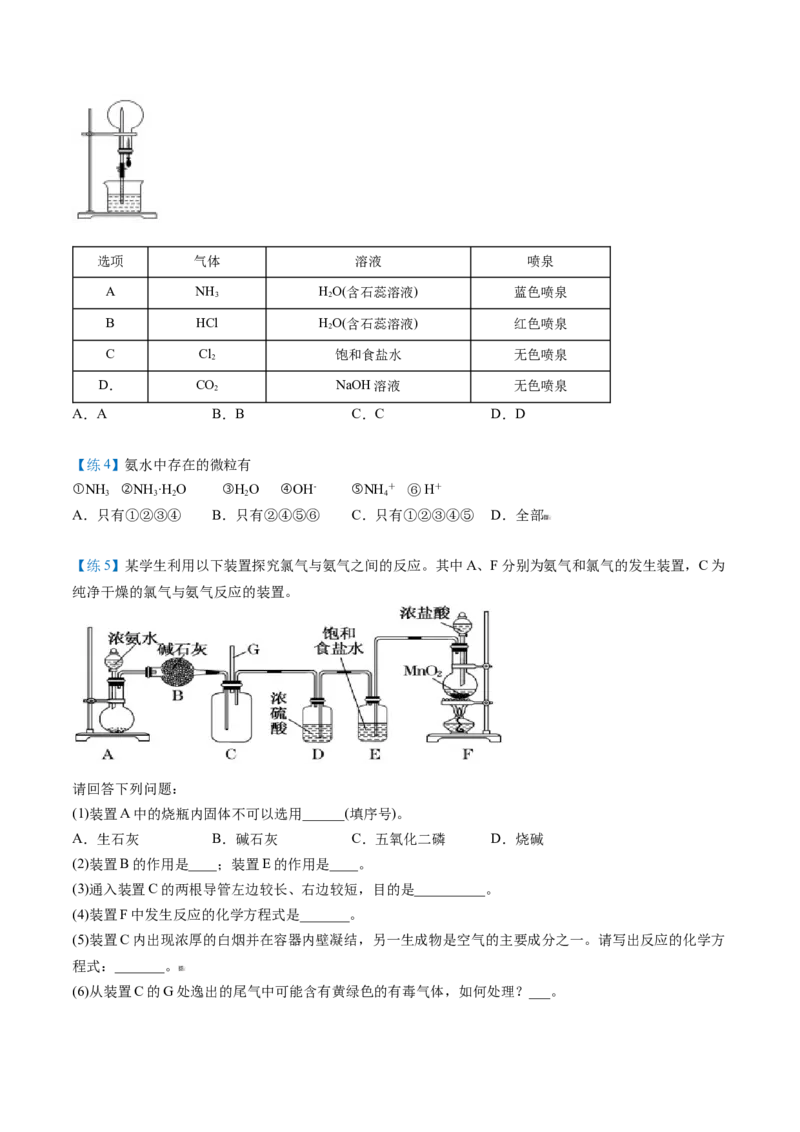
【练5】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为
纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用______(填序号)。
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(2)装置B的作用是____;装置E的作用是____。
(3)通入装置C的两根导管左边较长、右边较短,目的是__________。
(4)装置F中发生反应的化学方程式是_______。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方
程式:_______。
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?___。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育