文档内容
第 10 讲 影响化学平衡的因素
知识导航
小杨老师 15521324728 侵权必究
课前引入
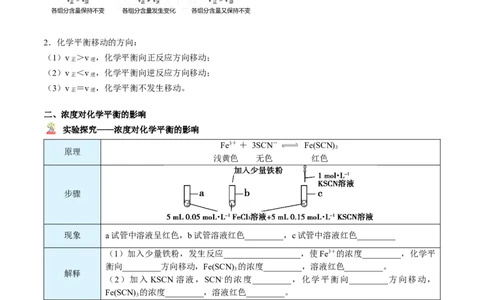
化学平衡的特征:
逆 化学平衡状态的研究对象是可逆反应
等
v =v ≠ 0,是一个动态平衡
正 逆
动
定 各组分浓度/物质的量/百分含量保持不变
变 外界条件改变时,原平衡状态被破坏,在新条件下建立平衡
在一定条件下,当一个可逆反应达到化学平衡状态后,如果改变浓度、压强、温度等条件,化学
平衡状态是否会发生变化?如何变化?
杨sir化学,侵权必究知识精讲
小杨老师 15521324728 侵权必究
一、化学平衡的移动
1.定义:在一定条件下,当可逆反应达到平衡状态后,如果改变反应条件,平衡状态被破坏,平衡体系的
物质组成也会随着改变,直到达到新的平衡状态。这种由原有的平衡状态达到新的平衡状态的过程叫做化
学平衡的移动。
2.化学平衡移动的方向:
(1)v >v ,化学平衡向正反应方向移动;
正 逆
(2)v <v ,化学平衡向逆反应方向移动;
正 逆
(3)v =v ,化学平衡不发生移动。
正 逆
杨sir化学,侵权必究
二、浓度对化学平衡的影响
实验探究——浓度对化学平衡的影响
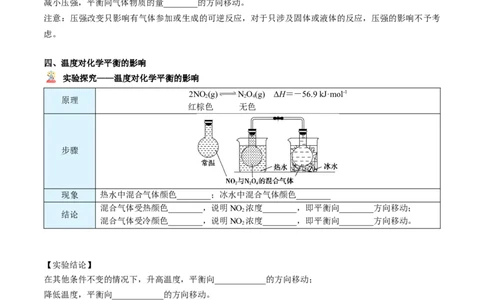
Fe3+ + 3SCN- Fe(SCN)
原理 3
浅黄色 无色 红色
步骤
现象 a试管中溶液呈红色,b试管溶液红色_________,c试管中溶液红色_________
(1)加入少量铁粉,发生反应__________________,使Fe3+的浓度_________,化学平
衡向_________方向移动,Fe(SCN) 的浓度_________,溶液红色_________。
3
解释
(2)加入 KSCN 溶液,SCN-的浓度_________,化学平衡向_________方向移动,
Fe(SCN) 的浓度_________,溶液红色_________。
3 杨sir化学,侵权必究
【实验结论】
在其他条件不变的情况下,增大反应物的浓度或减小生成物的浓度,都可以使平衡向_________方向移动;
增大生成物的浓度或减小反应物的浓度,都可以使平衡向_________方向移动。
三、压强对化学平衡的影响
实验探究——压强对化学平衡的影响
2NO (g) NO(g)
2 2 4
原理
(红棕色)
杨sir化学,侵权必究用50 mL注射器抽入20 mL NO 和NO 混合气体,将细管端用橡胶塞封闭
2 2 4
操作 将针筒活塞从10mL处迅速拉至 40 mL处(压
将针筒活塞迅速推至10 mL处(压强增大)
强减小)
现象 气体颜色_____________________________ 气体颜色_____________________________
压缩体积使压强增大时,c(NO )瞬间________ 增 大 体 积 使 压 强 减 小 时 , c(NO ) 瞬 间
2 2
解释
后又________,平衡向______移动 ________后又________,平衡向______移动
【实验结论】
在其他条件不变的情况下,增大压强,平衡向气体物质的量________的方向移动;
减小压强,平衡向气体物质的量________的方向移动。
注意:压强改变只影响有气体参加或生成的可逆反应,对于只涉及固体或液体的反应,压强的影响不予考
虑。
四、温度对化学平衡的影响
实验探究——温度对化学平衡的影响
2NO (g) NO(g) ΔH=-56.9 kJ·mol-1
原理 2 2 4
红棕色 无色
杨sir化学,侵权必究
步骤
现象 热水中混合气体颜色________;冰水中混合气体颜色________
混合气体受热颜色________,说明NO 浓度________,即平衡向________方向移动;
2
结论
混合气体受冷颜色________,说明NO 浓度________,即平衡向________方向移动。
2
【实验结论】
在其他条件不变的情况下,升高温度,平衡向____________的方向移动;
降低温度,平衡向____________的方向移动。
五、催化剂对化学平衡的影响
使用正催化剂,正、逆反应速率同时__________,且增大的倍数__________,化学平衡__________。
六、勒夏特列原理
如果改变影响平衡的一个条件(如温度、压强及参加反应的物质的浓度),平衡就向着能够减弱这种改变
的方向移动,该结论就是勒夏特列原理。
杨sir化学,侵权必究思考与交流:如何理解勒夏特列原理中的“减弱”一词?
对点训练
小杨老师 15521324728 侵权必究
题型一:浓度对化学平衡的影响
杨sir化学,侵权必究
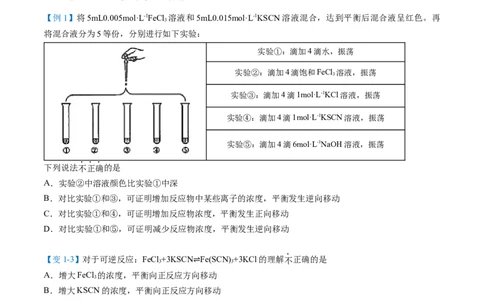
【例1】将5mL0.005mol·L-1FeCl 溶液和5mL0.015mol·L-1KSCN溶液混合,达到平衡后混合液呈红色。再
3
将混合液分为5等份,分别进行如下实验:
实验①:滴加4滴水,振荡
实验②:滴加4滴饱和FeCl 溶液,振荡
3
实验③:滴加4滴1mol·L-1KCl溶液,振荡
实验④:滴加4滴1mol·L-1KSCN溶液,振荡
实验⑤:滴加4滴6mol·L-1NaOH溶液,振荡
下列说法不正确的是
A.实验②中溶液颜色比实验①中深
B.对比实验①和③,可证明增加反应物中某些离子的浓度,平衡发生逆向移动
C.对比实验①和④,可证明增加反应物浓度,平衡发生正向移动
D.对比实验①和⑤,可证明减少反应物浓度,平衡发生逆向移动
【变1-3】对于可逆反应:FeCl +3KSCN Fe(SCN) +3KCl的理解不正确的是
3 3
A.增大FeCl 的浓度,平衡向正反应方向移动
3 ⇌
B.增大KSCN的浓度,平衡向正反应方向移动
C.增大Fe(SCN) 的浓度,平衡向逆反应方向移动
3
D.增大KCl的浓度,平衡向逆反应方向移动
杨sir化学,侵权必究
题型二:压强对化学平衡的影响
杨sir化学,侵权必究
【例2】在下列可逆反应中,增大压强或降低温度,均可使平衡正向移动的是
A.2SO (g)+O(g) 2SO (g) ΔH<0
2 2 3B.4NH (g)+5O(g) 4NO(g)+6H O(g)ΔH<0
3 2 2
C.2NH (g) N(g)+3H(g) ΔH>0
3 2 2
D.SO (g)+NO (g) SO (g)+NO(g) ΔH<0
2 2 3
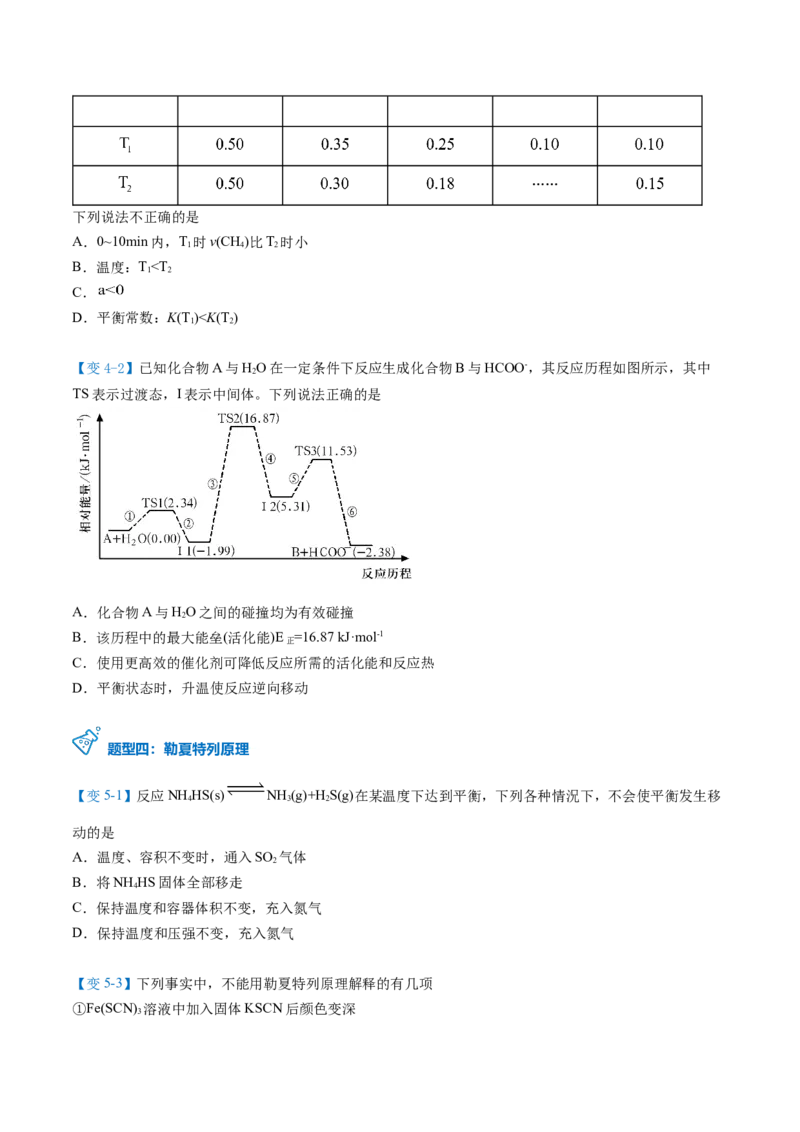
【变2-2】已知反应:2NO (红棕色) NO(无色) ΔH<0,将一定量的NO 充入注射器后封口,如
2 2 4 2
图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确
的是。
①b点的操作为拉伸注射器
②d点v <v
正 逆
③c点与a点相比,c(NO )增大,c(NO) 减小,
2 2 4
④若不忽略体系温度变化,且没有能量损失,则T(b)<T(c)
⑤若容器绝热,则平衡常数K>K
a c
A.①③⑤ B.②③④ C.①③④ D.②④⑤
【变3】在一密闭容器中,反应 aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新
的平衡时,A的浓度是原来的60% 则下列说法正确的是
⇌
A.平衡向正反应方向移动了
B.物质A的转化率减少了
C.物质B的物质的量分数增加了
D.a0
3 2 2 2
C.4NH (g)+5O(g) 4NO(g)+6H O(g) ΔH <0
3 2 2 3
D.H(g)+CO(g) C(s)+HO(g) ΔH >0
2 2 4题型六:勒夏特列原理综合大题
杨sir化学,侵权必究
【例8】探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以CO、H 为原料合成
3 3 2 2
CHOH涉及的主要反应如下:
3
I.CO(g)+3H(g)=CH OH(g)+H O(g) △H =-48.5 kJ∙mol−1
2 2 3 2 1
II.CO(g)+2H(g)=CH OH(g) △H =-92.4 kJ∙mol−1
2 3 2 杨sir化学,侵权必究
Ⅲ.CO(g)+H(g)=CO(g)+HO(g) △H
2 2 2 3
回答下列问题:
(1)△H=___________kJ∙mol−1
3
(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO 和3molH 发生上述反应,达到平衡时,
2 2
容器中CHOH(g)为amol,CO为bmol,此时H(g)的浓度为___________mol∙mol−1 (用含a、b、V的代数式
3 2
表示,下同),反应III的平衡常数为___________。
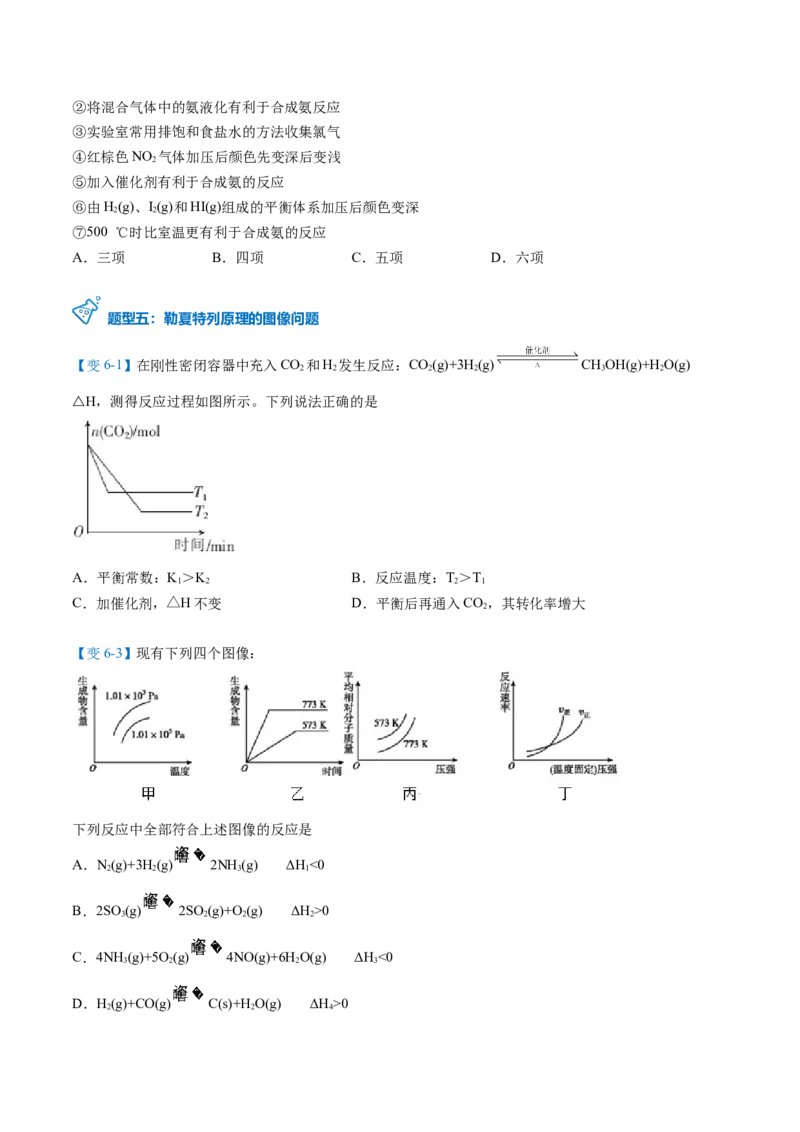
(3)不同压强下,按照n(CO):n(H )=1:3投料,实验测定CO 的平衡转化率和CHOH的平衡产率随温
2 2 2 3
度的变化关系如下图所示。
已知:CO 的平衡转化率= ×100%;CHOH的平衡产率= ×100%。
2 3
其中纵坐标表示CO 平衡转化率的是图___________(填“甲”或“乙”);压强p、p、p 由大到小的顺序为
2 1 2 3
___________;图乙中T 温度时,三条曲线几乎交于一点的原因是___________。
1
(4)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为___________(填字母代号)。
2 3
A.高温、高压 B.高温、低压
C.低温、高压 D.低温、低压
提分特训
小杨老师 15521324728 侵权必究
【题1】下列有关化学平衡的说法正确的是
A.对于恒温密闭容器中进行的反应N(g)+3H(g) 2NH (g),若N 的体积分数保持不变,则一定说明反
2 2 3 2
应已达到平衡状态
B.一定温度下,将2.0g CaCO 固体置于1L恒容密闭容器中充分反应后,c(CO)=0.0125mol/L,若保持温
3 2度不变,将容器体积扩大至2L,达到新平衡后c(CO)=0.01mol/L
2
C.反应:CH(g)+HO(g) CO(g)+3H(g) ∆H>0,在其它条件不变的情况下,升高温度、减小容器体积、
4 2 2
增大水蒸汽的浓度均能提高CH 的平衡转化率
4
D.一定温度下,恒容密闭容器中充入一定量NO 发生反应:2NO NO 达到平衡后,再向容器中充入
2 2 2 4
一定量的NO 并达到新的平衡,则NO 体积分数先增大后减小,但比原平衡小
2 2
【题2】等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达平衡:X(g)+2Y(g)
3Z(g) △H<0,当改变某个条件并达到新平衡后,下列叙述正确的是
A.升高温度,X的体积分数减小
B.增大压强,Z的浓度不变
C.保持容器体积不变,充入一定量的惰性气体,Y的浓度不变
D.保持容器体积不变,充入一定量的Z,X的体积分数增大
杨sir化学,侵权必究
【题4】利用CO 制备甲醇是温室气体资源化重要途径。在某CO 催化加氢制甲醇的反应体系中主要存在
2 2
如下反应:
反应I:CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=-48.2kJ·mol-1
2 2 3 2 1
反应II:CO(g)+H(g)=CO(g)+HO(g) ΔH=+42.5kJ·mol-1
2 2 2 2
反应III:CO(g)+2H(g)=CH OH(g)ΔH
2 3 3
向恒压、密闭容器中通入1molCO 和3molH ,平衡时CO、CO 和CHOH的物质的量分数随温度变化如图
2 2 2 3
所示。下列说法不正确的是
A.ΔH=-90.7kJ·mol-1
3
B.曲线a表示CO的物质的量分数随温度的变化
杨sir化学,侵权必究
C.在不改变反应时间和温度条件下,增大压强能提高CHOH的产量
3
D.在240~270℃内,温度改变对反应I和反应II平衡影响相反且程度接近
【题5】乙烯气相直接水合反应制备乙醇:C H(g)+HO(g) C HOH(g)。乙烯的平衡转化率随温度、
2 4 2 2 5
压强的变化关系如下[起始时,n(H O)=n(C H)=1 mol,容器体积为1 L]。
2 2 4下列分析不正确的是
A.乙烯气相直接水合反应的ΔH<0
B.图中压强的大小关系为p>p>p
1 2 3
C.图中a点对应的平衡常数K=
D.达到平衡状态a、b所需要的时间:a>b
杨sir化学,侵权必究
【题7】下列事实中,不能用勒夏特列原理解释的是
①Fe(SCN) 溶液中加入固体KSCN后颜色变深
3
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO 加压后颜色先变深后变浅
2
⑤加入催化剂有利于合成氨的反应
⑥由H(g)、I(g)和HI(g)组成的平衡体系加压后颜色变深
2 2
A.②⑤⑥ B.①③⑤ C.①②⑥ D.②③④
【题8】已知:(HF) (g) 2HF(g) >0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温
2
度下随压强的变化曲线如图所示。下列说法正确的是
A.温度:T<T
1 2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:υ(b)>υ(a)
杨sir化学,侵权必究
D.当 时,提分作业
小杨老师 15521324728 侵权必究
【练1】在水溶液中,CrO 呈黄色,Cr O 呈橙色,重铬酸钾(KCr O)在水溶液中存在以下平衡:
2 2 2 7
Cr O +HO 2CrO +2H+,下列说法正确的是
2 2
A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙色
B.该反应是氧化还原反应
C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大
D.向体系中加入少量水,平衡逆向移动
【练2】已知反应: ,把NO 、NO 的混合气体盛装在两个连通的烧瓶里,然后
2 2 4
用弹簧夹夹住橡皮管,把烧瓶A放入热水中,把烧瓶B放入冰水中,如图所示。与常温时烧瓶C内气体的
颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅。下列说法错误的是(A、B、C中初始
充入NO 、NO 的量相等)( )
2 2 4 杨sir化学,侵权必究
A.上述过程中,A烧瓶内正、逆反应速率均加快
B.上述过程中,B烧瓶内c(NO )减小,c(N O)增大
2 2 4
C.上述过程中,A、B烧瓶内气体密度均保持不变
D.反应 的逆反应为放热反应
【练3】对已经达到化学平衡的下列反应2X(g)+Y(g)⇌Z(g)减小压强时,对反应产生的影响是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
杨sir化学,侵权必究
D.正、逆反应速率都增大,平衡向正反应方向移动【练4】在密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g) N(g)+2CO (g);
2 2
ΔH=-746.4kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施有
①加催化剂同时升温
②加催化剂同时缩小容器体积
③升温同时充入N
2
④升温同时充入NO
A.1个 B.2个 C.3个 D.4个
【练5】在一密闭容器中,反应 3A(g)+B(s) 2C(g)+D(g) 达到平衡后,改变以下条件,下列说
法正确的是
A.增加A的浓度,平衡向正反应方向移动,平衡常数增大
B.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
杨sir化学,侵权必究
C.恒温恒容充入Ne,容器内压强增大,V(正)、V(逆)均增大
D.增加B的用量,正、逆反应速率不变,平衡不移动
【练6】一定条件下,CH 与HO(g)发生反应:CH(g)+HO(g) CO(g)+3H(g),设起始
4 2 4 2 2
n(H O)/n(CH )=Z,在恒压条件下,平衡时CH 的体积分数φ(CH)与Z和温度T的关系如图所示,下列说法
2 4 4 4
正确的是
A.图中X点对应的平衡混合物中n(H O)/n(CH )=3
2 4
B.图中Z的大小关系为a>3>b
C.该反应的焓变ΔH>0
杨sir化学,侵权必究
D.温度不变时,增大X点对应的平衡体系的压强后, φ(CH)减小
4
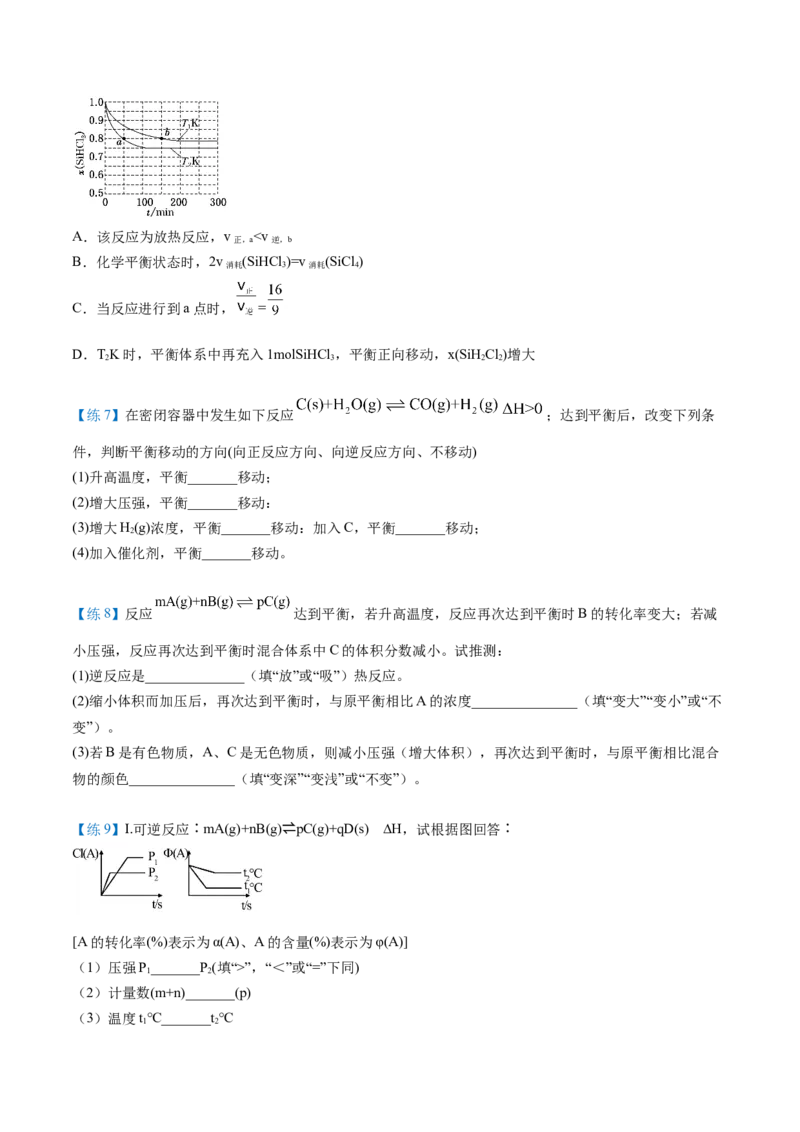
【练7】恒容条件下,1molSiHCl 发生如下反应:2SiHCl (g) SiHCl(g)+SiCl (g)。已知:v =v
3 3 2 2 4 正 消耗
(SiHCl )=k x2(SiHCl ),v =2v (SiHCl)=k x(SiHCl)·x(SiCl ),k 、k 分别为正、逆反应速率常数(仅
3 正 3 逆 消耗 2 2 逆 2 2 ⇌ 4 正 逆
与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl )随时间的变化。下列说法正确的是
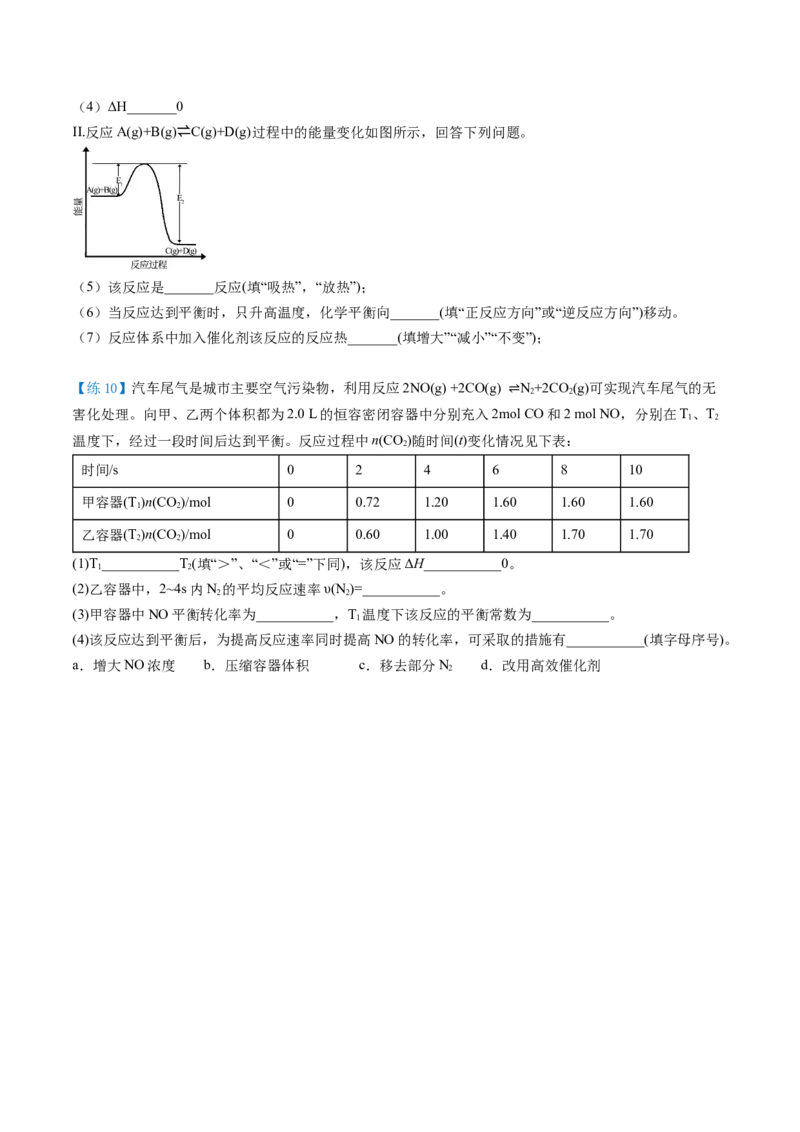
3A.该反应为放热反应,v ”,“<”或“=”下同)
1 2
(2)计量数(m+n)_______(p)
(3)温度t℃_______t℃
1 2(4)ΔH_______0
II.反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(5)该反应是_______反应(填“吸热”,“放热”);
(6)当反应达到平衡时,只升高温度,化学平衡向_______(填“正反应方向”或“逆反应方向”)移动。
(7)反应体系中加入催化剂该反应的反应热_______(填增大”“减小”“不变”);
【练10】汽车尾气是城市主要空气污染物,利用反应2NO(g) +2CO(g) N+2CO (g)可实现汽车尾气的无
2 2
害化处理。向甲、乙两个体积都为2.0 L的恒容密闭容器中分别充入2mol CO和2 mol NO,分别在T、T
⇌ 1 2
温度下,经过一段时间后达到平衡。反应过程中n(CO)随时间(t)变化情况见下表:
2 杨sir化学,侵权必究
时间/s 0 2 4 6 8 10
甲容器(T )n(CO)/mol 0 0.72 1.20 1.60 1.60 1.60
1 2
乙容器(T )n(CO)/mol 0 0.60 1.00 1.40 1.70 1.70
2 2
(1)T ___________T(填“>”、“<”或“=”下同),该反应ΔH___________0。
1 2
(2)乙容器中,2~4s内N 的平均反应速率υ(N )=___________。
2 2
(3)甲容器中NO平衡转化率为___________,T 温度下该反应的平衡常数为___________。
1
(4)该反应达到平衡后,为提高反应速率同时提高NO的转化率,可采取的措施有___________(填字母序号)。
a.增大NO浓度 b.压缩容器体积 c.移去部分N d.改用高效催化剂
2倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育