文档内容
第 12 讲 共价晶体
考点导航
知识精讲
知识点一:一、共价晶体的结构和性质
1.共价晶体的结构特点
(1)构成粒子及作用力
共价晶体
(2)空间结构:整块晶体是一个三维的共价键 结构,不存在单个的小分子,是一个“巨分子”。
2.共价晶体与物质的类别
物质种类 实例
某些 晶体硼、晶体硅、晶体锗、金刚石等
某些 碳化硅(SiC)、氮化硅(Si N)、氮化硼(BN)等
3 4
某些 二氧化硅(SiO)等
2
3.共价晶体的熔、沸点
(1)共价晶体由于原子间以较强的共价键相结合,熔化时必须破坏共价键,而破坏它们需要很高的温度,所
以共价晶体具有 的熔点。
(2)结构相似的共价晶体,原子半径越 ,键长越 ,键能越 ,晶体的熔点越 。
【即学即练1】
1.下表给出了几种物质的熔点和沸点:
单质B
熔点/℃ 801 710 -68 2300
沸点/℃ 1465 1418 57 2500下列说法中,错误的是A. 是分子晶体 B.单质B可能是共价晶体
C. 时, 呈气态 D. 水溶液不能导电
2.下列说法正确的是
A.HF和Br 分子中均含有s-pσ键
2
B.沸点:H O碳化硅>金刚石
D.酸性:CF COOH>CCl COOH>CH COOH
3 3 3
3.下列物质性质和解释不正确的是
A.HF、HCl、HBr的热稳定性依次减弱是因为非金属性逐渐减弱
B.HCl、HBr 、HI的沸点逐渐增大是因为其相对分子质量逐渐增大
C.NH 在水中的溶解度大于PH 是因为NH 的相对分子质量比PH 小
3 3 3 3
D.金刚石的熔点高于晶体硅是因为C- C键长比Si- Si键长短
知识点二: 二、典型的共价晶体
1.金刚石
(1)碳原子采取 杂化,C—C—C夹角为 。
(2)每个碳原子与周围紧邻的 个碳原子结合,形成共价键三维骨架结构。
(3)最小碳环由 个碳原子组成,且最小环上有4个碳原子在同一平面内;每个碳原子被12个六元环共
用。
2.二氧化硅晶体
(1)二氧化硅的结构
二氧化硅是自然界含量最高的固态二元氧化物,有多种结构,最常见的是低温石英(αSiO)。低温石英的结
2
构中有顶角相连的 形成螺旋上升的长链,这一结构决定了它具有手性(左、右型)。
石英的左、右型晶体①Si原子采取 杂化,正四面体内O—Si—O键角为 。
②每个Si原子与 个O原子形成 个共价键, 原子位于正四面体的中心, 原子位于正四面体的顶
点,同时每个O原子被 个硅氧正四面体共用;每个O原子和 个Si原子形成 个共价键,晶体中Si
原子与O原子个数比为 。
③最小环上有 个原子,包括 个O原子和 个Si原子。
(2)二氧化硅的用途
二氧化硅是制造水泥、玻璃、单晶硅、硅光电池、芯片和光导纤维的原料。
【即学即练2】
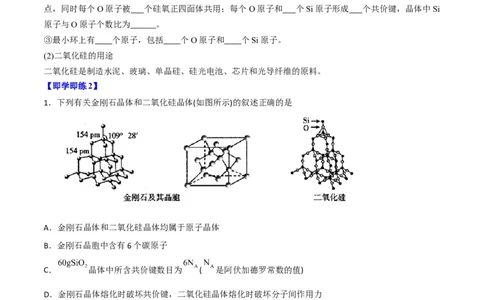
1.下列有关金刚石晶体和二氧化硅晶体(如图所示)的叙述正确的是
A.金刚石晶体和二氧化硅晶体均属于原子晶体
B.金刚石晶胞中含有6个碳原子
C. 晶体中所含共价键数目为 ( 是阿伏加德罗常数的值)
D.金刚石晶体熔化时破坏共价键,二氧化硅晶体熔化时破坏分子间作用力
2.美国《科学》杂志曾报道:在40GPa的高压下,用激光加热到1800K,人们成功制得了共价晶体CO ,
2
下列对该物质的推断一定不正确的是
A.该共价晶体中含有极性键
B.该共价晶体易汽化,可用作制冷材料
C.该共价晶体有很高的熔沸点
D.该共价晶体的硬度大,可用作耐磨材料
易错精析1.含有共价键的晶体都是共价晶体吗?
【细剖精析】
2.SiO 是二氧化硅的分子式吗?
2
【细剖精析】
3.金刚石晶体和富勒烯晶体的构成微粒相同吗?
【细剖精析】
4.金刚石晶体和富勒烯晶体受热熔化时克服的微粒间作用力相同吗?
【细剖精析】
5.以金刚石为例,说明共价晶体的微观结构与分子晶体有哪些不同?
【细剖精析】
6.分析金刚石、二氧化硅的晶体结构模型,判断共价晶体的化学式是否可以代表其分子式?
【细剖精析】
7.以金刚石为例,说明共价晶体的微观结构与分子晶体有哪些不同?
【细剖精析】
8.分析二氧化硅晶体结构模型,判断晶体中最小的环有多少个原子?1 mol SiO 中含有多少摩尔Si—O?
2
【细剖精析】
能力拓展
1.分子晶体和共价晶体的比较
晶体类型 分子晶体 共价晶体
分子间通过分子间作用力结合形成 相邻原子间以共价键结合而形成
定义
的晶体 的具有空间网状结构的晶体
组成微粒 分子 原子
金刚石、晶体硅、碳化硅、二氧
物质类别 多数非金属单质和共价化合物
化硅等
微粒间的作用力 分子间作用力 共价键
熔化时需
较弱的分子间作用力 很强的共价键
克服的作用力
熔、沸点 较低 很高
硬度 较小 很大
固态和熔融态时一般都不导电,但 固态和熔融态时多数不导电,但
物理性质
导电性 某些分子晶体溶于水能导电,如 晶体Si、晶体Ge为半导体,能
HCl 导电
溶解性 相似相溶 难溶于一般溶剂决定熔、沸点
分子间作用力的强弱 共价键的强弱
高低的因素
典型例子 干冰、冰 金刚石、二氧化硅
2.共价晶体与分子晶体熔、沸点高低的比较
(1)晶体类型不同:共价晶体>分子晶体
理由:共价晶体的熔、沸点与共价键有关,分子晶体的熔、沸点与分子间作用力有关。共价键的作用力远
大于分子间作用力。
(2)晶体类型相同
①共价晶体
一般来说,对结构相似的共价晶体来说,键长越短,键能越大,晶体的熔、沸点越高。例如:金刚石>碳
化硅>晶体硅。
②分子晶体
a.若分子间有氢键,则分子间作用力比结构相似的同类晶体大,故熔、沸点较高。如HF>HI;NH >
3
PH ;HO>HTe。
3 2 2
b.组成和结构相似的分子晶体,一般相对分子质量越大,范德华力越大,熔、沸点越高。如I >Br >Cl
2 2 2
>F;SnH >GeH >SiH>CH。
2 4 4 4 4
c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大,范德华力越大,熔、沸点越高。如
CO>N。
2
d.同类别的同分异构体,支链越多,熔、沸点越低。如正戊烷>异戊烷>新戊烷。
3.解共价晶体类题的注意事项
(1)共价晶体中一定存在共价键,但含有共价键的晶体不一定是共价晶体,只有原子间形成共价键三维骨架
结构时才形成共价晶体。
(2)共价晶体中不存在分子,晶体中所有原子全部参与形成共价键,故共价晶体熔化时破坏的作用力是共价
键。
(3)可以根据晶体的熔、沸点来判断晶体的类型,如分子晶体和共价晶体的物理性质的差别主要表现在两者
的硬度和熔、沸点大小上,前者远小于后者。
(4)结构相似的共价晶体,成键原子半径越小,键能越大,对应的共价晶体的熔、沸点越高。如熔点:金刚
石>碳化硅>晶体硅(键长Si—Si>C—Si>C—C,键能C—C>C—Si>Si—Si)。
金刚石(晶体硅)、碳化硅、二氧化硅的晶胞
金刚石晶胞 碳化硅晶胞 二氧化硅晶胞
4.金刚石(晶体硅)
金刚石(晶体硅)晶胞的每个顶角和面心均有1个C(Si)原子,晶胞内部有4个C(Si)原子,每个金刚石(晶体硅)晶胞中含有8个C(Si)原子。
5.碳化硅晶胞
(1)碳、硅原子都采取sp3杂化,C—Si夹角为109°28′。
(2)每个硅(碳)原子与周围紧邻的4个碳(硅)原子以共价键结合成正四面体结构,向空间伸展形成三维骨架结
构。
(3)最小碳环由6个原子组成且不在同一平面内,其中包括3个C原子和3个Si原子。
(4)每个SiC晶胞中含有4个C原子和4个Si原子。
6.二氧化硅晶胞
SiO 晶体结构相当于在晶体硅结构中每2个Si原子中间插入一个O原子,参照金刚石晶胞模型,在SiO 晶
2 2
胞中有8个Si原子位于立方晶胞的顶角,有6个Si原子位于立方晶胞的面心,还有4个Si原子与16个O
原子在晶胞内构成4个硅氧四面体,均匀排列于晶胞内。每个SiO 晶胞中含有8个Si原子和16个O原子。
2
分层提分
题组A 基础过关练
1.下列关于共价晶体、分子晶体的叙述中,正确的是
A.金刚石为共价键三维骨架结构,晶体中的最小环上有6个碳原子
B.分子晶体中一定存在共价键
C.HI的相对分子质量大于HF,所以HI的沸点高于HF
D.在SiO 晶体中,1个硅原子和2个氧原子形成2个共价键
2
2.碳有多种同分异构体,其中石墨烯与金刚石的晶体结构如图所示,下列说法不正确的是
A.在石墨烯晶体中,每个正六元环拥有的共价键和碳原子数之比为3:2
B.石墨烯中含碳碳双键
C.金刚石晶体中,碳原子采用 杂化
D.金刚石晶体中最小的碳环上有6个碳原子
3.下面排序不正确的是A.晶体的熔点由高到低排列
B.硬度由大到小:金刚石 碳化硅 晶体硅
C.熔点由高到低:
D.熔点由高到低:
4.下列关于各类物质的熔、沸点比较的说法错误的是
A.邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
B.金刚石、SiC、晶体硅的熔点依次降低
C.碱金属从Li到Cs熔点依次降低
D.NaCl、KCl、CO、N 的沸点依次降低
2
5.“天问一号”采用了我国自主研制的高性能碳化硅材料。碳化硅也叫金刚砂,硬度大,具有耐热性、
耐氧化性和耐腐蚀性等性能,结构如图,下列叙述不正确的是
A.碳化硅中只含有极性键 B.碳化硅的熔点比金刚石低
C. 碳化硅中含 键 D.碳化硅为原子晶体
6.下列说法中,正确的是
A.干冰熔化时,分子中C=O键发生断裂
B.金属晶体的熔、沸点一定比分子晶体的高
C.原子晶体中,共价键的键长越短,键能越大,熔点就越高
D.分子晶体中,分子间作用力越大,则分子越稳定
题组B 能力提升练
1.如图是石墨、足球烯( )、金刚石三种晶体的结构图,下列说法正确的是A.这三种物质是碳的同分异构体,燃烧产物相同
B.这三种物质熔化时,克服的粒子间作用力都是化学键
C.等物质的量的石墨、金刚石所含的C-C键数目之比为3:4
D.石墨晶体C-C键的键长短于金刚石的C-C键,则金刚石比石墨稳定
2.下列对一些实验事实及其理论解释都正确的是
选项 实验事实 理论解释
A 原子的第一电离能小于 原子 同周期元素原子的电离能随原子序数增大而增大
B 为直线形分子 分子中 为 杂化,键角为
C 金刚石的熔点高于石墨 金刚石是原子晶体,石墨是分子晶体
D 的沸点低于 的相对分子质量小于
A.A B.B C.C D.D
3.碳化硅(SiC)俗称金刚砂,与金刚石具有相似的晶体结构,硬度为9.5,熔点为2700℃,其晶胞结构如图
所示。下列说法错误的是
A.SiC品体中碳原子和硅原子均采用 杂化
B.距离硅原子最近的硅原子数为12
C.金刚石的熔点低于2700℃
D.若晶胞参数为apm,则该晶体的密度为
4.下列关于晶体的说法正确的组合是①所有分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H O、H S晶体的熔点依次降低
2 2
④离子晶体中只有离子键
⑤SiO 晶体中每个硅原子与4个氧原子以共价键相结合
2
⑥晶体中分子间作用力越大,分子越稳定
⑦氯化钠熔化时离子键被破坏
⑧含有共价键的晶体熔沸点都比较高,因为熔化时需要破坏共价键
A.①②⑤ B.③⑤⑦ C.⑤⑥⑧ D.④⑦⑧
5.现在已能在高压下将CO 转化为具有类似SiO 结构的原子晶体,下列关于CO 原子晶体的说法中正确的
2 2 2
是
A.CO 的原子晶体中存在范德华力,每1 mol CO 原子晶体中含有2N π键
2 2 A
B.在一定条件下,CO 原子晶体转化为CO 分子晶体是物理变化
2 2
C.熔点:金刚石>原子晶体CO
2
D.在CO 的原子晶体中,每个C原子周围结合4个O原子,每个O原子与两个C原子相结合
2
6.根据表给出的几种物质的熔沸点数据,判断下列说法中错误的是
晶体 NaCl MgCl AlCl SiCl 单质R
2 3 4
熔点/ 801 714 190 -70 2300
沸点/ 1465 1418 177.8 57 2500
A.SiCl 和A1Cl 都是分子晶体 ,熔融状态下不导电
4 3
B.MgCl 和NaCl都是离子晶体,熔融状态能导电且易溶于水
2
C.若单质R是原子晶体,其熔沸点的高低是由共价键的键能决定的
D.固态时可导电的一定是金属晶体
7.下列说法中,正确的是
A.共价晶体中,共价键的键长越短,键能越大,熔点就越高
B.碘单质升华时,分子中 键发生断裂
C.分子晶体中,共价键的键能越大,该物质的熔、沸点就越高
D.分子晶体中,分子间作用力越大,则分子越稳定
23.根据量子力学计算,氮化碳有五种结构,其中一种 氮化碳硬度超过金刚石晶体,成为首屈一指的
超硬新材料,已知该氮化碳的二维晶体结构如图所示。下列有关该氮化碳的说法不正确的是A.该晶体中的碳、氮原子核外最外层都满足8电子稳定结构
B.氮化碳中碳元素显 价,氮元素显 价
C.每个碳原子与四个氮原子相连,每个氮原子和三个碳原子相连
D.氮化碳的分子式为
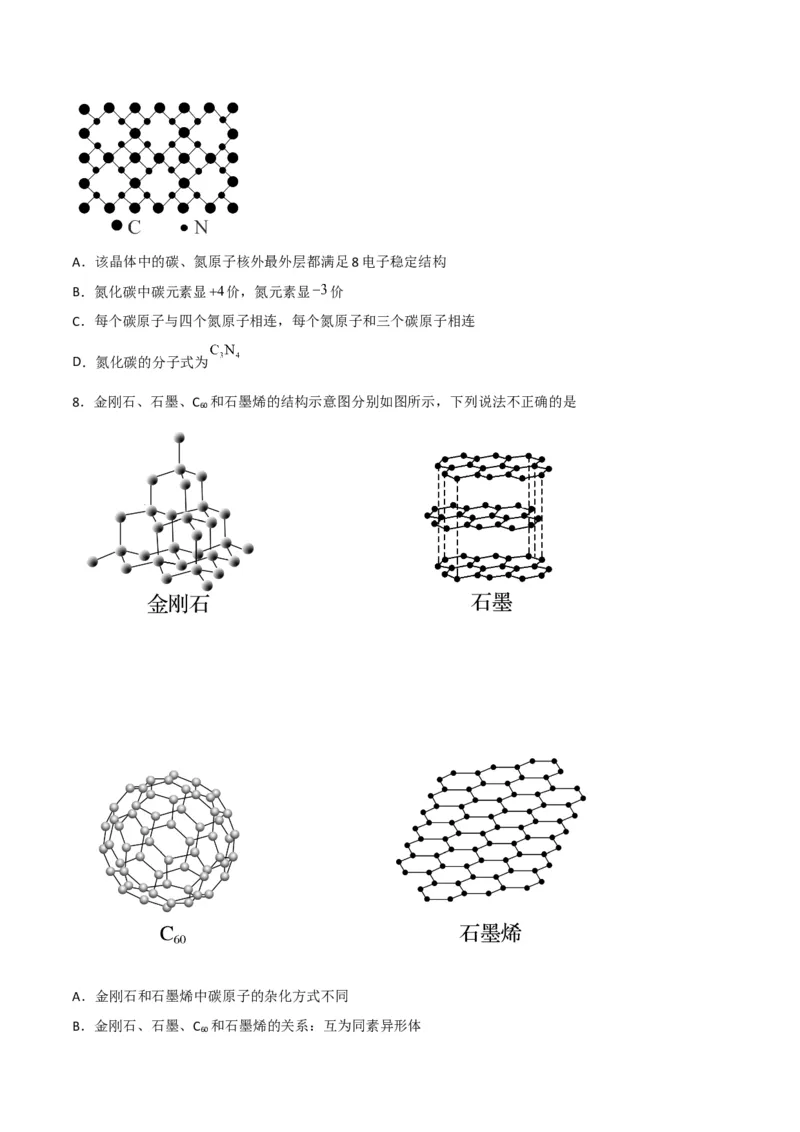
8.金刚石、石墨、C 和石墨烯的结构示意图分别如图所示,下列说法不正确的是
60
A.金刚石和石墨烯中碳原子的杂化方式不同
B.金刚石、石墨、C 和石墨烯的关系:互为同素异形体
60C.这四种物质完全燃烧后的产物都是CO
2
D.石墨与C 的晶体类型相同
60
【答案】D
9.有关晶体的结构如图所示,下列说法不正确的是
A. 晶体中,每个 周围等距且紧邻的 有6个
B. 晶体中,每个 被8个 包围
C.钛酸钙的化学式为
D.在金刚石晶体中,碳原子与碳碳键的个数之比为倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育