文档内容
第 09 讲 化学平衡常数
知识导航
小杨老师 15521324728 侵权必究
课前引入
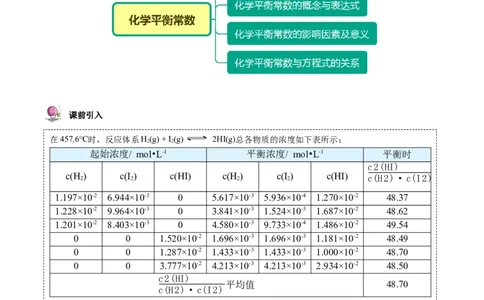
在457.6℃时,反应体系H(g) + I (g) 2HI(g)总各物质的浓度如下表所示:
2 2 杨sir化学,侵权必究
起始浓度/ mol•L-1 平衡浓度/ mol•L-1 平衡时
c2(HI)
c(H 2 ) c(I 2 ) c(HI) c(H 2 ) c(I 2 ) c(HI) c(H2)·c(I2)
1.197×10-2 6.944×10-3 0 5.617×10-3 5.936×10-4 1.270×10-2 48.37
1.228×10-2 9.964×10-3 0 3.841×10-3 1.524×10-3 1.687×10-2 48.62
1.201×10-2 8.403×10-3 0 4.580×10-3 9.733×10-4 1.486×10-2 49.54
0 0 1.520×10-2 1.696×10-3 1.696×10-3 1.181×10-2 48.49
0 0 1.287×10-2 1.433×10-3 1.433×10-3 1.000×10-2 48.70
0 0 3.777×10-2 4.213×10-3 4.213×10-3 2.934×10-2 48.50
c2(HI)
平均值 48.70
c(H2)·c(I2)
观察上表中的已知数据,思考:化学平衡体系中反应物浓度与生成物浓度之间有什么关系呢?知识精讲
小杨老师 15521324728 侵权必究
一、浓度商的概念与表达式
1.浓度商的概念
在任意时刻,生成物浓度幂之积与反应物浓度幂之积的比值,称为浓度商,常用Q表示。
2.表达式
杨sir化学,侵权必究
对于可逆反应mA(g) + nB(g) pC(g) + qD(g) 浓度商Q=_______
【答案】
二、化学平衡常数的概念与表达式
1.化学平衡常数的概念
在一定温度下,当一个可逆反应达到平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,
该常数就是该反应的化学平衡常数(简称平衡常数),用符号K表示。
2.表达式
对于可逆反应mA(g) + nB(g) pC(g) + qD(g),化学平衡常数K= 。
杨sir化学,侵权必究
注意
(1)在任意时刻,生成物浓度幂之积与反应物浓度幂之积的比值,都为浓度商,而化学平衡常数,则
是在一定温度下,可逆反应达到平衡时的浓度商。当反应中有关物质的浓度商等于平衡常数时,表明
该反应已达到化学平衡状态。
(2)固体或液体纯物质一般不列入浓度商和平衡常数。
(3)关于HO的浓度问题:当HO为液态时,其浓度为固定常数,不能代入平衡常数表达式;当
2 2
HO的是气态时,则需要代入平衡常数表达式。
2 杨sir化学,侵权必究
及时小练写出下列反应的化学平衡常数:
(1)2SO (g) + O(g) 2SO (g) K = _________________________
2 2 3
(2)4NH (g) + 5O(g) 4NO(g) + 6HO(g) K = _________________________
3 2 2
(3)H(g) + I(g) 2HI(g) K = _________________________
2 2
(4)C(s) + HO(g) CO(g) + H(g) K = _________________________
2 2
【答案】(1)
c2(SO
3
)
;(2)
c4(NO)·c6(H
2
O) ;(3)c2(HI)
;(4)
c2(SO )·c(O ) c4(NH )·c5(O ) c(H )·c(I )
2 2 3 2 2 2
c(CO)·c(H )
2
c(H O)
2
三、平衡常数的影响因素及意义
1.化学平衡常数的影响因素
杨sir化学,侵权必究
化学平衡常数是表明化学反应限度的一个特征值,通常情况下只受________影响。
【答案】温度
2.化学平衡常数的意义
(1)通常,K越大,说明平衡体系中________所占的比例越大,______反应进行的程度越大,即该反应进
行得越完全,平衡时反应物的转化率越大;反之,K越小,该反应进行得越不完全,平衡时反应物的转化
率越小。
(2)一般来说,当K>______时,该反应就进行得基本完全了。
【答案】生成物 正 105
3.化学平衡常数的应用
杨sir化学,侵权必究
判断正在进行的可逆反应进行的方向
(1)Q < K:反应向正反应方向进行,v > v ;
正 逆
(2)Q = K:反应处于化学平衡状态,v = v ;
正 逆
(3)Q > K:反应向逆反应方向进行,v < v 。
正 逆
思考与交流
分别写出下列方程式的平衡常数表达式,并思考,K 、K 、K 之间有何关系?
1 2 3 杨sir化学,侵权必究
H(g) + I(g) 2HI(g) K = _________
2 2 1
2HI(g) H(g) + I(g) K = _________
2 2 2
2H(g) + 2I(g) 4HI(g) K = _________
2 2 3【答案】c2(HI) c(H )·c(I )❑ c4(HI)
2 2
c(H )·c(I ) c2(HI) c2(H )·c2(I )
2 2 2 2
四、平衡常数与方程式的关系
1.对于同一可逆反应,正反应和逆反应的平衡常数互为倒数;
2.若化学方程式中各物质的化学计量数都扩大或缩小至原来的n倍,则化学平衡常数变为原来的n次幂或
次幂。
3.若干方程式相加,则总反应的平衡常数等于分步平衡常数之乘积;若干方程式相减,则总反应的平衡
常数等于分步平衡常数之商。
杨sir化学,侵权必究
举个例子
已知方程式A(g) C(g) K 和 B(g) D(g) K 用K 、K 表示下列反应的平衡常数。
1 2 1 2
(1)C(g) A(g) K = __________
3
(2)2B(g) 2D(g) K = __________
4
1 1
(3)A(g) + B(g) C(g) + D(g) K = __________
2 2 5
(4)2A(g) + D(g) B(g) + 2C(g) K = __________
6
1
【答案】(1)1/ K 1 (2)K 2 2 (3)K 1 · K 2 (4)2K 1 /K 2
2
对点训练
小杨老师 15521324728 侵权必究
题型一:平衡常数的概念、表达式与影响因素
杨sir化学,侵权必究
【变1-2】对于可逆反应:2SO (g)+O(g) 2SO (g),在一定温度下其平衡常数为K,下列条件的变化中,能
2 2 3
使K发生变化的是
⇌
A.缩小容器体积 B.降低体系温度
C.保持体积不变,充入O D.使用合适的催化剂
2
【答案】B
【详解】
化学平衡常数只与温度有关,与其它外界条件无关,故在上述变化中能使K发生变化的是降低体系温度,
故合理选项是B。
【例2】对于3Fe(s)+4H O(g) Fe O(s)+4H(g),反应的化学平衡常数的表达式为( )
2 3 4 2
⇌c(Fe O )⋅c(H ) c(Fe O )⋅c4 (H )
3 4 2 3 4 2
c(Fe)⋅c(H O) c(Fe)⋅c4 (H O)
A.K= 2 B.K= 2
杨sir化学,侵权必究
c4 (H O) c4 (H )
2 2
c4 (H ) c4 (H O)
C. K= 2 D.K= 2
【答案】D
解析:平衡常数是生成物浓度幂之积与反应物浓度幂之积的比值,但固体浓度视为定值,不写入平衡常数
计算式中,D项正确。答案:D
题型二:平衡常数与方程式的关系
杨sir化学,侵权必究
【变3-1】已知下列反应的平衡常数:①S(s)+O(g) SO (g),K ;②H(g)+S(s) HS(g),K ;
2 2 1 2 2 2
则反应H(g)+SO (g) O(g)+HS(g)的平衡常数是
2 2 2 2
A.K -K B.K -K C.K /K D.K /K
1 2 2 1 2 1 1 2
【答案】C
【详解】
由题干方程式可知, , ,反应H(g)+SO (g) O(g)+HS(g)的平衡常数
2 2 2 2
;
答案选C。
【变3-3】化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数
数值如下:
2NO(g) N(g)+O(g) K=1×1030
2 2 1
2H(g)+O(g) 2HO(g) K=2×1081
2 2 2 2
2CO(g) 2CO(g)+O(g) K=4×10-92
2 2 3
以下说法正确的是( )
c(N )⋅c(O )
2 2
c(NO)
A.常温下,NO分解产生O 的反应的平衡常数表达式为K=
2 1
B.常温下,NO、HO、CO 三种化合物分解放出O 的进行程度由大到小的顺序为NO>H O>CO
2 2 2 2 2C.常温下,水分解产生O,此时平衡常数的数值约为5×10-80
2
D.以上说法都不正确
【答案】B
c(N )⋅c(O )
2 2
c2 (NO)
解析:NO分解反应的K= ,A项错误;HO分解产生O 的平衡常数K=1/K =5×10-82,C项错
1 2 2 2
误;根据NO、HO、CO 分解的平衡常数,可判断放出O 的进行程度大小顺序为NO>H O>CO,B项正确;
2 2 2 2 2
D项错误。答案:B
题型三:平衡常数与“三段式”的计算
杨sir化学,侵权必究
【变4-1】在800℃时,体积为1升的密闭容器中,下列可逆反应达到化学平衡状态:CO(g)+HO(g)CO (g)
2 2
+H (g),已知CO和HO(g)的初始浓度为0.01mol·L-1时,H 平衡浓度为0.005mol·L-1.若此时再加入
2 2 2
0.02mol·L-1的HO(g),重新达到平衡时,H 平衡浓度为
2 2
A.0.025 mol·L-1 B.0.0075 mol·L-1 C.0.005 mol·L-1 D.0.015 mol·L-1
【答案】B
【详解】
两次反应的温度相同,所以平衡常数不变,据此可以求出结果:
此时 ,又加入0.02mol/LH O后:
2
此时 ,解得x=0.0025mol/L,此时氢气的浓度为
0.005+x=0.0075mol/L,正确选项为B。
【变4-3】已知可逆反应CO(g)+HO(g) CO(g) + H(g),K为平衡常数,只与温度有关,与浓度无关。
2 2 2
(1)830K时,若起始浓度:CO为1mol• L-1,HO为1.5mol• L-1,平衡时CO转化率为60%,则HO的转化
2 2
率为:_________;K值为:_________
(2)830K时,若起始浓度改为:CO为1mol• L-1,HO为3mol• L-1,平衡时HO的转化率为:
2 2_____________;
【答案】40% 1 25%
【分析】
由题给条件可知,知道转化率可以算出一氧化碳的转化量,同时可以水的消耗量,二氧化碳的生成量,氢
气的生成量,则可以算出水的转化率和平衡常数。浓度改变,温度不变,平衡常数不变,可以进行计算水
的转化率。
【详解】
(1)对于可逆反应CO(g)+HO(g) CO(g) + H(g),若起始浓度:CO为1mol• L-1,HO为1.5mol• L-1,
2 2 2 2
达到平衡时,平衡时CO转化率为60%,则CO的消耗量为1mol• L-1×60%=0.6mol/L,则水的消耗量为
0.6mol/L,而二氧化碳的生成量为0.6mol/L,氢气的生成量为0.6mol/L,而水的平衡浓度为1.5mol/
L-0.6mol/L=0.9mol/L,一氧化碳的平衡浓度为1mol/L-0.6mol/L=0.4mol/L,则HO的转化率为0.6mol/
2
L÷1.5mol/L=40%,平衡常数 ;故答案为40% ;1;
(2)830K时,若起始浓度改为:CO为1mol• L-1,HO为3mol• L-1,达到平衡时,一氧化碳的转化量为
2
xmol/L,则水的转化量为xmol/L,二氧化碳的生成量为xmol/L,氢气的生成量为xmol/L,则水的平衡浓度为(3-
x)mol/L,一氧化碳的平衡浓度为(1-x)mol/L,则根据平衡常数可以计算:xmol/L×xmol/L÷(3-x)mol/L×(1-
x)mol/L=1,求出x=0.75mol/L, H O的转化率为0.75 mol/L÷3mol/L=25%;故答案为:25%;
2
题型四:化学反应速率与化学平衡综合
杨sir化学,侵权必究
【例5】 时,将 气体放入 密闭容器中,发生反应N O (g)⇌2NO (g),实验数据如
2 4 2
图。已知 与 的消耗速率与各自的分压有如下关系: ,
。下列说法错误的是
A.混合气体的密度始终保持不变
B.a点v(正)>v(逆)C.前
杨sir化学,侵权必究
D.该温度下反应的平衡常数K 与k、k 间的关系为K·k=k
p 1 2 p 2 1
【答案】D
【详解】
A.混合气体密度计算公式为 , 与 相互转化,没有其他状态的物质生成, 不变,
该容器体积恒定为1L, 不变,即 不变,A不符合题意;
B.反应从 开始后,向 的正方向移动,根据图像60秒时才达到平衡,
所以a点并未达到平衡,正在正移,所以v(正)>v(逆),故B不符合题意;
C. ,故C不符合题意;
D.已知 , , ,根据反应速率与
计量系数成正比可知,v(NO )=2v(N O),平衡时正逆反应速率相等,则k•p2(NO )=2×k •p(N O), =
2 2 4 2 2 1 2 4
=K ,故D符合题意;
p
综上所述答案为D。
【例7】(I)已知在448℃时,反应H(g)+I (g) 2HI(g)的平衡常数K 为49,则该温度下反应2HI(g)
2 2 1
H(g)+I (g)的平衡常数K 为 ;反应1/2H (g)+1/2I (g) HI(g)的平衡常数K 为
2 2 2 2 2 3
(Ⅱ)在一定体积的密闭容器中进行如下化学反应:CO(g)+H(g) CO(g)+HO(g),其化学平衡常数(K)和
2 2 2
温度(t)的关系如下表所示:
t/℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K
(2)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变
杨sir化学,侵权必究
B.混合气体中c(CO)不变
C.v (H )=v (H O)
正 2 逆 2
D. c(CO )=c(CO)
2(3)某温度下,平衡浓度符合下式:c(CO)·c(H)=c(CO)·c(HO),试判断此时的温度为 ℃
2 2 2
(4)在 800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为 c(CO)为 2mol·L-1,c(H )为
2 2
1.5mol·L-1,c(CO)为1mol·L-1,c(H O)为3mol·L-1,此时反应 达到平衡(填“是”或“否”)。
2
c(CO)⋅c(H O)
2
c(CO )⋅c(H )
【答案】1/49 7 2 2 BC 830 否
解析: (I)第2个反应是第1个反应的逆反应,平衡常数互为倒数关系,第3个反应的化学计量数与第1个
√K
相比,缩小为原来的一半,平衡常数也会发生变化,得K= 1
3
(Ⅱ)(3)当c(CO)·c(H)=c(CO)·c(HO)时,K=1,由表中数据可知此时温度为830℃。(4)可根据Q与K的大小
2 2 2
c(CO)⋅c(H O)
2
c(CO )⋅c(H )
关系判断,此时刻下,Q= 2 2 =1>0.9,所以反应未达到平衡。
提分特训
小杨老师 15521324728 侵权必究
【题1】对于可逆反应:2SO (g)+O(g) 2SO (g),在一定温度下其平衡常数为K,下列条件的变化中,能
2 2 3
使K发生变化的是
⇌
A.缩小容器体积 B.降低体系温度
C.保持体积不变,充入O D.使用合适的催化剂
2
【答案】B
【详解】
化学平衡常数只与温度有关,与其它外界条件无关,故在上述变化中能使K发生变化的是降低体系温度,
故合理选项是B。
【题2】据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应的化学方程式为
2CO(g)+6H(g) CHCHOH(g)+3H O(g)。下列叙述正确的是( )
2 2 3 2 2
A.相同条件下,2 mol氢原子所具有的能量等于1 mol氢分子所具有的能量
B.当v(CO)=2v(CHCHOH)时,反应一定达到平衡状态
2 3 2
C.当平衡向正反应方向移动时,平衡常数一定增大
杨sir化学,侵权必究
D.增大压强,可提高CO 和H 的转化率
2 2
【答案】D
【解析】A.相同条件下,2 mol氢原子结合成H 时,会形成1 mol H-H键。形成化学键会释放能量,故2
2
mol氢原子所具有的能量大于1 mol氢分子所具有的能量,A错误;
B.未指明反应速率是正反应速率还是逆反应速率,因此不能据此判断反应是否处于平衡状态,B错误;
C.平衡常数只与温度有关,温度不变,化学平衡常数就不变。若改变外界条件是通过增大反应物浓度或
增大压强的方法,化学平衡正向移动,但平衡常数不变,C错误;D.该反应的正反应是气体体积减小的反应,增大压强,化学平衡向气体体积减小的正反应方向移动, 使
CO 和H 的转化率提高,D正确;
2 2
故答案为D。
【题3】加热NO 依次发生的分解反应为①NO NO+O,②NO NO+O;在2 L密闭容器
2 5 2 5 2 3 2 2 3 2 2
中充入8 mol N O ,加热到t ℃,达到平衡状态后O 为9 mol,NO 为3.4 mol,则t ℃时反应①的平衡常
2 5 2 2 3
数为( )
A.10.7 B.8.5
C.9.6 D.10.2
【答案】 B
【解析】 设平衡时NO 的浓度减小x,则
2 5
NONO+O,NONO+O
2 5 2 3 2 2 3 2 2
开始/(mol/L) 4 0 0 x x
转化/(mol/L) x x x
平衡/(mol/L) 4-x x x 1.7 4.5
所以4.5-x=x-1.7,所以x=3.1 mol/L,则t ℃时反应①的平衡常数为1.7×=8.5,答案选B。
【题4】某温度下,反应SO (g)+1/2O (g) SO (g)的平衡常数K=50,在同一温度下,反应SO (g)
2 2 3 1 3
SO (g)+O(g)的平衡常数K 的值为( )
2 2 2
A.2500 B.100 C.0.02 D.0.001
【答案】C
c(SO )
3
1
c(SO )⋅c2 (O )
【 解 析 】 SO (g)+1/2O (g) SO (g),K = 2 2 ; SO (g) SO (g)+1/2O (g),K =
2 2 3 1 3 2 2 2
1
c(SO )⋅c2 (O )
2 2
c(SO )
3 ;
1
1
K 50
K= 1 = 0.02,C项正确。答案:C
2
【题6】高炉炼铁中发生的基本反应之一如下:
FeO(固)+CO(气)⇌Fe(固)+CO
2
(气)ΔH>0
(1)则该反应中平衡常数表达式K=_________________
(2)已知1100℃时K=0.263。温度升高,化学平衡移动后达到新的平衡,高炉内CO 和CO的体积比值
2
_______平衡常数K值___(均填增大,减小或不变).
(3)1100℃时测得高炉中c(CO)=0.025mol·L-1,c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于平
2
衡状态________(选填是或否),此时化学反应速率v ____v (选填>,<,=)。
正 逆
【答案】 增大 增大 否 >【解析】(1)FeO(固)+CO(气) Fe(固)+CO (气) H>0,平衡常数K= ,
2
⇌ △
故答案为 ;
(2)已知1100℃时K=0.263,ΔH>0,反应是吸热反应,温度升高,化学平衡正向移动后达到新的平衡,高
炉内CO 和CO的体积比值会增大,平衡常数增大;
2
故答案为增大;增大;
(3)1100℃时测得高炉中c(CO)=0.025molL−1,c(CO)=0.1molL−1,浓度商Q= =0.25v ,
正 逆
故答案为否;>。
【题7】I.已知在448℃时,反应H(g)+I(g) 2HI(g)的平衡常数K 为49,则该温度下反应2HI(g)
2 2 1
H(g)+I(g)的平衡常数K 为____________;反应1/2H (g)+ I(g) HI(g)的平衡常数K 为
2 2 2 2 2 3
____________。
II.在一定体积的密闭容器中进行如下化学反应:CO(g)+H(g) CO(g)+HO(g),其化学平衡常数(K)和
2 2 2
温度(t)的关系如下表所示:
t/℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的逆反应为____________(填“吸热”或“放热”)反应。
(2)能判断该反应达到化学平衡状态的依据是____________。
A.混合气体中c(CO)不变
杨sir化学,侵权必究
B.c(CO)=c(CO)
2
C.v (H )=v (H O)
正 2 逆 2
D.容器中压强不变
(3)某温度下,平衡浓度符合下式:c(CO)•c(H )=c(CO)•c(H O),试判断此时的温度为____________℃,
2 2 2
在此温度下,加入2mol的CO和3mol的H,达到平衡时,CO的转化率为____________。
2
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO)为2mol•L-1,c(H)为
2 2
1.5mol•L-1,c(CO)为1mol•L-1,c(HO)为3mol•L-1,则下一时刻,反应将____________(填“正向”或“逆
2
向”)进行。【答案】 7 放热 AC 830 60% 逆向
【解析】I.由 和 可知, ,又由 可得 ,故答案为:
49、7;
II.(1)根据方程式CO(g)+H(g) CO(g)+HO(g),平衡常数与温度的关系变可知,平衡常数
2 2 2
随温度的升高而增大,平衡正向移动,则正反应为吸热反应,逆反应为放热反应,故
答案为:放热;
(2)在一定条件下,当一个可逆反应的正反应速率与逆反应速率相等时,反应物的浓度与生成物的浓度
不再改变(混合物中各组分的百分含量不再改变),达到一种表面静止的状态,即“化学平衡状态”,则
A.混合气体中c(CO)不变,A正确;
B.c(CO)=c(CO)不能说明正逆反应速率是否相等,则不一定处于平衡状态,B错误;
2
C.当 时,则说明该反应处于平衡状态,C正确;
D.根据方程式可知反应前后体积不变,压强始终不变,因此容器中压强不变不一定处于平衡状态,D错
误;
故答案为:AC;
(3)某温度下,平衡浓度符合下式:c(CO)•c(H )=c(CO)•c(H O),由平衡常数 可知
2 2 2
平衡常数 ,结合图表分析可知当 时的温度为830℃,由三段式可知
平衡时c(CO)•c(H )=c(CO)•c(H O)且反应前后体积不变,因此可得 ,解得x=1.2,即转
2 2 2
化率 ,故答案为:830℃、60%;
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO)为2mol•L-1,c(H)为
2 21.5mol•L-1,c(CO)为1mol•L-1,c(HO)为3mol•L-1,此时浓度熵为 >0.9,因此该反应向逆反应
2
方向移动,故答案为:逆向。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列关于平衡常数K的说法正确的是( )
A.加入催化剂可能会改变平衡常数K
B.改变反应物浓度能改变平衡常数K
C.平衡常数K与反应本身及温度有关
D.K越大,反应物的转化率越小
【答案】C
【详解】
化学平衡常数K与化学反应本身及温度有关,加入催化剂、改变反应物浓度等均不能改变平衡常数K;平
衡常数K越大,反应正向进行的程度越大,反应物的转化率越大,答案选C。
【练2】某温度时,N+3H 2NH 的平衡常数K=a,则此温度下,NH 1/2 N +3/2H 的平衡常数为
2 2 3 3 2 2
A.a-(1/2) B.a C.(1/2)a D.a-2
【答案】A
【详解】
对同一可逆反应(化学计量数相同),在相同温度下,正逆反应化学平衡常数互为倒数。N+3H 2NH 的
2 2 3
平衡常数K=a,故2NH N+3H 的平衡常数K= ,同一反应若化学计量数变为原来的n倍,平衡常数
3 2 2
变为原来的n次幂。故NH 1/2 N +3/2H 的平衡常数K= = a-(1/2),A选项正确。
3 2 2
故选A。
【练3】已知下列反应的平衡常数:
1 1
① SO (g) + O(g) SO (g) K ;②NO(g) + O(g) NO (g) K 。
2 2 3 1 2 2 2
2 2
则反应SO (g) + NO (g) SO (g) + NO(g)的平衡常数为( )
2 2 3 杨sir化学,侵权必究
K
A.K + K B.K ﹣K C. 1 D.K × K
1 2 2 1 K 1 2
2
【答案】C
【练4】在一定条件下,有下列分子数相同的可逆反应,其平衡常数K值分别是①H + F 2HF K=1047
2 2
②H + Cl 2HCl K=1017
2 2
③H + Br 2HBr K=109
2 2
④H + I 2HI K=1
2 2
比较K值大小,可知各反应的正反应进行的程度由大到小的顺序是( )
A.①②③④ B.④②③① C.①④③② D.无法确定
【答案】A
【练5】合成氨反应N(g)+3H(g) 2NH (g)在某温度下达到平衡时,各物质的浓度是c(N)=3mol/L ,
2 2 3 2
c(H)=9mol/L,c(NH )=4mol/L,则
2 3
(1)该温度时的平衡常数为 ;起始浓度c(N)=
2
(2)H 的转化率为 。
2
【答案】7.3×10-3 5mol·L-1 40%
c2 (NH ) 42
3
解析:(1)K=
c(N
2
)⋅c3 (H
2
)
=
3×93
≈7.3×10-3
设起始时N、H 的浓度分别为x、y
2 2
N(g)+3H(g) 2NH (g)
2 2 3
起始 x, y 0
平衡 3mol·L-1 9mol·L-1 4mol·L-1
x−3mol/L 1 y−9mol/L 3
= =
△c x-3mol·L-1 y-9mol·L-1 4mol·L-1
4mol/L 2
,则x=5mol·L-1;
4mol/L 2
,则
y=15mol·L-1
6mol/L
×100%
(2)H 的转化率=
15mol/L
=40%。
2
【练7】目前工业上可用CO 来生产燃料甲醇,有关反应为:CO(g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 2 3 2
=-49.0 kJ/mol。现向体积为1 L的密闭容器中,充入1 mol CO 和3 mol H ,反应过程中测得CO 和
2 2 2
CHOH(g)的浓度随时间的变化如图所示。
3
(1)若CO 的转化率为40%时,反应放出的热量为_________kJ;
2
(2)从反应开始到平衡,氢气的平均反应速率v(H )=________;
2
(3)判断该可逆反应达到化学平衡状态的标志是_________(填字母)。
杨sir化学,侵权必究
a.v (CHOH)=v (CO)
生成 3 消耗 2b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.CO、H、CHOH、HO的浓度均不再变化
2 2 3 2
(4)下列表示该反应速率最快的是__________;
a.v(H )=2 mol·L-1·min-1 b.v(CO)=4.5 mol·L-1·min-1
2 2
c.v(CHOH)=3 mol·L-1·min-1 d.v(H O)=0.2 mol·L-1·s-1
3 2
(5)该反应的平衡常数表达式为K=_________反应的平衡常数K 数值为_______。
【答案】19.6 0.225 cd d 5.3
【分析】
(1)根据反应放出的热量与反应的物质的物质的量呈正比计算;
(2)先计算v(CO),然后根据不同物质反应的速率关系计算v(H );
2 2
(3)根据平衡状态的特征判断;
(4)都转化为用CO 浓度变化表示反应速率,而且使速率单位相同,然后再进行比较;
2
(5)根据反应平衡常数的含义书写其表达式,将各种物质平衡浓度带入可得其K值。
【详解】
(1)根据反应方程式CO(g)+3H(g) CHOH(g)+H O(g) ΔH=-49.0 kJ/mol可知:每有1 mol完全反应,会
2 2 3 2
放出49.0 kJ的热量,现向体积为1 L的密闭容器中,充入1 mol CO 和3 mol H ,若CO 的转化率为40%时,
2 2 2
则反应的CO 的物质的量是0.4 mol,反应放出的热量为Q=0.4 mol×49.0 kJ/mol=19.6 kJ;
2
(2)根据图象可知:从反应开始到平衡v(CO)= =0.075mol/(L·min),根据方程式
2
可知v(H )=3v(CO)= 0.075mol/(L·min)×3=0.225 mol/(L·min);
2 2
(3)a.v (CHOH)=v (CO)表示的都是反应正向进行,不能据此判断反应是否处于平衡状态,a错误;
生成 3 消耗 2
b.反应在恒容密闭容器中进行,气体的体积不变,反应混合物都是气体,气体的质量不变,因此反应混
合气体的密度始终不变,因此不能根据密度不变来判断反应是否处于平衡状态,b错误;
c.该反应是反应气体气体的物质的量改变的反应,气体的质量不变,若混合气体的平均相对分子质量不
再改变,说明反应达到平衡状态,c正确;
d.CO、H、CHOH、HO的浓度均不再变化,说明反应达到了平衡状态,d正确;
2 2 3 2
故答案为cd;
(4)a.v(H )=2 mol·L-1·min-1,则v(CO)= v(H )= mol·L-1·min-1;
2 2 2
b.v(CO)=4.5 mol·L-1·min-1;
2
c.v(CHOH)=3 mol·L-1·min-1,则v(CO)=v(CHOH)=3 mol·L-1·min-1;
3 2 3
d.v(H O)=0.2 mol·L-1·s-1=12 mol·L-1·min-1,则v(CO)= v(H O)=12 mol·L-1·min-1;
2 2 2
可见上述反应中表示该反应速率最快的是v(CO)=12 mol·L-1·min-51,故答案为d;
2(5)根据化学平衡常数的含义可知反应CO(g)+3H(g) CHOH(g)+H O(g)的平衡常数表达式是K=
2 2 3 2
;
在反应开始时c(CO)=1 mol/L,c(H )=3 mol/L,达到平衡时c(CO)=0.25 mol/L,改变浓度是0.75 mol/L,则
2 2 2
共有物质转化关系可知平衡时c(H )=3 mol/L-3×0.75 mol/L=0.75 mol/L,c(H O)=0.75 mol/L,带入平衡常数
2 2
表达式可得K= =5.3。
【点睛】
本题考查反应热的计算及图象方法在化学反应速率和化学平衡的应用等知识。掌握有关概念的含义,清楚
平衡状态的特征是本题解答的关键。在比较化学反应速率快慢时,一定要根据用不同物质表示的反应速率
比等于化学方程式中相应物质的化学计量数的比,转化为用同一物质表示的反应速率,且速率单位相同,
此时速率数值越大,则其表示的反应速率越快。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育