文档内容
第 09 讲 化学平衡常数
知识导航
小杨老师 15521324728 侵权必究
课前引入
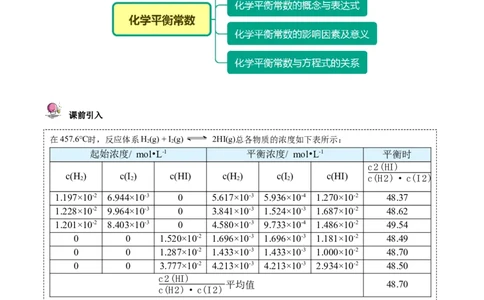
在457.6℃时,反应体系H(g) + I (g) 2HI(g)总各物质的浓度如下表所示:
2 2 杨sir化学,侵权必究
起始浓度/ mol•L-1 平衡浓度/ mol•L-1 平衡时
c2(HI)
c(H 2 ) c(I 2 ) c(HI) c(H 2 ) c(I 2 ) c(HI) c(H2)·c(I2)
1.197×10-2 6.944×10-3 0 5.617×10-3 5.936×10-4 1.270×10-2 48.37
1.228×10-2 9.964×10-3 0 3.841×10-3 1.524×10-3 1.687×10-2 48.62
1.201×10-2 8.403×10-3 0 4.580×10-3 9.733×10-4 1.486×10-2 49.54
0 0 1.520×10-2 1.696×10-3 1.696×10-3 1.181×10-2 48.49
0 0 1.287×10-2 1.433×10-3 1.433×10-3 1.000×10-2 48.70
0 0 3.777×10-2 4.213×10-3 4.213×10-3 2.934×10-2 48.50
c2(HI)
平均值 48.70
c(H2)·c(I2)
观察上表中的已知数据,思考:化学平衡体系中反应物浓度与生成物浓度之间有什么关系呢?知识精讲
小杨老师 15521324728 侵权必究
一、浓度商的概念与表达式
1.浓度商的概念
在任意时刻,生成物浓度幂之积与反应物浓度幂之积的比值,称为浓度商,常用Q表示。
2.表达式
杨sir化学,侵权必究
对于可逆反应mA(g) + nB(g) pC(g) + qD(g) 浓度商Q=_______
二、化学平衡常数的概念与表达式
1.化学平衡常数的概念
在一定温度下,当一个可逆反应达到平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,
该常数就是该反应的化学平衡常数(简称平衡常数),用符号K表示。
2.表达式
对于可逆反应mA(g) + nB(g) pC(g) + qD(g),化学平衡常数K= 。
杨sir化学,侵权必究
注意
(1)在任意时刻,生成物浓度幂之积与反应物浓度幂之积的比值,都为浓度商,而化学平衡常数,则
是在一定温度下,可逆反应达到平衡时的浓度商。当反应中有关物质的浓度商等于平衡常数时,表明
该反应已达到化学平衡状态。
(2)固体或液体纯物质一般不列入浓度商和平衡常数。
(3)关于HO的浓度问题:当HO为液态时,其浓度为固定常数,不能代入平衡常数表达式;当
2 2
HO的是气态时,则需要代入平衡常数表达式。
2 杨sir化学,侵权必究
及时小练写出下列反应的化学平衡常数:
(1)2SO (g) + O(g) 2SO (g) K = _________________________
2 2 3
(2)4NH (g) + 5O(g) 4NO(g) + 6HO(g) K = _________________________
3 2 2
(3)H(g) + I(g) 2HI(g) K = _________________________
2 2
(4)C(s) + HO(g) CO(g) + H(g) K = _________________________
2 2
三、平衡常数的影响因素及意义
1.化学平衡常数的影响因素
杨sir化学,侵权必究
化学平衡常数是表明化学反应限度的一个特征值,通常情况下只受________影响。
2.化学平衡常数的意义
(1)通常,K越大,说明平衡体系中________所占的比例越大,______反应进行的程度越大,即该反应进
行得越完全,平衡时反应物的转化率越大;反之,K越小,该反应进行得越不完全,平衡时反应物的转化
率越小。
(2)一般来说,当K>______时,该反应就进行得基本完全了。
3.化学平衡常数的应用
杨sir化学,侵权必究
判断正在进行的可逆反应进行的方向
(1)Q < K:反应向正反应方向进行,v > v ;
正 逆
(2)Q = K:反应处于化学平衡状态,v = v ;
正 逆
(3)Q > K:反应向逆反应方向进行,v < v 。
正 逆
思考与交流
分别写出下列方程式的平衡常数表达式,并思考,K 、K 、K 之间有何关系?
1 2 3 杨sir化学,侵权必究
H(g) + I(g) 2HI(g) K = _________
2 2 1
2HI(g) H(g) + I(g) K = _________
2 2 2
2H(g) + 2I(g) 4HI(g) K = _________
2 2 3
四、平衡常数与方程式的关系
1.对于同一可逆反应,正反应和逆反应的平衡常数互为倒数;
2.若化学方程式中各物质的化学计量数都扩大或缩小至原来的n倍,则化学平衡常数变为原来的n次幂或次幂。
3.若干方程式相加,则总反应的平衡常数等于分步平衡常数之乘积;若干方程式相减,则总反应的平衡
常数等于分步平衡常数之商。
杨sir化学,侵权必究
举个例子
已知方程式A(g) C(g) K 和 B(g) D(g) K 用K 、K 表示下列反应的平衡常数。
1 2 1 2
(1)C(g) A(g) K = __________
3
(2)2B(g) 2D(g) K = __________
4
1 1
(3)A(g) + B(g) C(g) + D(g) K = __________
2 2 5
(4)2A(g) + D(g) B(g) + 2C(g) K = __________
6
对点训练
小杨老师 15521324728 侵权必究
题型一:平衡常数的概念、表达式与影响因素
杨sir化学,侵权必究
【变1-2】对于可逆反应:2SO (g)+O(g) 2SO (g),在一定温度下其平衡常数为K,下列条件的变化中,能
2 2 3
使K发生变化的是
⇌
A.缩小容器体积 B.降低体系温度
C.保持体积不变,充入O D.使用合适的催化剂
2
【例2】对于3Fe(s)+4H O(g) Fe O(s)+4H(g),反应的化学平衡常数的表达式为( )
2 3 4 2
c(Fe O )⋅c(H ) c(Fe O )⋅c4 (H )
3 4 2 ⇌ 3 4 2
c(Fe)⋅c(H O) c(Fe)⋅c4 (H O)
A.K= 2 B.K= 2
杨sir化学,侵权必究
c4 (H O) c4 (H )
2 2
c4 (H ) c4 (H O)
C. K= 2 D.K= 2
题型二:平衡常数与方程式的关系
杨sir化学,侵权必究
【变3-1】已知下列反应的平衡常数:①S(s)+O(g) SO (g),K ;②H(g)+S(s) HS(g),K ;
2 2 1 2 2 2则反应H(g)+SO (g) O(g)+HS(g)的平衡常数是
2 2 2 2
A.K -K B.K -K C.K /K D.K /K
1 2 2 1 2 1 1 2
【变3-3】化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数
数值如下:
2NO(g) N(g)+O(g) K=1×1030
2 2 1
2H(g)+O(g) 2HO(g) K=2×1081
2 2 2 2
2CO(g) 2CO(g)+O(g) K=4×10-92
2 2 3
以下说法正确的是( )
c(N )⋅c(O )
2 2
c(NO)
A.常温下,NO分解产生O 的反应的平衡常数表达式为K=
2 1
B.常温下,NO、HO、CO 三种化合物分解放出O 的进行程度由大到小的顺序为NO>H O>CO
2 2 2 2 2
C.常温下,水分解产生O,此时平衡常数的数值约为5×10-80
2
D.以上说法都不正确
题型三:平衡常数与“三段式”的计算
杨sir化学,侵权必究
【变4-1】在800℃时,体积为1升的密闭容器中,下列可逆反应达到化学平衡状态:CO(g)+HO(g)CO (g)
2 2
+H (g),已知CO和HO(g)的初始浓度为0.01mol·L-1时,H 平衡浓度为0.005mol·L-1.若此时再加入
2 2 2
0.02mol·L-1的HO(g),重新达到平衡时,H 平衡浓度为
2 2
A.0.025 mol·L-1 B.0.0075 mol·L-1 C.0.005 mol·L-1 D.0.015 mol·L-1
【变4-3】已知可逆反应CO(g)+HO(g) CO(g) + H(g),K为平衡常数,只与温度有关,与浓度无关。
2 2 2
(1)830K时,若起始浓度:CO为1mol• L-1,HO为1.5mol• L-1,平衡时CO转化率为60%,则HO的转化
2 2
率为:_________;K值为:_________
(2)830K时,若起始浓度改为:CO为1mol• L-1,HO为3mol• L-1,平衡时HO的转化率为:
2 2
_____________;
题型四:化学反应速率与化学平衡综合
杨sir化学,侵权必究
【例5】 时,将 气体放入 密闭容器中,发生反应N O (g)⇌2NO (g),实验数据如
2 4 2
图。已知 与 的消耗速率与各自的分压有如下关系: ,
。下列说法错误的是A.混合气体的密度始终保持不变
B.a点v(正)>v(逆)
C.前
杨sir化学,侵权必究
D.该温度下反应的平衡常数K 与k、k 间的关系为K·k=k
p 1 2 p 2 1
【例7】(I)已知在448℃时,反应H(g)+I (g) 2HI(g)的平衡常数K 为49,则该温度下反应2HI(g)
2 2 1
H(g)+I (g)的平衡常数K 为 ;反应1/2H (g)+1/2I (g) HI(g)的平衡常数K 为
2 2 2 2 2 3
(Ⅱ)在一定体积的密闭容器中进行如下化学反应:CO(g)+H(g) CO(g)+HO(g),其化学平衡常数(K)和
2 2 2
温度(t)的关系如下表所示:
t/℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K
(2)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变
杨sir化学,侵权必究
B.混合气体中c(CO)不变
C.v (H )=v (H O)
正 2 逆 2
D. c(CO )=c(CO)
2
(3)某温度下,平衡浓度符合下式:c(CO)·c(H)=c(CO)·c(HO),试判断此时的温度为 ℃
2 2 2
(4)在 800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为 c(CO)为 2mol·L-1,c(H )为
2 2
1.5mol·L-1,c(CO)为1mol·L-1,c(H O)为3mol·L-1,此时反应 达到平衡(填“是”或“否”)。
2
提分特训
小杨老师 15521324728 侵权必究
【题1】对于可逆反应:2SO (g)+O(g) 2SO (g),在一定温度下其平衡常数为K,下列条件的变化中,能
2 2 3
使K发生变化的是
⇌
A.缩小容器体积 B.降低体系温度
C.保持体积不变,充入O D.使用合适的催化剂
2
【题2】据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应的化学方程式为2CO(g)+6H(g) CHCHOH(g)+3H O(g)。下列叙述正确的是( )
2 2 3 2 2
A.相同条件下,2 mol氢原子所具有的能量等于1 mol氢分子所具有的能量
B.当v(CO)=2v(CHCHOH)时,反应一定达到平衡状态
2 3 2
C.当平衡向正反应方向移动时,平衡常数一定增大
杨sir化学,侵权必究
D.增大压强,可提高CO 和H 的转化率
2 2
【题3】加热NO 依次发生的分解反应为①NO NO+O,②NO NO+O;在2 L密闭容器
2 5 2 5 2 3 2 2 3 2 2
中充入8 mol N O ,加热到t ℃,达到平衡状态后O 为9 mol,NO 为3.4 mol,则t ℃时反应①的平衡常
2 5 2 2 3
数为( )
A.10.7 B.8.5
C.9.6 D.10.2
【题4】某温度下,反应SO (g)+1/2O (g) SO (g)的平衡常数K=50,在同一温度下,反应SO (g)
2 2 3 1 3
SO (g)+O(g)的平衡常数K 的值为( )
2 2 2
A.2500 B.100 C.0.02 D.0.001
【题6】高炉炼铁中发生的基本反应之一如下:
FeO(固)+CO(气)⇌Fe(固)+CO
2
(气)ΔH>0
(1)则该反应中平衡常数表达式K=_________________
(2)已知1100℃时K=0.263。温度升高,化学平衡移动后达到新的平衡,高炉内CO 和CO的体积比值
2
_______平衡常数K值___(均填增大,减小或不变).
(3)1100℃时测得高炉中c(CO)=0.025mol·L-1,c(CO)=0.1mol·L-1,在这种情况下,该反应是否处于平
2
衡状态________(选填是或否),此时化学反应速率v ____v (选填>,<,=)。
正 逆
【题7】I.已知在448℃时,反应H(g)+I(g) 2HI(g)的平衡常数K 为49,则该温度下反应2HI(g)
2 2 1
H(g)+I(g)的平衡常数K 为____________;反应1/2H (g)+ I(g) HI(g)的平衡常数K 为
2 2 2 2 2 3
____________。
II.在一定体积的密闭容器中进行如下化学反应:CO(g)+H(g) CO(g)+HO(g),其化学平衡常数(K)和
2 2 2
温度(t)的关系如下表所示:
t/℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的逆反应为____________(填“吸热”或“放热”)反应。(2)能判断该反应达到化学平衡状态的依据是____________。
A.混合气体中c(CO)不变
杨sir化学,侵权必究
B.c(CO)=c(CO)
2
C.v (H )=v (H O)
正 2 逆 2
D.容器中压强不变
(3)某温度下,平衡浓度符合下式:c(CO)•c(H )=c(CO)•c(H O),试判断此时的温度为____________℃,
2 2 2
在此温度下,加入2mol的CO和3mol的H,达到平衡时,CO的转化率为____________。
2
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO)为2mol•L-1,c(H)为
2 2
1.5mol•L-1,c(CO)为1mol•L-1,c(HO)为3mol•L-1,则下一时刻,反应将____________(填“正向”或“逆
2
向”)进行。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列关于平衡常数K的说法正确的是( )
A.加入催化剂可能会改变平衡常数K
B.改变反应物浓度能改变平衡常数K
C.平衡常数K与反应本身及温度有关
D.K越大,反应物的转化率越小
【练2】某温度时,N+3H 2NH 的平衡常数K=a,则此温度下,NH 1/2 N +3/2H 的平衡常数为
2 2 3 3 2 2
A.a-(1/2) B.a C.(1/2)a D.a-2
【练3】已知下列反应的平衡常数:
1 1
① SO (g) + O(g) SO (g) K ;②NO(g) + O(g) NO (g) K 。
2 2 3 1 2 2 2
2 2
则反应SO (g) + NO (g) SO (g) + NO(g)的平衡常数为( )
2 2 3 杨sir化学,侵权必究
K
A.K + K B.K ﹣K C. 1 D.K × K
1 2 2 1 K 1 2
2
【练4】在一定条件下,有下列分子数相同的可逆反应,其平衡常数K值分别是
①H + F 2HF K=1047
2 2
②H + Cl 2HCl K=1017
2 2
③H + Br 2HBr K=109
2 2
④H + I 2HI K=1
2 2
比较K值大小,可知各反应的正反应进行的程度由大到小的顺序是( )
A.①②③④ B.④②③① C.①④③② D.无法确定【练5】合成氨反应N(g)+3H(g) 2NH (g)在某温度下达到平衡时,各物质的浓度是c(N)=3mol/L ,
2 2 3 2
c(H)=9mol/L,c(NH )=4mol/L,则
2 3
(1)该温度时的平衡常数为 ;起始浓度c(N)=
2
(2)H 的转化率为 。
2
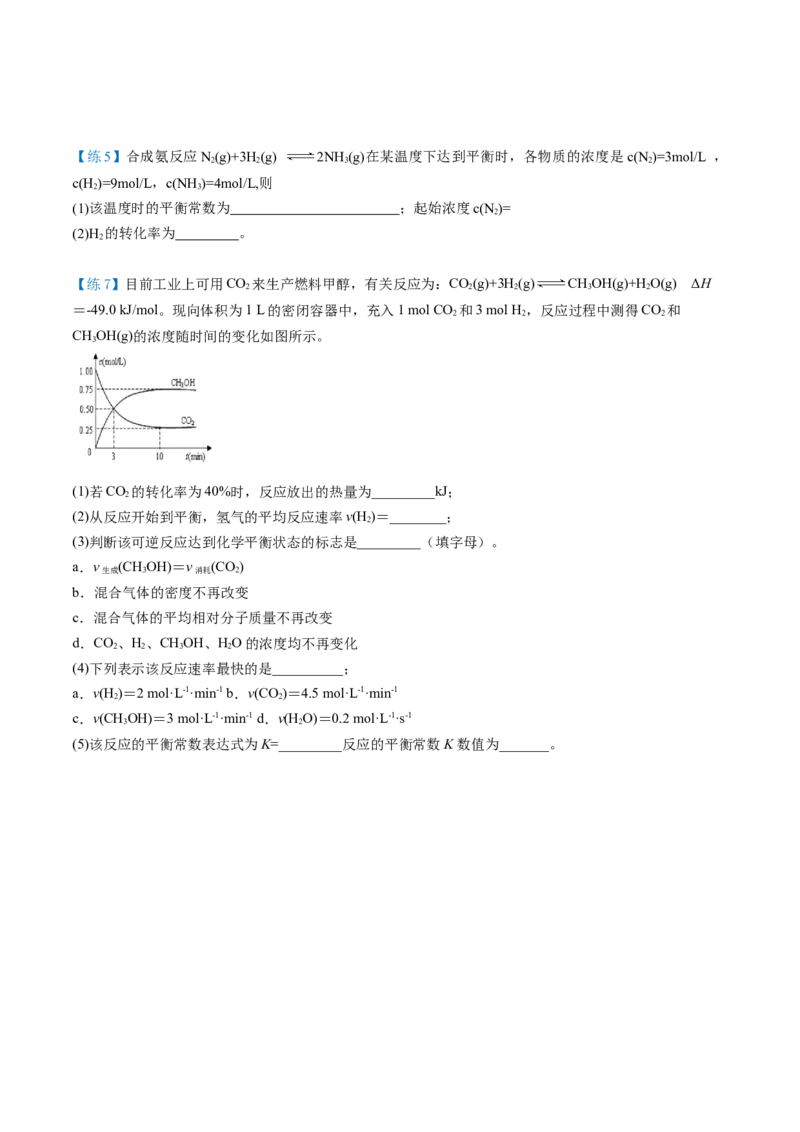
【练7】目前工业上可用CO 来生产燃料甲醇,有关反应为:CO(g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 2 3 2
=-49.0 kJ/mol。现向体积为1 L的密闭容器中,充入1 mol CO 和3 mol H ,反应过程中测得CO 和
2 2 2
CHOH(g)的浓度随时间的变化如图所示。
3
(1)若CO 的转化率为40%时,反应放出的热量为_________kJ;
2
(2)从反应开始到平衡,氢气的平均反应速率v(H )=________;
2
(3)判断该可逆反应达到化学平衡状态的标志是_________(填字母)。
杨sir化学,侵权必究
a.v (CHOH)=v (CO)
生成 3 消耗 2
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.CO、H、CHOH、HO的浓度均不再变化
2 2 3 2
(4)下列表示该反应速率最快的是__________;
a.v(H )=2 mol·L-1·min-1 b.v(CO)=4.5 mol·L-1·min-1
2 2
c.v(CHOH)=3 mol·L-1·min-1 d.v(H O)=0.2 mol·L-1·s-1
3 2
(5)该反应的平衡常数表达式为K=_________反应的平衡常数K 数值为_______。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育