文档内容
第 09 讲 氢键 溶解性 分子的手性
考点导航
知识精讲
知识点一:一、氢键及其对物质性质的影响
1.氢键的概念及表示方法
(1)概念:氢键是由已经与电负性很大的原子形成共价键的 (如水分子中的氢)与另一个电负性很大的
原子(如水分子中的氧)之间的作用力。
(2)表示方法:
氢键的通式可用X—H…Y—表示。式中X和Y为 ,“—”表示,“…”表示形成的 。
微点拨
一般来说,能形成氢键的元素有N、O、F。所以氢键一般存在于含N—H、H—O、H—F的物质中,
或有机化合物中的醇类和羧酸类等物质中。
2.氢键的特征
(1) 氢键不是化学键,而是特殊的分子间作用力,其键能比化学键 ,比范德华力 。
(2)氢键具有一定的方向性和饱和性
X—H与Y形成分子间氢键时,氢原子只能与一个Y原子形成氢键,3个原子总是尽可能沿直线分布,这
样可使X与Y尽量远离,使两原子间电子云的排斥作用力最小,体系能量最低,形成的氢键最强、最稳定
(如下图)。
3.氢键的类型(1) 氢键,如水中O—H…O—。
(2) 氢键,如 。
4.氢键对物质性质的影响
(1)当形成 氢键时,物质的熔、沸点将 。
(2)当形成 氢键时,物质的熔、沸点将 。
(3)氢键也影响物质的电离、 等过程。
【即学即练1】
1.关于氢键,下列说法中正确的是
A.氢键比范德华力强,所以它属于化学键
B.分子间形成的氢键使物质的熔点和沸点升高
C.含氢原子的物质之间均可形成氢键
D.H O是一种非常稳定的化合物,这是由于水分子间存在氢键
2
2.下列现象与氢键有关的是
①HF的熔、沸点比HCl的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④HF、NH 都极易溶于水
3
⑤水分子高温下也很稳定
A.①②③④⑤ B.②③④⑤ C.①②③⑤ D.①②③④
3.下图为冰层表面的分子结构示意图。下列说法错误的是
A.温度升高时,“准液体”中水分子与下层冰连接的氢键断裂,使冰面变滑
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成的氢键比固态冰中少
D.由于氢键的存在,水分子的稳定性好,高温下也很难分解知识点二: 二、溶解性
1.相似相溶规律
非极性溶质一般能溶于 溶剂,极性溶质一般能溶于 溶剂。如蔗糖和氨易溶于水,难溶于四氯
化碳;而萘和碘却易溶于四氯化碳,难溶于水。
2.影响物质溶解性的因素
(1)外界因素:主要有 、 等。
(2)氢键:溶剂和溶质之间的氢键作用力越大,溶解性越好。
(3)分子结构的相似性:溶质和溶剂的分子结构相似程度越大,其溶解性越 。如乙醇与水 ,而戊
醇在水中的溶解度明显减小。
(4)溶质是否与水反应:溶质与水发生反应,溶质的溶解度会 。如SO 与水反应生成的HSO 可溶于
2 2 3
水,故SO 的溶解度 。
2
【即学即练2】
1.下列现象不能用“相似相溶”规律解释的是
A.甲烷不溶于水 B.氯化氢易溶于水
C.单质碘易溶于苯 D.氯气易溶于NaOH溶液
2.根据“相似相溶”规则和实际经验,下列叙述不正确的是
A.白磷(P )易溶于CS ,也易溶于水 B.NaCl易溶于水,难溶于CCl
4 2 4
C.碘易溶于苯,微溶于水 D.卤化氢易溶于水,难溶于CCl
4
3.下列对分子的结构或性质的解释中,不正确的是
A.水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致
B.在同一能级上运动的两个电子,其运动状态肯定也不相同
C.碘单质易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”规律解释
D.由图知酸性: ,因为 中非羟基氧原子数大于次氯酸中非羟基氧原子数
知识点三:三、分子的手性
1.手性异构体
具有完全相同的 和 的一对分子,如同左手与右手一样互为 ,却在三维空间里不能
,互称手性异构体(或对映异构体)。
2.手性分子有 的分子叫做手性分子。
如乳酸( )分子。
【即学即练3】
1.下列说法中正确的是
A.互为手性异构体的分子互为镜像,且分子组成相同,性质也相同
B.由酸性 FCH COOH>CH COOH,可知酸性 ClCH COOH>CH COOH
2 3 2 3
C.由 AgCl 和 AgBr 都能溶于氨水中,而 AgI 不能溶解在氨水中,可知 AgI 在水中的溶解度最大
D.除 HF 外,其他卤化氢沸点随着相对分子质量的增大而升高,是因为氢键的键能逐渐增大所致
2.下列关于化合物 的叙述正确的是
A.该分子是手性分子 B.分子中既有极性键又有非极性键
C.1分子中有7个 键和3个 键 D.该分子在水中的溶解度小于2-丁烯
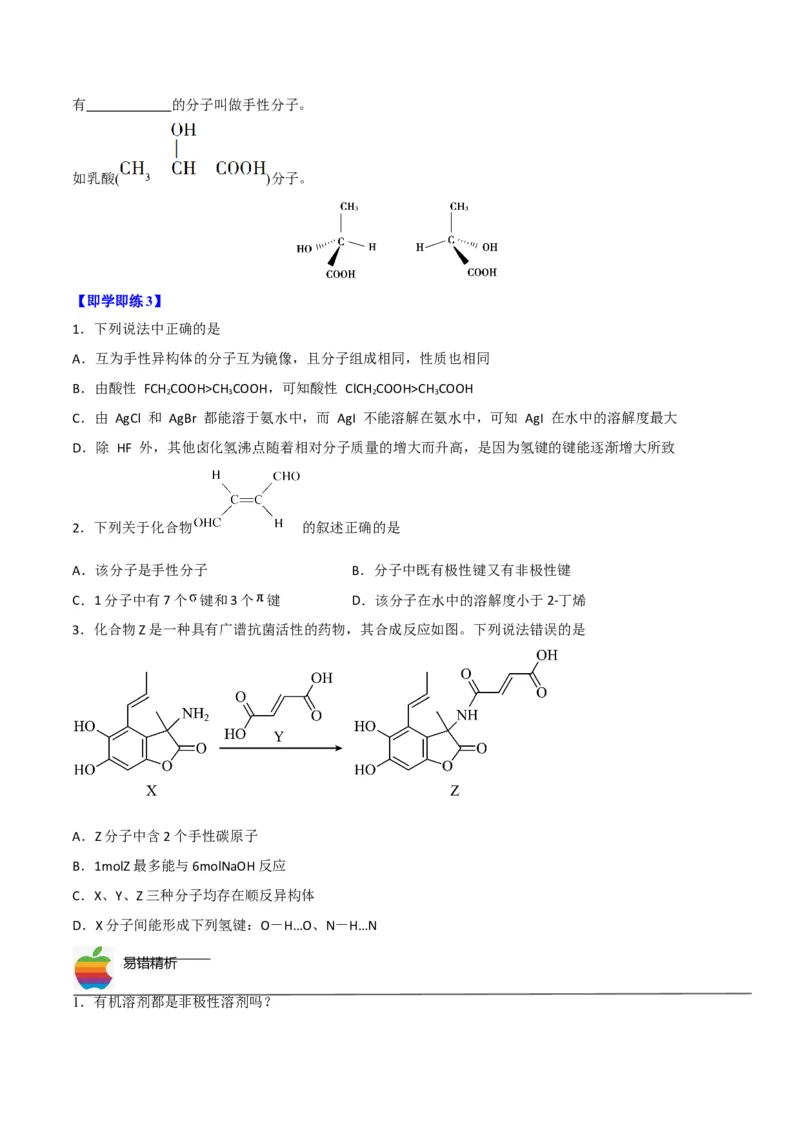
3.化合物Z是一种具有广谱抗菌活性的药物,其合成反应如图。下列说法错误的是
A.Z分子中含2个手性碳原子
B.1molZ最多能与6molNaOH反应
C.X、Y、Z三种分子均存在顺反异构体
D.X分子间能形成下列氢键:O-H…O、N-H…N
易错精析
1.有机溶剂都是非极性溶剂吗?【细剖精析】
2.具有手性,其与H 发生加成反应后,其产物还有手性吗?
2
【细剖精析】
3.通电情况下水的分解过程中化学键有哪些变化?
【细剖精析】
4.冰融化成水的过程中是否存在化学键的变化?是否存在能量的变化?分子间作用力是否有变化?
【细剖精析】
5.常温下CCl 是液体,CF 是气体,CI 是固体,为什么?
4 4 4
【细剖精析】
6.互为手性分子的物质是同一种物质吗? 二者具有什么关系?
【细剖精析】
7.互为手性分子的物质化学性质几乎完全相同,分析其原因。
【细剖精析】
8.为什么NH 极易溶于水,而CH 难溶于水?
3 4
【细剖精析】
能力拓展
1.范德华力、氢键、化学键的比较
范德华力 氢键 共价键
已经与电负性很强的原子形成共价
物质分子之间普遍存在 原子间通过共用电子对
概念 键的氢原子与另一个电负性很强的
的一种作用力 所形成的相互作用
原子之间的静电作用
作用
分子 H与N、O、F 原子
粒子
有方向性
特征 无方向性和饱和性 有方向性和饱和性
和饱和性
强度 共价键>氢键>范德华力
①随分子极性的增大而
影响 增大 成键原子半径和共用电
强度 ②组成和结构相似的分 对于X—H…Y,X、Y的电负性越 子对数目。键长越短,
的因 子构成的物质,相对分 大,Y原子的半径越小,作用越强 键能越大,共价键越稳
素 子质量越大,范德华力 定
越大
①影响物质的熔点、沸
对物 ①分子间氢键的存在,使物质的
点、溶解度等物理性质 共价键键能越大,分子
质性 熔、沸点升高,在水中的溶解度增
②组成和结构相似的物 稳定性越强
质的 大。如熔、沸点:HO>HS
2 2
质,随相对分子质量的增大,物质的熔、沸点
②分子内存在氢键时,降低物质的
影响 升高。如熔、沸点:
熔、沸点
CFPH ;同分
3 3
异构体分子间形成氢键的物质比分子内形成氢键的物质熔、沸点高,如邻羟基苯甲酸<对羟基苯甲酸。
(2)氢键对物质溶解度的影响:溶剂和溶质之间形成氢键使溶质的溶解度增大,如NH 、甲醇、甲酸等易溶
3
于水。
(3)氢键对物质密度的影响:氢键的存在会使某些物质的密度反常,如水的密度比冰的密度大。
(4)氢键对物质电离性质的影响:如邻苯二甲酸的电离平衡常数K 与对苯二甲酸的电离平衡常数K 相差较
a1 a1
大。
3.手性分子的判断
有机物分子具有手性是由于其分子中含有手性碳原子。如果1个碳原子所连接的4个原子或基团各不相同,
那么该碳原子为手性碳原子,用*C来表示。如 ,R 、R 、R 、R 是互不相同的原子或基团。
1 2 3 4
所以,判断一种有机物是否为手性分子,就看其含有的碳原子是否连有4个不同的原子或基团。
4.手性合成
生产手性药物必须把手性异构体分离开,因为对于手性药物,一个手性异构体往往能治病、没有毒副作用,
而另一个可能是无效甚至是有害的。按照获得2001年诺贝尔化学奖的三位科学家的合成方法,可以只得到
或者主要得到一种手性分子,这种独特的合成方法称为手性合成。手性催化剂只催化或者主要催化一种手
性分子的合成。手性分子在生命科学和药物生产方面有广泛的应用。手性合成是当代化学的热点之一,是
21世纪化学研究的重要领域。
分层提分
题组A 基础过关练
1.下列各组物质能形成分子间氢键的是
A. 和 B. 和
C. 和 D. 和HI
2.下列关于氢键X-H…Y的说法中,错误的是
A.X、Y元素具有强电负性,是氢键形成的基本条件B.氢键是共价键的一种
C.某些物质因分子之间存在氢键,导致沸点反常升高
D.同一分子内也可能形成氢键
3.氢键对物质的溶解度影响很大,下列物质在水中的溶解度跟氢键无关的是
A.Cl B.CH CH OH
2 3 2
C.HF D.HNO
3
4.下列“类比”结果正确的是
A.H S晶体中一个H S分子周围有12个H S紧邻,则冰中一个水分子周围也有12个紧邻分子
2 2 2
B.AlCl 中Al原子是sp2杂化,则Al Cl 中Al原子也是sp2杂化
3 2 6
C.Mg在过量氧气中燃烧生成MgO,则锂在过量氧气燃烧也生成Li O
2
D.乙醇CH CH OH能与水互溶,则戊醇CH CH CH CH CH OH也能与水互溶
3 2 3 2 2 2 2
5.下列各气体在水中溶解度最大的是
A.H B.HCl C.CO D.Cl
2 2 2
6.下列关于分子的结构和性质的描述中,不正确的是
A.水很稳定(1 000 ℃以上才会部分分解)是水中含有大量氢键所致
B.乳酸( )分子中含有一个手性碳原子
C.碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”原理解释
D.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
7.下列叙述正确的是
A.H O的沸点比H S的高与氢键无关
2 2
B. 中价电子对互斥理论模型名称与离子的立体构型名称不一致
C.由于乳酸( )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
D.冰和固体碘晶体中相互作用力类型相同
8.二甘醇的结构简式是 。下列有关二甘醇的叙述正确的是
A.二甘醇分子中有一个手性碳原子 B.分子间能形成氢键
C.分子间不存在范德华力 D.能溶于水,不溶于乙醇9.下列对分子的性质的解释中,正确的是
A. 在水中的溶解度很小,是由于 属于极性分子
B.乳酸( )分子中含有一个手性碳原子,该碳原子是 杂化
C.碘易溶于四氯化碳, 难溶于水都可用“相似相溶”原理解释
D.甲烷可以形成甲烷水合物,是因为甲烷分子与水分子之间形成了氢键
题组B 能力提升练
1.下列有关氢键的说法正确的是
A.H O比H S稳定是因为水分子间能形成氢键
2 2
B.形成氢键的(X-H···Y)三原子一定在一条直线上
C.氢键能增大很多物质分子之间的作用力,导致沸点升高
D.可燃冰( )中甲烷分子和水分子之间形成了氢键
2.如图分别表示冰晶体、干冰晶体的结构,下列关于这两种晶体的说法不正确的是
A.冰晶体中只存在范德华力和氢键两种作用力
B.沸点:冰>干冰
C.冰晶体中的一个水分子和周围四个水分子形成4个氢键
D.干冰晶体中每个 周围距离相等且最近的 有12个
3.下列物质中,分子内和分子间均可形成氢键的是A.NH B.
3
C.H O D.C H OH
2 2 5
4.胆矾的化学式为CuSO ·5H O,可改写成[Cu(H O) ]SO ·H O,其结构示意图如下:
4 2 2 4 4 2
下列有关胆矾的说法正确的是
A.氧原子参与形成配位键和氢键两种化学键
B.胆矾可用于实验过程中检验水蒸气
C.胆矾中的水分子均与中心Cu2+之间存在配位键
D.胆矾中的水分子在不同温度下会分步失去
5.下列说法正确的是
A.手性分子具有完全相同的组成和原子排列,化学性质完全相同
B.无机含氧酸分子中所含氧原子个数越多,酸性越强
C.氯气易溶于氢氧化钠溶液符合相似相溶原理
D.蛋白质分子间可形成氢键,分子内也存在氢键
6.下列说法中正确的是
A.互为手性异构体的分子互为镜像,且分子组成相同,性质也相同
B.由酸性 ,可知酸性
C. 易溶于 溶液中可以用相似相溶来解释
D.除 外,其它卤化氢的沸点随着相对分子质量的增大而升高,是因为氢键的作用逐渐增强所致
7.下列有关说法不正确的是
A.水分子间存在氢键,故水很稳定,1000°C以 上才会部分分解
B.乳酸( )分子中含有一个手性碳原子C.碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”原理解释
D.MgO的熔点比MgCl 高主要是因为MgO的晶格能比MgCl 大
2 2
8.下列说法正确的是
A.H O很稳定,是因为水分子之间存在氢键
2
B.液态氟化氢中氟化氢分子之间形成氢键,可写为(HF) , 则NO 分子间也是因氢键而聚合形成N O
n 2 2 4
C.HCl极易溶于水,原因是HCl分子与水分子之间形成了氢键
D.NH 的沸点比PH 的高,是因为NH 分子之间形成了氢键
3 3 3
9.下列现象不能用“相似相溶”规律解释的是
A.氯化氢易溶于水 B.碘易溶于 C.酒精易溶于水 D.氯气易溶于NaOH溶液
10.下列叙述中错误的是
A.CS 的熔沸点比CO 高,与分子间的范德华力有关系
2 2
B.热稳定性:NH >PH ,与氨气分子之间存在氢键有关系
3 3
C. 分子中σ键与π键个数比为4∶1
D.I 易溶于CS ,可用相似相溶规律解释
2 2倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育