文档内容
第 10 讲 影响化学平衡的因素
知识导航
小杨老师 15521324728 侵权必究
课前引入
化学平衡的特征:
逆 化学平衡状态的研究对象是可逆反应
等
v =v ≠ 0,是一个动态平衡
正 逆
动
定 各组分浓度/物质的量/百分含量保持不变
变 外界条件改变时,原平衡状态被破坏,在新条件下建立平衡
在一定条件下,当一个可逆反应达到化学平衡状态后,如果改变浓度、压强、温度等条件,化学
平衡状态是否会发生变化?如何变化?
杨sir化学,侵权必究知识精讲
小杨老师 15521324728 侵权必究
一、化学平衡的移动
1.定义:在一定条件下,当可逆反应达到平衡状态后,如果改变反应条件,平衡状态被破坏,平衡体系的
物质组成也会随着改变,直到达到新的平衡状态。这种由原有的平衡状态达到新的平衡状态的过程叫做化
学平衡的移动。
2.化学平衡移动的方向:
(1)v >v ,化学平衡向正反应方向移动;
正 逆
(2)v <v ,化学平衡向逆反应方向移动;
正 逆
(3)v =v ,化学平衡不发生移动。
正 逆
杨sir化学,侵权必究
二、浓度对化学平衡的影响
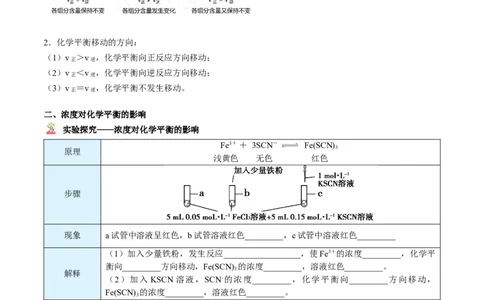
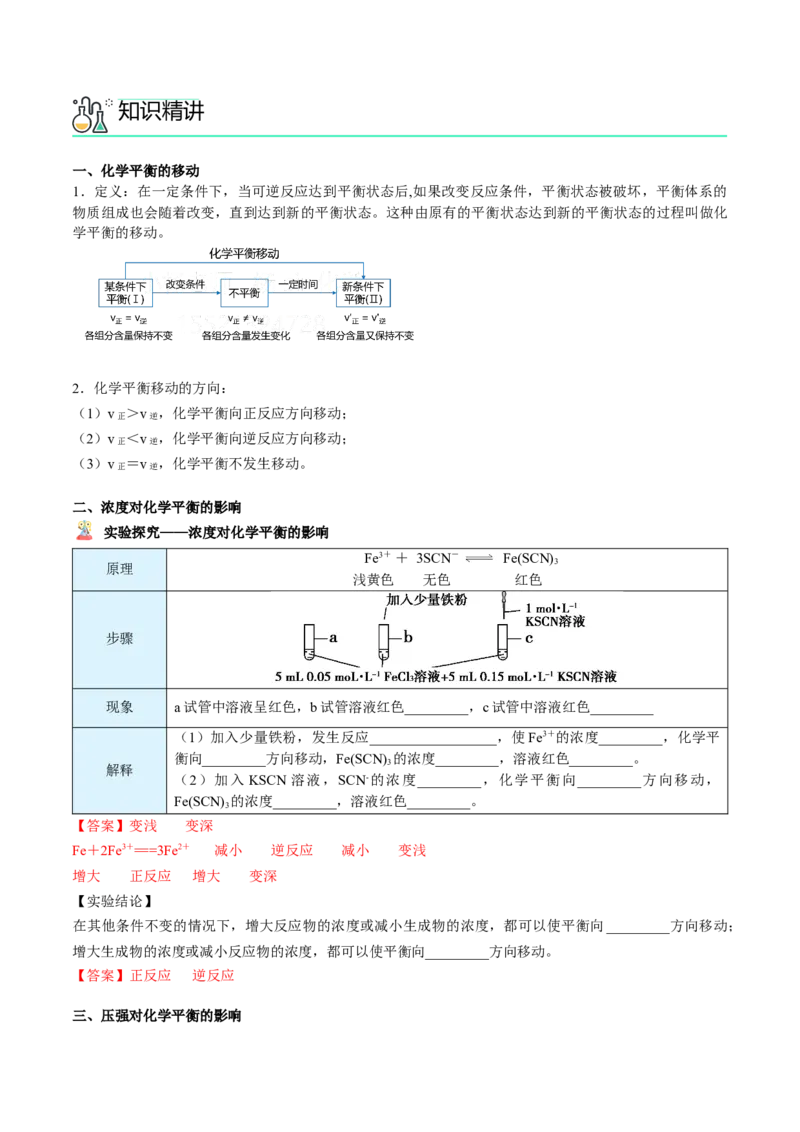
实验探究——浓度对化学平衡的影响
Fe3+ + 3SCN- Fe(SCN)
原理 3
浅黄色 无色 红色
步骤
现象 a试管中溶液呈红色,b试管溶液红色_________,c试管中溶液红色_________
(1)加入少量铁粉,发生反应__________________,使Fe3+的浓度_________,化学平
衡向_________方向移动,Fe(SCN) 的浓度_________,溶液红色_________。
3
解释
(2)加入 KSCN 溶液,SCN-的浓度_________,化学平衡向_________方向移动,
Fe(SCN) 的浓度_________,溶液红色_________。
3 杨sir化学,侵权必究
【答案】变浅 变深
Fe+2Fe3+===3Fe2+ 减小 逆反应 减小 变浅
增大 正反应 增大 变深
【实验结论】
在其他条件不变的情况下,增大反应物的浓度或减小生成物的浓度,都可以使平衡向_________方向移动;
增大生成物的浓度或减小反应物的浓度,都可以使平衡向_________方向移动。
【答案】正反应 逆反应
三、压强对化学平衡的影响实验探究——压强对化学平衡的影响
2NO (g) NO(g)
2 2 4
原理
(红棕色)
杨sir化学,侵权必究
用50 mL注射器抽入20 mL NO 和NO 混合气体,将细管端用橡胶塞封闭
2 2 4
操作 将针筒活塞从10mL处迅速拉至 40 mL处(压
将针筒活塞迅速推至10 mL处(压强增大)
强减小)
现象 气体颜色_____________________________ 气体颜色_____________________________
压缩体积使压强增大时,c(NO )瞬间________ 增 大 体 积 使 压 强 减 小 时 , c(NO ) 瞬 间
2 2
解释
后又________,平衡向______移动 ________后又________,平衡向______移动
【答案】先变深,后变浅,最终比原来深 先变浅,后变深,最终比原来浅
变大 减小 左
减小 增大 右
【实验结论】
在其他条件不变的情况下,增大压强,平衡向气体物质的量________的方向移动;
减小压强,平衡向气体物质的量________的方向移动。
注意:压强改变只影响有气体参加或生成的可逆反应,对于只涉及固体或液体的反应,压强的影响不予考
虑。
【答案】减小 增大
四、温度对化学平衡的影响
实验探究——温度对化学平衡的影响
2NO (g) NO(g) ΔH=-56.9 kJ·mol-1
原理 2 2 4
红棕色 无色
杨sir化学,侵权必究
步骤
现象 热水中混合气体颜色________;冰水中混合气体颜色________
混合气体受热颜色________,说明NO 浓度________,即平衡向________方向移动;
2
结论
混合气体受冷颜色________,说明NO 浓度________,即平衡向________方向移动。
2
【答案】变深 变浅
变深 增大 逆反应
变浅 减小 正反应
【实验结论】
在其他条件不变的情况下,升高温度,平衡向____________的方向移动;降低温度,平衡向____________的方向移动。
【答案】吸热反应 放热反应
五、催化剂对化学平衡的影响
使用正催化剂,正、逆反应速率同时__________,且增大的倍数__________,化学平衡__________。
【答案】增大 相同 不移动
六、勒夏特列原理
如果改变影响平衡的一个条件(如温度、压强及参加反应的物质的浓度),平衡就向着能够减弱这种改变
的方向移动,该结论就是勒夏特列原理。
杨sir化学,侵权必究
思考与交流:如何理解勒夏特列原理中的“减弱”一词?
【答案】平衡移动的结果是“减弱”外界条件的影响,但不能 “消除”外界条件的影响,即“减弱但不抵
消”。
对点训练
小杨老师 15521324728 侵权必究
题型一:浓度对化学平衡的影响
杨sir化学,侵权必究
【例1】将5mL0.005mol·L-1FeCl 溶液和5mL0.015mol·L-1KSCN溶液混合,达到平衡后混合液呈红色。再
3
将混合液分为5等份,分别进行如下实验:
实验①:滴加4滴水,振荡
实验②:滴加4滴饱和FeCl 溶液,振荡
3
实验③:滴加4滴1mol·L-1KCl溶液,振荡
实验④:滴加4滴1mol·L-1KSCN溶液,振荡
实验⑤:滴加4滴6mol·L-1NaOH溶液,振荡
下列说法不正确的是
A.实验②中溶液颜色比实验①中深
B.对比实验①和③,可证明增加反应物中某些离子的浓度,平衡发生逆向移动
C.对比实验①和④,可证明增加反应物浓度,平衡发生正向移动
D.对比实验①和⑤,可证明减少反应物浓度,平衡发生逆向移动
【答案】B【分析】
将5mL0.005mol·L-1FeCl 溶液和5mL0.015mol·L-1KSCN溶液混合发生Fe3++3SCN- Fe(SCN) (红色)。
3 3
【详解】
A.对比实验①和②,FeCl 浓度增加,平衡发生正向移动,实验②中溶液颜色比实验①中深,故A正确;
3
B.对比实验①和③,KCl实际不参加反应,且溶液总体积变大,浓度减小,不能证明增加反应物浓度,
平衡发生逆向移动,故B错误;
C.对比实验①和④,KSCN浓度变化,则证明增加反应物浓度,平衡发生正向移动,故C正确;
D.对比实验①和⑤,加NaOH可降低铁离子浓度,证明减少反应物浓度,平衡发生逆向移动,故D正确;
故选B。
【变1-3】对于可逆反应:FeCl +3KSCN Fe(SCN) +3KCl的理解不正确的是
3 3
A.增大FeCl 的浓度,平衡向正反应方向移动
3 ⇌
B.增大KSCN的浓度,平衡向正反应方向移动
C.增大Fe(SCN) 的浓度,平衡向逆反应方向移动
3
D.增大KCl的浓度,平衡向逆反应方向移动
杨sir化学,侵权必究
【答案】D
【详解】
该可逆反应的本质为Fe3++3SCN- Fe(SCN) ,K+、Cl-既不是反应物,也不是生成物,增大KCl的浓度,
3
对该离子反应无影响,故平衡不移动。
⇌
故选D。
题型二:压强对化学平衡的影响
杨sir化学,侵权必究
【例2】在下列可逆反应中,增大压强或降低温度,均可使平衡正向移动的是
A.2SO (g)+O(g) 2SO (g) ΔH<0
2 2 3
B.4NH (g)+5O(g) 4NO(g)+6H O(g)ΔH<0
3 2 2
C.2NH (g) N(g)+3H(g) ΔH>0
3 2 2
D.SO (g)+NO (g) SO (g)+NO(g) ΔH<0
2 2 3
【答案】A
【详解】
增大压强或降低温度均可使化学平衡向正反应方向移动,说明正反应为气体体积减小的放热反应;
A.正反应为气体体积减小的放热反应,符合题意,故A正确;
B.正反应为放热反应,但正反应是体积增大的反应,故B错误;
C.正反应为气体体积增大的吸热反应,不符合,故C错误;D.正反应为放热反应,但反应前后气体的体积不变,故D错误;
故选A。
【变2-2】已知反应:2NO (红棕色) NO(无色) ΔH<0,将一定量的NO 充入注射器后封口,如
2 2 4 2
图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确
的是。
①b点的操作为拉伸注射器
②d点v <v
正 逆
③c点与a点相比,c(NO )增大,c(NO) 减小,
2 2 4
④若不忽略体系温度变化,且没有能量损失,则T(b)<T(c)
⑤若容器绝热,则平衡常数K>K
a c
A.①③⑤ B.②③④ C.①③④ D.②④⑤
【答案】D
【详解】
b点时,透光率突然下降,说明c (NO)突然增大,则操作是压缩注射器,①错误;
2
②d点,透光率下降,则c (NO)增大,平衡逆向移动,v(正) < v(逆),②正确;
2
③c点是在a点的基础上压缩注射器,则c(NO )增大,c(NO)增大,C错误;
2 2 4
④由b点到c点,压缩注射器,反应正向进行,放出热量,混合气体的温度升高,则T(b)<T(c),④正确;
⑤若容器绝热,a点到c点,压缩注射器,反应正向进行,T(a)<T(c),该反应正向放热,温度越高平衡常
数越低,故平衡常数K>K,⑤正确;
a c
故选D。
【变3】在一密闭容器中,反应 aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新
的平衡时,A的浓度是原来的60% 则下列说法正确的是
⇌
A.平衡向正反应方向移动了
B.物质A的转化率减少了
C.物质B的物质的量分数增加了
D.aK(T ),D项错误;
1 1 2
综上所述答案为D。
【变4-2】已知化合物A与HO在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,其中
2
TS表示过渡态,I表示中间体。下列说法正确的是A.化合物A与HO之间的碰撞均为有效碰撞
2 杨sir化学,侵权必究
B.该历程中的最大能垒(活化能)E =16.87 kJ·mol-1
正
C.使用更高效的催化剂可降低反应所需的活化能和反应热
D.平衡状态时,升温使反应逆向移动
【答案】D
【详解】
A.由图可知,化合物A与HO的反应历程经历了3个阶段,说明该反应的反应速率不快,化合物A与
2
HO之间的碰撞并没有都发生反应,即化合物A与HO之间的碰撞不均为有效碰撞,A错误;
2 2
B.该历程中的最大能垒(活化能) E =16.87 kJ/mo1-(-1.99kJ/mo1)=18.86 kJ/mo1,B错误;
正
C.催化剂可降低反应所需的活化能,改变反应速率,但不能改变反应的始态和终态,不能改变反应始态
△
和终态的总能量,即不能改变反应热,C错误;
D.由图可知:反应物具有的能量大于生成物具有的能量,则该反应是放热反应。升高温度,化学平衡向
吸热的逆反应方向移动,D正确;
故合理选项是D。
题型四:勒夏特列原理
杨sir化学,侵权必究
【变5-1】反应NH HS(s) NH (g)+HS(g)在某温度下达到平衡,下列各种情況下,不会使平衡发生移
4 3 2
动的是
A.温度、容积不变时,通入SO 气体
2
B.将NH HS固体全部移走
4
C.保持温度和容器体积不变,充入氮气
D.保持温度和压强不变,充入氮气
【答案】C
【详解】
A.通入SO 气体与HS(g)反应生成S,生成物浓度减小,平衡正向移动,故A不选;
2 2
B.将NH HS固体全部移走,可看成起始加入生成物,平衡逆向移动,故B不选;
4
C.保持温度和容器体积不变,充入氮气,反应体系中各物质的浓度不变,平衡不移动,故C选;D.保持温度和压强不变,充入氮气,体积增大,相等于减小压强,平衡正向移动,故D不选;
故选:C。
【变5-3】下列事实中,不能用勒夏特列原理解释的有几项
①Fe(SCN) 溶液中加入固体KSCN后颜色变深
3
②将混合气体中的氨液化有利于合成氨反应
③实验室常用排饱和食盐水的方法收集氯气
④红棕色NO 气体加压后颜色先变深后变浅
2
⑤加入催化剂有利于合成氨的反应
⑥由H(g)、I(g)和HI(g)组成的平衡体系加压后颜色变深
2 2
⑦500 ℃时比室温更有利于合成氨的反应
杨sir化学,侵权必究
A.三项 B.四项 C.五项 D.六项
【答案】A
【分析】
勒沙特列原理的内容为︰如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种
改变的方向移动.勒沙特列原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用勒沙特列原理
解释,以此进行判断。
【详解】
①Fe(SCN) 溶液中加入固体KSCN,SCN-的离子浓度增大,平衡向着生成Fe(SCN) 的逆反应方向移动,导
3 3
致溶液颜色变深,能够用勒夏特列原理解释,①不符合题意;
②N 与H 合成氨气的反应是气体体积减小的可逆反应,将混合气体中的氨液化,平衡正向移动,有利于氨
2 2
的合成,能够用勒夏特列原理解释,②不符合题意;
③Cl 在水中存在化学平衡:Cl+H O H++Cl-+HClO,饱和食盐水中c(Cl-)浓度比水中大,增大c(Cl-),
2 2 2
平衡逆向移动,Cl 溶解、反应消耗减少,有利于Cl 的收集,能够用勒夏特列原理解释,③不符合题意;
2 2
④NO 气体在容器中存在化学平衡:2NO NO,平衡体系中增加压强,体积变小,气体浓度增大,
2 2 2 4
颜色变深;由于该反应的正反应是气体体积减小的反应,所以加压后平衡正向移动,使气体浓度又略微减
小,气体颜色变浅,能用勒夏特列原理解释,④不符合题意;
⑤催化剂只能影响化学反应速率,不能使化学平衡发生移动,故不能用勒夏特列原理解释,⑤符合题意;
⑥由H、I(g)、HI气体组成的平衡,反应前后气体体积不变,加压后平衡不动,但由于体积减小使物质浓
2 2
度增大,气体颜色变深,不能用勒夏特列原理解释,⑥符合题意;
⑦合成氨反应为放热反应,升高温度平衡逆向移动,不利用氨的合成,但升温却可提高反应速率,不能用
勒夏特列原理解释,⑦符合题意;
综上所述可知:不能用勒夏特列原理解释的是⑤⑥⑦三项,故合理选项是A。
题型五:勒夏特列原理的图像问题
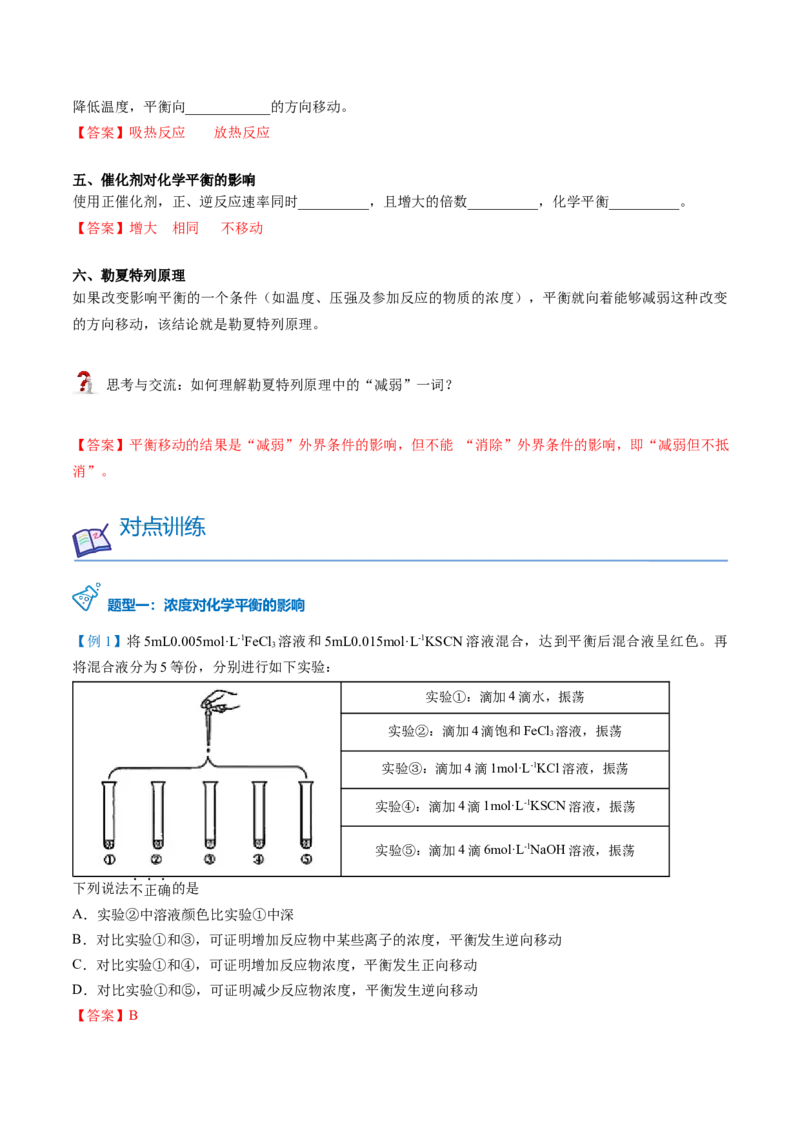
杨sir化学,侵权必究【变6-1】在刚性密闭容器中充入CO 和H 发生反应:CO(g)+3H(g) CHOH(g)+H O(g)
2 2 2 2 3 2
△H,测得反应过程如图所示。下列说法正确的是
A.平衡常数:K>K B.反应温度:T>T
1 2 2 1
C.加催化剂,△H不变 D.平衡后再通入CO,其转化率增大
2
【答案】C
【详解】
A.由图像知,根据先拐先平衡,数字大,T 先达到平衡,温度较高,从T 到T,降低温度,CO 物质的
1 1 2 2
量减小,平衡正向移动,说明正反应是放热反应,即 大于 ,故A错误;
B.根据先拐先平衡,数字大,反应温度:T>T,故B错误;
1 2
C.催化剂改变速率,不改变平衡,反应热不变,故C正确;
D.平衡后,增大 浓度, 的平衡转化率减小, 的平衡转化率增大,故D错误。
综上所述,答案为C。
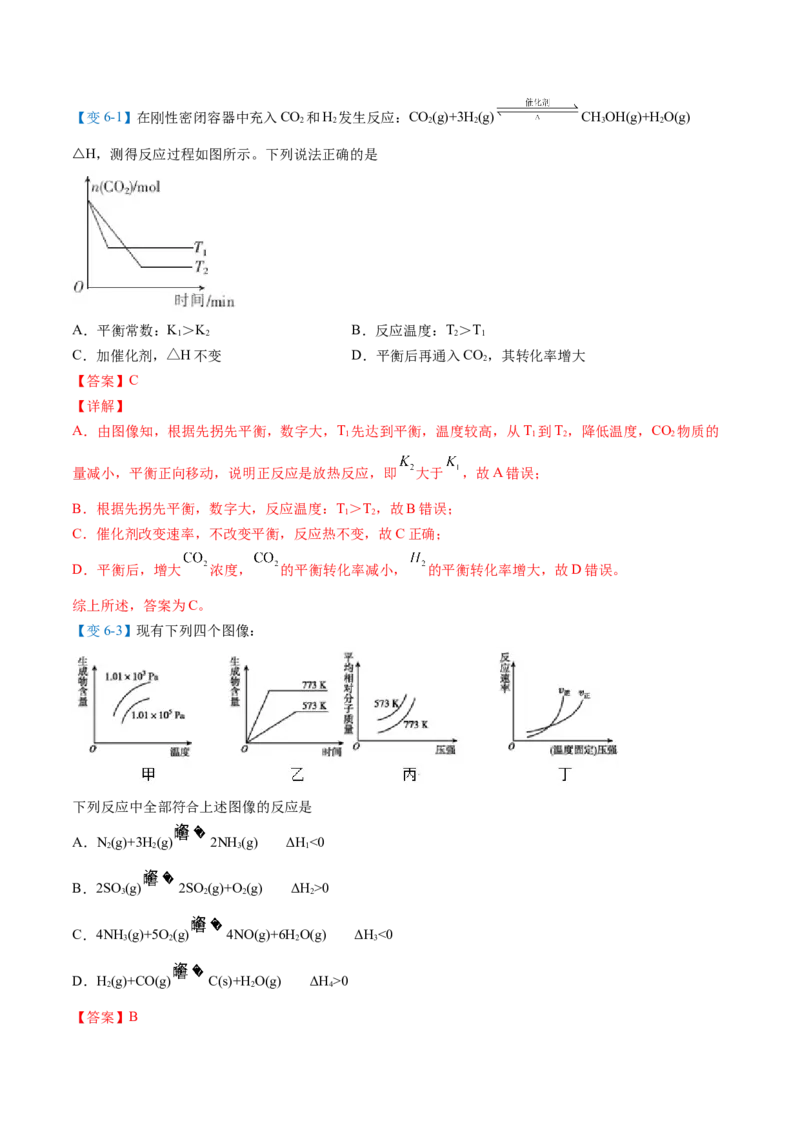
【变6-3】现有下列四个图像:
下列反应中全部符合上述图像的反应是
A.N(g)+3H(g) 2NH (g) ΔH <0
2 2 3 1
B.2SO (g) 2SO (g)+O(g) ΔH >0
3 2 2 2
C.4NH (g)+5O(g) 4NO(g)+6H O(g) ΔH <0
3 2 2 3
D.H(g)+CO(g) C(s)+HO(g) ΔH >0
2 2 4
【答案】B【分析】
由题给四个图像可知,符合图像的化学反应为气体体积增大的吸热反应,反应中混合气体的平均相对分子
质量减小。
【详解】
A.合成氨反应是一个气体体积减小的放热反应,故A不符合题意;
B.三氧化硫的分解反应是一个气体体积增大的吸热反应,反应中混合气体的平均相对分子质量减小,故
B符合题意;
C.氨气与氧气生成一氧化氮和水蒸气的反应是一个气体体积减小的放热反应,故C不符合题意;
D.氢气与一氧化碳反应生成碳固体和水蒸气的反应是一个气体体积减小的吸热反应,故D不符合题意;
故选B。
题型六:勒夏特列原理综合大题
杨sir化学,侵权必究
【例8】探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以CO、H 为原料合成
3 3 2 2
CHOH涉及的主要反应如下:
3
I.CO(g)+3H(g)=CH OH(g)+H O(g) △H =-48.5 kJ∙mol−1
2 2 3 2 1
II.CO(g)+2H(g)=CH OH(g) △H =-92.4 kJ∙mol−1
2 3 2 杨sir化学,侵权必究
Ⅲ.CO(g)+H(g)=CO(g)+HO(g) △H
2 2 2 3
回答下列问题:
(1)△H=___________kJ∙mol−1
3
(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO 和3molH 发生上述反应,达到平衡时,
2 2
容器中CHOH(g)为amol,CO为bmol,此时H(g)的浓度为___________mol∙mol−1 (用含a、b、V的代数式
3 2
表示,下同),反应III的平衡常数为___________。
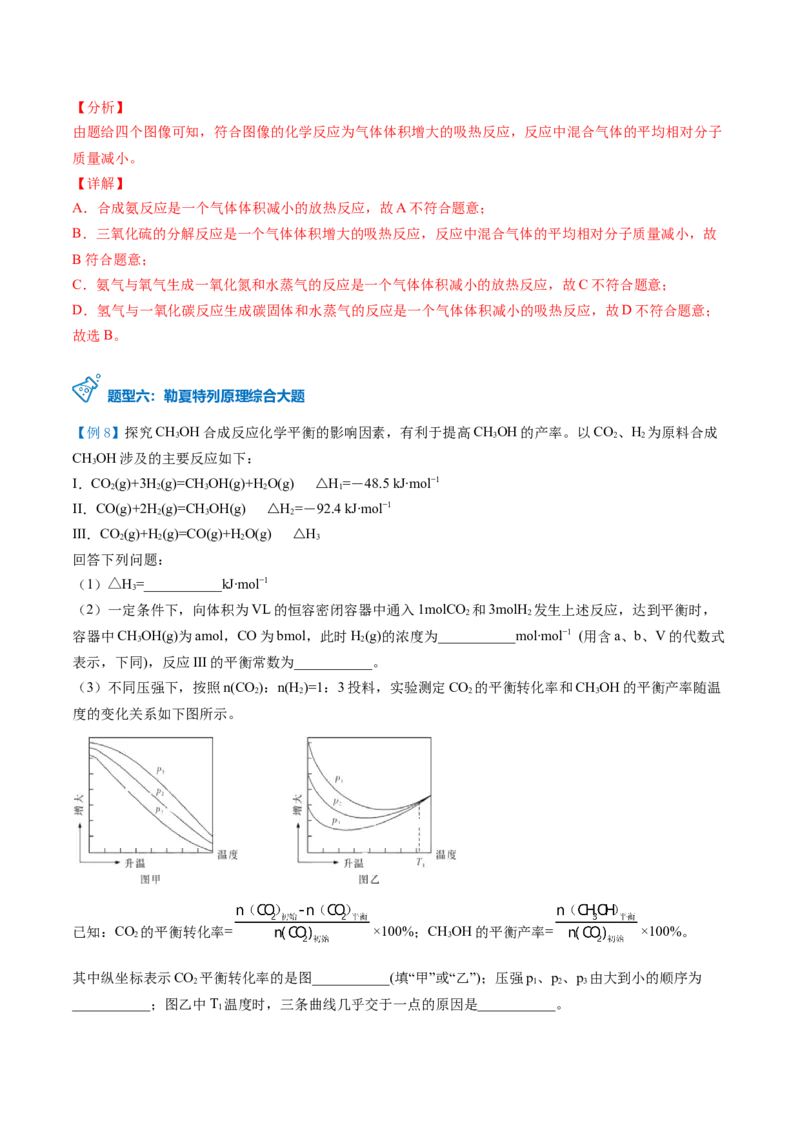
(3)不同压强下,按照n(CO):n(H )=1:3投料,实验测定CO 的平衡转化率和CHOH的平衡产率随温
2 2 2 3
度的变化关系如下图所示。
已知:CO 的平衡转化率= ×100%;CHOH的平衡产率= ×100%。
2 3
其中纵坐标表示CO 平衡转化率的是图___________(填“甲”或“乙”);压强p、p、p 由大到小的顺序为
2 1 2 3
___________;图乙中T 温度时,三条曲线几乎交于一点的原因是___________。
1(4)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为___________(填字母代号)。
2 3
A.高温、高压 B.高温、低压
C.低温、高压 D.低温、低压
【答案】
(1)+43.9
(2)
(3) 乙 p>p>p T 时以反应III为主,反应III前后气体分子数相等,压强改变对平衡几乎
1 2 3 1
没有影响
(4)C
【分析】
(1)
将反应I减去反应II得到反应Ⅲ,即△H=-48.5 kJ∙mol−1-(-92.4 kJ∙mol−1)= +43.9kJ∙mol−1;故答案为:
3
+43.9。
(2)
一定条件下,向体积为VL的恒容密闭容器中通入1molCO 和3molH 发生上述反应,达到平衡时,容器中
2 2
CHOH(g)为amol,CO为bmol,根据上述信息建立三段式, ,
3
, ,y−z=b,x+z=a,得到
x+y=a+b,H(g)物质的量为3−3x−y−2z=3−3(x+z) +z−y=3−3(x+z) –(y−z)=3−3a−b,此时H(g)的浓度为
2 2
mol∙mol−1,此时CO(g)物质的量浓度为 mol∙mol−1,CO(g)物质的量浓度为 mol∙mol−1,
2
HO(g)物质的量浓度为 mol∙mol−1,反应III的平衡常数为 ;
2
故答案为: ; 。
(3)I、II反应是放热反应,Ⅲ是吸热反应,升高温度,对I、II平衡逆向移动,对Ⅲ是平衡正向移动,但由于
I、II平衡逆向移动,CO浓度增大,对反应Ⅲ也有逆向移动的趋势,因此CO 转化率减小,即纵坐标表示
2
CO 平衡转化率的是图乙;反应I、II是体积减小的反应,反应Ⅲ是等体积反应,因此加压,转化率增大,
2
即压强p、p、p 由大到小的顺序为p>p>p;图乙中T 温度时,三条曲线几乎交于一点的原因是T 时
1 2 3 1 2 3 1 1
以反应III为主,反应III前后气体分子数相等,压强改变对平衡几乎没有影响;故答案为:乙;p>p>
1 2
p;T 时以反应III为主,反应III前后气体分子数相等,压强改变对平衡几乎没有影响。
3 1
(4)
根据图中信息为同时提高CO 的平衡转化率和CHOH的平衡产率,低温、高压时CO 的平衡转化率大,
2 3 2
因此应选择的反应条件为低温、高压;故答案为:C。
提分特训
小杨老师 15521324728 侵权必究
【题1】下列有关化学平衡的说法正确的是
A.对于恒温密闭容器中进行的反应N(g)+3H(g) 2NH (g),若N 的体积分数保持不变,则一定说明反
2 2 3 2
应已达到平衡状态
B.一定温度下,将2.0g CaCO 固体置于1L恒容密闭容器中充分反应后,c(CO)=0.0125mol/L,若保持温
3 2
度不变,将容器体积扩大至2L,达到新平衡后c(CO)=0.01mol/L
2
C.反应:CH(g)+HO(g) CO(g)+3H(g) ∆H>0,在其它条件不变的情况下,升高温度、减小容器体积、
4 2 2
增大水蒸汽的浓度均能提高CH 的平衡转化率
4
D.一定温度下,恒容密闭容器中充入一定量NO 发生反应:2NO NO 达到平衡后,再向容器中充入
2 2 2 4
一定量的NO 并达到新的平衡,则NO 体积分数先增大后减小,但比原平衡小
2 2
【答案】D
【详解】
【题2】等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达平衡:X(g)+2Y(g)
3Z(g) △H<0,当改变某个条件并达到新平衡后,下列叙述正确的是
A.升高温度,X的体积分数减小
B.增大压强,Z的浓度不变
C.保持容器体积不变,充入一定量的惰性气体,Y的浓度不变
D.保持容器体积不变,充入一定量的Z,X的体积分数增大
杨sir化学,侵权必究
【答案】C
【详解】
A.正反应放热,升高温度,平衡向逆反应方向移动,X的体积分数增大,故A错误;
B.增大压强,平衡不移动,但缩小体积,Z的浓度增大,故B错误;C.保持容器体积不变,充入一定量的惰性气体,平衡不发生移动,Y的浓度不变,故C正确;
D.保持容器体积不变,充入一定量的Z,相当于增大压强,平衡不移动,X的体积分数不变,故D错误;
故选C。
【题4】利用CO 制备甲醇是温室气体资源化重要途径。在某CO 催化加氢制甲醇的反应体系中主要存在
2 2
如下反应:
反应I:CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=-48.2kJ·mol-1
2 2 3 2 1
反应II:CO(g)+H(g)=CO(g)+HO(g) ΔH=+42.5kJ·mol-1
2 2 2 2
反应III:CO(g)+2H(g)=CH OH(g)ΔH
2 3 3
向恒压、密闭容器中通入1molCO 和3molH ,平衡时CO、CO 和CHOH的物质的量分数随温度变化如图
2 2 2 3
所示。下列说法不正确的是
A.ΔH=-90.7kJ·mol-1
3
B.曲线a表示CO的物质的量分数随温度的变化
杨sir化学,侵权必究
C.在不改变反应时间和温度条件下,增大压强能提高CHOH的产量
3
D.在240~270℃内,温度改变对反应I和反应II平衡影响相反且程度接近
【答案】B
【详解】
A.根据盖斯定律可知反应I-II可得反应III,所以 H= H- H=-48.2kJ/mol-42.5kJ/mol=-90.7kJ/mol,故
3 1 2
A正确;
△ △ △
B. H<0, H<0,即生成甲醇的反应均为放热反应,所以温度升高平衡时甲醇的物质的量分数应减小,
1 3
H>0,生成CO的反应为吸热反应,所以随温度升高CO平衡时的物质的量分数会变大,二者共同作用
2△ △
导致水蒸气减小幅度小于甲醇,a代表CHOH,b代表CO,故B错误;
△ 3
C.反应I、III都能生成CHOH,温度不变,增大压强,平衡正向移动,CHOH的产量提高,故C正确;
3 3
D. H<0, H>0,根据勒夏特列原理,温度改变时,反应i和反应ii平衡移动方向相反,且平衡移动
1 2
程度相近,故D正确;
△ △
故选:B。
【题5】乙烯气相直接水合反应制备乙醇:C H(g)+HO(g) C HOH(g)。乙烯的平衡转化率随温度、
2 4 2 2 5
压强的变化关系如下[起始时,n(H O)=n(C H)=1 mol,容器体积为1 L]。
2 2 4下列分析不正确的是
A.乙烯气相直接水合反应的ΔH<0
B.图中压强的大小关系为p>p>p
1 2 3
C.图中a点对应的平衡常数K=
D.达到平衡状态a、b所需要的时间:a>b
杨sir化学,侵权必究
【答案】B
【详解】
A.依据图像分析,在同一压强下,随着温度的升高,乙烯的平衡转化率降低,说明该反应正方向为放热
反应,即ΔH<0,A项正确;
B.由方程式C H(g)+HO(g) C HOH(g)可知,该反应的正反应是气体体积减小的反应,所以增大压强,
2 4 2 2 5
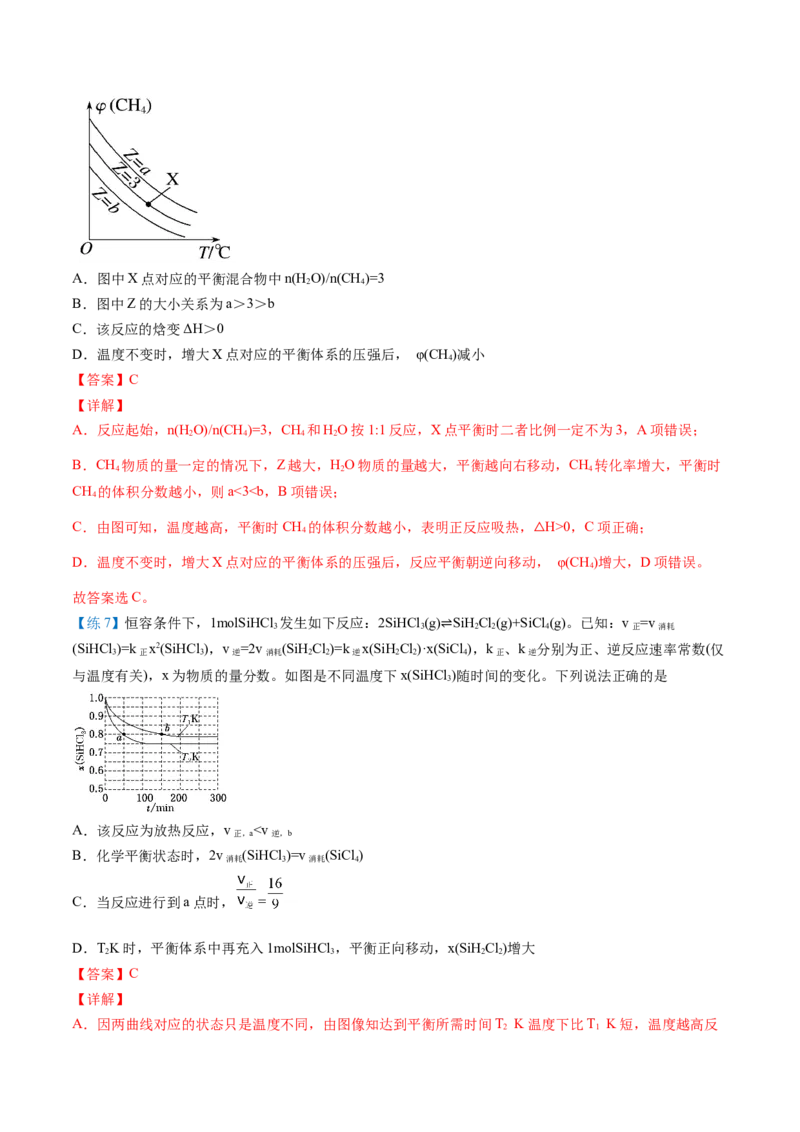
平衡正向移动,乙烯的平衡转化率提高,因此压强的大小关系是p0,C项正确;
4
D.温度不变时,增大X点对应的平衡体系的压强后,反应平衡朝逆向移动△, φ(CH)增大,D项错误。
4
故答案选C。
【练7】恒容条件下,1molSiHCl 发生如下反应:2SiHCl (g) SiHCl(g)+SiCl (g)。已知:v =v
3 3 2 2 4 正 消耗
(SiHCl )=k x2(SiHCl ),v =2v (SiHCl)=k x(SiHCl)·x(SiCl ),k 、k 分别为正、逆反应速率常数(仅
3 正 3 逆 消耗 2 2 逆 2 2 ⇌ 4 正 逆
与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl )随时间的变化。下列说法正确的是
3
A.该反应为放热反应,v T,又因T K下达到平衡时SiHCl 的物质的量分数
2 1 2 3
比T K时小,说明升温平衡向正反应方向移动,由此推知该反应为吸热反应,A项错误;
1
B.各物质的化学反应速率之比等于化学方程式中相应化学计量数之比,化学平衡状态时,v
消耗
(SiHCl )=2v (SiCl ),B项错误;
3 消耗 4
C.2SiHCl (g) SiHCl(g)+SiCl (g)的反应前后分子数不变,即反应开始至达到平衡的过程中混合气体
3 2 2 4
总物质的量始终为1 mol,由图像知,T K下达到平衡时SiHCl 的物质的量分数为0.75,则此时SiHCl 和
2 3 2 2
SiCl 的物质的量分数均为0.125,因为平衡时v =v ,v =k x2(SiHCl )=0.752k ,v =k
4 正 逆 正 正 3 正 逆 逆
x(SiHCl)·x(SiCl )=0.1252k ,则0.752k =0.1252k , ,因k 和k 只与温度有关,反应进
2 2 4 逆 正 逆 正 逆
行到a点时,v =k x2(SiHCl )=0.82k ,v =k x(SiHCl)·x(SiCl )=0.12k , = × = × = ,
正 正 3 正 逆 逆 2 2 4 逆
C项正确;
D.恒温恒容条件下再充入1 mol SiHCl ,相当于增大压强,而2SiHCl (g) SiHCl(g)+SiCl (g)是反应前
3 3 2 2 4
后气体分子数不变的反应,所以改变压强,平衡不移动,再次达到平衡时x(SiHCl)不变,D项错误;
2 2
答案选C。
【练7】在密闭容器中发生如下反应 ;达到平衡后,改变下列条
件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
(1)升高温度,平衡_______移动;
(2)增大压强,平衡_______移动:
(3)增大H(g)浓度,平衡_______移动:加入C,平衡_______移动;
2
(4)加入催化剂,平衡_______移动。
杨sir化学,侵权必究
【答案】向正反应方向 向逆反应方向 向逆反应方向 不 不
【详解】
(1)该反应正反应是吸热反应,升高温度,平衡向吸热反应方向移动,即升高温度,平衡向正反应方向移动;
(2)增大压强,平衡向气体分子数减小的方向移动,即平衡向逆反应方向移动:
(3)氢气是生成物,增大H(g)浓度,平衡向逆反应方向移动:C是固体,加入C,平衡不移动;
2
(4)加入催化剂,可以加快反应速率,但平衡不移动。
【练8】反应 达到平衡,若升高温度,反应再次达到平衡时B的转化率变大;若减
小压强,反应再次达到平衡时混合体系中C的体积分数减小。试推测:
(1)逆反应是______________(填“放”或“吸”)热反应。
(2)缩小体积而加压后,再次达到平衡时,与原平衡相比A的浓度_______________(填“变大”“变小”或“不
变”)。
(3)若B是有色物质,A、C是无色物质,则减小压强(增大体积),再次达到平衡时,与原平衡相比混合物的颜色_______________(填“变深”“变浅”或“不变”)。
杨sir化学,侵权必究
【答案】放 变大 变浅
【详解】
(1)升高温度,B的平衡转化率变大,说明升温平衡正向移动,得出正反应为吸热反应,故逆反应为放热反
应,故答案为:放;
(2)减压后平衡时混合体系中C的体积分数减小,说明减压平衡逆向移动,逆反应是一个气体分子数增大的
反应,则增大压强(压缩体积)后,平衡正向移动,但根据勒·夏特列原理可知,平衡向减弱这种改变的方
向移动,但一般不能抵消这种改变,故与原平衡相比,达到新平衡时A的浓度变大,故答案为:变大;
(3)与(2)同理,减小压强(增大体积),平衡时各气体的浓度均减小,混合物的颜色变浅,故答案为:变浅。
【练9】I.可逆反应∶mA(g)+nB(g)⇌pC(g)+qD(s) ∆H,试根据图回答∶
[A的转化率(%)表示为α(A)、A的含量(%)表示为φ(A)]
(1)压强P_______P(填“>”,“<”或“=”下同)
1 2
(2)计量数(m+n)_______(p)
(3)温度t℃_______t℃
1 2
(4)ΔH_______0
II.反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(5)该反应是_______反应(填“吸热”,“放热”);
(6)当反应达到平衡时,只升高温度,化学平衡向_______(填“正反应方向”或“逆反应方向”)移动。
(7)反应体系中加入催化剂该反应的反应热_______(填增大”“减小”“不变”);
【答案】
(1)<
(2)<
(3)>
(4)>
(5)放热
(6)逆反应方向
(7)不变
【分析】(1)
由前图可知,P 较先达到平衡状态,则P>P,故答案为:<;
2 2 1
(2)
P>P,压强越大,A的转化率越低,说明增大压强平衡向逆方向移动,则(m+n)<(p),故答案为:<;
2 1
(3)
由后图可知t 先达到平衡状态,则t>t,故答案为:>。
1 1 2
(4)
由图2知,温度从t 降低到t,A的含量升高,说明平衡逆向移动,说明正反应方向为吸热反应,则ΔH>
1 2
0,故答案为:>;
(5)
由图示知,反应物的总能量高于生成物的总能量,该反应为放热反应,故答案为:放热;
(6)
该反应为放热反应,根据勒夏特列原理,当反应达到平衡时,只升高温度,化学平衡向逆方向移动,故答
案为:逆反应方向;
(7)
加入催化剂只改变反应速率,反应的热效应不变,则体系中加入催化剂该反应的反应热不变,故答案为:
不变。
【练10】汽车尾气是城市主要空气污染物,利用反应2NO(g) +2CO(g) N+2CO (g)可实现汽车尾气的无
2 2
害化处理。向甲、乙两个体积都为2.0 L的恒容密闭容器中分别充入2mol CO和2 mol NO,分别在T、T
⇌ 1 2
温度下,经过一段时间后达到平衡。反应过程中n(CO)随时间(t)变化情况见下表:
2 杨sir化学,侵权必究
时间/s 0 2 4 6 8 10
甲容器(T )n(CO)/mol 0 0.72 1.20 1.60 1.60 1.60
1 2
乙容器(T )n(CO)/mol 0 0.60 1.00 1.40 1.70 1.70
2 2
(1)T ___________T(填“>”、“<”或“=”下同),该反应ΔH___________0。
1 2
(2)乙容器中,2~4s内N 的平均反应速率υ(N )=___________。
2 2
(3)甲容器中NO平衡转化率为___________,T 温度下该反应的平衡常数为___________。
1
(4)该反应达到平衡后,为提高反应速率同时提高NO的转化率,可采取的措施有___________(填字母序号)。
a.增大NO浓度 b.压缩容器体积 c.移去部分N d.改用高效催化剂
2
【答案】> < 0.05mol/(L·s) 80% 160 b
【分析】
根据表格数据,甲容器中达到平衡时间短,反应的温度高,结合温度对平衡的影响和v= ,利用三段式
分析解答。
【详解】
(1) 2NO(g) +2CO(g) N+2CO (g),向甲、乙两个体积都为2.0L的恒容密闭容器中分别充入2mol CO和2
2 2
⇌mol NO,分别在T、T 温度下,经过一段时间后达到平衡,甲容器达到平衡需要的时间短,则反应速率快,
1 2
说明反应温度T>T;达到平衡状态时,乙中CO 的物质的量大于甲中CO 的物质的量,说明降低温度,
1 2 2 2
平衡正向进行,则正反应为放热反应, H<0,故答案为:>;<;
△
(2)乙容器中,2~4s内N 的平均反应速率v(N )= v(CO)= × =0.05mol•L-1•s-1,故答案为:
2 2 2
0.05mol•L-1•s-1;
(3) 甲容器中,
NO平衡转化率= ×100%=80%;容器的体积为2L,则平衡常数K= =160,故答案为:
80%;160;
(4)a.增大NO浓度,NO的转化率降低,故a不选;b.压缩容器体积,压强增大,反应速率加快,平
衡正向移动,NO的转化率增大,故b选;c.移去部分N,反应速率减慢,故c不选;d.改用高效催化
2
剂,平衡不移动,NO的转化率不变,故d不选;故答案为:b。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育