文档内容
第 11 讲 氧化钠和过氧化钠
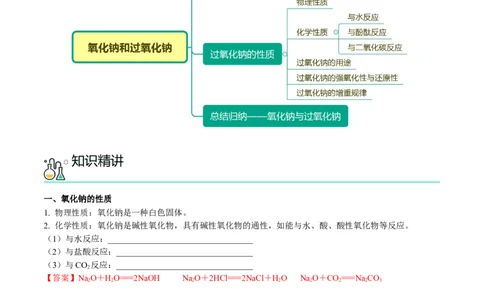
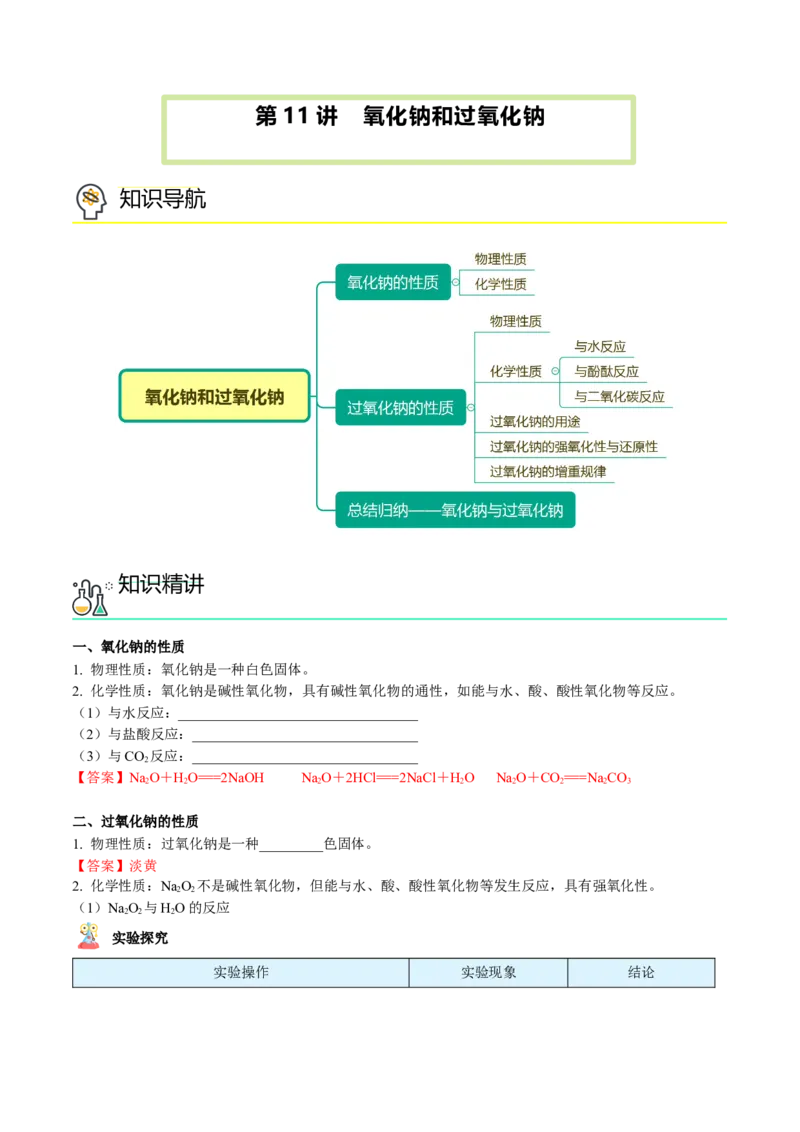
知识导航
知识精讲
一、氧化钠的性质
1. 物理性质:氧化钠是一种白色固体。
2. 化学性质:氧化钠是碱性氧化物,具有碱性氧化物的通性,如能与水、酸、酸性氧化物等反应。
(1)与水反应:__________________________________
(2)与盐酸反应:________________________________
(3)与CO 反应:________________________________
2
【答案】NaO+HO===2NaOH NaO+2HCl===2NaCl+HO NaO+CO===Na CO
2 2 2 2 2 2 2 3
二、过氧化钠的性质
1. 物理性质:过氧化钠是一种_________色固体。
【答案】淡黄
2. 化学性质:NaO 不是碱性氧化物,但能与水、酸、酸性氧化物等发生反应,具有强氧化性。
2 2
(1)NaO 与HO的反应
2 2 2
实验探究
实验操作 实验现象 结论将1~2 mL水滴入盛有1~2g过氧化
剧烈反应,产生大量气
钠固体的试管中,立即把带火星的 反应产生________
泡,带火星的木条复燃
木条伸入试管中
用手轻轻触摸试管外壁 试管壁发烫 反应____热
向反应后的溶液中滴入无色酚酞溶 反应生成________
无色酚酞溶液_______
液,并振荡试管 NaO 具有_______
2 2
【实验结论】过氧化钠与水反应有氧气和碱性物质生成,且过氧化钠有漂白性。
过氧化钠与水反应的化学方程式:_______________________________________
【答案】O 放 先变红后褪色 碱 漂白性
2
2NaO + 2HO === 4NaOH + O↑
2 2 2 2
资料卡片——NaO 使酚酞先变红后褪色的原因
2 2
将NaO 投入滴有酚酞的水中, NaO 与水反应生成NaOH,使酚酞先变红;同时,NaO 与水反应过程
2 2 2 2 2 2
中,还生成了不是很稳定的中间产物HO,具有漂白性,使变色后的酚酞氧化褪色。
2 2
(2)NaO 与CO 反应
2 2 2
过氧化钠能与二氧化碳反应生成碳酸钠和氧气,化学方程式为:__________________________________。
【答案】2NaO + 2CO === 2NaCO + O
2 2 2 2 3 2
3.NaO 的用途
2 2
(1)强氧化剂、漂白剂;
(2)供氧剂。
资料卡片——过氧化钠的强氧化性与还原性
NaO 中氧元素为-1价,处于中间价态,既有氧化性又有还原性。NaO 主要表现较强的氧化性:
2 2 2 2
(1)NaO 与SO 反应:NaO+SO ===Na SO
2 2 2 2 2 2 2 4
(2)NaO 投入NaSO 溶液中,可将SO2-氧化成SO2-
2 2 2 3 3 4
(3)NaO 投入FeCl 溶液中,可将Fe2+氧化Fe3+,同时生成Fe(OH) 沉淀
2 2 2 3
(4)NaO 投入氢硫酸中,可将HS氧化成单质硫,溶液变浑浊
2 2 2
(5)NaO 投入品红溶液中,可使品红溶液褪色
2 2
(6)NaO 能使酚酞试液先变红后褪色
2 2
NaO 也有还原性,如遇KMnO 等强氧化剂时,被氧化成O。
2 2 4 2
思考与交流:写出NaO 作供氧剂的原理,并分别用双线桥、单线桥表示其电子转移。
2 2注意
NaO 与CO、HO反应时,氧化剂、还原剂都是NaO。
2 2 2 2 2 2
4. NaO 的增重问题
2 2
思考与交流
(1)a g H 在O 中完全燃烧,将其燃烧产物通过足量的NaO 固体,NaO 固体质量增加多少克?
2 2 2 2 2 2
(2)a g CO在O 中完全燃烧,将其燃烧产物通过足量的NaO 固体,NaO 固体质量增加多少克?
2 2 2 2 2
(3)如果是a g H 和CO的混合气体在O 中完全燃烧,产物通过足量NaO 呢?
2 2 2 2
(4)若a g某物质O 中完全燃烧,产物通过足量的NaO 固体,NaO 固体增加a g,那么,该物质需
2 2 2 2 2
要满足什么条件?
【答案】(1)a g (2)a g (3)a g (4)通式为(CO) (H ) 推导过程参考如下:
m 2 n
(1)2H+O=====2HO ① 2NaO+2HO===4NaOH+O↑ ② ①+②得:H+NaO===2NaOH
2 2 2 2 2 2 2 2 2 2
(2)2CO+O=====2CO ① 2NaO+2CO===2NaCO+O ② ①+②得:CO+NaO===NaCO
2 2 2 2 2 2 3 2 2 2 2 3
归纳总结——Na O 的增重规律
2 2
(1)若题目只给出CO 或HO的质量,可通过CO 或HO的质量,求出CO或H 的质量,则固体增
2 2 2 2 2
重就是CO或H 的质量。
2
(2)w g 符合通式为(CO) (H ) 的物质,在O 中充分燃烧后,将其产物通过足量的NaO 固体,反应
m 2 n 2 2 2
完毕,固体增重也必是 w g。如甲醛(CHO)、甲醇(CHO)、乙酸(C HO)、葡萄糖(C H O)等。
2 4 2 4 2 6 12 6
总结归纳——氧化钠与过氧化钠NaO NaO
2 2 2
颜色 白色 淡黄色
阴阳离子个数比 1∶2 1∶2
氧元素的化合价 -2 -1
是否为碱性氧化物 是 否
与HO反应 NaO + HO === 2NaOH 2NaO + 2HO === 4NaOH + O↑
2 2 2 2 2 2 2
与CO 反应 NaO + CO === NaCO 2NaO + 2CO === 2NaCO + O
2 2 2 2 3 2 2 2 2 3 2
与盐酸反应 NaO + 2HCl === 2NaCl + HO 2NaO + 4HCl === 4NaCl + 2HO + O↑
2 2 2 2 2 2
氧化性/漂白性 无 有
主要用途 制备NaOH 强氧化剂、漂白剂、供氧剂
对点训练
题型一:氧化钠和过氧化钠的基本性质
【例1】(2021·全国高一课时练习)下列关于钠的氧化物的说法正确的是
A.向包有NaO 粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明NaO 与HO反应放热且有氧气
2 2 2 2 2
生成
B.NaO与NaO 中阳、阴离子的个数比不相同
2 2 2
C.将金属钠切开,表面变暗,最终得到淡黄色固体
D.保持温度不变,向饱和烧碱溶液中加入2 g Na O,充分反应后,溶液中Na+浓度增大
2 2
【答案】A
【详解】
A.脱脂棉燃烧需要具备两个条件,一是氧气助燃,二是达到着火点,该现象能够说明时放热反应且有氧
气生成,A正确;
B.NaO是由Na+与O2-构成,阳离子和阴离子个数比均为2:1;NaO 是Na+与 构成,阳离子和阴离子
2 2 2
个数比也为2:1,B错误;
C.Na暴漏与空气中表面变暗,生成的白色的氧化钠,不能产生过氧化钠,C错误;
D.过氧化钠与水反应后生成氢氧化钠,因为是饱和烧碱溶液,所以温度不变溶液中NaCl饱和溶液的浓度
仍然不变,则溶液中钠离子浓度不变,D错误;
故合理选项是A。
【变1】(2021·全国)下列对于NaO、NaO 的比较,正确的一项是
2 2 2
A.NaO、NaO都是钠的氧化物,都是白色固体
2 2 2
B.NaO、NaO 与水反应均只生成NaOH
2 2 2C.NaO 在和HO的反应中既是氧化剂又是还原剂
2 2 2
D.NaO、NaO均可作供氧剂
2 2 2
【答案】C
【详解】
A.过氧化钠是淡黄色的固体,故A错误;
B.过氧化钠和水反应生成氢氧化钠和氧气,氧化钠和水反应只生成氢氧化钠,故B错误;
C.2NaO + 2H O = 4NaOH + O ↑,反应中只有NaO 中O元素的化合价变化,NaO 既是氧化剂,又是
2 2 2 2 2 2 2 2
还原剂,故C正确;
D.NaO 可与水、二氧化碳反应生成氧气,可作供氧剂,NaO不能作供氧剂,故D错误;
2 2 2
故选C。
【例2】(2020·河北正定中学高一月考)下列叙述正确的是
A.金属钠着火时,可用泡沫灭火器灭火
B.将一小块钠投入CuSO 溶液中可置换出红色的固体
4
C.向某待测溶液中滴入盐酸酸化的AgNO 溶液,产生白色沉淀,说明待测溶液中含Cl-
3
D.NaO与NaO 中阳、阴离子的个数比均为2∶1
2 2 2
【答案】D
【详解】
A.钠和水反应生成氢气,钠燃烧生成的过氧化钠和水、二氧化碳反应,钠着火时,不可用水或泡沫灭火
器灭火,A错误;
B.钠投入硫酸铜溶液中,会先和水反应,生成的氢氧化钠再和硫酸铜反应,故不能置换出金属铜,B错
误;
C.加入盐酸引入了氯离子,故向某待测溶液中滴入盐酸酸化的AgNO 溶液,产生白色沉淀,不能说明待
3
测溶液中含Cl-,应改为用硝酸酸化的硝酸银,C错误;
D.氧化钠由2个钠离子和1个氧离子构成,而过氧化钠由2个钠离子和1个过氧根构成,故两者中阳离子
和阴离子的个数之比均为2: 1,D正确;
答案选D。
【变2】(2021·全国)下列叙述正确的是
①NaO与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②NaO与CO 发生化合反应生成NaCO,NaO 与CO 发生置换反应生成O
2 2 2 3 2 2 2 2
③NaO是淡黄色物质,NaO 是白色物质
2 2 2
④NaO 可作供氧剂,而NaO不可
2 2 2
A.都正确 B.①③④ C.②③⑤ D.④
【答案】D
【详解】
①NaO和水反应只生成碱,是碱性氧化物,NaO 和水反应生成氢氧化钠和氧气,不是碱性氧化物,①错
2 2 2
误;
②NaO 与CO 反应生成O 和碳酸钠,反应物为两种化合物,不属于置换反应,②错误;
2 2 2 2③氧化钠为白色,过氧化钠为淡黄色,③错误;
④NaO 能与二氧化碳、水反应生成氧气,而NaO与二氧化碳、水反应不能产生O,所以NaO 可作供氧
2 2 2 2 2 2
剂,而NaO不行,④正确;
2
故选D。
题型二:过氧化钠的化学性质
【例3】(2021·辽宁鞍山·高二期末)某溶液中含大量 、 、 、 、 ,向其中加
入足量的 固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A. B. 、 C. D.
【答案】C
【详解】
溶液中加入足量 固体后,会发生反应 ,溶液中 和OH-浓度增加,再
发生 和 ,使 和 离子浓度减少, 离子浓度增加,
所以只有 离子浓度基本保持不变,故答案为:C。
【变3】(2020·镇平县第一高级中学)下列说法中正确的有
①将钠投入到滴有紫色石蕊试液的水中后,溶液变红
②钠在水蒸气中反应(密闭容器)时因温度高会发生燃烧现象
③钠与CuSO 溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出了金属铜
4
④过氧化钠投入到滴有酚酞的溶液中,溶液变红
⑤利用加热法可除去NaO中少量的NaO 杂质
2 2 2
⑥含等质量钠元素的NaO与NaO 固体,加入等量且足量水中充分反应后,所得溶液溶质的质量分数相等
2 2 2
⑦2 g H 充分燃烧后产物被NaO 完全吸收,NaO 固体增重1 g
2 2 2 2 2
⑧将2.3 g Na投入97.7 g水中形成的溶液溶质质量分数为4.0%
A.1项 B.4项 C.6项 D.7项
【答案】A
【详解】
①钠与水反应产生氢氧化钠和氢气,氢氧化钠溶液显碱性,使紫色石蕊试液变为蓝色,①错误;
②钠与水反应产生NaOH和H,H 是可燃性气体,但在高温下水蒸气中环境中无氧气,因此不会发生燃烧
2 2
现象,②错误;
③钠与CuSO 溶液中的水先反应产生NaOH和H,反应产生的NaOH再与溶质CuSO 发生复分解反应生成
4 2 4的Cu(OH) 蓝色沉淀和NaSO ,这两个反应都是放热反应,反应放出的热量使固体Cu(OH) 部分分解为黑
2 2 4 2
色CuO,导致沉淀上有时出现暗斑,③错误;
④过氧化钠与水反应产生氢氧化钠和氧气,过氧化钠具有强氧化性,具有漂白性,使滴有酚酞的溶液先变
红后褪色,④错误;
⑤加热时NaO会反应变为NaO,导致完全变质,不能达到除杂的目的,⑤错误;
2 2 2
⑥含等质量钠元素的NaO与NaO 固体的物质的量相等,根据方程式NaO+HO=2NaOH,
2 2 2 2 2
2NaO+2H O=4NaOH+O ↑可知:加入等量且足量水中充分反应后,反应消耗的水相同,产生的NaOH的
2 2 2 2
物质的量相同,因此所得溶液中溶质的质量分数也相等,⑥正确;
⑦2 g H 的物质的量是1 mol,充分燃烧后产物HO的物质的量是1 mol,根据反应方程式
2 2
2NaO+2H O=4NaOH+O ↑可知:1 mol H O被NaO 完全吸收后,NaO 固体增重为HO中H元素的质量,
2 2 2 2 2 2 2 2 2 2
即2 gH 的质量,⑦错误;
2
⑧将2.3 g Na的物质的量是0.1 mol,投入97.7g水中反应产生NaOH和气体H,溶液质量小于2.3 g+97.7
2
g=100 g,产生NaOH的质量为4 g,故形成的溶液溶质质量分数大于4.0%,⑧错误;
综上所述可知:说法正确的序号为⑥,故合理选项是A。
【例4】(2020·河南郑州一中高一月考)现有一定量含NaO杂质的NaO 试样,某化学兴趣小组设计了如
2 2 2
图装置测定NaO 试样的纯度。(提示:根据气体体积可得出气体的质量)
2 2
(1)仪器A为分液漏斗,盛放的试剂___,仪器B为圆底烧瓶,盛放的试剂为____。
(2)实验中发生反应的化学方程式为___,___。
【答案】
(1) HO NaO 试样
2 2 2
(2) NaO+HO=2NaOH 2NaO+2H O=4NaOH+O ↑
2 2 2 2 2 2
【分析】
用水与过氧化钠反应,根据收集到的气体体积计算出过氧化钠的纯度,A装置盛放的试剂为水,B装置为
圆底烧瓶,盛放的试剂为过氧化钠的样品,通过排水法测出生成O 的体积,计算出O 的物质的量,再根
2 2
据2NaO+2H O=4NaOH+O ↑计算NaO 的量,从而计算出纯度。
2 2 2 2 2 2
(1)
根据分析,A装置盛放的试剂为水;B装置盛放的试剂为NaO 试样;
2 2
(2)
实验中,NaO和NaO 分别与水发生反应,方程式为NaO+HO=2NaOH、2NaO+2H O=4NaOH+O ↑。
2 2 2 2 2 2 2 2 2题型三:Na O 的增重问题
2 2
【例5】(2020·郑州市第七中学高一月考)在一定条件下,使12gCO和O 的混合气体充分反应,所得混
2
合物在常温下跟足量的NaO 固体反应,结果固体增重7g,则原混合气体中O 的质量分数可能是
2 2 2
①33.3% ②41.7% ③58.3% ④66.7%
A.①② B.①③ C.②③ D.②④
【答案】A
【详解】
设CO 的质量为x,根据差量法可得:
2
,解得x=11g,n(CO)= =0.25mol;
2
根据2CO+O=2CO ,若O 过量,n(CO)= n(CO )=0.25mol,m(CO)=28g/mol×0.25mol=7g,
2 2 2 2
m(O)=12g-7g=5g,O 的质量分数为 ≈41.7%;若CO过量,n(O )= n(CO)=0.125mol,
2 2 2
m(O)=32g/mol×0.125mol=4g,O 的质量分数为 ≈33.3%;①②符合题意,故选A。
2 2
【变5-1】8.8 g CO 通入装有足量NaO 的干燥管中,干燥管增重的质量为( )
2 2 2
A.2.8 g B.5.6 g C.8.8 g D.11.2 g
【答案】 B
【变5-2】(2014·上海市建平中学高二月考)一定温度下,Wg下列物质在足量氧气中充分燃烧,产物与
过量的过氧化钠完全反应,过氧化钠固体增重Wg,符合此要求的是
①H ②CO ③CO和H ④HCOOCH ⑤HOOC-COOH
2 2 3
A.全部 B.仅④⑤ C.仅①②③ D.除⑤以外
【答案】D
【详解】
H、CO在整个过程中发生的化学方程式为:2H+O 2HO、2NaO+2H O=4NaOH+O ↑;2CO+O
2 2 2 2 2 2 2 2 2
2CO、2NaO+2CO =2Na CO+O ,由反应方程式可知,过氧化钠增加的质量即为H、CO的质量,
2 2 2 2 2 3 2 2
因此只要是CO或H 或它们的混合气体或化学组成符合(CO) •(H ),则过氧化钠固体增重质量都等于原物
2 m 2 n
质的质量,则①②③符合,HCOOCH 可以改写成(CO) •(H ),HOOC-COOH可以改写成(CO) •(OH) ,故
3 2 2 2 2 2
④符合,⑤不符合,故选D。
【变5-3】(2019·四川成都实外)下列物质各3g,在氧气中完全燃烧,于150℃时将产物通过足量的NaO
2 2
固体后,固体增重大于3g的是( )A.HCOOH B.CHCOOH C.C HOH D.C H O
3 2 5 6 12 8
【答案】C
【分析】
ag有机物能改写成(CO) (H ) 的有机物在氧气中充分燃烧,生成的产物通入足量过氧化钠中,增加的质量
m 2 n
就为ag。过氧化钠会吸收CO 中CO,吸收水中的H。
2 2
【详解】
A选项,HCOOH能改写成(CO)(H ),增加的质量等于3g,故A不符合题意;
2 n
B选项,CHCOOH能改写成(CO) (H ),增加的质量等于3g,故B不符合题意;
3 2 2 2
C选项,C HOH能改写成(CO)(H )C,C燃烧变为CO,过氧化钠会吸收CO 中CO,因此增加的质量大
2 5 2 3 2 2
于3g,故C符合题意;
D选项,C H O 能改写成(CO) (H )O,O 不会被过氧化钠吸收,因此增加的质量等于3g,故D不符合题
6 12 8 6 2 6 2 2
意。
综上所述,答案为C。
题型四:Na O 的性质探究
2 2
【例6】(2021·全国高一课时练习)某化学兴趣小组学习NaO 的性质后,进行过氧化钠与水反应的探究
2 2
实验。回答下列问题:
(1)探究该反应的热效应
实验装置如图所示,调节U型管内两侧液面相平,向试管中加入a g Na O 粉末,再滴加10 mL蒸馏水及2
2 2
~3滴酚酞试液,试管内产生大量气泡,溶液先变红后褪色。
①观察到U型管内液面_______(填标号),说明该反应为放热反应。
A.左侧较高 B.右侧较高 C.左、右两侧一样高
②写出该反应的离子方程式_______。
(2)探究溶液红色褪去的原因
限选仪器及试剂:试管、胶头滴管、温度计、蒸馏水、酚酞试液、MnO 粉末。
2
①提出合理猜想:
猜想一:反应放热,酚酞受热分解,使溶液红色褪去;
猜想二:_______。
②设计方案证明猜想:向a g Na O 中加入10 mL蒸馏水,所得溶液分别置于试管1和试管2中,请将实验
2 2
操作、现象和结论补充完整:
实验操作 实验现象 实验结论将试管1中溶液冷却至室温,滴加
_______ 猜想一不成立
2~3滴酚酞
向试管2中加入少量MnO 粉末,
2
振荡时,产生大量气泡;滴加酚酞后,_______ 猜想二成立
充分振荡,滴加2~3滴酚酞
③在试管2中,加入少量MnO 粉末的作用是_______。
2
【答案】B 2NaO+2HO=4Na++4OH-+O↑ 反应过程中生成漂白性物质HO,使溶液红色褪去
2 2 2 2 2 2
溶液先变红,后褪色 溶液变红,不褪色 作催化剂,将产生的HO 催化分解
2 2
【详解】
(1)①试管中NaO 与水反应放热,使锥形瓶中的气体受热膨胀,故U型管内液面左低右高,故选B。
2 2
②NaO 与水反应的离子方程式为2NaO+2HO=4Na++4OH-+O↑。
2 2 2 2 2 2
(2)①根据物质的性质,猜想二为反应过程中生成漂白性物质HO,使溶液红色褪去;
2 2
②猜想一是反应放热,酚酞受热分解,使溶液红色褪去,先冷却至室温后证明猜想一不成立,故实验现象
为溶液先变红,后褪色;要证明猜想二成立,即证明反应生成了HO,故实验现象为:溶液变红,不褪色;
2 2
③在试管2中,加入少量MnO 粉末的作用是作催化剂,将产生的HO 催化分解。
2 2 2
【例7】(2021·山东兰陵四中高三月考)NaO 具有强氧化性,H 具有还原性,某同学根据氧化还原反应
2 2 2
的知识推测NaO 与H 能发生反应。为了验证此推测结果,该同学设计并进行如图实验:
2 2 2
(1)步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并____,然后装入药品。
步骤2:打开K、K,在氢气流经装有NaO 的硬质玻璃管的过程中,未观察到明显现象。
1 2 2 2
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)步骤1中组装好仪器后的操作是___。
(2) 装置中所盛放的试剂是___,其作用是___。
(3)步骤3中的必要操作为打开K、K,____(请按正确的顺序填入下列步骤的字母)。
1 2
A.加热至NaO 逐渐熔化,反应一段时间 B.用小试管收集气体并检验其纯度
2 2
C.关闭K D.停止加热,充分冷却
1
(4)由上述实验可推出NaO 与H 反应的化学方程式为____。
2 2 2
(5)若只用水和酚酞试液___(填“能”或者“不能”)检验C中NaO 是否反应完全,若出现____,则NaO 可
2 2 2 2
能没有反应完全(若不能,此空不填)。
【答案】
(1)检查气密性
(2) 碱石灰 除去H 中的HCl和HO
2 2(3)BADC
(4)NaO+H 2NaOH
2 2 2
(5) 能 溶液先变红后褪色
【分析】
由实验装置图可知,装置A中锌与稀盐酸反应制氢气,装置B中盛有的碱石灰用于氢气中含氯化氢气体、
水蒸气,装置C中氢气与过氧化钠反应生成氢氧化钠,装置D中盛有的无水硫酸铜用于具有是否有水生成。
(1)
步骤1中组装好仪器后,要先检查装置的气密性,再装入试剂进行实验,故答案为:检查气密性;
(2)
锌与稀盐酸反应制得的氢气中含氯化氢气体、水蒸气,氯化氢气体、水蒸气都能与过氧化钠反应,干扰氢
气与过氧化钠的反应,则装置B中盛有的碱石灰用于氢气中含氯化氢气体、水蒸气,防止干扰实验,故答
案为:碱石灰;除去H 中的HCl和HO;
2 2
(3)
步骤3中的必要操作为打开K、K,为防止空气与氢气混合加热发生爆炸,先用小试管收集气体并检验其
1 2
纯度,检验完纯度后,点燃C处酒精灯加热,加热至过氧化钠逐渐熔化,反应一段时间,淡黄色的粉末慢
慢变成了白色固体,反应后熄灭酒精灯,停止加热,待硬质玻璃管充分冷却后,关闭K,停止通入氢气,
1
则打开K、K 后的必要操作为BADC,故答案为:BADC;
1 2
(4)
由淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色可知,硬质试管中发生的反应为过氧化钠与氢气
共热反应生成氢氧化钠,化学方程式为NaO+H 2NaOH,故答案为:NaO+H 2NaOH;
2 2 2 2 2 2
(5)
过氧化钠具有强氧化性,能使有机色质漂白褪色,若过氧化钠没有完全反应,将反应后的固体加入水配成
溶液后,滴入酚酞试液,溶液会先变红后褪色,则只用水和酚酞试液能检验C中氧化钠是否完全反应,故
答案为:能;溶液先变红后褪色。
提分特训
【题1】(2020·郑州市第七中学高一月考)下列叙述正确的是
A.利用加热法可除去NaO中少量的NaO 杂质
2 2 2
B.钠和钾的合金在室温下呈液态,可做核电工业原子反应堆的导电剂
C.NaO与CO 发生化合反应生成NaCO,NaO 与CO 发生置换反应生成O
2 2 2 3 2 2 2 2D.将一小块钠放入盛有饱和食盐水的烧杯中,烧杯底部有固体析出
【答案】D
【详解】
A.氧化钠在加热条件下会被空气中氧气氧化生成过氧化钠,则不能用加热法可除去氧化钠中的少量过氧
化钠杂质,故A错误;
B.钠和钾的合金在室温下呈液态,可做核电工业原子反应堆的导热剂,故B错误;
C.过氧化钠与二氧化碳发生歧化反应生成碳酸钠和氧气,故C错误;
D.钠与饱和食盐水中的水反应生成氢氧化钠和氢气,溶液中水的量减少,饱和溶液会变成过饱和溶液,
会有氯化钠固体析出沉在烧杯底部,故D正确;
故选D。
【题2】(2022·安徽)下列有关钠及其化合物的叙述错误的是
A. 吸收 产生 ,可用作呼吸面具供氧剂
B.高压钠灯发出的黄光透雾能力强,可用于道路和广场照明
C.氢氧化钠具有强碱性,可用于制胃酸中和剂
D.钠长期暴露在空气中的最终产物是
【答案】C
【详解】
A. 吸收 产生 ,所以 可用作呼吸面具供氧剂,A正确;
B.钠的焰色反应为黄色,则可用作透雾能力强的高压钠灯,B正确;
C.氢氧化钠具有腐蚀性,不能用于中和胃酸,一般用氢氧化铝、碳酸镁、碳酸氢钠等,C错误;
D.钠与氧气反应生成氧化钠,氧化钠与水反应生成氢氧化钠,氢氧化钠潮解,氢氧化钠溶液吸收二氧化
碳生成碳酸钠晶体,碳酸钠晶体风化得到碳酸钠,D正确。
故选C。
【题3】(2020·沁阳市第一中学高一月考)下列有关钠及其化合物的叙述中,正确的是( )
①金属钠着火时用泡沫灭火器灭火
②二氯化碳通过NaO 粉末,反应后固体物质增重
2 2
③切开的金属钠暴露在空气中, 光亮表面逐渐变暗2Na+O==Na O
2 2 2
④Na O 用作呼吸面具的供氧剂
2 2
⑤将钠粒投入硫酸铜溶液中会析出紫红色固体
A.①③ B.②③④⑤ C.②③⑤ D.②④
【答案】D
【分析】
①金属钠着火生成过氧化钠,与泡沫灭火器喷出的二氧化碳反应;
②二氧化碳通过过氧化钠后,固体变为Na2CO3;③钠在空气中与氧气反应生成氧化钠;
④过氧化钠与水、二氧化碳反应生成氧气;
⑤钠性质活泼,与硫酸铜溶液反应时先和水反应生成氢氧化钠和氢气,最后生成氢氧化铜沉淀。
【详解】
①金属钠着火时不能用水或泡沫灭火器灭火,而应用细沙盖灭,故①错误;
②二氧化碳通过过氧化钠后,固体变为NaCO,故固体的质量增大,故②正确;
2 3
③切开的金属钠暴露在空气中,光亮表面逐渐变暗是因为4Na+O=Na O,故③错误;
2 2
④过氧化钠与水、二氧化碳反应生成氧气,所以可以用作供氧剂,故④正确;
⑤钠性质活泼,与硫酸铜溶液反应时先和水反应生成氢氧化钠和氢气,最后生成氢氧化铜沉淀,故⑤错误;
故答案选:D。
【题4】在NaO 与水反应中,叙述正确的是( )
2 2
A.O 是还原产物
2
B.NaO 是氧化剂,水是还原剂
2 2
C.NaOH是氧化产物
D.氧化剂与还原剂的质量比是1∶1
【答案】 D
【题5】(双选)(2021·全国高三专题练习)下列说法正确的是
A.NaO在空气中加热可得固体NaO
2 2 2
B.NaO 在空气中放置后由淡黄色变为白色,反应的化学方程式为2NaO=2Na O+O↑
2 2 2 2 2 2
C.室温下Na与空气中O 反应制取NaO
2 2 2
D.钠与水反应生成氢氧化钠和氢气
【答案】AD
【详解】
A.无水状态下NaO 比NaO更稳定,NaO在空气中加热可以生成更稳定的NaO,故A正确;
2 2 2 2 2 2
B.NaO 在空气中放置后由淡黄色变为白色发生的反应为NaO 与CO 反应生成NaCO 和O,反应的化
2 2 2 2 2 2 3 2
学方程式为2NaO+2CO=2Na CO+O,故B错误;
2 2 2 2 3 2
C.常温下,Na与空气中的氧气反应生成NaO;加热条件下,钠与氧气反应生成NaO,故C错误;
2 2 2
D.钠具有强还原性,能与冷水反应生成氢氧化钠和氢气,故D正确;
故选AD。
【题6】(2021·河北易县中学高二月考)取10.8g平均相对分子质量为7.2的CO与H 组成的混合气体,与
2
足量的O 充分反应后,立即将产物通入足量的NaO 固体中,反应后NaO 固体质量增加为
2 2 2 2 2
A.3.6g B.7.2g C.10.8g D.无法确定
【答案】C
【详解】
CO在氧气中完全燃烧生成CO,CO 和再与NaO 反应,方程式为2CO+O 2CO、
2 2 2 2 2 22CO+2Na O=2Na CO+O ,总方程式为:CO+Na O=Na CO,可知过氧化钠增重为CO的质量;H 在氧
2 2 2 2 3 2 2 2 2 3 2
气中完全燃烧,生成HO,HO再与NaO 反应,方程式为2H+O 2HO、2HO+2Na O=4NaOH+O,
2 2 2 2 2 2 2 2 2 2 2
总反应方程式为:H+Na O=2NaOH,可知反应后固体质量增加为氢气质量,故由10.8gCO和H 组成的混
2 2 2 2
合物在足量的O 中充分燃烧,立即通入足量的NaO 固体,固体质量增加应为CO和H 的质量,即固体增
2 2 2 2
重为10.8g,故选C。
【题7】(2019·邵东市第十中学高三月考)a g下列物质在氧气中充分燃烧后的气体(1.01×105 Pa,
120℃),通过足量的过氧化钠充分反应后,过氧化钠增重b g,符合b>a 的选项有
A.HCHO B.CHCOOCH CH C.HOOCCOOH D.HCOOH
3 2 3
【答案】B
【详解】
A、HCHO可以改写出CO(H),agHCHO充分燃烧后的气体通过足量过氧化钠,过氧化钠增重ag,故A
2
错误;
B、CHCOOCH CH 可以改写出(CO)(H)C ,组成中碳原子增多,agCHCOOCH CH 充分燃烧后的
3 2 3 2 2 4 2 3 2 3
气体通过足量过氧化钠,过氧化钠增重大于ag,故B正确;
C、HOOCCOOH可以改写出(CO)(H)O,组成中氧原子增多,agHOOCCOOH充分燃烧后的气体通
2 2 2
过足量过氧化钠,过氧化钠增重小于ag,故C错误;
D、HCOOH可以改写出(CO)(H)O,ag HCOOH充分燃烧后的气体通过足量过氧化钠,过氧化钠增
2
重小于ag, 故D错误。
答案选B。
【题8】(2021·黑龙江实验中学高三开学考试)某化学小组用下列装置,模拟呼吸面具中的有关反应原理
测定样品中NaO 的纯度。
2 2
(1)装置中a的作用是___________,装置A中发生的离子反应方程式___________。
(2)装置C中发生反应的化学方程式为___________。
(3)上述装置存在一处缺陷,会导致测定NaO 的纯度偏高,改进的方法是___________。
2 2
(4)实验装置改进后,向C中加入10.0g样品进行实验,实验结束后共收集到标准状况下336mL气体,
则样品中NaO 的纯度___________。
2 2【答案】
(1) 保持上下压强一致,使稀盐酸顺利滴下
(2) ,
(3)在装置CD之间增加装有NaOH溶液的洗气瓶
(4)23.4%
【分析】
由实验装置图可知,装置A中碳酸钙和稀盐酸发生反应制备二氧化碳气体,装置B中盛有的饱和碳酸氢钠
溶液用于除去二氧化碳中混有的氯化氢气体,装置C中过氧化钠与二氧化碳、水蒸气反应生成氧气,装置
D和E用于测量氧气的体积,该装置存在一处缺陷,C中末反应完全的二氧化碳会随氧气进入到D中,会
导致测得氧气的量偏大,使测定过氧化钠的纯度偏高。
(1)
装置中a为恒压分液漏斗,其作用是保持上下压强一致,使稀盐酸顺利滴下;装置A中发生的反应为碳酸
钙与稀盐酸反应生成氯化钙、二氧化碳和水,反应的离子反应方程式为CaCO +2H+=Ca2++H O+CO↑;故答
3 2 2
案为:恒压分液漏斗;保持上下压强一致,使液体顺利滴下;CaCO +2H+=Ca2++H O+CO↑;
3 2 2
(2)
装置C中发生的反应有过氧化钠与二氧化碳反应生成碳酸钠和氧气,与水蒸气反应生成氢氧化钠和氧气,
反应的化学方程式为2NaO+2H O=4NaOH+O ↑,2NaO+2CO =2Na CO+O ↑,故答案为:
2 2 2 2 2 2 2 2 3 2
2NaO+2H O=4NaOH+O ↑,2NaO+2CO =2Na CO+O ↑;
2 2 2 2 2 2 2 2 3 2
(3)
该装置存在一处缺陷,C中末反应完全的二氧化碳会随氧气进入到D中,会导致测得氧气的量偏大,使测
定过氧化钠的纯度偏高,应该在CD之间增加吸收二氧化碳的洗气瓶,故答案为:在装置CD之间增加装
有NaOH溶液的洗气瓶;
(4)
由方程式可知,不论过氧化钠与水还是与二氧化碳反应,过氧化钠和氧气的物质的量比恒定为2:1,由实
验结束后共收集到标准状况下336mL氧气可知,样品中过氧化钠的纯度为
×100%=23.4%,故答案为:23.4%。
【题9】(2021·石家庄市第四中学高一期中)如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持
仪器略)。(1)B装置可除去A装置中可能挥发出的某种气体,反应的离子方程式为_______。
(2)C装置为O 的发生装置,反应的化学方程式为_______。
2
(3)D装置可除去C装置中未反应的某种气体,反应的离子方程式为_______。
(4)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为:取少量C装置中反应后的固体溶
于水,向溶液中滴入过量CaCl 溶液,若有白色沉淀生成,则证明固体中含有NaCO,过滤,向滤液中滴
2 2 3
入几滴酚酞溶液,若现象为_______,则证明固体中含有NaOH而不含有NaO。
2 2
【答案】
(1)HCO +H+═HO+CO↑
2 2
(2)2NaO+2CO ═2NaCO+O
2 2 2 2 3 2
(3)2OH-+CO ═CO ++H O
2 2
(4)溶液变红且不褪色
【分析】
实验室研究潜水艇中供氧体系反应机理:A装置:稀盐酸和大理石制取二氧化碳,B装置:用饱和的碳酸
氢钠除去二氧化碳中的氯化氢,C装置:二氧化碳、水分别和过氧化钠反应2NaO+2CO ═2Na CO+O 、
2 2 2 2 3 2
2NaO+2H O═4NaOH+O↑,D装置:用氢氧化钠吸收未反应的二氧化碳,E装置:用排水法收集制得的氧
2 2 2 2
气。
(1)
A中盐酸会挥发出HCl气体,用碳酸氢钠溶液除去氯化氢,离子反应式为:HCO +H+═H O+CO↑;
2 2
(2)
A装置制得的二氧化碳能够与过氧化钠反应产生氧气,化学反应方程式为:2NaO+2CO ═2Na CO+O ;
2 2 2 2 3 2
(3)
未反应的二氧化碳与氢氧化钠反应生成碳酸钠和水,离子反应式为:2OH-+CO ═CO ++H O;
2 2
(4)
C装置中固体由淡黄色NaO 完全变为白色为碳酸钙钠,反应为2NaO+2CO ═2Na CO+O ,检验固体成分
2 2 2 2 2 2 3 2
实际为检验碳酸根离子,可用氯化钡、或氯化钙溶液与碳酸根离子反应生成或碳酸钙、碳酸钡白色沉淀验
证碳酸根离子的存在,过滤沉淀,向滤液中滴入几滴酚酞试液,若溶液变红且不褪色,则证明固体中含有
氢氧化钠。提分作业
【练1】(2021·金华市第八中学高一月考)下列说法不正确的是
A.金属钠和氧气反应的产物和反应的条件有关
B.Na在空气中点燃,生成的主要产物为白色的NaO
2
C.可用水来检验某NaO样品中是否含有NaO
2 2 2
D.过氧化钠为淡黄色固体,其中氧元素的化合价为负一价
【答案】B
【详解】
A.金属钠和氧气反应的产物和反应的条件有关,室温生成氧化钠,加热生成过氧化钠,A正确;
B.Na在空气中点燃,生成的主要产物为淡黄色的NaO,B错误;
2 2
C.氧化钠与水生成氢氧化钠,过氧化钠与水生成氢氧化钠和氧气会产生气泡,C正确;
D.过氧化钠为淡黄色固体,化学式为NaO,其中氧元素的化合价为负一价,D正确;
2 2
答案选B。
【练2】关于NaO和NaO 的叙述正确的是( )
2 2 2
A.都是白色的固体 B.都是碱性氧化物 C.都能和水反应形成强碱溶液 D.都是强氧化剂
【答案】C
【练3】(2021·全国高一课时练习)下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量
比),化学反应的本质并不改变的是
A.Na和O B.NaOH和CO C.NaO 和CO D.木炭(C)和O
2 2 2 2 2 2
【答案】C
【详解】
A.Na与O 常温下反应生成NaO,Na与O 加热时反应生成NaO,不符合题意;
2 2 2 2 2
B.CO 过量时与NaOH反应生成碳酸氢钠,CO 少量时与NaOH反应生成碳酸钠和水,不符合题意;
2 2
C.过氧化钠和二氧化碳反应只能生成碳酸钠和氧气,符合题意;
D.氧气过量时与木炭反应生成CO,氧气不足时与木炭反应生成CO,不符合题意;
2
答案选C。
【练4】下列叙述正确的是( )
①NaO与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②NaO 中O元素的化合价为-2价
2 2
③NaO是淡黄色物质,NaO 是白色物质
2 2 2
④NaO 可作供氧剂,而NaO不可
2 2 2
⑤向NaO 与水反应后的溶液中加酚酞,溶液先变红后褪色
2 2
A.都正确 B.④⑤ C.②③⑤ D.②③④⑤
【答案】B
【练5】(2019·上饶中学)在一定条件下,使CO和O 的混合气体26克充分反应,所得混合物在常温下
2与足量的NaO 固体反应,结果固体增重14克,则原混合气体中的CO和O 的质量比是( )
2 2 2
A.4 :9 B.7 :4 C.7 :6 D.6 :7
【答案】C
【分析】
根据2NaO+2CO =2Na CO+O ,可知混合物在常温下跟足量的NaO 固体反应生成固体为NaCO,
2 2 2 2 3 2 2 2 2 3
1molNa O 生成1molNa CO,质量增加28g,恰好为CO的质量。
2 2 2 3
【详解】
由反应2NaO+2CO =2Na CO+O ,可知混合物在常温下跟足量的NaO 固体反应生成固体为NaCO,
2 2 2 2 3 2 2 2 2 3
1molNa O 生成1molNa CO,质量增加28g,恰好为CO的质量,
2 2 2 3
固体增重14g,说明混合气体中CO为14g,则O 为26g-14g=12g,
2
原混合气体中CO和O 的质量比为14g:12g=7:6,
2
故选C。
【练6】关于钠元素的单质及其化合物的叙述不正确的是( )
A.钠是银白色金属,质软,熔点相对较低,密度比水小
B.大量的钠着火时可以用沙扑灭,不能用水或泡沫灭火剂灭火
C.金属钠在空气中长期放置,最终变为碳酸钠
D.NaO和NaO 都能由金属钠和氧气化合生成,NaO和NaO 氧的价态也相同
2 2 2 2 2 2
【答案】 D
【练7】一定温度下,w 克下列物质在足量的O 中充分燃烧后,产物与足量的NaO 充分反应,增重w 克,
1 2 2 2 2
若w=w ,则符合此条件的物质是( )
1 2
①H ②CO ③H 和CO的混合气体 ④HCOOCH ⑤CHCHO ⑥C H O
2 2 3 3 6 12 6
A.①②③⑥ B.①②③ C.①②③④⑥ D.①②③⑤
【答案】C
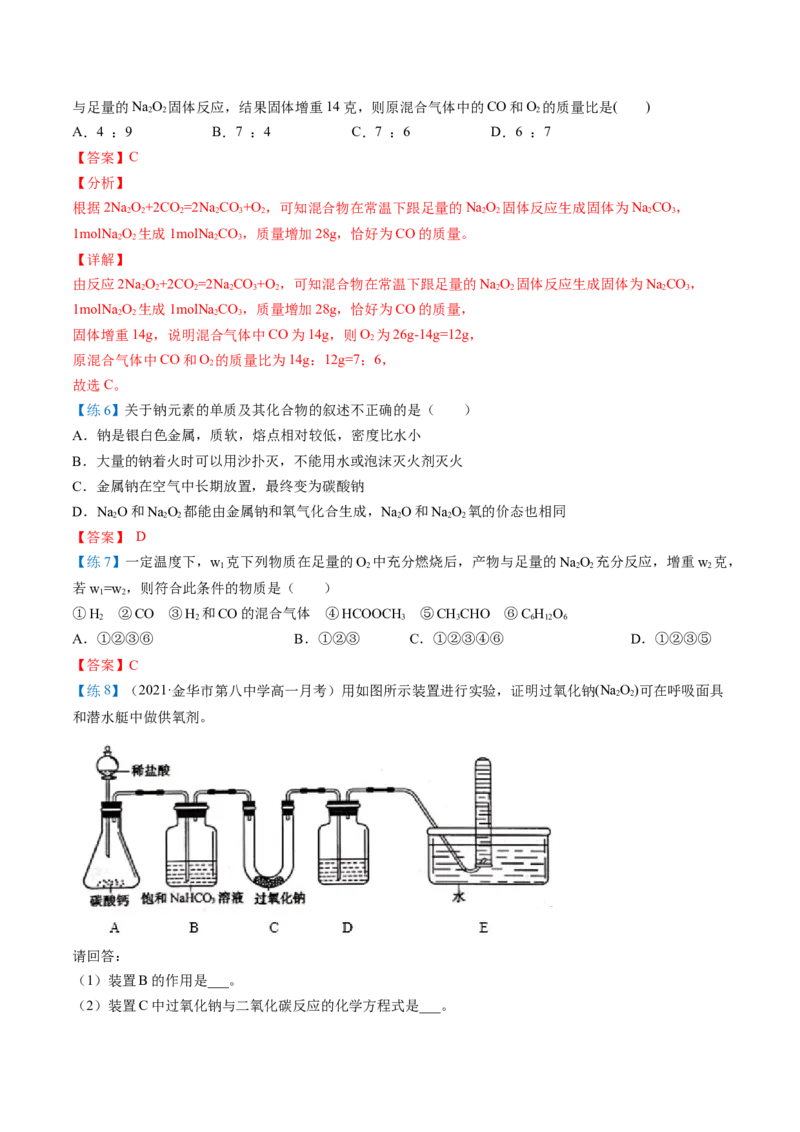
【练8】(2021·金华市第八中学高一月考)用如图所示装置进行实验,证明过氧化钠(Na O)可在呼吸面具
2 2
和潜水艇中做供氧剂。
请回答:
(1)装置B的作用是___。
(2)装置C中过氧化钠与二氧化碳反应的化学方程式是___。(3)装置D中盛放的试剂是___。
(4)当装置内气流平稳后开始用试管收集气体,该气体能___,证明过氧化钠可做供氧剂。
【答案】
(1)除去二氧化碳气体中的氯化氢
(2)2NaO+2CO =2Na CO+O
2 2 2 2 3 2
(3)氢氧化钠溶液
(4)使带火星的木条复燃
【分析】
在A装置中盐酸与碳酸钙反应生成二氧化碳、氯化钙和水;将混合气体(主要含二氧化碳和少量的氯化氢
和水蒸气)通入盛有饱和碳酸氢钠溶液的B装置中以除去氯化氢;然后将混合气体(主要为二氧化碳以及少
量水蒸气)通入到盛有过氧化钠的U型管C中,使其反应生成氧气;再将混合气体通入盛有氢氧化钠溶液
的D装置中,以便除去反应后剩余的二氧化碳;最后在E中用排水法收集所产生的氧气。
(1)
装置B可以除去二氧化碳气体中的氯化氢;
(2)
过氧化钠与二氧化碳反应生成碳酸钠和氧气,化学方程式为2NaO+2CO =2Na CO+O ;
2 2 2 2 3 2
(3)
装置D中盛放的试剂为氢氧化钠溶液,除去反应后剩余的二氧化碳;
(4)
生成的气体为氧气,能使带火星的木条复燃,证明过氧化钠可做供氧剂。关注更新免费领取,淘宝唯一每月更新店铺:知二教育