文档内容
《物质及其变化》单元测试(培优提升)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共45分)
1.(本题3分)(2021·安徽滁州·高一期中)下列物质分类正确的是
A.NaO、FeO、Al O 均为碱性氧化物
2 2 3
B.烧碱、纯碱、熟石灰均为碱
C.空气、碘酒、浓盐酸均为混合物
D.稀豆浆、氢氧化铁胶体、硫酸铜溶液均为胶体
【答案】C
【详解】
A.Al O 为两性氧化物,不是碱性氧化物,A错误;
2 3
B.纯碱是NaCO 的俗称,由金属阳离子和酸根离子构成,属于盐,不是碱,B错误;
2 3
C.空气、碘酒、浓盐酸中都含有多种构成物质的基本微粒,因此均为混合物,C正确;
D.硫酸铜溶液属于溶液,不是胶体,D错误;
故合理选项是C。
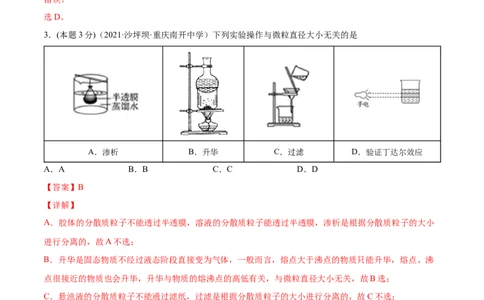
2.(本题3分)(2021·全国高一课时练习)如图所示,将淀粉胶体和食盐溶液的混合物放入半透膜的袋子中,
放入蒸馏水中,一段时间后,Na+和Cl-通过半透膜进入蒸馏水中,重复几次,可以得到纯净的淀粉胶体,
该方法称为渗析。下列说法中不正确的是
A.粒子直径小于1nm(10-9m)的分子和离子能通过半透膜
B.淀粉分子的直径在1nm~100nm之间
C.渗析法可以用来提纯胶体
D.用滤纸可以分离胶体和溶液
【答案】D
【分析】由题目所给的信息可知,Na+和Cl-能通过半透膜,淀粉分子不能通过半透膜,因此直径小于1nm的分子或
离子能通过半透膜,直径在1nm~100nm之间的粒子(即胶体粒子)不能通过半透膜。
【详解】
A. 溶液中粒子能透过半透膜,粒子直径小于1nm(10-9m)的分子和离子能通过半透膜,故A正确;
B.淀粉分子不能通过半透膜,因此直径在1nm~100nm之间,故B正确;
C.根据题目信息可知用半透膜能将小分子或离子与胶体分离,可以用渗析法来提纯胶体,故C正确;
D.滤纸的空隙较大,当粒子直径大于100nm时,不能通过滤纸,胶体和溶液的粒子都能通过滤纸,故D
错误。
选D。
3.(本题3分)(2021·沙坪坝·重庆南开中学)下列实验操作与微粒直径大小无关的是
A.渗析 B.升华 C.过滤 D.验证丁达尔效应
A.A B.B C.C D.D
【答案】B
【详解】
A.胶体的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜,渗析是根据分散质粒子的大小
进行分离的,故A不选;
B.升华是固态物质不经过液态阶段直接变为气体,一般而言,熔点大于沸点的物质只能升华,熔点、沸
点很接近的物质也会升华,升华与物质的熔沸点的高低有关,与微粒直径大小无关,故B选;
C.悬浊液的分散质粒子不能通过滤纸,过滤是根据分散质粒子的大小进行分离的,故C不选;
D.胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应,丁达尔效应
和粒子直径大小有关,故D不选;
故选B。
4.(本题3分)(2020·石家庄市第十中学)下烈说法中正确的是
A.某物质不属于电解质,就属于非电解质
B.SO 溶于水可导电,SO 属于电解质
3 3
C.NaCl属于电解质,所以NaCl晶体可导电D.已知氧化铝在熔融状态下能导电,则氧化铝在熔融状态下能电离
【答案】D
【详解】
A.某物质可能是纯净物,也可能是混合物。若是混合物,则该物质既不属于电解质,也不属于非电解质;
而电解质、非电解质是化合物,在水溶液中或熔融状态下能够导电的化合物,非电解质是在水溶液中和熔
融状态下都不能够导电的化合物,因此某物质若不属于电解质,也不一定就属于非电解质,A错误;
B.SO 溶于水,与水反应产生HSO ,HSO 电离产生自由移动的离子而可导电,所以离子不是SO 电离
3 2 4 2 4 3
产生的,因此化合物SO 属于非电解质,B错误;
3
C.NaCl是盐,溶于水或受热熔化时会电离产生自由移动的离子而能够导电,因此属于电解质,但在NaCl
晶体中存在的离子不能自由移动,因此不可导电,C错误;
D.氧化铝是离子化合物,在熔融状态下发生电离而能导电,因此氧化铝在熔融状态下能电离,D正确;
故合理选项是D。
5.(本题3分)(2020·天津市滨海新区汉沽第六中学高一月考)下列叙述正确的是
A.所有离子方程式都可表示同一类型反应
B.H++OH-=H O可表示所有酸和碱的中和反应
2
C.凡是易溶于水的化合物都可以写成离子形式
D.单质和氧化物在离子方程式中不用离子符号表示
【答案】D
【详解】
A.离子方程式不一定表示同一类型反应,如Zn+2CH COOH=Zn2++2CH COO-+H ↑仅表示Zn与醋酸之间
3 3 2
的反应,A错误;
B.H++OH-=H O仅表示可溶性强酸和可溶性强碱反应产生可溶性盐和水的中和反应,B错误;
2
C.易溶性非电解质及加入的可溶性固体化合物,在书写离子方程式时仍然用化学式表示,不能拆写为离
子形式,C错误;
D.单质和氧化物在离子方程式书写时要保留化学式,不用离子符号表示,D正确;
故合理选项是D。
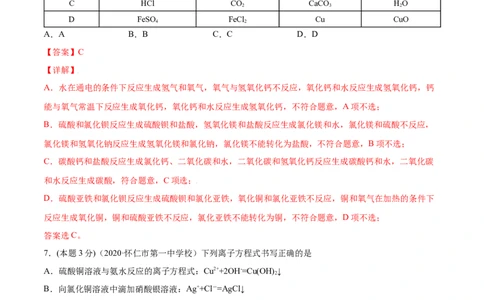
6.(本题3分)(江西省赣州市会昌县第五中学2021-2022学年高一上学期开学考测试新化学试题)如图所
示甲、乙、丙、丁四种物质间相互关系中的反应,均为初中化学常见反应(“—”表示相连的两种物质能反应,
“→”表示通过一步反应能实现转化),下列达项符合图示关系的是选项 甲 乙 丙 丁
A HO O CaO Ca(OH)
2 2 2
B HSO HCl MgCl Mg(OH)
2 4 2 2
C HCl CO CaCO HO
2 3 2
D FeSO FeCl Cu CuO
4 2
A.A B.B C.C D.D
【答案】C
【详解】
A.水在通电的条件下反应生成氢气和氧气,氧气与氢氧化钙不反应,氧化钙和水反应生成氢氧化钙,钙
能与氧气常温下反应生成氧化钙,氧化钙和水反应生成氢氧化钙,不符合题意,A项不选;
B.硫酸和氯化钡反应生成硫酸钡和盐酸,氢氧化镁和盐酸反应生成氯化镁和水,氯化镁和硫酸不反应,
氯化镁和氢氧化钠反应生成氢氧化镁和氯化钠,氯化镁不能转化为盐酸,不符合题意,B项不选;
C.碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,二氧化碳和氢氧化钙反应生成碳酸钙和水,二氧化碳
和水反应生成碳酸,符合题意,C项选;
D.硫酸亚铁和氯化钡反应生成硫酸钡和氯化亚铁,氧化铜和氯化亚铁不反应,铜和氧气在加热的条件下
反应生成氧化铜,铜和硫酸亚铁不反应,氯化亚铁不能转化为铜,不符合题意,D项不选;
答案选C。
7.(本题3分)(2020·怀仁市第一中学校)下列离子方程式书写正确的是
A.硫酸铜溶液与氨水反应的离子方程式:Cu2++2OH-=Cu(OH) ↓
2
B.向氯化铜溶液中滴加硝酸银溶液:Ag++Cl-=AgCl↓
C.氢氧化钡和稀硫酸反应的离子方程式:Ba2++OH-+H++ =BaSO↓+H O
4 2
D.盐酸和碳酸氢钠溶液反应:2H++ =H O+CO↑
2 2
【答案】B
【详解】
A.NH ·H O为弱碱,不能拆成离子形式,正确的离子方程为 A错误;
3 2B.向氯化铜溶液中滴加硝酸银溶液时,Ag+和Cl-反应生成AgCl沉淀,反应的离子方程式为Ag++Cl-
=AgCl↓,B正确;
C.氢氧化钡和稀硫酸反应的离子方程式:Ba2++2OH-+2H++ =BaSO↓+2H O,C错误;
4 2
D.盐酸和碳酸氢钠溶液反应:H++ =H O+CO↑,D错误。
2 2
答案选B。
8.(本题3分)(2020·沙坪坝·重庆八中高一期中)反应物之间的用量不同,往往导致离子反应的书写也不
相同,下列离子方程式能正确表示反应的是
A.NaOH溶液中通入过量CO:CO+2OH−= +H O
2 2 2
B.向碳酸钠溶液中通入少量CO: +CO +H O=2
2 2 2
C.NaCO 溶液中逐滴滴加少量盐酸: +2H+=H O+CO↑
2 3 2 2
D.向Ba(OH) 溶液中滴加少量NaHSO 溶液:2H++ +Ba2++2OH−=BaSO ↓+2H O
2 4 4 2
【答案】B
【详解】
A.二氧化碳过量时,二者反应生成碳酸氢钠,离子方程式为:CO+OH-= ,故A错误;
2
B.二者反应生成碳酸氢钠,离子方程式为: +CO +H O=2 ,故B正确;
2 2
C.稀盐酸少量时,二者反应生成碳酸氢钠和氯化钠,离子方程式为: +H+= ,故C错误;
D.硫酸氢钠少量时,二者反应生成硫酸钡、水和NaOH,离子方程式为:H++ +Ba2++OH-
=BaSO ↓+H O,故D错误;
4 2
答案选B。
9.(本题3分)(2021·吉林延边二中高一月考)下列说法正确的是
A.pH<7的溶液:Cu2+、Na+、Mg2+、NO
B.滴加酚酞溶液显红色的溶液:Ba2+、NH 、Cl−、NOC.取少量某溶液,向其中加入盐酸酸化的BaCl 溶液,通过观察是否有白色沉淀生成,可证明该溶液中是
2
否含有SO
D.H++OH-=H O可描述所有酸碱中和反应的实质
2
【答案】A
【详解】
A.pH<7的溶液:Cu2+、Na+、Mg2+、NO 相互间不会发生反应,可以大量共存,A正确;
B. 滴加酚酞溶液显红色的溶液显碱性,NH 不可以大量共存,B错误;
C.氯化银,硫酸钡等白色沉淀不溶于酸。加入盐酸酸化的BaCl 溶液,通过观察是否有白色沉淀生成,则
2
该溶液中是否可能含有SO 、Ag+等,C错误;
D. H++OH-=H O不可描述所有酸碱中和反应的实质,可描述强酸和强碱之间生成可溶性盐的中和反应,
2
D错误;
答案选A。
10.(本题3分)(2019·罗平县第二中学高一期中)某溶液中含有较大量的Cl-、 、OH-三种阴离子,如
果只取一次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中, 正确的是
①滴加Mg(NO) 溶液 ②过滤 ③滴加AgNO 溶液 ④滴加Ba(NO ) 溶液
3 2 3 3 2
A.①②④②③ B.④②③②① C.①②③②④ D.④②①②③
【答案】D
【分析】
检验氯离子选择硝酸银溶液;检验氢氧根离子,选择硝酸镁溶液;检验碳酸根离子选择硝酸钡溶液,用三
种试剂将三种离子检验出来,每加一种试剂能够检验出一种离子,此时要注意每加入一种试剂只能与一种
离子结合,来选择加入试剂顺序及操作步骤。
【详解】
Cl-用含有AgNO 溶液检验,二者反应生成白色沉淀AgCl; 用Ba(NO ) 溶液检验,二者反应生成白
3 3 2
色沉淀BaCO ;OH-用Mg(NO) 溶液检验,二者反应生成白色沉淀Mg(OH) 。Cl-、 、OH-都和AgNO
3 3 2 2 3溶液反应, 、OH-都和Mg(NO) 溶液反应生成白色沉淀;只有 和Ba(NO ) 溶液反应生成白色沉淀,
3 2 3 2
为了防止干扰,应该先检验Ba(NO )、再检验OH-,故加入试剂顺序是④②①②③,故合理选项是B。
3 2
11.(本题3分)(2020·浙江)氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴
影部分的是( )
A.Cu+2AgNO =Cu(NO)+2Ag
3 3 2
B.S+O SO
2 2
C.2FeCl +Cu=2FeCl +CuCl
3 2 2
D.2NaHCO NaCO+H O+CO↑
3 2 3 2 2
【答案】C
【分析】
阴影部分表示的是不是四种基本反应类型,但是氧化还原反应。
【详解】
A.Cu+2AgNO =Cu(NO)+2Ag是置换反应,且是氧化还原反应,故A错误;
3 3 2
B.S+O SO 是化合反应,且是氧化还原反应,故B错误;
2 2
C.2FeCl +Cu=2FeCl +CuCl 不属于四种基本反应类型,但是氧化还原反应,故C正确;
3 2 2
D.2NaHCO NaCO+H O+CO↑是分解反应,也不是氧化还原反应,故D错误;
3 2 3 2 2
故答案为C。
12.(本题3分)(2021·南宁市银海三美学校高一月考)一定条件下硝酸铵受热分解的化学方程式(未配平)
为 ,下列说法正确的是
A.配平后HO的系数为8
2B.氧化产物和还原产物的物质的量之比为1∶2
C.N 只是还原产物
2
D.被氧化与被还原的氮原子数之比为5∶3
【答案】D
【分析】
由方程式可知,反应中铵根离子中氮元素化合价升高被氧化,硝酸根离子中化合价部分降低被还原,氮气
即是氧化产物又是还原产物,由得失电子数目守恒和原子个数守恒可知,硝酸铵受热分解的化学方程式为
5NH NO 2HNO+4N ↑+9H O。
4 3 3 2 2
【详解】
A.由分析可知,配平后水的系数为9,故A错误;
B.由分析可知,反应中氮气即是氧化产物又是还原产物,由得失电子数目守恒可知,氧化产物和还原产
物的物质的量之比为5∶3,故B错误;
C.由分析可知,反应中氮气即是氧化产物又是还原产物,故C错误;
D.由分析可知,被氧化与被还原的氮原子数之比为5∶3,故D正确;
故选D。
13.(本题3分)(2021·全国高一课时练习)已知 在酸性溶液中易被还原成 ,且还原性:
。下列反应在水溶液中不可能发生的是
A. B.
C. D.
【答案】A
【详解】
A.根据氧化性是: Cl >FeCl >I ,因此氯气可以氧化Fe2+,也可以氧化I-,但是碘离子还原性强于亚铁离子,
2 3 2
碘离子会先被氯气氧化,正确的离子方程式是:Cl 不足时,Cl+2I-=2Cl-+I, Cl 过量时,3Cl+2Fe2++4I-=
2 2 2 2 2
6C1-+2I +2Fe3+,所以A不可能发生,故A符合题意;
2
B.根据反应: ,得出氧化性是: Cl>I ,和题意相符合,反应可能发生,故B不
2 2
符合题意;C.根据反应: ,得出氧化性是: >Cl, 和题意相符合,反应可
2
能发生,故C不符合题意;
D.根据反应 ,得出氧化性是:FeCl >I ,和题意相符合,反应可能发生,故D不符合
3 2
题意;
故选A。
14.(本题3分)(2019·山东省淄博第七中学高一月考)检验加碘盐含“KIO ”可通过在酸性条件下,加入
3
碘化钾溶液和淀粉来实现。反应原理如下:KIO +KI+HCl—I+KCl+H O(未配平) 下列有关说法正确的是
3 2 2
A.KI 是氧化剂 B.KIO 被氧化
3
C.该反应配平后系数为:1,5,6,3,6,3D.每生成3个I 分子,转移6个电子
2
【答案】C
【分析】
KIO +KI+HCl—I+KCl+H O反应中,KIO 中I元素的化合价从+5价降低到0价,KI中I元素的化合价从-1
3 2 2 3
价升高到0价,根据得失电子守恒和原子守恒配平方程式为KIO +5KI+6HCl═3I +6KCl+3H O。
3 2 2
【详解】
A.KI中I元素的化合价从-1价升高到0价,反应中KI为还原剂,故A错误;
B.KIO 中I元素的化合价从+5价降低到0价,反应中KIO 被还原,故B错误;
3 3
C.该反应配平后系数为:1,5,6,3,6,3,故C正确;
D.反应中生成3个I 转移5个 电子,故D错误;
2
故选C。
15.(本题3分)(2021·浙江高三开学考试)某种制备 的反应机理如图。下列说法不正确的是
A.总反应可表示为
B.该过程中 的化合价有0和 两种C. 和 可循环利用
D.①、②、③均为氧化还原反应
【答案】D
【详解】
A.由反应过程图可知,氢气和氧气在[PdC1 ]2-的作用下生成过氧化氢,反应方程式为:
4
,A项正确;
B.Pd元素在[PdC1 ]2-、[PdCl O]2-中的化合价均为+2价,Pd单质是0价,B项正确;
4 2 2
C.依据过程图可知, 和 可循环利用,C项正确;
D.①、②均为氧化还原反应,③不是氧化还原反应,D项错误;
故选D。
二、填空题(共55分)
16.(本题10分)(福建省泉州市泉港区第一中学2019-2020学年高一上学期期中考试化学试题)Ⅰ.下列三
组物质中,均有一种物质的类别与其他三种不同。
①MgO、NaO、CO、CuO
2 2
②HCl、HO、HSO 、HNO
2 2 4 3
③NaOH、NaCO、KOH、Cu(OH)
2 3 2
(1)三种物质依次是(填化学式):①________;②________;③________。
(2)这三种物质相互作用可生成一种新物质NaHCO ,写出该反应的化学反应方程式:_________该反应
3
________(填“是”或“不是”)氧化还原反应。
(3)NaHCO 的电离方程式为__________________________
3
Ⅱ.现有以下物质:①NaCl晶体 ②液态HCl ③CaCO 固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO
3 2
⑧HSO ⑨KOH溶液
2 4
(1)以上物质中能导电的是________。(填序号)
(2)以上物质中属于非电解质的是________。(填序号)
【答案】CO HO NaCO CO+H O+Na CO=2NaHCO 不是 NaHCO =Na++HCO-
2 2 2 3 2 2 2 3 3 3 3
④⑥⑨ ⑤⑦【分析】
Ⅰ.(1)依据物质的性质,组成、结构判断解答;
(2)有化合价变化的反应为氧化还原反应;
(3)NaHCO 在水中完全电离产生Na+、HCO -;
3 3
Ⅱ.电解质:在水溶液中或熔融状态下能导电的化合物;如:酸、碱、盐,金属氧化物等;
非电解质:在水溶液中和熔融状态下不能导电的化合物;如:有机物,非金属氧化物等;
水溶液或者熔融状态能完全电离电离的电解质为强电解质,部分电离的为弱电解质;
物质导电条件:存在自由电子或者存在自由移动的离子。
【详解】
(1)①MgO、NaO、CuO,是金属氧化物,CO 是非金属氧化物,故答案是CO;
2 2 2
②HCl、HSO 、HNO 都是含氧酸,HO是氧化物,故答案是HO;
2 4 3 2 2
③NaOH、KOH、Cu(OH) 都是碱,NaCO 是盐,故答案是NaCO;
2 2 3 2 3
(2)碳酸钠、二氧化碳和水反应生成碳酸氢钠,反应方程式为:CO+H O+Na CO=2NaHCO,在这个反应过
2 2 2 3 3
程中没有化合价变化,因此该反应不属于氧化还原反应;
(3) NaHCO 在水中完全电离产生Na+、HCO -,则电离方程式为:NaHCO =Na++HCO-;
3 3 3 3
Ⅱ.(1)④熔融KCl含有自由移动的离子K+、Cl-,能导电; ⑥铜含有自由电子,能导电;其余物质无自
由移动的电子或离子,不能导电,故能导电的物质序号为:④⑥;
(1)①NaCl晶体,②液态HCl ③CaCO 固体 ④熔融KCl ⑧HSO ⑨KOH固体,在水溶液或者熔融
3 2 4
状态能导电,属于电解质;⑤蔗糖水溶液和熔融状态都不导电,是非电解质;⑦CO 本身不能电离产生自
2
由移动的离子,是非电解质;
所以以上物质中能导电的是:④⑥⑨;属于非电解质的是:⑤⑦。
【点睛】
本题考查了物质的分类,电离方程式、离子方程式的书写。明确有关物质的基本概念,了解物质导电的原
因,熟悉物质电离产生的离子是解题关键,注意物质导电条件。
17.(本题10分)(辽宁省六校协作体2020-2021学年高一上学期第一次联考化学试题)离子反应是中学化
学中重要的反应类型,回答下列问题:
Ⅰ.下列物质:①铜②纯碱③Ba(OH) 固体④Cu (OH) CO⑤盐酸溶液⑥酒精⑦熔融的NaCl⑧二氧化碳
2 2 2 3
(1)属于盐类的是_______。
(2)属于非电解质是_______。
(3)属于电解质的是_______。
Ⅱ.将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、SO 、OH-、CO 和Cl-,取该溶液进行如下实验:
Ⅰ.取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
Ⅱ.取少许溶液滴入BaCl 溶液,无白色沉淀产生。
2
Ⅲ.取少许溶液先滴加硝酸再加AgNO 溶液,产生白色沉淀。
3
Ⅳ.再取少许原溶液滴入少量HSO 溶液,有白色沉淀产生。
2 4
①根据以上现象判断,原溶液中肯定不存在的离子是_______。
②写出实验Ⅲ中可能发生反应的离子方程式_______,_______。
③如溶液中各种离子数相等,确定溶液中_______(填有或无)K+。判断依据是_______。
【答案】②④⑦ ⑥⑧ ②③④⑦ Mg2+、Fe3+、SO 、CO H++OH-=H O Cl-+Ag+=AgCl↓
2
无 溶液中一定有Ba2+、Cl-、OH-,数目相等时电荷守恒,所以无K+
【分析】
Ⅰ.①铜是单质,既不是电解质又不是非电解质;②纯碱是碳酸钠,由金属阳离子和酸根阴离子构成,属于
盐,水溶液能导电,碳酸钠属于电解质;③Ba(OH) 固体由金属阳离子和氢氧根离子构成,属于碱,水溶
2
液能导电,Ba(OH) 属于电解质;④Cu (OH) CO 由金属阳离子、氢氧根离子、碳酸根离子构成,属于盐,
2 2 2 3
熔融状态能导电,属于电解质;⑤盐酸溶液是混合物,既不是电解质又不是非电解质;⑥酒精是有机物,
不能电离,属于非电解质;⑦熔融的NaCl由金属阳离子和酸根离子构成,属于盐,能导电,属于电解质;
⑧二氧化碳是非金属氧化物,自身不能电离,属于非电解质;
【详解】
根据以上分析,(1) ②纯碱、④Cu (OH) CO、⑦熔融的NaCl都由金属阳离子和酸根阴离子构成,属于盐
2 2 3
类的是②④⑦;
(2) ⑥酒精是自身不能电离的化合物,属于非电解质;⑧二氧化碳是自身不能电离的化合物,属于非电解,
属于非电解质是⑥⑧;
(3) ②纯碱是碳酸钠,碳酸钠水溶液能导电,碳酸钠属于电解质;③Ba(OH) 的水溶液能导电,Ba(OH) 属
2 2
于电解质;④Cu (OH) CO 熔融状态能导电,属于电解质;⑦熔融的NaCl能导电,属于电解质;属于电解
2 2 3
质的是②③④⑦;
Ⅱ.将两种化合物一起溶于水得到一种无色透明溶液,说明不含Fe3+;
Ⅰ.取少量溶液滴入紫色石蕊试液,溶液呈蓝色,说明一定含有OH-,一定不含Mg2+;
Ⅱ.取少许溶液滴入BaCl 溶液,无白色沉淀产生,说明一定不含SO 或CO ;
2
Ⅲ.取少许溶液先滴加硝酸再加AgNO 溶液,产生白色沉淀,说明一定含有Cl-;
3Ⅳ.再取少许原溶液滴入少量HSO 溶液,有白色沉淀产生,说明一定含有Ba2+;
2 4
①综上所述,溶液中一定含有Ba2+、Cl-、OH-,一定不含Mg2+、Fe3+、SO 、CO ;
②实验Ⅲ中硝酸和OH-反应生成水,离子方程式是H++OH-=H O;银离子和氯离子反应生成氯化银沉淀,
2
反应的离子方程式是Cl-+Ag+=AgCl↓;
③溶液中一定有Ba2+、Cl-、OH-,离子数目相等时,正负电荷数相等,所以无K+。
【点睛】
本题考查物质分类和离子推断,明确物质分类的依据、离子共存的条件是解题关键,熟悉电解质、非电解
质的定义,掌握常见的离子的性质和反应,会根据电荷守恒判断离子是否存在。
18.(本题10分)(2020·青铜峡市高级中学高三开学考试)正确书写下列离子反应方程式
(1)将少量NaHSO 溶液滴加到Ba(OH) 溶液中,当恰好完全沉淀时,反应的离子方程式为____。
4 2
(2)在酸性条件下,向含铬废水中加入FeSO ,可将 还原为Cr3+,该过程的离子反应方程式为_。
4
(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为____。
(4)MnO 与浓盐酸制备氯气的离子方程式:_____。
2
(5)已知酸性环境下,ClO-可将Mn2+氧化成MnO ,自身被还原成Cl-,该过程的离子反应方程式为_。
2
【答案】Ba2++H++OH-+ =BaSO↓+HO +6Fe2++14H+=2Cr3++6Fe3++7HO ClO-+2I-+HO=
4 2 2 2
I+Cl-+2OH- MnO +4H++2Cl- Mn2++Cl↑+2HO HO+ClO-+Mn2+=MnO +2H++Cl-
2 2 2 2 2 2
【详解】
(1)将少量NaHSO 溶液滴加到Ba(OH) 溶液中,当恰好完全沉淀时生成硫酸钡、氢氧化钠和水,反应的离
4 2
子方程式为Ba2++H++OH-+ =BaSO↓+HO。
4 2
(2)在酸性条件下,向含铬废水中加入FeSO ,可将 还原为Cr3+,其中亚铁离子被氧化为铁离子,则
4
该过程的离子反应方程式为 +6Fe2++14H+=2Cr3++6Fe3++7HO。
2
(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,碘离子被氧化为单质碘,
反应的离子方程式为ClO-+2I-+HO=I+Cl-+2OH-。
2 2(4)MnO 与浓盐酸制备氯气的离子方程式为MnO +4H++2Cl- Mn2++Cl↑+2HO。
2 2 2 2
(5)已知酸性环境下,ClO-可将Mn2+氧化成MnO ,自身被还原成Cl-,根据电子得失守恒可知该过程的离
2
子反应方程式为HO+ClO-+Mn2+=MnO +2H++Cl-。
2 2
19.(本题12分)(2020·河北石家庄二十三中高一月考)回答下列问题:
(1)①H+CuO Cu+H O
2 2
②CaCO +2HCl=CaCl +CO ↑+H O
3 2 2 2
③3S+6NaOH=2Na S+Na SO +3H O
2 2 3 2
④NH NO +Zn=ZnO+N ↑+2H O
4 3 2 2
⑤Cu O+4HCl=2HCuCl +H O。
2 2 2
上述反应中, 属于氧化还原反应的是___________(填序号)。
(2)用双线桥法表示下述反应电了转移的方向和数目___________。MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
(3)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反成来制备单质碘,其化学方程式为
2NaIO +5NaHSO =3NaHSO +2Na SO +I +H O
3 3 4 2 4 2 2
①反应中___________元素被氧化,___________是氧化剂;
②用单线桥标法出电了转移方向和数目___________。
【答案】
(1)①③④
(2)
(3) S NaIO
3
【分析】
(1)
氧化还原反应的特征是元素化合价的升降。在上述反应中,反应①③④中有元素化合价的变化,因此这几个反应为氧化还原反应,因此属于氧化还原反应的序号是①③④。
(2)
在反应MnO +4HCl(浓) MnCl +Cl↑+2H O中,MnO →MnCl ,Mn元素化合价降低2价,得到电子2e-;
2 2 2 2 2 2
HCl→Cl ,Cl元素化合价升高1×2=2价,失去电子2×e-。由于化合价升降最小公倍数是2等于反应过程中
2
电子转移总数,所以用双线桥法表示下述反应电了转移的方向和数目为:
。
(3)
①在反应2NaIO +5NaHSO =3NaHSO +2Na SO +I +H O中,S元素化合价由反应前NaHSO 中的+4价变为
3 3 4 2 4 2 2 3
反应后NaHSO、NaSO 中的+6价,化合价升高,失去电子被氧化,所以S元素被氧化;I元素化合价由
4 2 4
反应前NaIO 中的+5价变为反应后I 中的0价,化合价降低,得到电子被还原,所以NaIO 为氧化剂;
3 2 3
②在反应2NaIO +5NaHSO =3NaHSO +2Na SO +I +H O中,S元素化合价由反应前NaHSO 中的+4价变为
3 3 4 2 4 2 2 3
反应后NaHSO、NaSO 中的+6价,化合价升高2×5=10价,失去电子2×5e-;I元素化合价由反应前NaIO
4 2 4 3
中的+5价变为反应后I 中的0价,化合价降低5×2=10价,得到电子5×2e-,用单线桥法表示电子转移为:
2
。
20.(本题13分)(2020·梅州市梅江区梅州中学高一月考)Ⅰ.实验室可用KMnO 和浓盐酸反应制取氯气,
4
反应原理如下:2KMnO +l6HC1(浓)=2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
(1)用双线桥标出电子得失情况。_______
(2)由此反应可以推断氧化性强弱KMnO _______Cl(填“>”、“<”、“=”)
4 2
(3)浓盐酸在反应中显示出来的性质是_______(填序号)
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(4)若参加反应的HCl是73g,则被氧化的HCl有_______g(保留一位小数点)。
Ⅱ.(5)某同学设计如下实验研究HO 的性质:
2 2序号 实验 实验现象
a.溶液紫色褪去
ⅰ 向5%HO 溶液中滴加酸性KMnO 溶液
2 2 4 b.有大量气泡产生
ⅱ 向5%HO 溶液中滴加淀粉碘化钾溶液 c.溶液变蓝
2 2
①从理论上看HO 既有氧化性又有还原性,具有还原性的原因是_______。
2 2
②能证明HO 具有还原性的实验是_______(填序号)。可作为证据的实验现象是_______(填字母序号)。
2 2
Ⅲ.(6)先将下述反应配平,再用单线桥标出该反应中电子转移的方向和数目。_______OH-+_______ClO-
+_______Fe3+=_______ +_______Cl-+_______H O,_______、_______
2
【答案】 > ② 45.6 过氧化氢中氧元素的化合
价为-1价,化合价可升高,被氧化 ⅰ ab 10OH-+3ClO-+2Fe3+=2 +3Cl-+5H O
2
【详解】
(1)Mn元素得到2×5e-,化合价从+7价降低到+2价,被还原,Cl元素失去10×1e-,化合价从-1升高到0价,
被氧化,用双线桥标出电子得失情况: ,故答案为:
;
(2)Mn元素化合价降低,被还原,KMnO 作氧化剂,Cl元素化合价升高,被氧化,Cl 是氧化产物,因此
4 2
氧化性:KMnO >Cl,故答案为:>;
4 2(3)浓HCl中一部分Cl化合价升高,被氧化,作还原剂,显还原性,一部分Cl化合价不变,显酸性,故答
案为:②;
(4)结合(1)可知,每16molHCl参与反应,有10HCl被氧化,即有 的HCl被氧化,则参加反应的HCl
是73g时,有73× g=45.625g≈45.6g被氧化,故答案为:45.6;
(5)①从理论上看HO 中O为-1价,可升高,被氧化,做还原剂,具有还原性,故答案为:过氧化氢中氧
2 2
元素的化合价为-1价,化合价可升高,被氧化;
②实验ⅰ中酸性高锰酸钾是强氧化剂,酸性高锰酸钾溶液遇到过氧化氢紫色褪去、有大量气泡产生(从反应
物价态看,气体只能是氧气),说明过氧化氢被氧化,过氧化氢体现还原性,故答案为:ⅰ;ab;
(6)Cl元素化合价由+1降低到-1价,降低2,Fe元素化合价由+3价升高到+6价,升高3,则ClO-和Cl-前配
3,Fe3+和 前配2,根据电荷守恒在OH-前配10,最后根据原子守恒在HO前配5,配平后离子方程式
2
为10OH-+3ClO-+2Fe3+=2 +3Cl-+5H O;Cl元素得到3×2e-=6e-,Fe元素失去2×3e-=6e-,用单线桥标出
2
电子转移的方向和数目: ,故答案为:
。关注更新免费领取,淘宝唯一每月更新店铺:知二教育