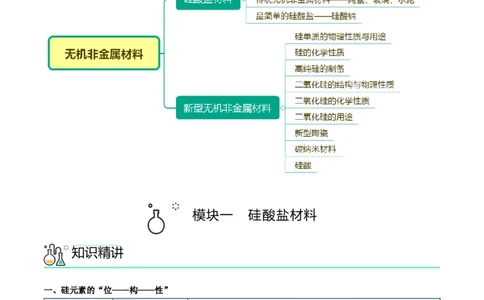
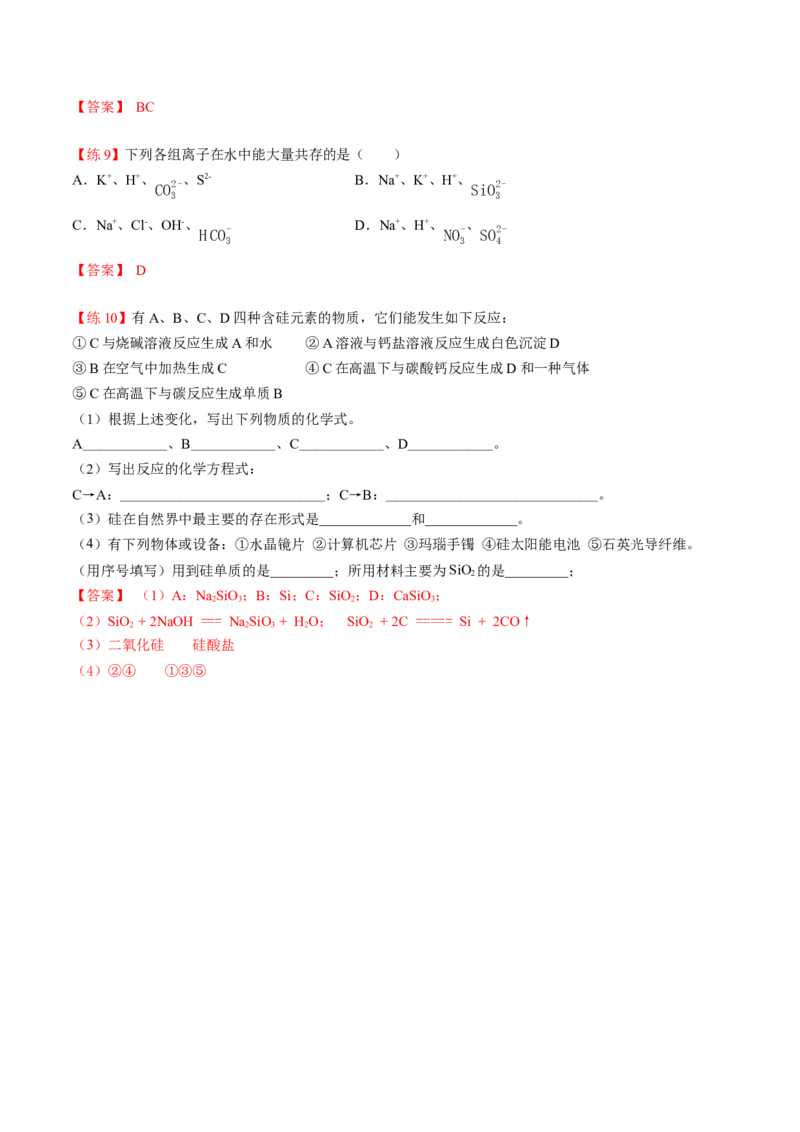文档内容
第 05 讲 无机非金属材料
知识导航
模块一 硅酸盐材料
知识精讲
一、硅元素的“位——构——性”
元素位置 原子结构 元素性质
第三周期
既不容易得到也不容易失去电子,主要形成四价的共价化合物
第IVA族
硅元素在地壳中含量仅次于氧,居第二位。硅有亲氧性,在自然界中仅以________态存在,即硅酸盐和氧
化物的形式。
【答案】化合
二、硅酸盐的概念、结构与特点
1.概念:由硅元素、氧元素和金属元素组成的化合物。2.结构:在硅酸盐中,Si和O构成了硅氧四面体。每个Si结合4个O,Si在中心,O
在四面体的4个顶角;许多这样的四面体还可以通过顶角的 O相互连接,每个O为两
个四面体所共有,与2个Si相结合。
3.特点:硅酸盐材料大多具有硬度高、熔点高、难溶于水、化学性质稳定、耐腐蚀等
特点。
资料卡片——硅酸盐的表示方法
硅酸盐矿物的成分复杂,多用氧化物的形式表示它们的组成,如:
硅酸钠(NaSiO)→ NaO·SiO
2 3 2 2
高岭石(Al HSi O)→Al O·2SiO·2HO
2 4 2 9 2 3 2 2
钾云母(KH Al Si O )→KO·3Al O·6SiO·2HO
2 3 3 12 2 2 3 2 2
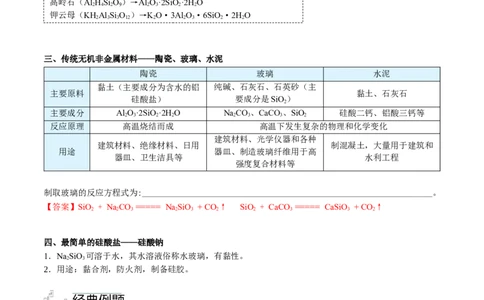
三、传统无机非金属材料——陶瓷、玻璃、水泥
陶瓷 玻璃 水泥
黏土(主要成分为含水的铝 纯碱、石灰石、石英砂(主
主要原料 黏土、石灰石
硅酸盐) 要成分是SiO)
2
主要成分 Al O·2SiO·2HO NaCO、CaCO 、SiO 硅酸二钙、铝酸三钙等
2 3 2 2 2 3 3 2
反应原理 高温烧结而成 高温下发生复杂的物理和化学变化
建筑材料、光学仪器和各种
建筑材料、绝缘材料、日用 制混凝土,大量用于建筑和
用途 器皿、制造玻璃纤维用于高
器皿、卫生洁具等 水利工程
强度复合材料等
制取玻璃的反应方程式为:____________________________________________________________________。
【答案】SiO + NaCO ===== NaSiO + CO↑ SiO + CaCO ===== CaSiO + CO↑
2 2 3 2 3 2 2 3 3 2
四、最简单的硅酸盐——硅酸钠
1.NaSiO 可溶于水,其水溶液俗称水玻璃,有黏性。
2 3
2.用途:黏合剂,防火剂,制备硅胶。
经典例题
传统无机非金属材料
【例1】《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙黏土而为之”“凡坯既成,干燥之后,则
堆积窖中燃薪举火”“浇水转釉(主要为青色),与造砖同法”。下列说法错误的是( )
A.“燃薪举火”使黏土发生了复杂的物理化学变化
B.沙子和黏土的主要成分为硅酸盐
C.烧制后自然冷却成红瓦,浇水冷却成青瓦D.黏土是制作砖瓦和陶瓷的主要原料
【答案】B
【变1-1】最近全面通车的沪昆高速铁路是国家重要的交通线路,在工程建设中用量最大的硅酸盐材料是
( )
A.钢筋 B.水泥 C.玻璃 D.陶瓷
【答案】B
【变1-2】小明参观了举世瞩目的北京大兴国际机场,该机场建设时应用了许多先进技术,其中之一是“重
载水泥混凝土铺面技术”。下列原料可用于制造普通水泥的是( )
A.胆矾 B.纯碱 C.石膏 D.小苏打
【答案】B
模块二 新型无机非金属材料
知识精讲
一、硅单质的物理性质与用途
1.物理性质:硅单质是带有金属光泽的灰黑色固体,其结构与金刚石类似,为空间网状结构,所以晶体
硅的硬度大、熔点高。
2.用途:硅在元素周期表中处于金属与非金属的交界处,晶体硅的导电性介于导体与绝缘体之间,是一
种良好的_________材料,因此晶体硅常用于制作集成电路板(硅芯片)和太阳能电池极板。
【答案】半导体
二、硅的化学性质
1.与非金属单质反应
(1)与F:Si + 2F === SiF ;
2 2 4
(2)与Cl:Si + 2Cl ===== SiCl ;
2 2 4
(3)与O:Si + O ===== SiO ;
2 2 2
(4)与C:Si + C ===== SiC
2.与酸、碱反应
(1)非金属单质一般不与非氧化性酸反应,但Si能与HF反应:Si + 4HF === SiF↑+ 2H↑;
4 2
(2)硅与强碱溶液反应生成氢气:Si + 2NaOH + HO === Na SiO + 2H↑。
2 2 3 2三、硅的制备
制备原理 用焦炭还原石英砂,得到含少量杂质的粗硅,然后转化为三氯硅烷,再经氢气还原。
制备流程
反应方程式
【答案】SiO 2 + 2C ========== Si + 2CO↑ Si + 3HCl ====== SiHCl 3 + H 2 SiHCl 3 + H 2 ====== Si +
3HCl
经典例题
硅的性质
【例2】下列关于硅的说法不正确的是( )
A.硅是非金属元素,但它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质起反应
D.当加热到一定程度时,硅能与氧气、氢气等非金属反应
【答案】C
【变2】有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中
具有重要的作用。下列关于硅的说法不正确的是( )
A.高纯度的单质硅被广泛用于制作计算机芯片
B.硅可由二氧化硅还原制得
C.常温时硅与水、空气和酸不反应,但能与氢氟酸反应
D.自然界硅元素的贮量丰富,并存在大量的单质硅
【答案】D
硅的制备
【例3】芯片是中美经贸摩擦的焦点之一、制造芯片的高纯硅可以用下述方法制取(反应条件略),下列说法
错误的是( )
A.SiCl 中 Si的化合价为+4
4
B.制造芯片的高纯硅具有一定导电性
C.反应①、②、③均为氧化还原反应
D.SiO 既能与碱溶液反应又能与酸溶液反应,SiO 是两性氧化物
2 2【答案】D
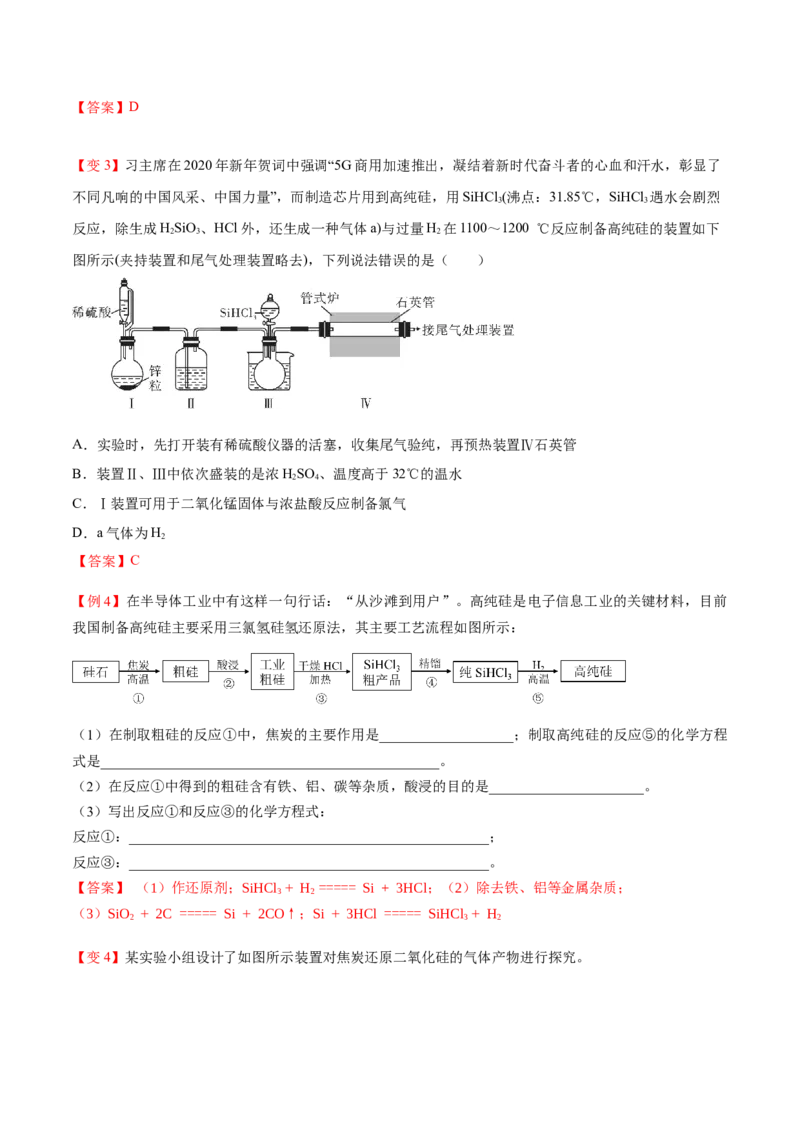
【变3】习主席在2020年新年贺词中强调“5G商用加速推出,凝结着新时代奋斗者的心血和汗水,彰显了
不同凡响的中国风采、中国力量”,而制造芯片用到高纯硅,用SiHCl (沸点:31.85℃,SiHCl 遇水会剧烈
3 3
反应,除生成HSiO、HCl外,还生成一种气体a)与过量H 在1100~1200 ℃反应制备高纯硅的装置如下
2 3 2
图所示(夹持装置和尾气处理装置略去),下列说法错误的是( )
A.实验时,先打开装有稀硫酸仪器的活塞,收集尾气验纯,再预热装置Ⅳ石英管
B.装置Ⅱ、Ⅲ中依次盛装的是浓HSO 、温度高于32℃的温水
2 4
C.Ⅰ装置可用于二氧化锰固体与浓盐酸反应制备氯气
D.a气体为H
2
【答案】C
【例4】在半导体工业中有这样一句行话:“从沙滩到用户”。高纯硅是电子信息工业的关键材料,目前
我国制备高纯硅主要采用三氯氢硅氢还原法,其主要工艺流程如图所示:
(1)在制取粗硅的反应①中,焦炭的主要作用是___________________;制取高纯硅的反应⑤的化学方程
式是________________________________________________。
(2)在反应①中得到的粗硅含有铁、铝、碳等杂质,酸浸的目的是______________________。
(3)写出反应①和反应③的化学方程式:
反应①:___________________________________________________;
反应③:___________________________________________________。
【答案】 (1)作还原剂;SiHCl + H ===== Si + 3HCl;(2)除去铁、铝等金属杂质;
3 2
(3)SiO + 2C ===== Si + 2CO↑;Si + 3HCl ===== SiHCl + H
2 3 2
【变4】某实验小组设计了如图所示装置对焦炭还原二氧化硅的气体产物进行探究。已知: 溶液可用于检验CO,反应的化学方程式为 (产生黑
色金属钯,使溶液变浑浊)。
(1)实验时要长时间通入 ,其目的是________________________________。
(2)装置B的作用是__________________________________________________。
(3)装置C、D中所盛试剂分别为_____________、_____________,若装置C,D中溶液均变浑浊,且经
检测两气体产物的物质的量相等,则该反应的化学方程式为__________________________。
(4)该装置的缺点是__________________________________________________。
【答案】(1)排尽装置内的空气,避免空气中的 、 ,水蒸气对实验产生干扰
(2)作安全瓶,防止倒吸
(3)澄清石灰水 溶液
(4)无尾气吸收装置
知识精讲
资料卡片——SiO 的结构与物理性质
2
如图所示,二氧化硅晶体是由Si原子和O原子按1:2的比例所组成的立体网状
结构的晶体,所以我们通常用SiO 来表示二氧化硅的组成。
2
SiO 是不溶于水的固体,熔、沸点高,硬度大。
2
四、SiO 的化学性质
2
1.二氧化硅虽然不溶于水,但它是一种酸性氧化物
(1)与NaOH反应:_______________________________________;(2)与CaO反应:SiO + CaO ===== CaSiO
2 3
2.二氧化硅的特性
与HF反应:_______________________________________________;
3.二氧化硅可与某些盐反应制备玻璃
SiO + NaCO ===== NaSiO + CO↑ SiO + CaCO ===== CaSiO + CO↑
2 2 3 2 3 2 2 3 3 2
【答案】(1)SiO + 2NaOH === NaSiO + HO (2)SiO + 4HF === SiF↑+ 2HO
2 2 3 2 2 4 2
及时小练
指出下列反应中二氧化硅主要表现的化学性质或作用(只选一个)。
(1)SiO + 2NaOH === Na SiO + HO( )
2 2 3 2
(2)SiO + Na CO ===== Na SiO + CO↑( )
2 2 3 2 3 2
(3)SiO + 2C ===== Si + 2CO↑( )
2
(4)SiO + 3C ===== SiC + 2CO↑( )
2
(5)SiO + 4HF === SiF↑+ 2HO( )
2 4 2
A.作为玻璃的成分被消耗而使玻璃被腐蚀
B.氧化性
C.酸性氧化物的通性
D.将挥发性的酸酐从其盐中“置换”出来
E.未参加氧化还原反应
【答案】 (1)C;(2)D;(3)B;(4)E;(5)A
五、SiO 的用途
2
1.用于生产____________;
2.水晶、玛瑙等饰品;
3.制作耐高温的化学仪器。
【答案】光导纤维
明辨是非
(1)SiO 是一种空间立体网状结构的晶体,熔点高,硬度大( )
2
(2)硅石常用作光导纤维、光学仪器的原料( )
(3)SiO 既能与KOH溶液反应又能与浓盐酸反应( )
2
(4)SiO、NaOH、HF三者两两均能反应( )
2
(5)SiO 可与HF反应,因而氢氟酸不能保存在玻璃瓶中( )
2
(6)可用石英坩埚加热NaOH固体( )
【答案】 (1)~(3)√√× ; (4)~(6)√√×六、新型陶瓷
新型陶瓷包括高温结构陶瓷、压电陶瓷、透明陶瓷和超导陶瓷等,在组成上不再限于传统的硅酸盐体
系,在光学、热学、电学、磁学等方面具有很多新的特性和功能。
例如,碳化硅(SiC)俗称金刚砂,其中的碳原子和硅原子通过共价键连接,具有类似金刚石的结构,
硬度很大,可用作砂纸和砂轮的磨料。碳化硅还具有优异的高温抗氧化性能,使用温度可达1600℃,大大
超过了普通金属材料所能承受的温度,可用作耐高温结构材料、耐高温半导体材料等。
资料卡片——新型陶瓷
①高温结构陶瓷:一般用碳化硅、氮化硅或某些金属氧化物等在高温下烧结而成,具有耐高温、抗氧
化、耐磨蚀等优良性能。与金属材料相比,更能适应严酷的环境,可用于火箭发动机、汽车发动机和
高温电极材料等。
②压电陶瓷:主要有钛酸盐和锆酸盐等,能实现机械能与电能的相互转化,可用于滤波器、扬声器、
超声波探伤器和点火器等。
③透明陶瓷:主要有氧化铝、氧化钇等氧化物透明陶瓷和氮化铝、氟化钙等非氧化物透明陶瓷,具有
优异的光学性能,耐高温,绝缘性好,可用于高压钠灯、激光器和高温探测窗等。
④超导陶瓷:在某一临界温度下电阻为零,具有超导性,用于电力、交通、医疗等领域。
七、碳纳米材料
碳纳米材料是近年来人们十分关注的一类新型无机非金属材料,主要包括富勒烯、碳纳米管、石墨烯等,
在能源、信息、医药等领域有着广阔的应用前景。
富勒烯 碳纳米管 石墨烯
由碳原子构成的一系列笼形分子 由石墨片层卷成的管状物, 只有一个碳原子直径厚度的单层石
的总称,其中的C 是富勒烯的 具有纳米尺度的直径。比表 墨,其独特的结构使其电阻率低、热
60
代表物。C 的发现为纳米科学提 面积大,有相当高的强度和 导率高,具有很高的强度。其在光电
60
供了重要的研究对象,开启了碳 优良的电学性能,可用于生 器件、超级电容器、电池和复合材料
纳米材料研究和应用的新时代。 产复合材料、电池和传感器 等方面的应用研究正在不断深入。
等。八、硅酸
1.HSiO 的弱酸性:硅酸是难溶于水的弱酸,其酸性比碳酸弱。
2 3
2.HSiO 的不稳定性:硅酸受热易分解,HSiO ===== SiO + HO。
2 3 2 3 2 2
3.硅酸的制备(强酸制弱酸):
NaSiO + 2HCl === 2NaCl + HSiO(胶体)
2 3 2 3
NaSiO + CO + HO === HSiO(胶体) + NaCO
2 3 2 2 2 3 2 3
经典例题
SiO 的性质
2
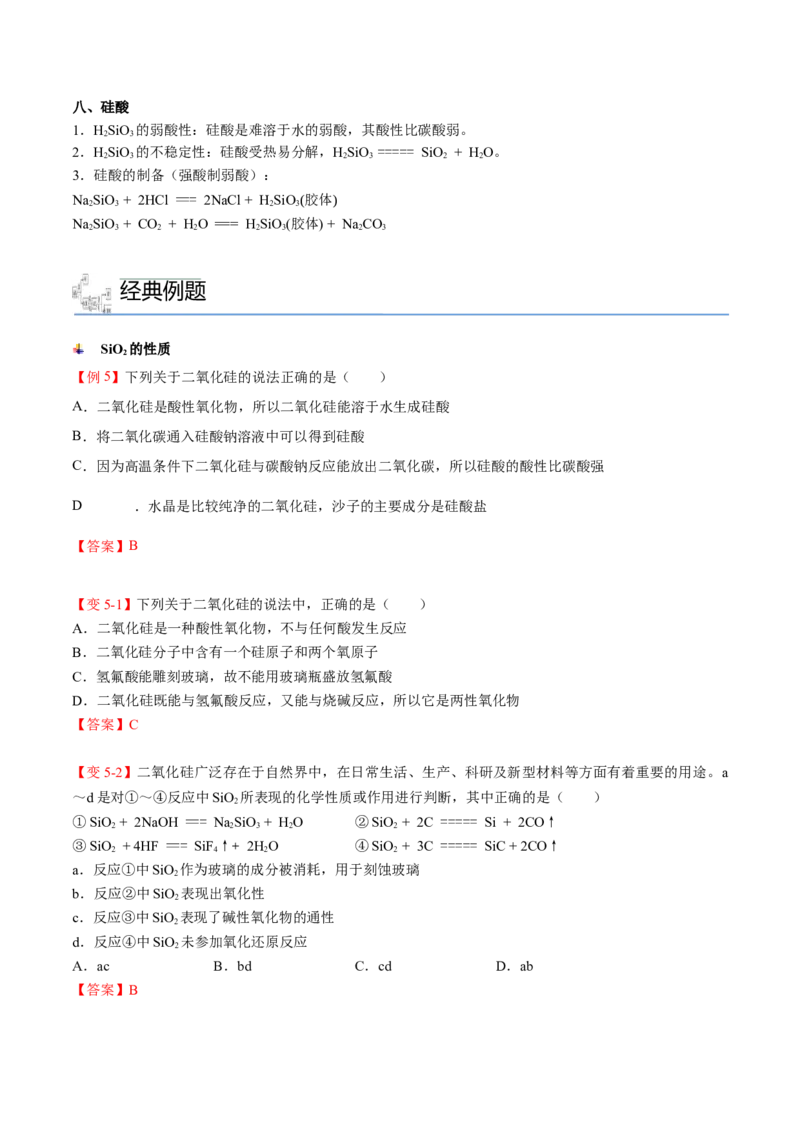
【例5】下列关于二氧化硅的说法正确的是( )
A.二氧化硅是酸性氧化物,所以二氧化硅能溶于水生成硅酸
B.将二氧化碳通入硅酸钠溶液中可以得到硅酸
C.因为高温条件下二氧化硅与碳酸钠反应能放出二氧化碳,所以硅酸的酸性比碳酸强
D .水晶是比较纯净的二氧化硅,沙子的主要成分是硅酸盐
【答案】B
【变5-1】下列关于二氧化硅的说法中,正确的是( )
A.二氧化硅是一种酸性氧化物,不与任何酸发生反应
B.二氧化硅分子中含有一个硅原子和两个氧原子
C.氢氟酸能雕刻玻璃,故不能用玻璃瓶盛放氢氟酸
D.二氧化硅既能与氢氟酸反应,又能与烧碱反应,所以它是两性氧化物
【答案】C
【变5-2】二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等方面有着重要的用途。a
~d是对①~④反应中SiO 所表现的化学性质或作用进行判断,其中正确的是( )
2
①SiO + 2NaOH === NaSiO + HO ②SiO + 2C ===== Si + 2CO↑
2 2 3 2 2
③SiO + 4HF === SiF↑+ 2HO ④SiO + 3C ===== SiC + 2CO↑
2 4 2 2
a.反应①中SiO 作为玻璃的成分被消耗,用于刻蚀玻璃
2
b.反应②中SiO 表现出氧化性
2
c.反应③中SiO 表现了碱性氧化物的通性
2
d.反应④中SiO 未参加氧化还原反应
2
A.ac B.bd C.cd D.ab
【答案】BSiO 的用途
2
【例6】下列物品的主要成分不是SiO 的是( )
2
A.水泥 B.玛瑙饰物 C.光导纤维 D.水晶花瓶
【答案】A
新型无机非金属材料
【例7】下列哪些材料是新型无机材料( )
① 氧化铝陶瓷 ② 氮化硅陶瓷 ③ 碳化硅陶瓷 ④ 氮化铝陶瓷
⑤ 氮化钛陶瓷 ⑥ 硅化硼陶瓷 ⑦ 二硅化铜陶瓷
A.①②③ B.①③④⑤ C.①⑤⑥ D.全部
【答案】D
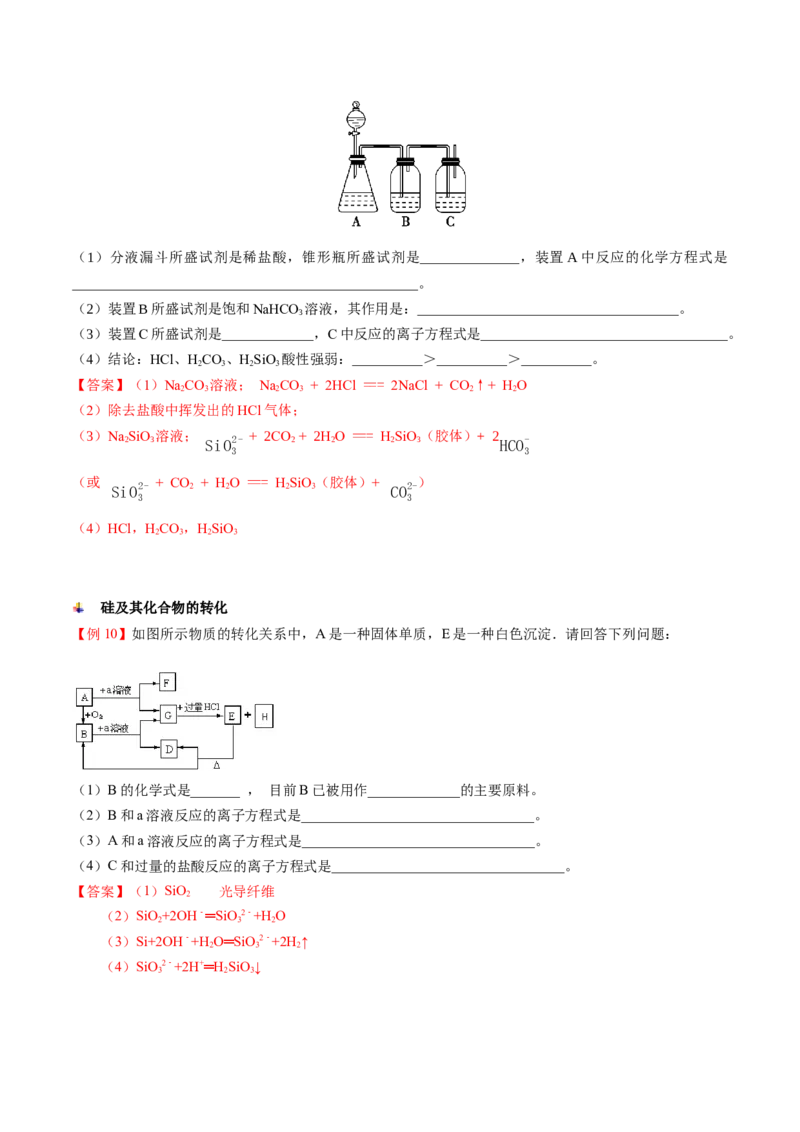
【变7-1】石墨烯目前是世上最薄却也是最坚硬的纳米材料,它是一种透明、良好的导体;石墨烯是由碳
原子构成的单层二维蜂窝状晶格结构(如图所示)的一种碳单质新材料,它是构建富勒烯、碳纳米管的基
本单元。利用石墨烯可制造晶体管、太阳能电池板等。下列有关石墨烯的说法不正确的是( )
A.石墨烯具有优良的导电、导热性能
B.石墨烯是一种新型的无机非金属材料
C.石墨烯与富勒烯的结构相同
D.石墨烯、富勒烯、碳纳米管都是由碳元素组成的
【答案】C
【变7-2】澳大利亚科学家发现了纯碳新材料“碳纳米泡沫”,每个泡沫含有约4 000个碳原子,直径约6~9
nm,在低于-183 ℃时,泡沫具有永久磁性,下列叙述正确的是( )
A.“碳纳米泡沫”与石墨互为同位素
B.把“碳纳米泡沫”分散到适当的溶剂中,能产生丁达尔效应
C.“碳纳米泡沫”是一种新型的碳化合物
D.“碳纳米泡沫”和金刚石的性质相同【答案】B
【变7-3】硅是构成无机非金属材料的一种主要元素,下列有关硅的化合物的叙述错误的是( )
A.氮化硅陶瓷是一种新型无机非金属材料,其化学式为Si N
3 4
B.碳化硅(SiC)的硬度大,熔点高,可用于制作高温结构陶瓷和轴承
C.光导纤维是一种新型无机非金属材料,遇强碱不会“断路”
D.磷酸钙陶瓷可以用于制造人造骨骼,这是利用了该材料的生物特性
【答案】 C
【例8】氮化硅陶瓷因其熔点高,对于金属及氧化物熔体具有相当的高温稳定性,越来越多被应用于热工
各个领域,如陶瓷烧成棚板、辊棒,以及高温轴承、涡轮叶片等,工业上曾普遍采用高纯硅与纯氮在1300
℃时反应获得。
(1)下列关于氮化硅陶瓷的说法正确的是________。
A.硅粉合成氮化硅的反应属于氧化还原反应
B.氮化硅陶瓷属于硅酸盐
C.氮化硅陶瓷可用于制造磨刀材料
D.太阳能光伏产业的主体材料为氮化硅
(2)在烧结氮化硅陶瓷的过程中,二氧化硅、碳、氮气以物质的量之比3:6:2反应生成两种化合物。
①该反应的化学方程式为_________________________________________________。
②该反应中氧化剂与还原剂的质量比为________。
(3)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应。试推测该陶瓷被氢氟酸腐蚀的化
学方程式:________________________________________。
(4)现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅及氯化氢,反应
的化学方程式为________________________________________。
【答案】(1)AC (2)3SiO+2N+6C=====Si N+6CO 7:9
2 2 3 4
(3)SiN+12HF===3SiF↑+4NH↑ (4)3SiCl+2N+6H=====SiN+12HCl
3 4 4 3 4 2 2 3 4
硅酸的制备
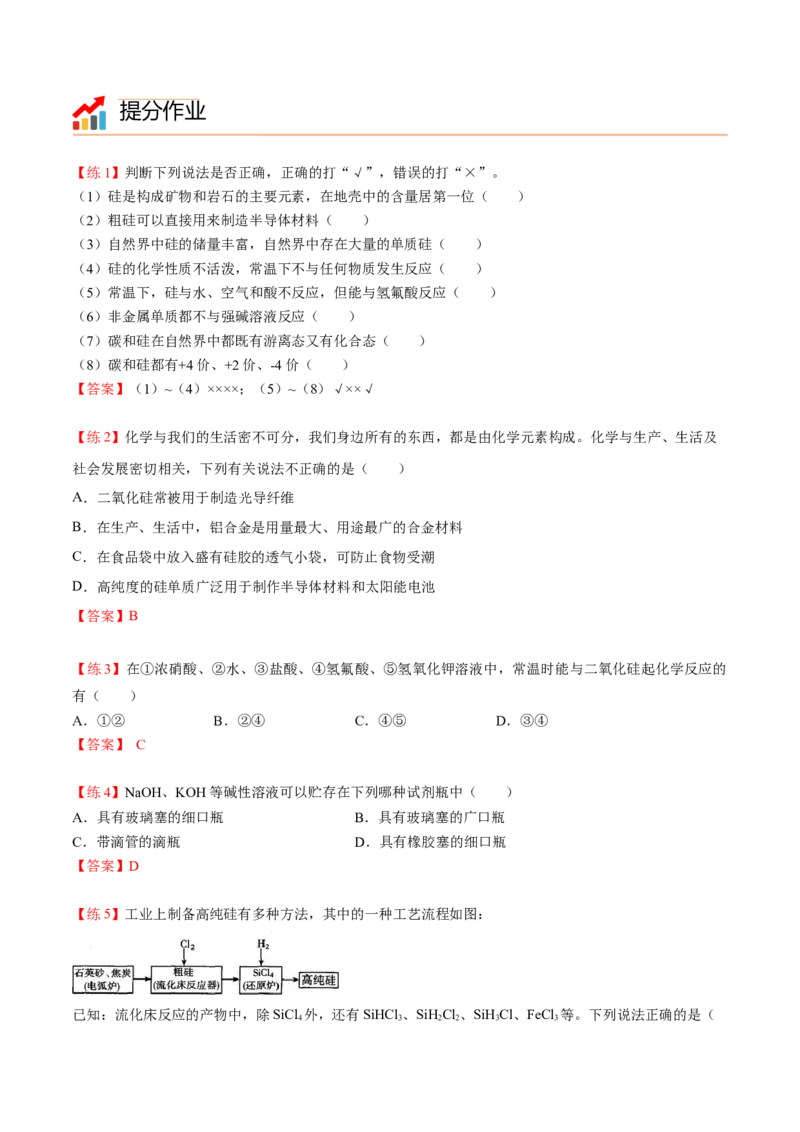
【例9】利用“强酸制弱酸”原理可用来设计酸性强弱比较的实验,如比较HCl、HCO、HSiO 酸性强弱:
2 3 2 3(1)分液漏斗所盛试剂是稀盐酸,锥形瓶所盛试剂是______________,装置A中反应的化学方程式是
_________________________________________________。
(2)装置B所盛试剂是饱和NaHCO 溶液,其作用是:_____________________________________。
3
(3)装置C所盛试剂是_____________,C中反应的离子方程式是___________________________________。
(4)结论:HCl、HCO、HSiO 酸性强弱:__________>__________>__________。
2 3 2 3
【答案】(1)NaCO 溶液; NaCO + 2HCl === 2NaCl + CO↑+ HO
2 3 2 3 2 2
(2)除去盐酸中挥发出的HCl气体;
(3)NaSiO 溶液; + 2CO + 2HO === HSiO(胶体)+ 2
2 3 SiO2- 2 2 2 3 HCO-
3 3
(或 + CO + HO === HSiO(胶体)+ )
SiO2- 2 2 2 3 CO2-
3 3
(4)HCl,HCO,HSiO
2 3 2 3
硅及其化合物的转化
【例10】如图所示物质的转化关系中,A是一种固体单质,E是一种白色沉淀.请回答下列问题:
(1)B的化学式是_______ , 目前B已被用作_____________的主要原料。
(2)B和a溶液反应的离子方程式是_________________________________。
(3)A和a溶液反应的离子方程式是_________________________________。
(4)C和过量的盐酸反应的离子方程式是_________________________________。
【答案】(1)SiO 光导纤维
2
(2)SiO+2OH﹣═SiO 2﹣+H O
2 3 2
(3)Si+2OH﹣+H O═SiO 2﹣+2H ↑
2 3 2
(4)SiO2﹣+2H+═H SiO↓
3 2 3提分作业
【练1】判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)硅是构成矿物和岩石的主要元素,在地壳中的含量居第一位( )
(2)粗硅可以直接用来制造半导体材料( )
(3)自然界中硅的储量丰富,自然界中存在大量的单质硅( )
(4)硅的化学性质不活泼,常温下不与任何物质发生反应( )
(5)常温下,硅与水、空气和酸不反应,但能与氢氟酸反应( )
(6)非金属单质都不与强碱溶液反应( )
(7)碳和硅在自然界中都既有游离态又有化合态( )
(8)碳和硅都有+4价、+2价、-4价( )
【答案】(1)~(4)××××;(5)~(8)√××√
【练2】化学与我们的生活密不可分,我们身边所有的东西,都是由化学元素构成。化学与生产、生活及
社会发展密切相关,下列有关说法不正确的是( )
A.二氧化硅常被用于制造光导纤维
B.在生产、生活中,铝合金是用量最大、用途最广的合金材料
C.在食品袋中放入盛有硅胶的透气小袋,可防止食物受潮
D.高纯度的硅单质广泛用于制作半导体材料和太阳能电池
【答案】B
【练3】在①浓硝酸、②水、③盐酸、④氢氟酸、⑤氢氧化钾溶液中,常温时能与二氧化硅起化学反应的
有( )
A.①② B.②④ C.④⑤ D.③④
【答案】 C
【练4】NaOH、KOH等碱性溶液可以贮存在下列哪种试剂瓶中( )
A.具有玻璃塞的细口瓶 B.具有玻璃塞的广口瓶
C.带滴管的滴瓶 D.具有橡胶塞的细口瓶
【答案】D
【练5】工业上制备高纯硅有多种方法,其中的一种工艺流程如图:
已知:流化床反应的产物中,除SiCl 外,还有SiHCl 、SiHCl、SiHCl、FeCl 等。下列说法正确的是(
4 3 2 2 3 3)
A.电弧炉中发生的反应为C+SiO CO↑+Si
2 2
B.SiCl 进入还原炉之前需要经过蒸馏提纯
4
C.每生成1mol高纯硅,需要44.8LCl 标准状况
2
D.该工艺Si的产率高且无副产物,符合绿色化学要求
【答案】B
【练6】含硅元素的物质有很多用途,下列说法不正确的是( )
A.硅晶片是生产芯片的基础材料,其主要成分为
B.高压输电线路使用的陶瓷绝缘材料属于硅酸盐材料
C.水玻璃是硅酸钠的水溶液,可用作木材防火剂的原料
D.高温超导陶瓷具有超导性,可应用于电力和交通领域
【答案】A
【练7】世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“中国至少在距今3 000年以前,就
已经使用玻璃了。”下列有关普通玻璃的说法不正确的是( )
A.制普通玻璃的原料主要是纯碱、石灰石和石英
B.玻璃在加热熔化时有固定的熔点
C.普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅
D.盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅反应生成硅酸钠而使瓶塞与瓶口粘
在一起
【答案】B
【练8】(双选)下列离子方程式不正确的是( )
A.石英与烧碱反应:SiO + 2OH- === + HO
2 SiO2- 2
3
B.硅与烧碱反应:Si + 2OH- === + H↑
SiO2- 2
3
C.硅酸钠溶液中通入少量CO: + 2CO + 2HO === + HSiO↓
2 SiO2- 2 2 HCO- 2 3
3 3
D.往水玻璃中加入盐酸:2H+ + === HSiO↓
SiO2- 2 3
3【答案】 BC
【练9】下列各组离子在水中能大量共存的是( )
A.K+、H+、 、S2- B.Na+、K+、H+、
CO2- SiO2-
3 3
C.Na+、Cl-、OH-、 D.Na+、H+、 、
HCO- NO- SO2-
3 3 4
【答案】 D
【练10】有A、B、C、D四种含硅元素的物质,它们能发生如下反应:
①C与烧碱溶液反应生成A和水 ②A溶液与钙盐溶液反应生成白色沉淀D
③B在空气中加热生成C ④C在高温下与碳酸钙反应生成D和一种气体
⑤C在高温下与碳反应生成单质B
(1)根据上述变化,写出下列物质的化学式。
A____________、B____________、C____________、D____________。
(2)写出反应的化学方程式:
C→A:_____________________________;C→B:______________________________。
(3)硅在自然界中最主要的存在形式是_____________和_____________。
(4)有下列物体或设备:①水晶镜片 ②计算机芯片 ③玛瑙手镯 ④硅太阳能电池 ⑤石英光导纤维。
(用序号填写)用到硅单质的是_________;所用材料主要为SiO 的是_________;
2
【答案】 (1)A:NaSiO;B:Si;C:SiO;D:CaSiO ;
2 3 2 3
(2)SiO +2NaOH === Na SiO + HO; SiO +2C ===== Si + 2CO↑
2 2 3 2 2
(3)二氧化硅 硅酸盐
(4)②④ ①③⑤