文档内容
《化学反应的热效应》单元测试(基础巩固)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共51分)
1.(本题3分) 关于能量转化,下列说法不正确的是
A.燃气灶具中的能量转化:化学能主要转化为光能
B.太阳能电池的能量转化:光能(太阳能)→电能
C.生物光合作用中的能量转化:光能(太阳能)→生物质能(化学能)
杨sir化学,侵权必究
D.化学反应过程中,除了物质变化外,一定伴有能量变化
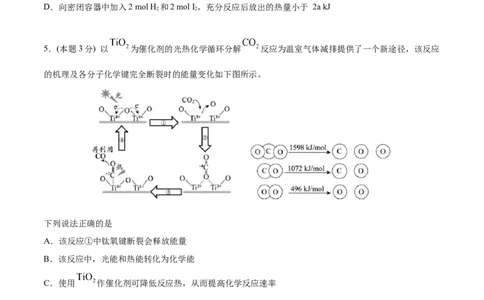
2.(本题3分) 如图所示,有关化学反应和能量变化的说法正确的是
A.铝热反应属于氧化还原反应,故能量变化不符合该图
B.Ba(OH) ·8H O晶体和NH Cl晶体反应能量变化如图所示
2 2 4
C.反应物总键能小于产物总键能的反应符合该图的能量变化
D.符合该能量变化的化学反应均可用于设计成原电池
3.(本题3分) 下列关于中和反应反应热测定实验的说法不正确的是
A.简易量热计的隔热层是为了减少实验过程中的热量损失
B.使用玻璃搅拌器既可以搅拌又避免损坏温度计
C.向盛装酸的量热计内筒中加碱时要小心缓慢
D.测酸液温度后的温度计要用水清洗擦干后再测碱液的温度
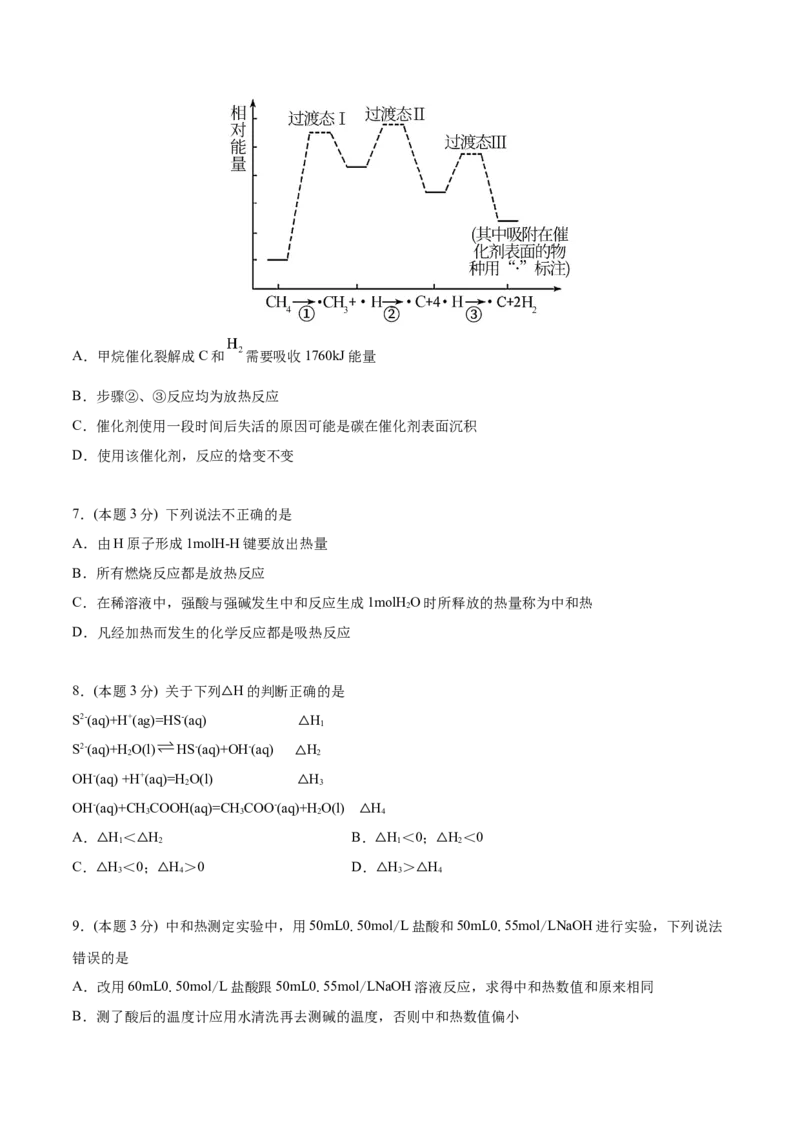
4.(本题3分) H 和 I 在一定条件下能发生反应:H(g)+I(g) 2HI(g) ΔH=—a kJ·mol-1,已知:a、
2 2 2 2
b、c均大于零,下列说法不正确的是A.反应物的总能量高于生成物的总能量
B.断开 1 mol H—H 键所需能量小于断开1 mol I—I键所需能量
C.断开 2 mol H—I键所需能量约为(c+b+a) kJ
D.向密闭容器中加入2 mol H 和2 mol I ,充分反应后放出的热量小于 2a kJ
2 2
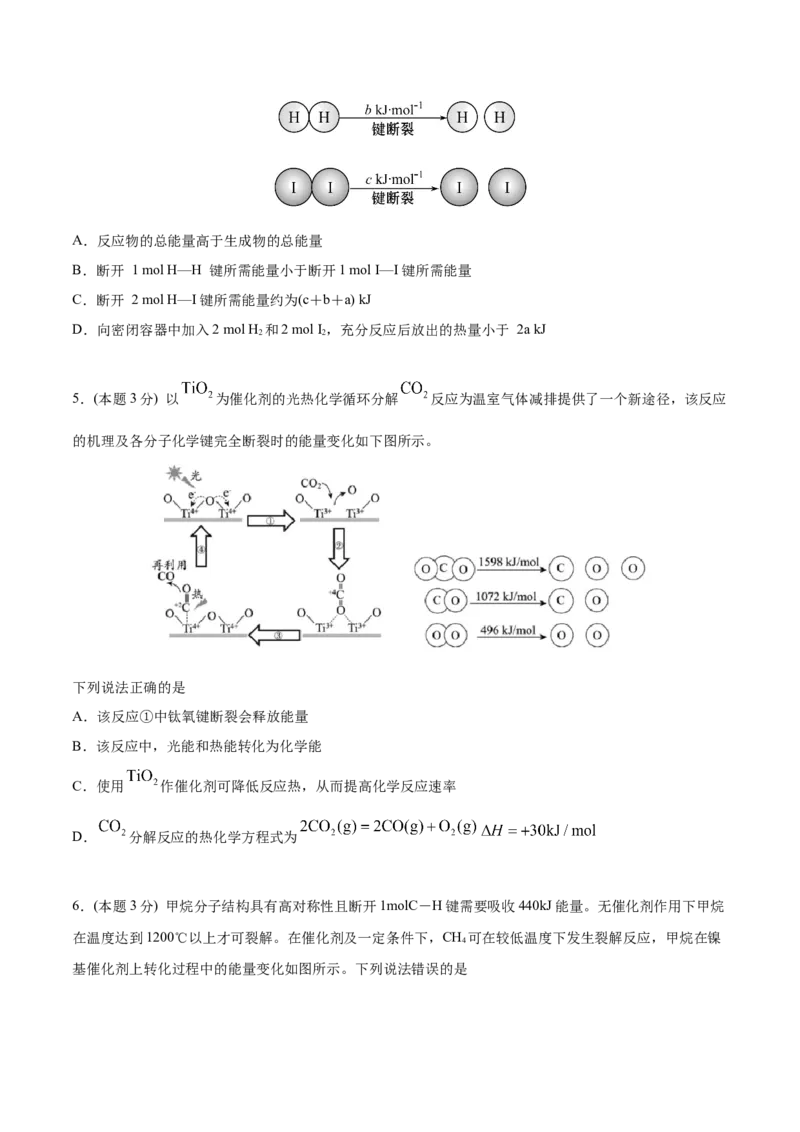
5.(本题3分) 以 为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应
的机理及各分子化学键完全断裂时的能量变化如下图所示。
杨sir化学,侵权必究
下列说法正确的是
A.该反应①中钛氧键断裂会释放能量
B.该反应中,光能和热能转化为化学能
C.使用 作催化剂可降低反应热,从而提高化学反应速率
D. 分解反应的热化学方程式为
6.(本题3分) 甲烷分子结构具有高对称性且断开1molC-H键需要吸收440kJ能量。无催化剂作用下甲烷
在温度达到1200℃以上才可裂解。在催化剂及一定条件下,CH 可在较低温度下发生裂解反应,甲烷在镍
4
基催化剂上转化过程中的能量变化如图所示。下列说法错误的是A.甲烷催化裂解成C和 需要吸收1760kJ能量
B.步骤②、③反应均为放热反应
C.催化剂使用一段时间后失活的原因可能是碳在催化剂表面沉积
D.使用该催化剂,反应的焓变不变
7.(本题3分) 下列说法不正确的是
A.由H原子形成1molH-H键要放出热量
B.所有燃烧反应都是放热反应
C.在稀溶液中,强酸与强碱发生中和反应生成1molH O时所释放的热量称为中和热
2
D.凡经加热而发生的化学反应都是吸热反应
8.(本题3分) 关于下列 H的判断正确的是
S2-(aq)+H+(ag)=HS-(aq) △ H 1
S2-(aq)+H
2
O(l) HS-(aq)+OH-(aq) △H
2
OH-(aq) +H+(aq)=H
2
O(l) △H
3
OH-(aq)+CH
3
COOH(aq)=CH
3
COO-(aq)△+H
2
O(l) H
4
A. H
1
< H
2
B△. H
1
<0; H
2
<0
C.△H
3
<0△; H
4
>0 D.△H
3
> H△4
△ △ △ △
9.(本题3分) 中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法
错误的是
A.改用60mL0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液反应,求得中和热数值和原来相同
B.测了酸后的温度计应用水清洗再去测碱的温度,否则中和热数值偏小C.酸碱混合时,量筒中NaOH溶液应慢慢倒入小烧杯中以免溶液溅出,再用环形玻璃搅拌棒搅拌
D.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热、减少热量损失
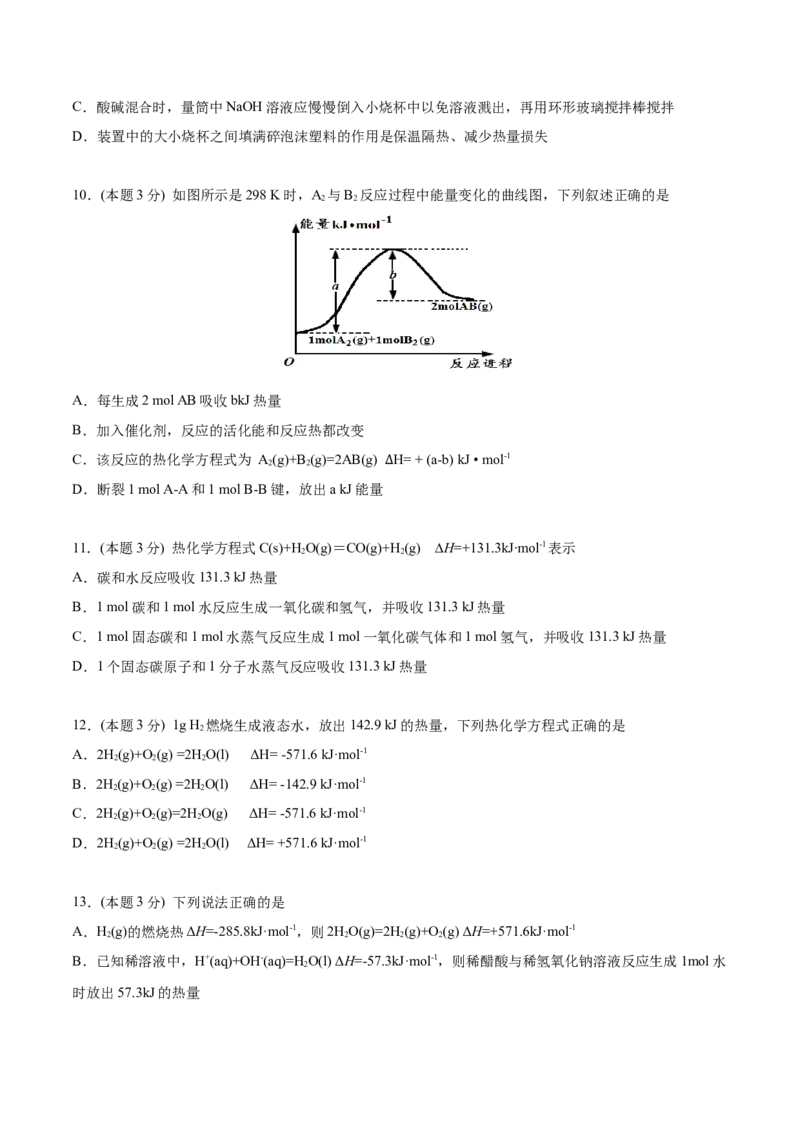
10.(本题3分) 如图所示是298 K时,A 与B 反应过程中能量变化的曲线图,下列叙述正确的是
2 2
A.每生成2 mol AB吸收bkJ热量
B.加入催化剂,反应的活化能和反应热都改变
C.该反应的热化学方程式为 A(g)+B (g)=2AB(g) H= + (a-b) kJ • mol-1
2 2
D.断裂1 mol A-A和1 mol B-B键,放出a kJ能量∆
11.(本题3分) 热化学方程式C(s)+HO(g)=CO(g)+H(g) ∆H=+131.3kJ∙mol-1表示
2 2
A.碳和水反应吸收131.3 kJ热量
B.1 mol碳和1 mol水反应生成一氧化碳和氢气,并吸收131.3 kJ热量
C.1 mol固态碳和1 mol水蒸气反应生成1 mol一氧化碳气体和1 mol氢气,并吸收131.3 kJ热量
D.1个固态碳原子和1分子水蒸气反应吸收131.3 kJ热量
12.(本题3分) 1g H 燃烧生成液态水,放出142.9 kJ的热量,下列热化学方程式正确的是
2
A.2H(g)+O(g) =2H O(l) ΔH= -571.6 kJ·mol-1
2 2 2
B.2H(g)+O(g) =2H O(l) ΔH= -142.9 kJ·mol-1
2 2 2
C.2H(g)+O(g)=2HO(g) ΔH= -571.6 kJ·mol-1
2 2 2
D.2H(g)+O(g) =2H O(l) ΔH= +571.6 kJ·mol-1
2 2 2
13.(本题3分) 下列说法正确的是
A.H(g)的燃烧热ΔH=-285.8kJ·mol-1,则2HO(g)=2H (g)+O(g) ΔH=+571.6kJ·mol-1
2 2 2 2
B.已知稀溶液中,H+(aq)+OH-(aq)=H O(l) ΔH=-57.3kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol水
2
时放出57.3kJ的热量C.C(g)+ O(g)=CO(g) ΔH=-110.52kJ·mol-1,则碳的燃烧热ΔH=-110.52kJ·mol-1
2
D.C(石墨,s)=C(金刚石,s) ΔH>0,说明石墨比金刚石稳定
14.(本题3分) 已知:1mol晶体硅中含有2molSi—Si键,1molSiO 中含有4molSi—O键。有关键能数据
2
如下表:
化学键 Si—O O=O Si—Si
键能/kJ·mol-1 x 500 180
晶体硅在氧气中燃烧的热化学方程式:Si(s)+O(g)=SiO (s) ΔH=-990kJ·mol-1,则表中的x的值为
2 2
A.462.5 B.460 C.920 D.423.3
15.(本题3分) 下列各组热化学方程式中,化学反应的ΔH前者大于后者的是
A.C(s)+O(g)=CO (g);C(s)+ O(g)=CO(g)
2 2 2
B.S(s)+O (g)=SO(g);S(g)+O(g)=SO(g)
2 2 2 2
C.2H(g)+O(g)=2HO(l);H(g)+ O(g)=HO(l)
2 2 2 2 2 2
D.2KOH(aq)+H SO (浓)=K SO (aq)+2H O(l);2KOH(aq)+H SO (aq)=K SO (aq)+2H O(l)
2 4 2 4 2 2 4 2 4 2
16.(本题3分) 已知:①
②
③
则下列说法正确的是
A. 的燃烧热
B.
C.等质量的 和 完全燃烧生成 和液态水, 放出的热量多
D. 在足量氧气中完全燃烧生成气态水放出的热量大于571.6kJ17.(本题3分) 已知:HO(l)=HO(g) ΔH=+Q kJ·mol-1
2 2 1
2HO(g)=2H (g)+O(g) ΔH=+Q kJ·mol-1
2 2 2 2
CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-Q kJ·mol-1
4 2 2 2 3
则H 和CH 的燃烧热的比值为
2 4
A. B. C. D.
二、填空题(共37分)
18.(本题8分) 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请
回答下列问题:
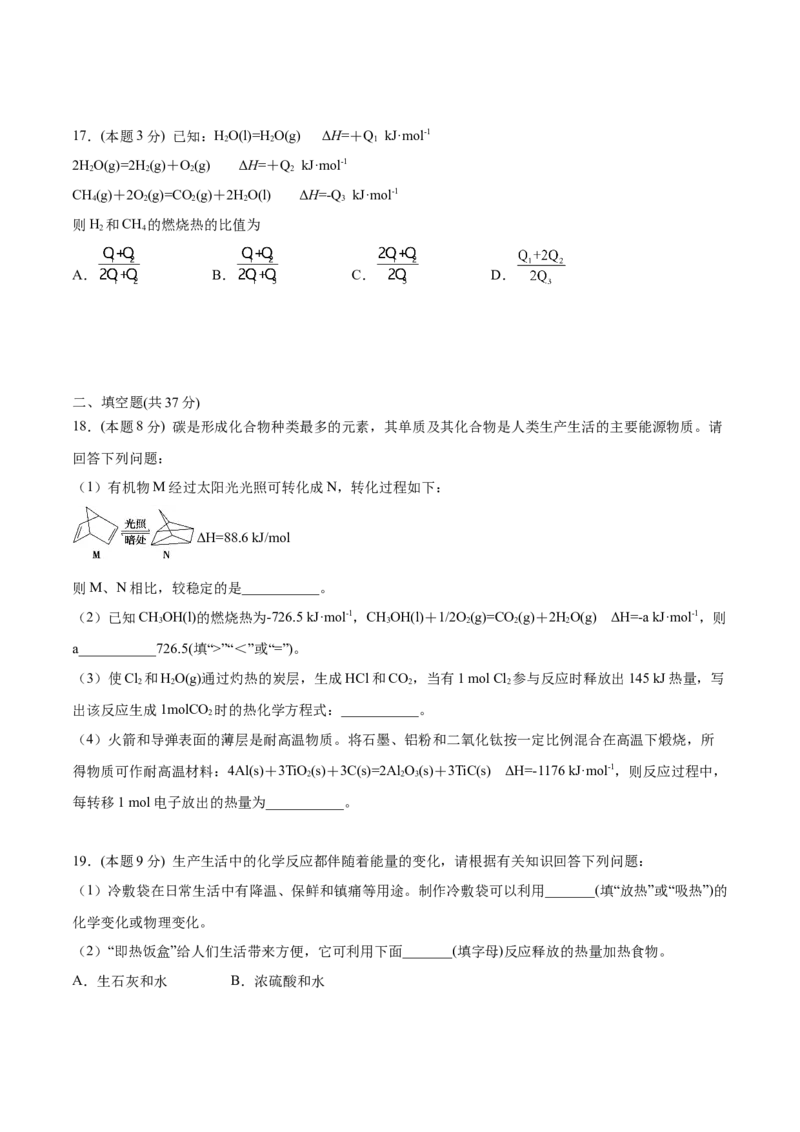
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
ΔH=88.6 kJ/mol
则M、N相比,较稳定的是___________。
(2)已知CHOH(l)的燃烧热为-726.5 kJ·mol-1,CHOH(l)+1/2O (g)=CO (g)+2HO(g) ΔH=-a kJ·mol-1,则
3 3 2 2 2
a___________726.5(填“>”“<”或“=”)。
(3)使Cl 和HO(g)通过灼热的炭层,生成HCl和CO,当有1 mol Cl 参与反应时释放出145 kJ热量,写
2 2 2 2
出该反应生成1molCO 时的热化学方程式:___________。
2
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所
得物质可作耐高温材料:4Al(s)+3TiO(s)+3C(s)=2Al O(s)+3TiC(s) ΔH=-1176 kJ·mol-1,则反应过程中,
2 2 3
每转移1 mol电子放出的热量为___________。
19.(本题9分) 生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______(填“放热”或“吸热”)的
化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______(填字母)反应释放的热量加热食物。
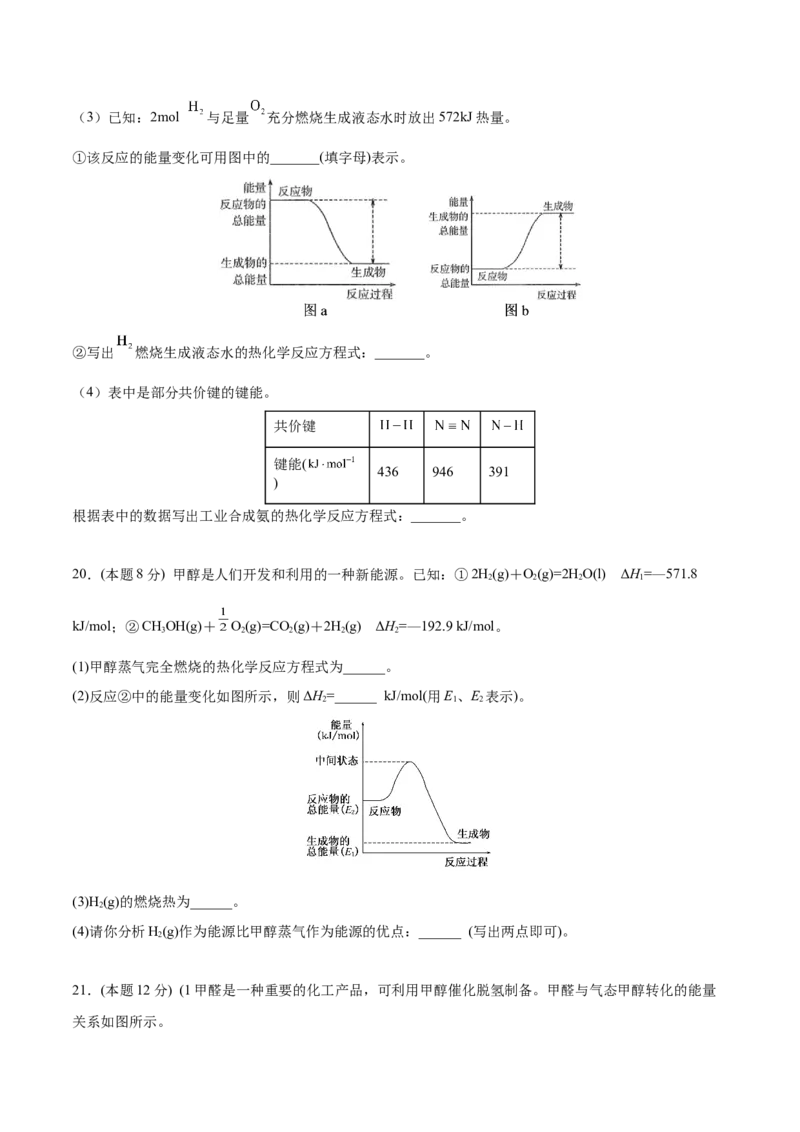
A.生石灰和水 B.浓硫酸和水(3)已知:2mol 与足量 充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的_______(填字母)表示。
②写出 燃烧生成液态水的热化学反应方程式:_______。
(4)表中是部分共价键的键能。
共价键
键能(
436 946 391
)
根据表中的数据写出工业合成氨的热化学反应方程式:_______。
20.(本题8分) 甲醇是人们开发和利用的一种新能源。已知:①2H(g)+O(g)=2HO(l) ΔH=—571.8
2 2 2 1
kJ/mol;②CHOH(g)+ O(g)=CO (g)+2H(g) ΔH=—192.9 kJ/mol。
3 2 2 2 2
(1)甲醇蒸气完全燃烧的热化学反应方程式为______。
(2)反应②中的能量变化如图所示,则ΔH=______ kJ/mol(用E、E 表示)。
2 1 2
(3)H (g)的燃烧热为______。
2
(4)请你分析H(g)作为能源比甲醇蒸气作为能源的优点:______ (写出两点即可)。
2
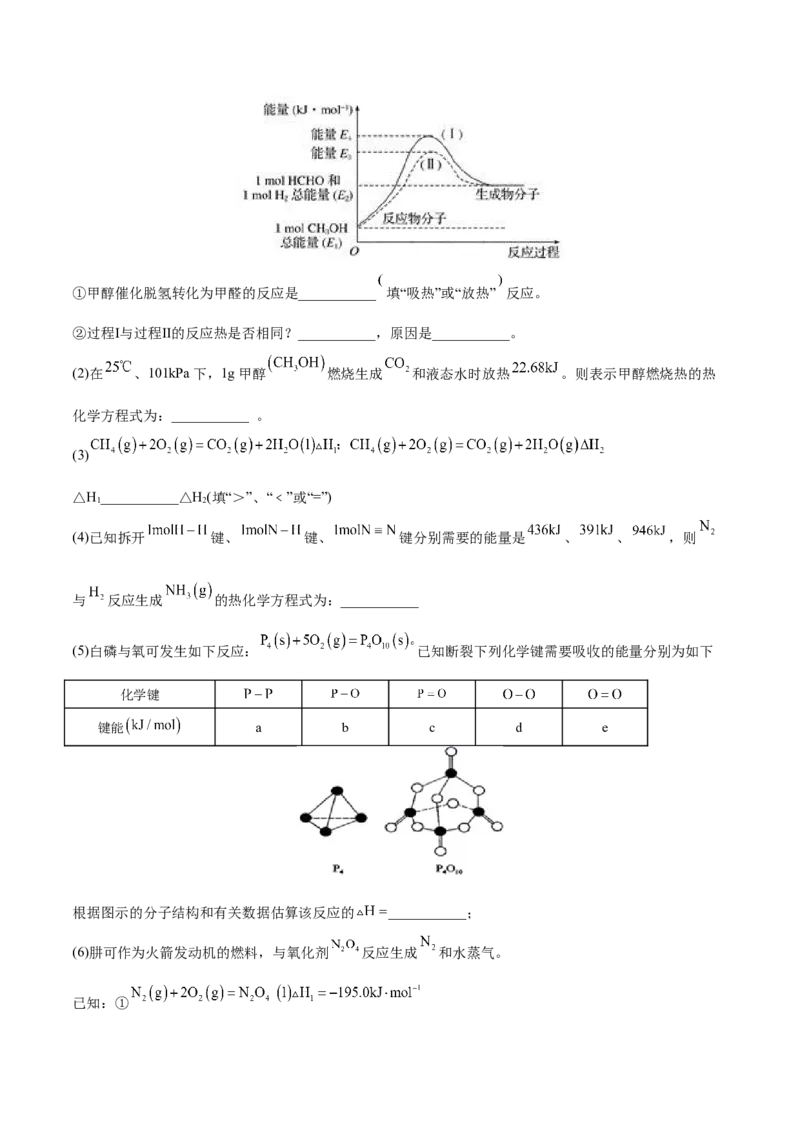
21.(本题12分) (1甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量
关系如图所示。①甲醇催化脱氢转化为甲醛的反应是___________ 填“吸热”或“放热” 反应。
②过程Ⅰ与过程Ⅱ的反应热是否相同?___________,原因是___________。
(2)在 、101kPa下,1g甲醇 燃烧生成 和液态水时放热 。则表示甲醇燃烧热的热
化学方程式为:___________ 。
(3)
△H___________△H(填“>”、“﹤”或“=”)
1 2
(4)已知拆开 键、 键、 键分别需要的能量是 、 、 ,则
与 反应生成 的热化学方程式为:___________
(5)白磷与氧可发生如下反应: 已知断裂下列化学键需要吸收的能量分别为如下
化学键
键能 a b c d e
根据图示的分子结构和有关数据估算该反应的 ___________;
(6)肼可作为火箭发动机的燃料,与氧化剂 反应生成 和水蒸气。
已知:①②
写出肼和 反应的热化学方程式___________。
三、实验题(共12分)
22.(本题12分) 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体_______g。
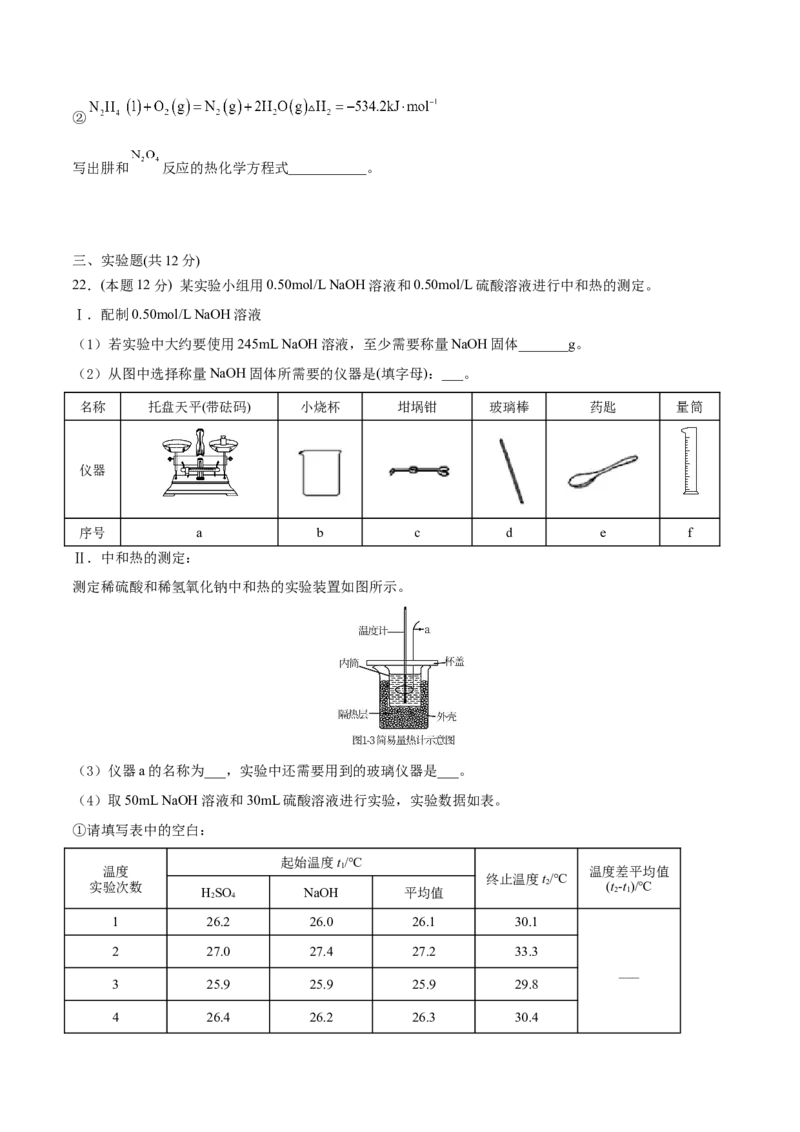
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):___。
名称 托盘天平(带砝码) 小烧杯 坩埚钳 玻璃棒 药匙 量筒
仪器
序号 a b c d e f
Ⅱ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(3)仪器a的名称为___,实验中还需要用到的玻璃仪器是___。
杨sir化学,侵权必究
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
起始温度t/℃
温度 1 温度差平均值
终止温度t/℃
实验次数 2 (t-t)/℃
HSO NaOH 平均值 2 1
2 4
1 26.2 26.0 26.1 30.1
2 27.0 27.4 27.2 33.3
___
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容
c=4.18J/(g·℃)。则中和热△H=___________(取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是_____(填字母)。
a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液时俯视刻度线读数
杨sir化学,侵权必究
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数
(5)实验中改用30mL0.50mol/L的硫酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所
放出的热量_________(填“相等”或“不相等”),所求中和热的数值会_____________(填“相等”或“不相等”)。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育