文档内容
1.1.1 反应热 焓变
【学习目标】
1、理解反应热的概念
2、 能以中和热的测定为例掌握反应热的测定方法;
3、能从宏观和微观两个角度解释反应热产生的原因及掌握反应热的计算方法。
【学习重难点】
重点:反应热、焓变的含义;中和热的测定
难点:焓变、ΔH的“+”与“-”的理解与应用、中和热的测定
【自主预习】
1.体系与环境
被研究的 称为体系,与体系相互影响的其他部分称为 。
热量是指因 不同而在体系与环境之间交换或传递的 。
【举例】将试管中的盐酸、NaOH溶液及发生的反应等看作一个反应体系;盛溶液的试管
和溶液之外的空气等看作环境。
2.反应热
在 条件下,化学反应体系向环境 或从环境 的热量,称为化学反
应的 ,简称反应热。
【合作探究】
一.实验探究:中和反应反应热的测定
(1)测定原理:环境温度 时,根据测得的体系的温度变化和有关物质的
等来计算反应热。即利用公式 进行计算。
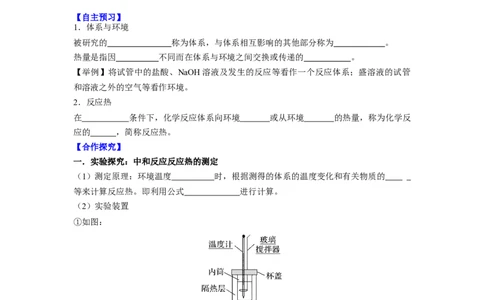
(2)实验装置
①如图:
②各部分仪器的作用
a.玻璃搅拌器的作用是使 混合均匀充分接触。
b.隔热层的作用是 热量的散失。
c.温度计的作用是测定反应前后 的温度。
【思考讨论1】①测量哪些数据?
②如何利用数据计算反应热?
③如何提高实验的准确度?
(3)实验步骤
①反应物温度测量(t):测量混合前50 mL 0.50 mol·L-1 、50 mL 0.55 mol·L-1
1
溶液的温度,取两温度 ,记录为起始温度t。
1
②反应后体系温度测量(t):将 溶液迅速混合,用 轻轻搅动
2
溶液,并准确读取混合溶液的 ,记录为终止温度t。
2
③重复实验操作两次,记录每次的实验数据,取其平均值作为计算依据。
【做一做】
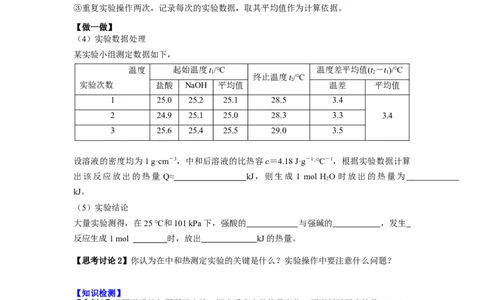
(4)实验数据处理
某实验小组测定数据如下,
温度 起始温度t/℃ 温度差平均值(t-t)/℃
1 2 1
终止温度t/℃
2
实验次数 盐酸 NaOH 平均值 温差 平均值
1 25.0 25.2 25.1 28.5 3.4
2 24.9 25.1 25.0 28.3 3.3 3.4
3 25.6 25.4 25.5 29.0 3.5
设溶液的密度均为1 g·cm-3,中和后溶液的比热容c=4.18 J·g-1·℃-1,根据实验数据计算
出该反应放出的热量 Q≈ kJ,则生成 1 mol H O 时放出的热量为
2
kJ。
(5)实验结论
大量实验测得,在25 ℃和101 kPa下,强酸的 与强碱的 ,发生
反应生成1 mol 时,放出 kJ的热量。
【思考讨论2】你认为在中和热测定实验的关键是什么?实验操作中要注意什么问题?
【知识检测】
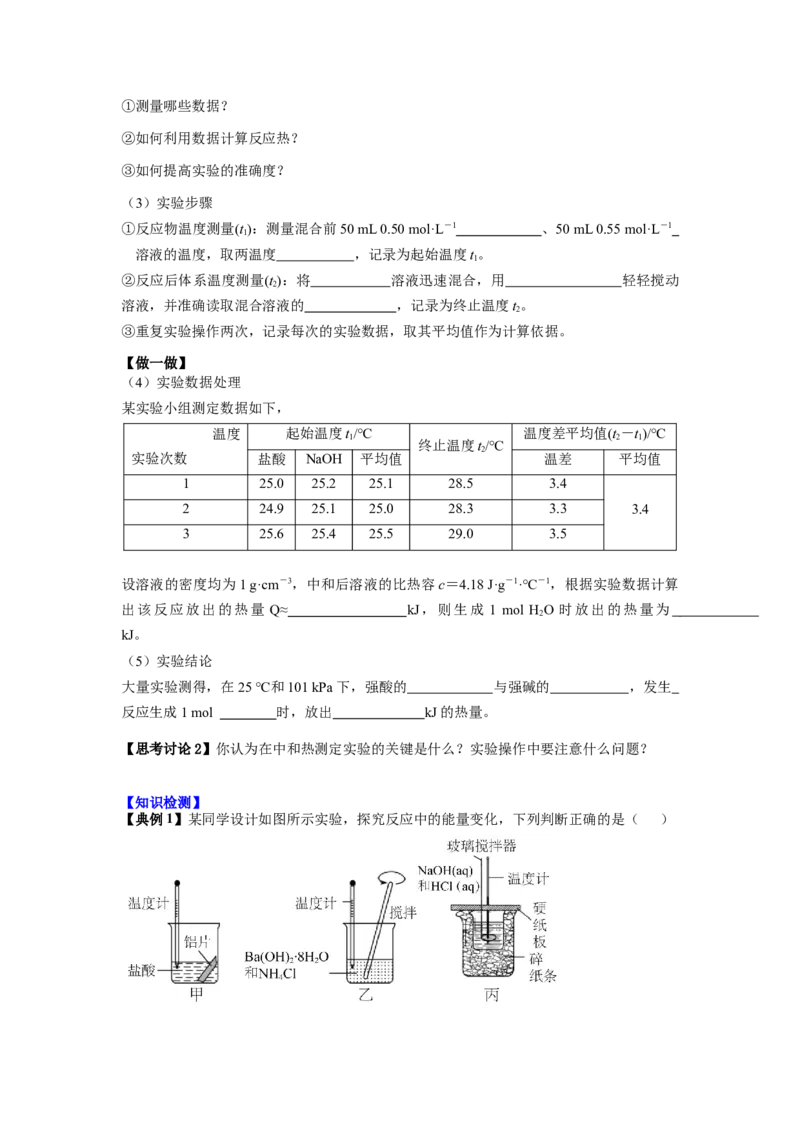
【典例1】某同学设计如图所示实验,探究反应中的能量变化,下列判断正确的是( )A.由实验可知,甲、乙、丙所涉及的反应都能使温度计读数上升
B.将实验甲中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验丙中将玻璃搅拌器改为铁质搅拌棒对实验结果没有影响
D.实验丙中若用 代替 ,则测出 变小
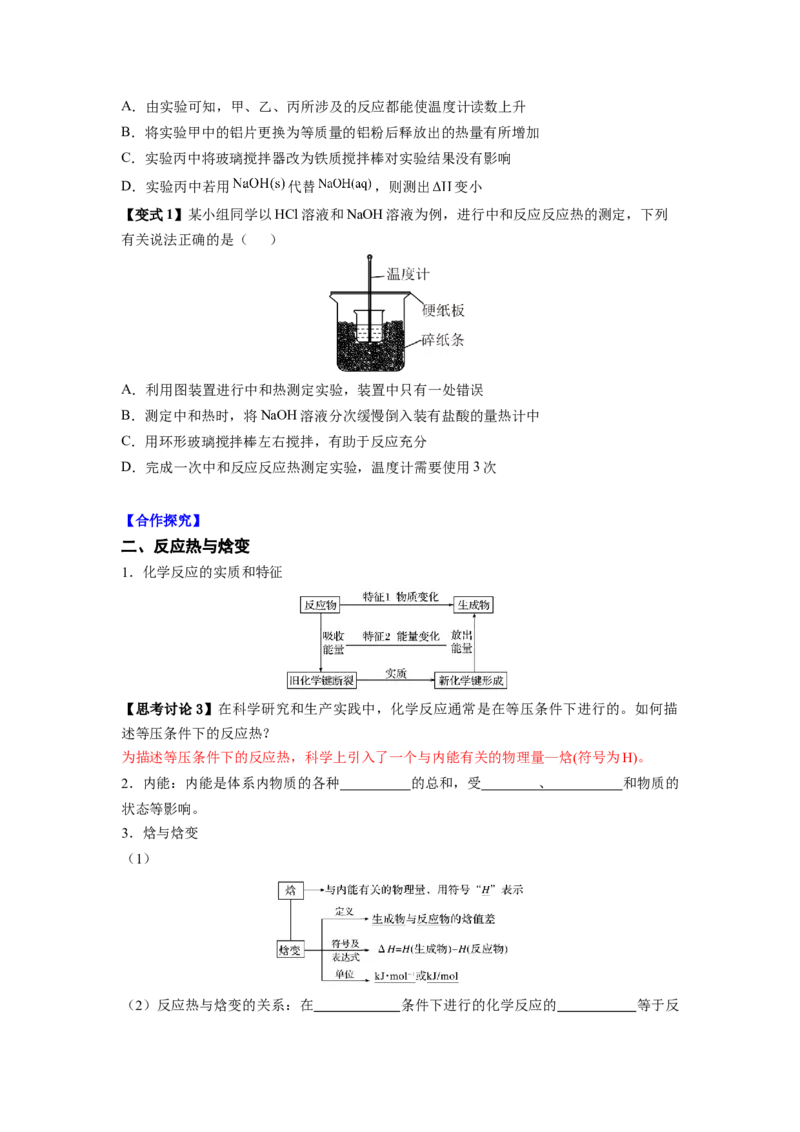
【变式1】某小组同学以HCl溶液和NaOH溶液为例,进行中和反应反应热的测定,下列
有关说法正确的是( )
A.利用图装置进行中和热测定实验,装置中只有一处错误
B.测定中和热时,将NaOH溶液分次缓慢倒入装有盐酸的量热计中
C.用环形玻璃搅拌棒左右搅拌,有助于反应充分
D.完成一次中和反应反应热测定实验,温度计需要使用3次
【合作探究】
二、反应热与焓变
1.化学反应的实质和特征
【思考讨论3】在科学研究和生产实践中,化学反应通常是在等压条件下进行的。如何描
述等压条件下的反应热?
为描述等压条件下的反应热,科学上引入了一个与内能有关的物理量—焓(符号为H)。
2.内能:内能是体系内物质的各种 的总和,受 、 和物质的
状态等影响。
3.焓与焓变
(1)
(2)反应热与焓变的关系:在 条件下进行的化学反应的 等于反应的 ,因此常用 表示反应热。
(3)焓变与吸热反应和放热反应的关系
①放热反应:反应体系向环境 能量,反应体系的焓 ,ΔH 为
。
②吸热反应:反应体系从环境中 能量,反应体系的焓 ,ΔH 为
。
【做一做】焓变的表示方法
①在25℃和101 kPa下,1 molH2与1 mol Cl2反应生成2 mol HCl时放出184.6 kJ的
热量,则该反应的反应热为:
②在25 ℃和101 kPa下,1 mol C(如无特别说明,C均指石墨)与1 mol H2O(g)反应,
生成1 mol CO和1 mol H2,需要吸收131.5 kJ的热量,则该反应的反应热为:
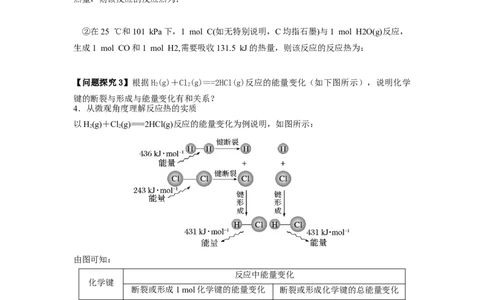
【问题探究3】根据H(g)+Cl(g)===2HCl(g)反应的能量变化(如下图所示),说明化学
2 2
键的断裂与形成与能量变化有和关系?
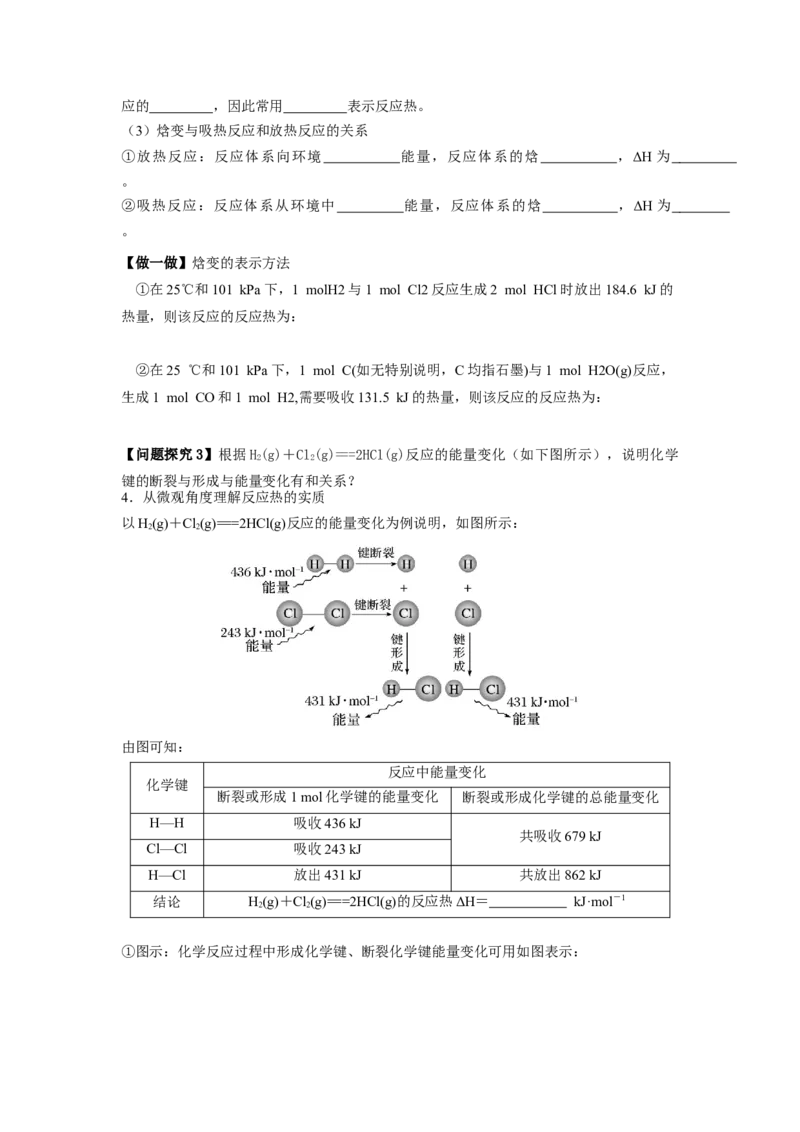
4.从微观角度理解反应热的实质
以H(g)+Cl(g)===2HCl(g)反应的能量变化为例说明,如图所示:
2 2
由图可知:
反应中能量变化
化学键
断裂或形成1 mol化学键的能量变化 断裂或形成化学键的总能量变化
H—H 吸收436 kJ
共吸收679 kJ
Cl—Cl 吸收243 kJ
H—Cl 放出431 kJ 共放出862 kJ
结论 H(g)+Cl(g)===2HCl(g)的反应热ΔH= kJ·mol-1
2 2
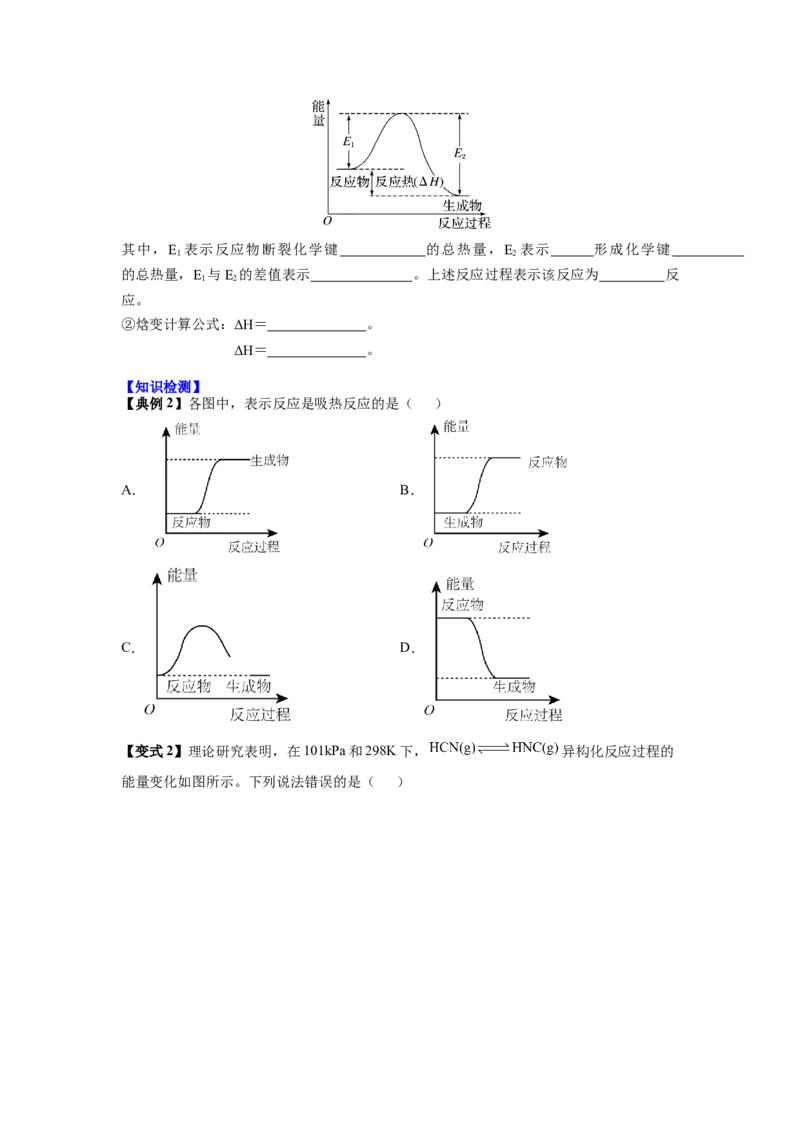
①图示:化学反应过程中形成化学键、断裂化学键能量变化可用如图表示:其中,E 表示反应物断裂化学键 的总热量,E 表示 形成化学键
1 2
的总热量,E 与E 的差值表示 。上述反应过程表示该反应为 反
1 2
应。
②焓变计算公式:ΔH= 。
ΔH= 。
【知识检测】
【典例2】各图中,表示反应是吸热反应的是( )
A. B.
C. D.
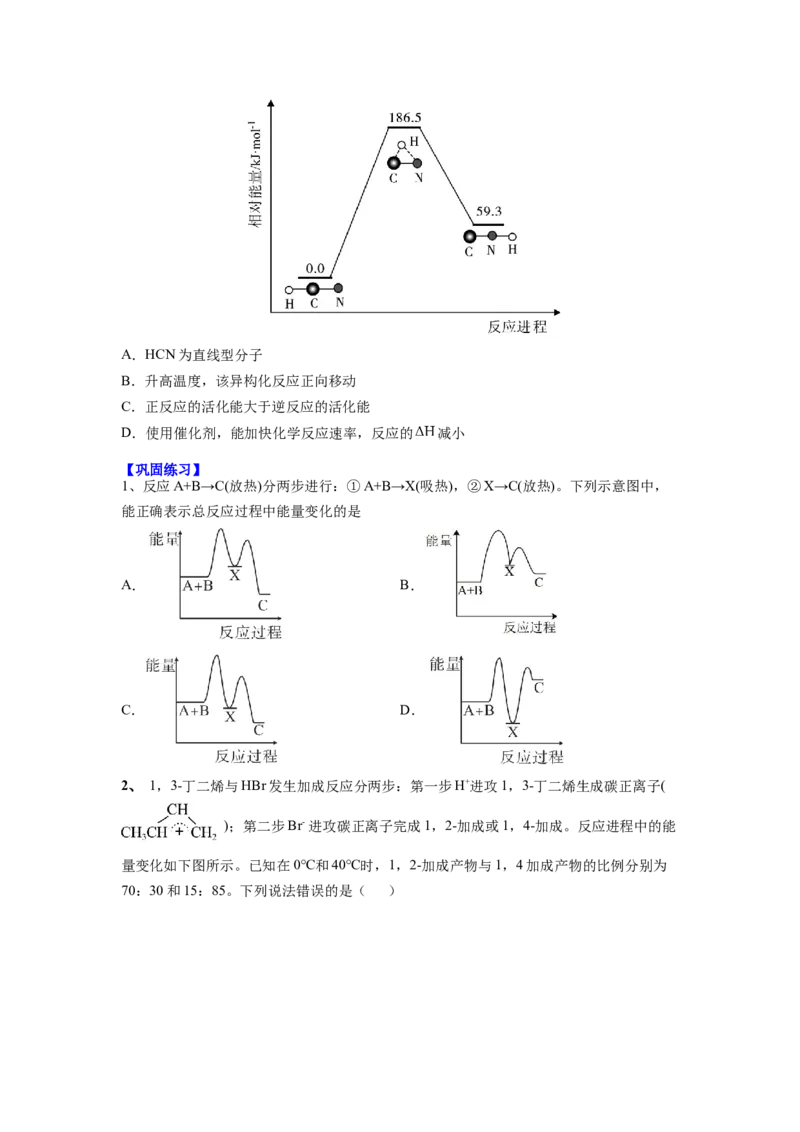
【变式2】理论研究表明,在101kPa和298K下, 异构化反应过程的
能量变化如图所示。下列说法错误的是( )A.HCN为直线型分子
B.升高温度,该异构化反应正向移动
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,能加快化学反应速率,反应的 减小
【巩固练习】
1、反应A+B→C(放热)分两步进行:①A+B→X(吸热),②X→C(放热)。下列示意图中,
能正确表示总反应过程中能量变化的是
A. B.
C. D.
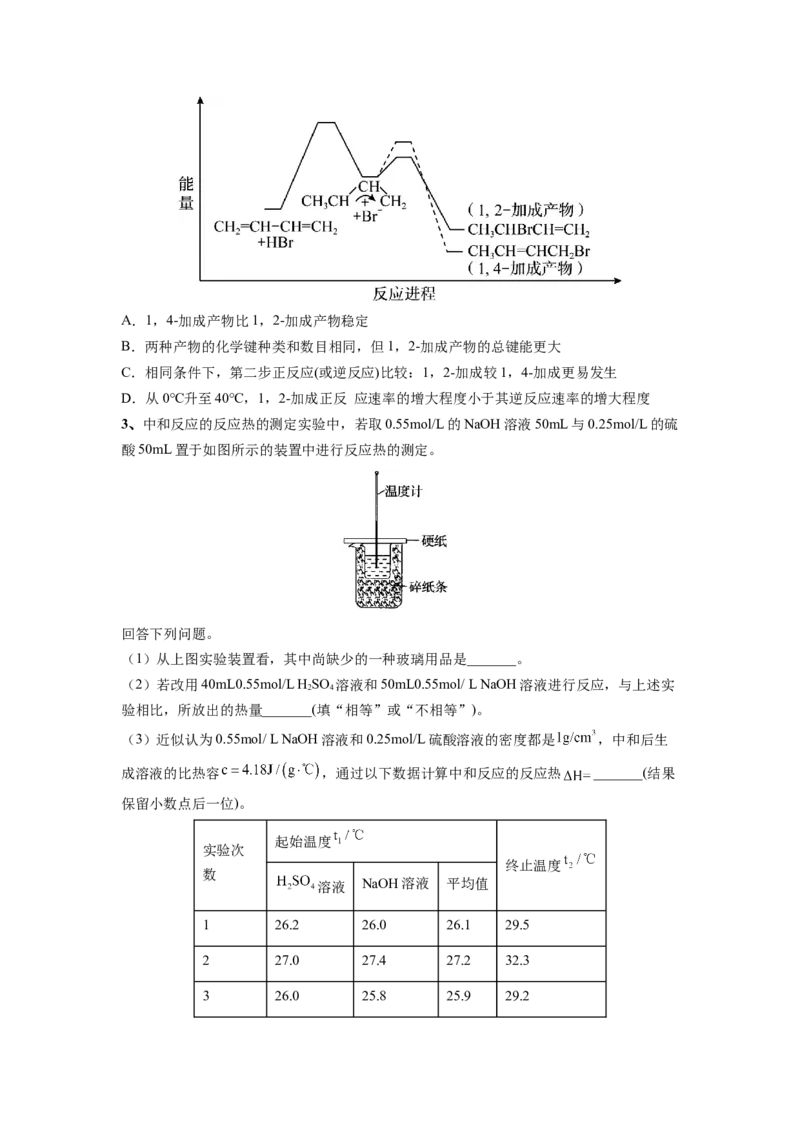
2、 1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(
);第二步Br- 进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能
量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4加成产物的比例分别为
70:30和15:85。下列说法错误的是( )A.1,4-加成产物比1,2-加成产物稳定
B.两种产物的化学键种类和数目相同,但1,2-加成产物的总键能更大
C.相同条件下,第二步正反应(或逆反应)比较:1,2-加成较1,4-加成更易发生
D.从0℃升至40℃,1,2-加成正反 应速率的增大程度小于其逆反应速率的增大程度
3、中和反应的反应热的测定实验中,若取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫
酸50mL置于如图所示的装置中进行反应热的测定。
回答下列问题。
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_______。
(2)若改用40mL0.55mol/L H SO 溶液和50mL0.55mol/ L NaOH溶液进行反应,与上述实
2 4
验相比,所放出的热量_______(填“相等”或“不相等”)。
(3)近似认为0.55mol/ L NaOH溶液和0.25mol/L硫酸溶液的密度都是 ,中和后生
成溶液的比热容 ,通过以下数据计算中和反应的反应热 _______(结果
保留小数点后一位)。
起始温度
实验次
终止温度
数
溶液 NaOH溶液 平均值
1 26.2 26.0 26.1 29.5
2 27.0 27.4 27.2 32.3
3 26.0 25.8 25.9 29.24 26.4 26.2 26.3 29.8
(4)上述实验结果与 相比有偏差,产生偏差的原因可能是_______(填字
母)。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
4、实验室利用如图所示装置测定中和热的实验步骤如下:
步骤一:用量筒量取 盐酸倒入小烧杯中,测出盐酸温度;步骤二:用另一
量筒量取 溶液,并用同一温度计测出其温度;步骤三:将 溶液
倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
①碎泡沫塑料的作用是_______。
②将一定量的稀氢氧化钠溶液分别和稀盐酸、浓硫酸、稀醋酸溶液恰好完全反应,其反应
热分别为 、 、 ,则 、 、 的大小关系为_______。
③假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
。为了计算中和热,某学生实验记录数据如下
起始温度 终止温度
实验序
号 氢氧化钠溶
盐酸 混合溶液
液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 23.6
依据该学生的实验数据计算,该实验测得的中和热 _______(结果保留一位小数)。
④该同学通过实验测出的中和热有误差,造成这一结果的原因不可能的是_______。
A.实验装置保温、隔热效果差
B.用量筒量取盐酸时仰视读数C.分多次将 溶液倒入小烧杯中
D.用测量盐酸的温度计直接测定 溶液的温度
【课后反思】本节课学习中,你有哪些收获,还有哪些问题?