文档内容
1.2.2 反应热的计算(分层作业)
【基础检测题】
一、单选题
1.强酸和强碱稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H O(l) H=-57.3kJ•mol-1
2
已知:①HCl(aq)+NH
3
•H
2
O(aq)=NH
4
Cl(aq)+H
2
O(l) H
1
=akJ•mol-△1
②HCl(aq)+NaOH(aq)=NaCl(aq)+H
2
O(l) H
2
=bkJ•△mol-1
③HNO
3
(aq)+KOH(aq)=KNO
3
(aq)+H
2
O(l)△ H
3
=ckJ•mol-1
则a、b、c三者的大小关系为 △
A.a>b>c B.b>c>a C.a>b=c D.a=b<c
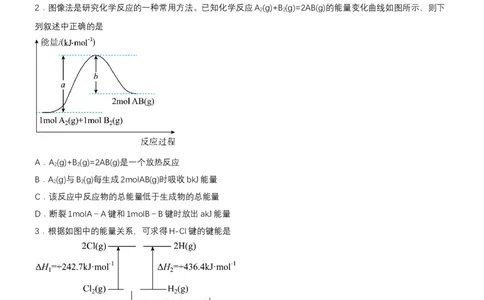
2.图像法是研究化学反应的一种常用方法。已知化学反应A (g)+B (g)=2AB(g)的能量变化曲线如图所示,则下
2 2
列叙述中正确的是
A.A (g)+B (g)=2AB(g)是一个放热反应
2 2
B.A (g)与B (g)每生成2molAB(g)时吸收bkJ能量
2 2
C.该反应中反应物的总能量低于生成物的总能量
D.断裂1molA-A键和1molB-B键时放出akJ能量
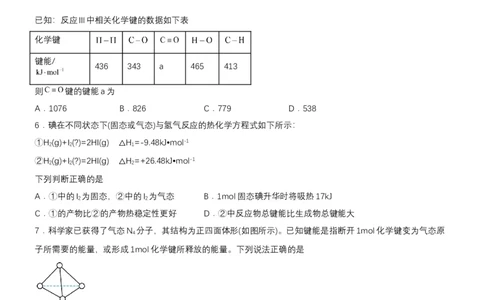
3.根据如图中的能量关系,可求得H-Cl键的键能是
A.431.8 kJ⋅mol B.247.3 kJ⋅mol
C.863.6 kJ⋅mol D.494.6 kJ⋅mol
4.已知几种化学键的键能如表所示:
化学键
键能 a 436 463 750根据热化学方程式: ,计算表中的a为
A.484.5 B.969 C.872 D.1938
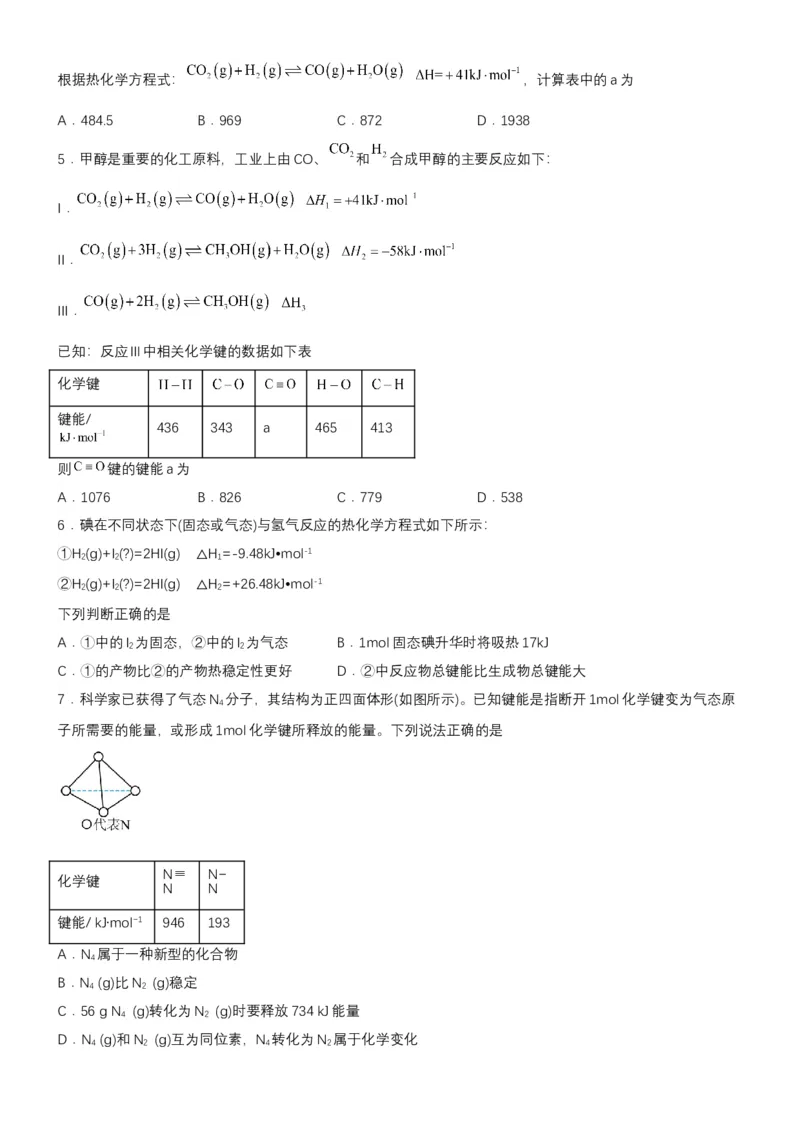
5.甲醇是重要的化工原料,工业上由CO、 和 合成甲醇的主要反应如下:
I.
II.
III.
已知:反应Ⅲ中相关化学键的数据如下表
化学键
键能/
436 343 a 465 413
则 键的键能a为
A.1076 B.826 C.779 D.538
6.碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H (g)+I (?)=2HI(g) H =-9.48kJ•mol-1
2 2 1
②H
2
(g)+I
2
(?)=2HI(g) △H
2
=+26.48kJ•mol-1
下列判断正确的是 △
A.①中的I 为固态,②中的I 为气态 B.1mol固态碘升华时将吸热17kJ
2 2
C.①的产物比②的产物热稳定性更好 D.②中反应物总键能比生成物总键能大
7.科学家已获得了气态N 分子,其结构为正四面体形(如图所示)。已知键能是指断开1mol化学键变为气态原
4
子所需要的能量,或形成1mol化学键所释放的能量。下列说法正确的是
N≡ N−
化学键
N N
键能/ kJ∙mol−1 946 193
A.N 属于一种新型的化合物
4
B.N (g)比N (g)稳定
4 2
C.56 g N (g)转化为N (g)时要释放734 kJ能量
4 2
D.N (g)和N (g)互为同位素,N 转化为N 属于化学变化
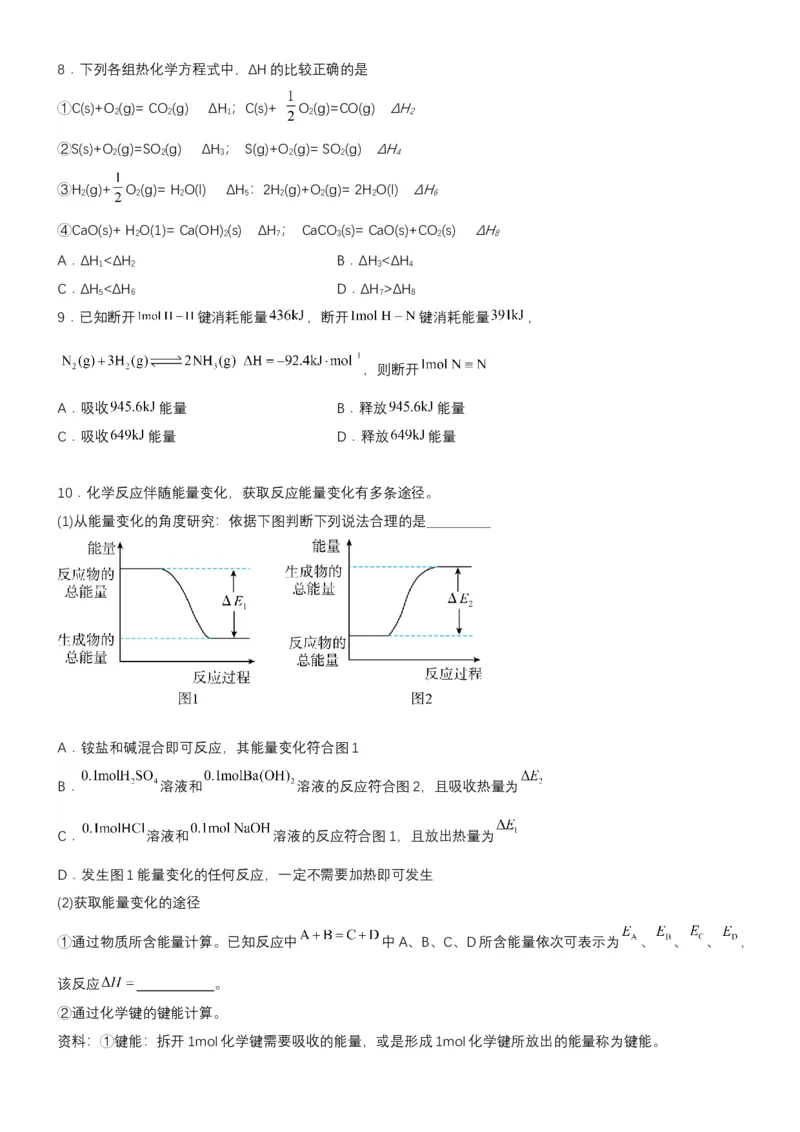
4 2 4 28.下列各组热化学方程式中,ΔH的比较正确的是
①C(s)+O (g)= CO (g) ΔH ;C(s)+ O (g)=CO(g) ΔH
2 2 1 2 2
②S(s)+O (g)=SO (g) ΔH ; S(g)+O (g)= SO (g) ΔH
2 2 3 2 2 4
③H (g)+ O (g)= H O(l) ΔH :2H (g)+O (g)= 2H O(l) ΔH
2 2 2 5 2 2 2 6
④CaO(s)+ H O(1)= Ca(OH) (s) ΔH ; CaCO (s)= CaO(s)+CO (s) ΔH
2 2 7 3 2 8
A.ΔH <ΔH B.ΔH <ΔH
1 2 3 4
C.ΔH <ΔH D.ΔH >ΔH
5 6 7 8
9.已知断开 键消耗能量 ,断开 键消耗能量 ,
,则断开
A.吸收 能量 B.释放 能量
C.吸收 能量 D.释放 能量
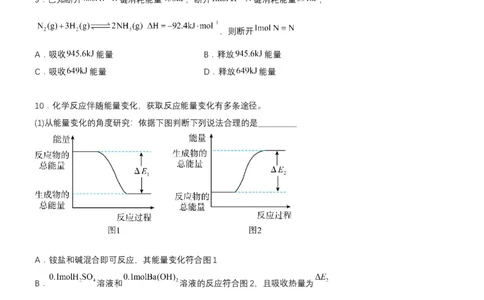
10.化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)从能量变化的角度研究:依据下图判断下列说法合理的是___________
A.铵盐和碱混合即可反应,其能量变化符合图1
B. 溶液和 溶液的反应符合图2,且吸收热量为
C. 溶液和 溶液的反应符合图1,且放出热量为
D.发生图1能量变化的任何反应,一定不需要加热即可发生
(2)获取能量变化的途径
①通过物质所含能量计算。已知反应中 中A、B、C、D所含能量依次可表示为 、 、 、 ,
该反应 。
②通过化学键的键能计算。
资料:①键能:拆开1mol化学键需要吸收的能量,或是形成1mol化学键所放出的能量称为键能。如下图所示, 分子结构与白磷分子相似,呈正四面体结构。已知断裂 键吸收193kJ热量,断裂
键吸收941kJ热量,则 气体转化为 时要 (填“吸收”或“放出”)热量
kJ。
(3)同温同压下,下列各组热化学方程式中, 的是___________
A. ;
B. ;
C. ;
D. ;
11.请运用反应热的知识填写下列空白:
(1)已知: (s,白磷)= (s,黑磷) ;
(s,白磷)= (s,红磷) ;
由此推知,其中最稳定的磷单质是 。
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl 气体和H ,放出225 kJ热量,该反应的热化学方程式为
3 2
。
②在 25℃ 和 101kPa时,4 g硫粉在O 中完全燃烧生成SO 气体,放出37 kJ的热量,写出表示S燃烧热的热
2 2
化学方程式: 。
(3)已知上述反应中相关的化学键键能数据如下:
C- H-
化学键 C=O C O(CO)
H H
键能/kJ·mol−1 413 745 436 1075
则该反应的 ΔH = 。
(4)将 氢化为 有三种方法,对应的反应依次为:
①②
③
反应③的 ΔH = (用ΔH ,ΔH 表示)
3 1 2
(5)①2Cu O(s) + O (g) =4CuO(s) ΔH =-277kJ·mol-1
2 2 1
②8CuO(s) + CH (g)=4Cu O(s) + CO (g)+2H O(g) ΔH =-348kJ·mol-1
4 2 2 2 2
反应CH (g) +2O (g)=CO (g)+2H O(g) ΔH= kJ·mol-1
4 2 2 2
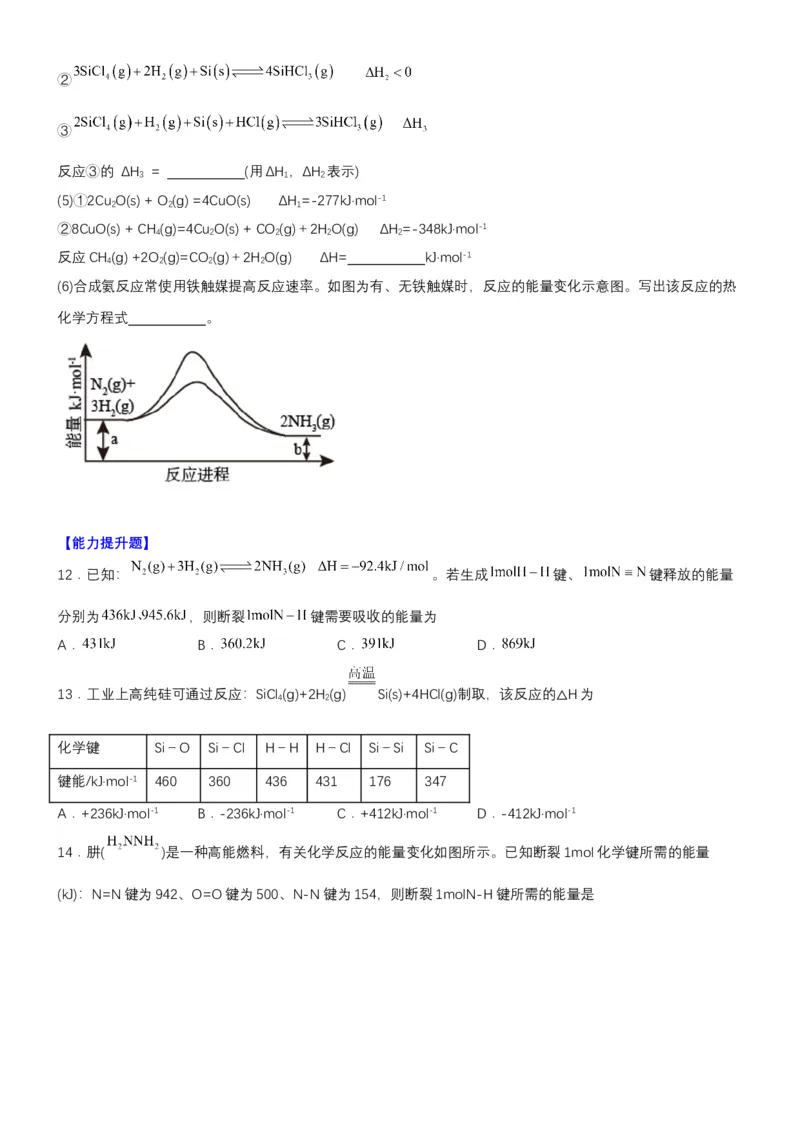
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热
化学方程式 。
【能力提升题】
12.已知: 。若生成 键、 键释放的能量
分别为 ,则断裂 键需要吸收的能量为
A. B. C. D.
13.工业上高纯硅可通过反应:SiCl (g)+2H (g) Si(s)+4HCl(g)制取,该反应的 H为
4 2
△
化学键 Si-O Si-Cl H-H H-Cl Si-Si Si-C
键能/kJ·mol-1 460 360 436 431 176 347
A.+236kJ·mol-1 B.-236kJ·mol-1 C.+412kJ·mol-1 D.-412kJ·mol-1
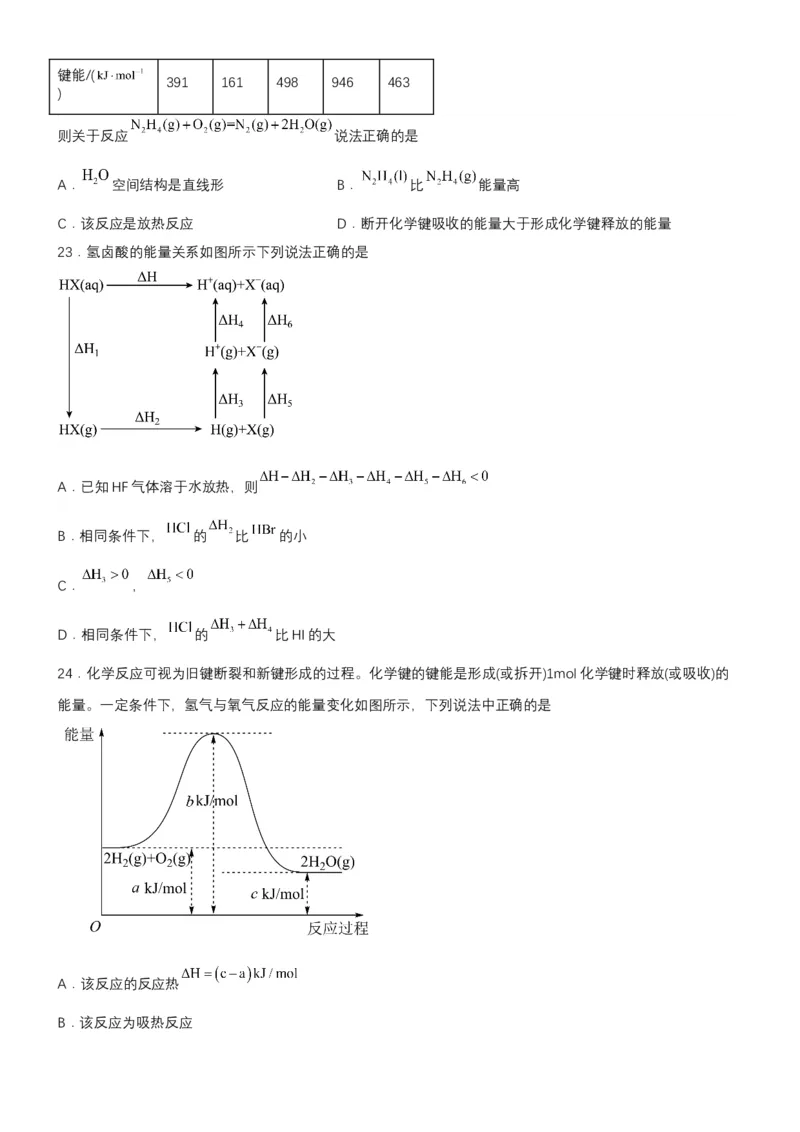
14.肼( )是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1mol化学键所需的能量
(kJ):N=N键为942、O=O键为500、N-N键为154,则断裂1molN-H键所需的能量是A.194kJ B.391kJ C.516kJ D.658kJ
15.在25℃和101kPa的条件下, 和 完全反应生成 的能量变化如图所示,下列说法
不正确的是
A.H-H的键能为436kJ/mol
B.形成 中的化学键释放出431kJ的能量
C.该反应的热化学方程式:
D.共价键断裂和形成时的能量变化是该化学反应能量变化的主要原因
16.对于反应: ,下列说法不正确的是
A.1mol S(s)与1mol (g)的总能量比1mol (g)的总能量高
B.
C.
D.1mol S(g)与1mol (g)反应生成1mol (g)放出热量少于297.2kJ
17.氢卤酸的能量关系如图所示:下列说法正确的是A.已知HF气体溶于水放热,则HF的
B.相同条件下,HCl的 比HBr的小
C.相同条件下,HCl的( )比HI的大
D.一定条件下,气态原子生成1mol H-X键放出a kJ能量,则该条件下
18.化学反应N (g)+3H (g) 2NH (g)的能量变化如图所示:
2 2 3
已知断裂1molN≡N、1molN-H分别需吸收946kJ、391kJ的能量,则下列说法不正确的是
A.该反应为放热反应
B.ΔE—ΔE=92kJ•mol-1
2 1
C.拆开1molH 中化学键需要吸收436kJ的能量
2
D.生成2molNH (l)放出的热量小于92kJ
3
19.50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过
程中所放出的热量可计算中和反应的反应热。(1)①从实验装置看,图中还缺少的一种玻璃仪器是 。
②中和热测定时采用稍过量的氢氧化钠的原因: 。
③测定稀硫酸和稀氢氧化钠中和热(中和热为57.3kJ/mol)的实验装置如图所示。某兴趣小组的实验数值结果小于
57.3kJ/mol原因可能是 (填字母)。
A.实验装置保温、隔热效果差
B.读取混合液的最高温度记为终点温度
C.一次就把NaOH溶液全倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后未洗涤,直接测定H SO 溶液的温度
2 4
④用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和反应的中和热的数值与57.3kJ•mol-1相比
较会 (填“偏大”“偏小”或“无影响”)。
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如图:
反应I:2H SO (l)=2SO (g)+2H O(g)+O (g) H =+551kJ•mol-1
2 4 2 2 2 1
反应III:S(s)+O
2
(g)=SO
2
(g) H
3
=-297kJ•△mol-1
反应II的热化学方程式: 。△
(3)由气态基态原子形成1mol化学键释放的最低能量叫键能。已知表中所列键能数据:
N≡
化学键 H-H N-H
N
键能kJ/mol a b c
则N (g)+3H (g) 2NH (g) H= kJ•mol-1(用小写字母表示)。
2 2 3
△
(4)一定条件下,在水溶液均为1mol以下离子Cl-、ClO-、ClO 、ClO 、ClO 的能量(kJ)相对大小如图所示,则
3ClO-(aq)=ClO +2Cl-(aq)的 H= kJ•mol-1。
△20.化学反应都会伴随能量变化,还可以进行化学能与热能、电能、光能等各种形式能量之间的转化。
(1)化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列说法错误的是_______
A.该过程中电能转化为了化学能 B.该过程属于氮的固定
C.太阳能为可再生资源 D.断裂 键会释放出能量
(2)下列反应中,生成物总能量高于反应物总能量的是_______
A.强酸强碱的中和反应 B.酒精燃烧
C. 与氯化铵(s)混合 D. 催化氧化制取
(3)研究表明,在一定条件下,气态HCN(a)与HNC(b)两种分子的互变反应过程能量变化如图所示。下列说法正
确的是_______
A. 比 更稳定
B. 转化为 ,反应条件一定要加热
C.
D.加入催化剂,可以减小反应的热效应
(4)已知乙炔与苯蒸气完全燃烧的热化学方程式如下所示:
①
②
① 的燃烧热为 。② 完全燃烧生成液态水时 (填“>、<或=”,下同),相同条件下,等质量
与 完全燃烧,热值: 。
③ 转化为 反应的 。
(5) 是大气污染物之一,通过化学方法消除污染是当今环境化学研究的热点: 产生的原因之一是汽车发
动机工作时引发 和 反应,根据表中数据,书写反应的热化学方程式: 。
物质
键能 954 498 630
(6)科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
则甲烷直接将 还原为 的热化学方程式为 。
【拔尖训练题】
21. 和 在一定条件下能发生反应: 已知: 键能:
键能: 。下列说法正确的是
A.该反应为放热反应,放热反应不需要加热就一定能够发生
B.1mol 分解制得0.5mol 需要吸收92kJ的能量
C.断开1mol 和3mol 中的化学键吸收的总能量大于形成2mol 中的化学键所放出的总能量
D. 键能为
22.肼( )是一种高能燃料,共价键的键能与热化学方程式信息如下表:
共价键键能/(
391 161 498 946 463
)
则关于反应 说法正确的是
A. 空间结构是直线形 B. 比 能量高
C.该反应是放热反应 D.断开化学键吸收的能量大于形成化学键释放的能量
23.氢卤酸的能量关系如图所示下列说法正确的是
A.已知HF气体溶于水放热,则
B.相同条件下, 的 比 的小
C. ,
D.相同条件下, 的 比HI的大
24.化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的
能量。一定条件下,氢气与氧气反应的能量变化如图所示,下列说法中正确的是
A.该反应的反应热
B.该反应为吸热反应C.断裂 和 放出 的能量
D. 燃烧热的热化学方程式为:
25.已知:CO (g)+3H (g) CH OH(g)+H O(g)ΔH=—50kJ•mol-1; CO(g)+2H (g) CH OH(g)ΔH=—
2 2 3 2 2 3
91kJ•mol-1,则1molCO断键吸收的能量为
C=O H-H H-O
键能/(kJ•mol-1) 803 436 463
A.1075kJ B.1157kJ C.735kJ D.817kJ
26. 常用于有机合成,其合成原理为 ,反应过程中的能量变化如下图所示,
下列有关说法正确的是
A.该反应为吸热反应
B.该反应中每生成 放出热量
C.形成 中的化学键吸收热量
D. 所具有能量比 所具有能量低
27.已知:①反应 , 发生该反应放出热量 ;
②白磷 、 的分子结构如图所示;
③P—P、O=O、P—O键的键能分别为 、 、 。
则a的值为A.1200 B.300 C.240 D.200
28.将2 mol 和3 mol 置于密闭容器中,在250℃下只发生如下两个反应:
kJ/mol
kJ/mol
一段时间后, 和 恰好全部消耗,共放出303 kJ热量。
已知:部分化学键的键能如下表所示
化学键 (ClF中) ( 中)
键能/(kJ/mol) 157 243 248 X
则X的值为
A.172 B.202 C.238 D.258
29.I.作为国之重器,火箭的发射牵动了亿万人民的心。就像汽车、飞机需要添加汽油、航空煤油一样,火箭专
用燃料被称为“推进剂”。在火箭推进器中装有强还原剂肼 和强氧化剂 ,当它们混合时,即产生大
量的 和水蒸气,并放出大量热。已知 液态肼和足量 反应,生成氮气和水蒸气,放出 的
热量。
(1)写出该反应的热化学方程式 。
(2)已知 ,则 液态肼燃烧生成氮气和液态水时,放出的热量是
kJ。(计算保留1位小数)
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是
。
II.“长征五号”被称为“冰箭”,这缘于长征五号“肚子”里满满的深低温液氢液氧燃料,填补了我国大推力无毒无污
染液体火箭发动机的空白,实现了绿色环保的研制理念。氢能是一种极具发展潜力的清洁能源,发展氢能正受
到世界各国广泛关注。(4)中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如图所示。
下列说法不正确的是___________。
A.整个过程实现了光能向化学能的转化
B.过程II吸收能量
C.III发生的反应:
D.过程的总反应:
30.研究化学反应中的能量变化有利于更好的开发和使用化学能源。
(1)已知H 、CO、CH 的燃烧热分别为285.8kJ·mol-1、283.0kJ·mol-1、890.3kJ·mol-1。
2 4
①相同条件下,等质量的H 、CO、CH 分别完全燃烧,放出热量最多的是 。
2 4
②2CH (g)+3O (g)=2CO(g)+4H O(l) ΔH= kJ·mol-1。
4 2 2
③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a 途径b(填“>”、“<”或“=”)
途径a:CH CO+H CO +H O
4 2 2 2
途径b:CH CO +H O
4 2 2
(2)已知白磷(P )和P O 的分子结构和部分化学键的键能分别如下图、表所示:
4 4 6
O= P-
化学键 P-P
O O
键能(kJ·mol-1) a b c
①写出白磷与氧气反应生成P O 固体的热化学方程式: 。
4 6
②已知P (白磷,s)=4P(红磷,s)ΔH=-16.7kJ·mol-1。白磷和红磷互为 (填“同系物”、“同位素”、“同素
4
异形体”或“同分异构体”),比较稳定的是 。等质量的白磷、红磷分别完全燃烧,放出热量更多的是
。