文档内容
第一章 化学反应的热效应
第1节 反应热
课题:1.2.1 盖斯定律 课时 1 授课年级 高二
教学内容
本节内容介绍了盖斯定律。教科书以登山经验“山的高度与上山的途径无关”,浅显地
教材 对特定化学反应的反应热进行形象的比喻,帮助学生理解盖斯定律。然后再通过对能量守
分析 恒定律的反证来论证盖斯定律的正确性。最后通过实例使学生感受盖斯定律的应用,并以
此说明盖斯定律在科学研究中的重要意义。
[能力目标]
①知道盖斯定律的内容;
②掌握运用盖斯定律解决具体问题:③初步学会化学反应热的有关计算。
教学目标
[素养目标]
通过实例感受盖斯定律,并以此说明盖斯定律在科学研究中的重要作用。体会化学对生活
的贡献。
教学重、 重点:盖斯定律的理解及应用
难点:盖斯定律的理解及应用
难点
前面学生已经定性地了解了化学反应与能量的关系,通过实验感受到了反应热,并且
了解了物质发生反应产生能量变化与物质的质量的关系,及燃烧热的概念。在此基础上,
学情分析 本节介绍了盖斯定律,并从定量的角度来进一步认识物质发生化学反应伴随的热效应。注
意引导学生准确理解反应热、燃烧热、盖斯定律等理论概念,熟悉热化学方程式的书写,
重视概念和热化学方程式的应用。
教学方法 自主学习、合作交流、探究与验证
教学环节一:温故知新引出课题。
教师活动 学生活动 设计意图
1、温故知新:
请结合以下数据计算H 的燃烧热 ,写出表示H 燃
2 2
烧热的热化学方程式?
复习燃烧热
①H(g)+1/2O(g)=HO(g) ΔH=-241.8kJ/mol
2 2 2 1 学生思考回答。 和热化学方
②H 2 O(g)=H 2 O(l) ΔH 2 =-44kJ/mol 程 式 的 书
写。
教学环节二:盖斯定律的内容
教师活动 学生活动 设计意图
1. 【展示盖斯定律】 【写一写】 以登山经验1840年,盖斯(G.H.Hess,俄国化学家)从
大量的实验事实中总结出一条规律:化学反应不管
是一步完成还是分几步完成,其__反应热___是相
同的。也就是说,化学反应的_焓变___只与反应的
_始态__和__终态___有关,而与具体反应进行的__
过程___无关。如果一个反应可以分几步进行,则
各分步反应的反应热之和与该反应一步完成时的反 “山的高度
应热是__相同_____的,这就是盖斯定律。 与上山的途
径无关”,
浅显地对特
2. 【讲解盖斯定律】 定化学反应
的反应热进
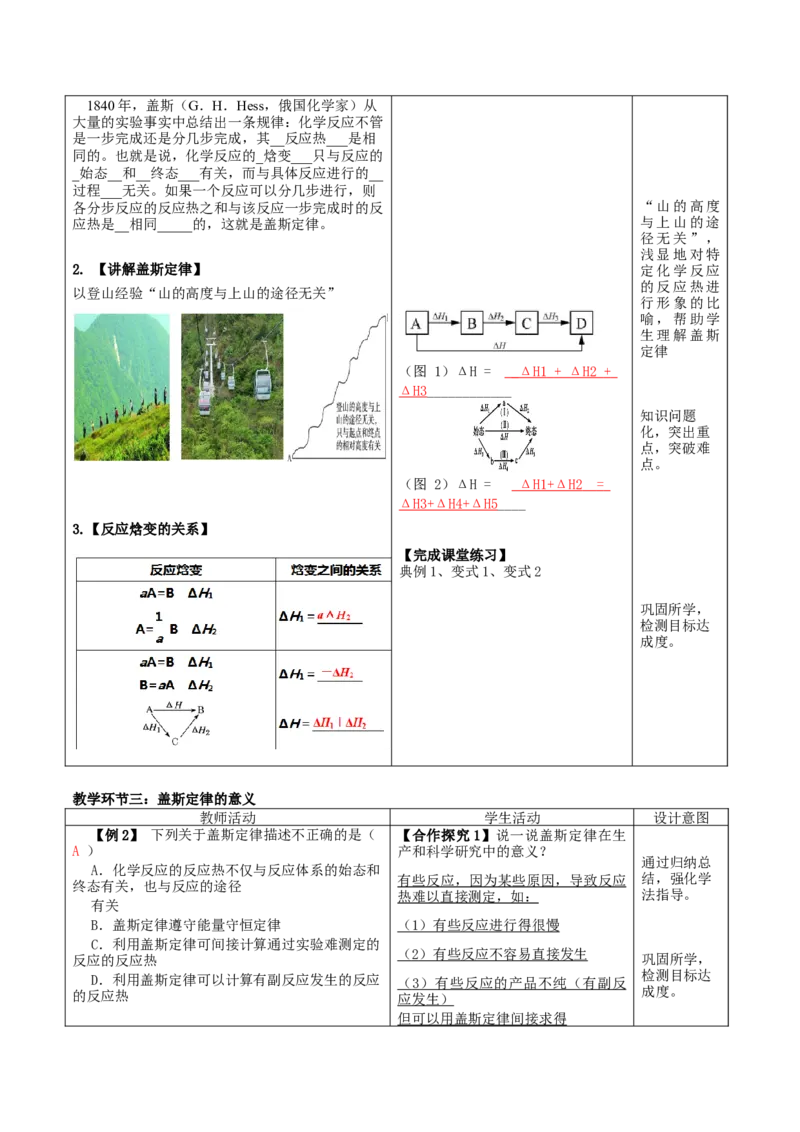
以登山经验“山的高度与上山的途径无关”
行形象的比
喻,帮助学
生理解盖斯
定律
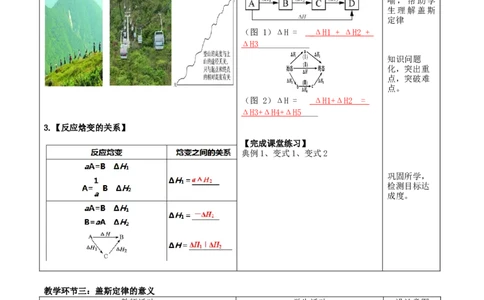
(图 1)ΔH = _ΔH 1 + ΔH 2 +
ΔH3____________
知识问题
化,突出重
点,突破难
点。
(图 2)ΔH = _ΔH1+ΔH 2 =
ΔH3+ΔH4+ΔH5____
3.【反应焓变的关系】
【完成课堂练习】
典例1、变式1、变式2
巩固所学,
检测目标达
成度。
教学环节三:盖斯定律的意义
教师活动 学生活动 设计意图
【例2】 下列关于盖斯定律描述不正确的是( 【合作探究1】说一说盖斯定律在生
A ) 产和科学研究中的意义?
通过归纳总
A.化学反应的反应热不仅与反应体系的始态和
有些反应,因为某些原因,导致反应 结,强化学
终态有关,也与反应的途径
热难以直接测定,如: 法指导。
有关
B.盖斯定律遵守能量守恒定律 ( 1 )有些反应进行得很慢
C.利用盖斯定律可间接计算通过实验难测定的
( 2 )有些反应不容易直接发生
反应的反应热 巩固所学,
检测目标达
D.利用盖斯定律可以计算有副反应发生的反应 ( 3 )有些反应的产品不纯(有副反
成度。
的反应热 应发生)
但可以用盖斯定律间接求得【完成课堂练习】
典例2、变式1、变式2
教学环节四:盖斯定律的应用
教师活动 学生活动 设计意图
【典例3】已知:①2C(s)+O(g)=2CO(g) ΔH=-
2
221.0 kJ·mol-1;
【思考讨论2】热化学反应方程式
②2H(g)+O(g)=2HO(g) ΔH=
2 2 2 加和的方法,目标方程式如何通过
-483.6 kJ·mol-1。 知识问题
“四则运算式”导出?
则制备水煤气的反应C(s)+HO(g)=CO(g)+H(g)的 化,突出重
2 2
ΔH为( D ) 方法总结:写出目标方程式, 点,突破难
点。
A.+262.6 kJ·mol-1 B.-131.3 确定“过渡物质” ( 要消去的物
kJ·mol-1 质 ) ,
C.-352.3 kJ·mol-1 D.+131.3
然后用消元法逐一消去“过渡物
kJ·mol-1
质”,导出“四则运算式”。
【解析】根据盖斯定律,由题意知:①×1/2-
【思考讨论3】利用盖斯定律求反
②×1/2得:
应热的步骤:
ΔH=(-221.0 kJ·mol-1)×1/2-(-483.6
kJ·mol-1)×1/2=+131.3 kJ·mol-1。 ( 1 )确定要求反应热的待求
方程式(目标方程式)。
【典例4】已知:
( 2 )分析其反应物、生成物在条
① CO(g) + 1/2O(g) = CO(g) ΔH1 = - 283.0
2 2 件方程式中的位置,明确根据已知
kJ·mol-1
方程式如何得到目标方程式(加减
② H(g) + 1/2O(g) = HO(l) ΔH2 = - 285.8 乘除)。
2 2 2
kJ·mol-1
“同边相减,不同边相加”(消
③CHOH(l)+3O(g)=2CO g)+3HO(l) ΔH3=-
2 5 2 2( 2
元)
1370 kJ·mol-1
试计算④2CO(g)+4H(g)=HO(l)+CHOH(l)的ΔH
2 2 2 5 ( 3 )根据方程式的运算方式得出
巩固所学,
【解析】①×2+②×4-③=④ △ H 的计算方式 (△ H 必须带符号
检测目标达
ΔH=ΔH1×2+ΔH2×4-ΔH3 进行计算)。
成度。
=-283.2 kJ·mol-1×2-285.8
kJ·mol-1×4+1 370 kJ·mol-1 【完成课堂练习】
典例3、变式1、变式2
=-339.6 kJ·mol-1
教学环节五:课堂检测和作业布置
教师活动 学生活动 设计意图
【课堂检测】
1、(1)已知:①2C(s)+O(g)=2CO(g) △H1=
2
-221.0 kJ·mol-1
【作业布置】
巩固所学,
② 2H(g)+O(g)=2HO(g) △H2=-
2 2 2 1、自我梳理本节课知识点,并 检测目标达
483.6kJ·mol-1
以思维导图或形式整理。完成本 成度。
则制备水煤气的反应③C(s)+H 2 O(g)=CO(g)+H 2 (g) 节内容盖斯定律的配套练习
的△H等于_ + 131. 3 kJ·mo l - 1 2、完成课后提升题。
(2)已知反应: 3、预习下一节内容反应热的计
①H(g) + O(g) = HO(g) ΔH1 算,并完成导学案
2 2 2
② N(g) + O(g) = NO(g) ΔH2
2 2 2
③ N(g) + H(g) =NH(g) ΔH3
2 2 3
则 反 应 2NH(g) + O2(g) =2NO(g) + 3HO(g) 的
3 2 2ΔH=__
2、近年来,随着聚酯工业的快速发展,氯气的需求量
和氯化氢的产出量也随之迅速增长。因此,将氯化氢
转化为氯气的技术成为科学研究的热点。回答下列问
题:
(2)Deacon直接氧化法可按下列催化过程进行:
CuCl(s)=CuCl(s)+1/2Cl(g)
2 2
ΔH1=+83 kJ·mol− 1
CuCl(s)+1/2O
2
(g)=CuO(s)+1/2Cl
2
(g) ΔH2=− 20
kJ·mol− 1
CuO(s)+2HCl(g)=CuCl
2
(s)+H
2
O(g) ΔH3=−121
kJ·mol− 1
则4HCl(g)+O(g)=2Cl(g)+2HO(g)的 ΔH=
2 2 2
教学环节六:板书设计
教师活动 学生活动 设计意图
一.盖斯定律的内容
定义:化学反应不管是一步完成还是分几步完
成,其__反应热___是相同的。也就是说,化学反应
的_焓变___只与反应的_始态__和__终态___有关,
理论性知
而与具体反应进行的__过程___无关。如果一个反应
识,方便学
可以分几步进行,则各分步反应的反应热之和与该 总结本课知识点,及时发现问题
生梳理本课
反应一步完成时的反应热是__相同_____的,这就是
知识点
盖斯定律。
二、盖斯定律的意义
三、盖斯定律的应用
教学环节七:教学评价与反馈
教师活动 教学评价 设计意图
评价任务一:学生理解盖斯定律内
容
对学生掌握
教学反思:本节课侧重于学生技能的掌握,因此要 知识、形成
特别注意讲练结合,在教学过程中多关注学生的实 能力的状况
评价任务二:学生理解盖斯定律应
际掌握情况,给予方法上的指导。 作出准确及
用
时的评价和
反馈