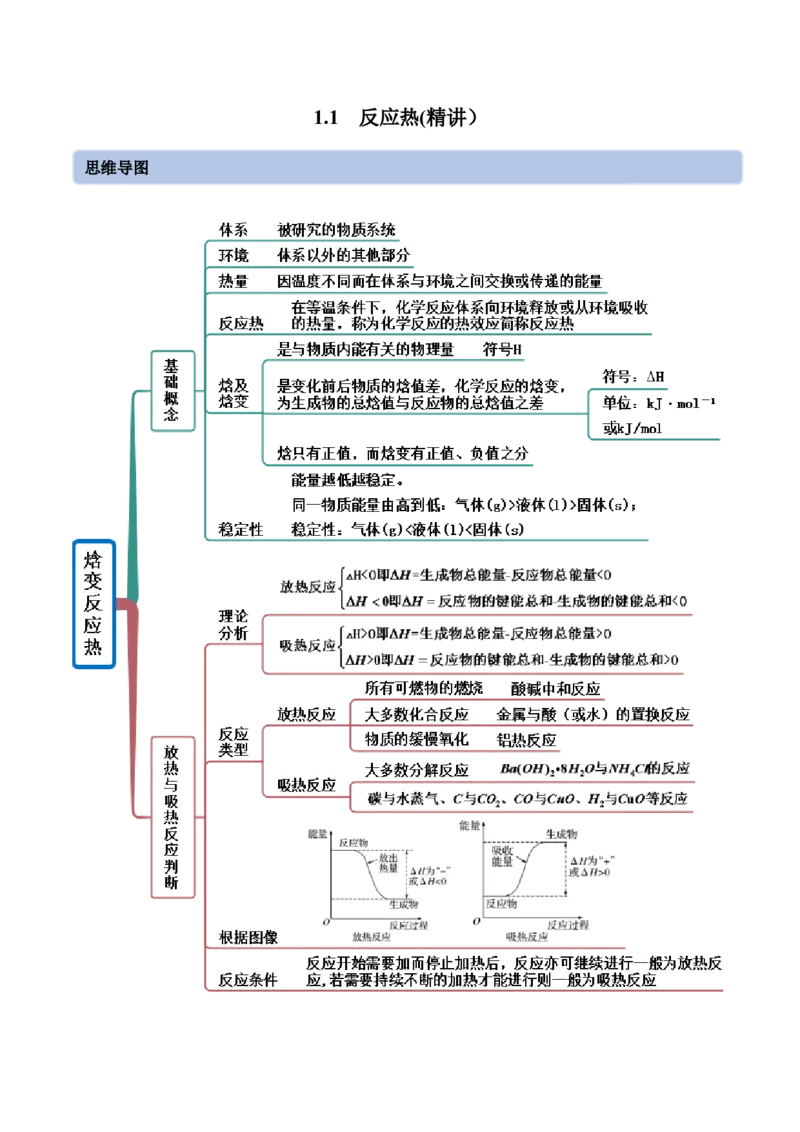
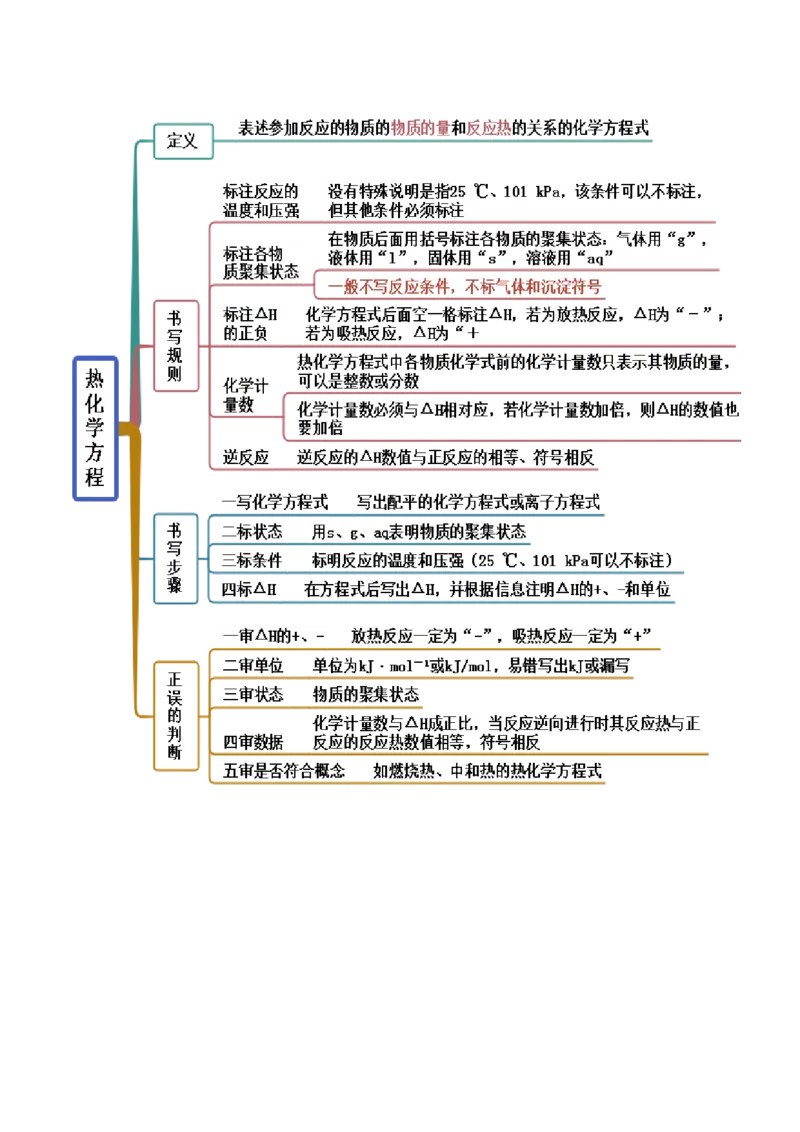
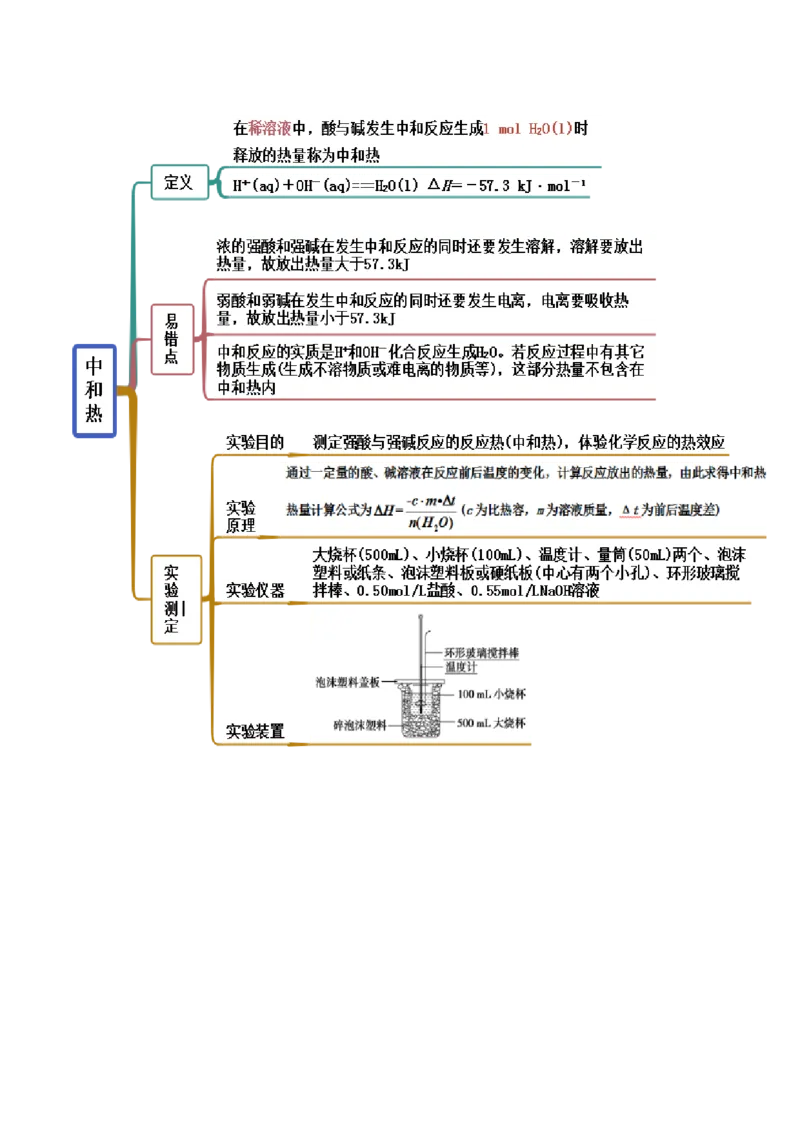
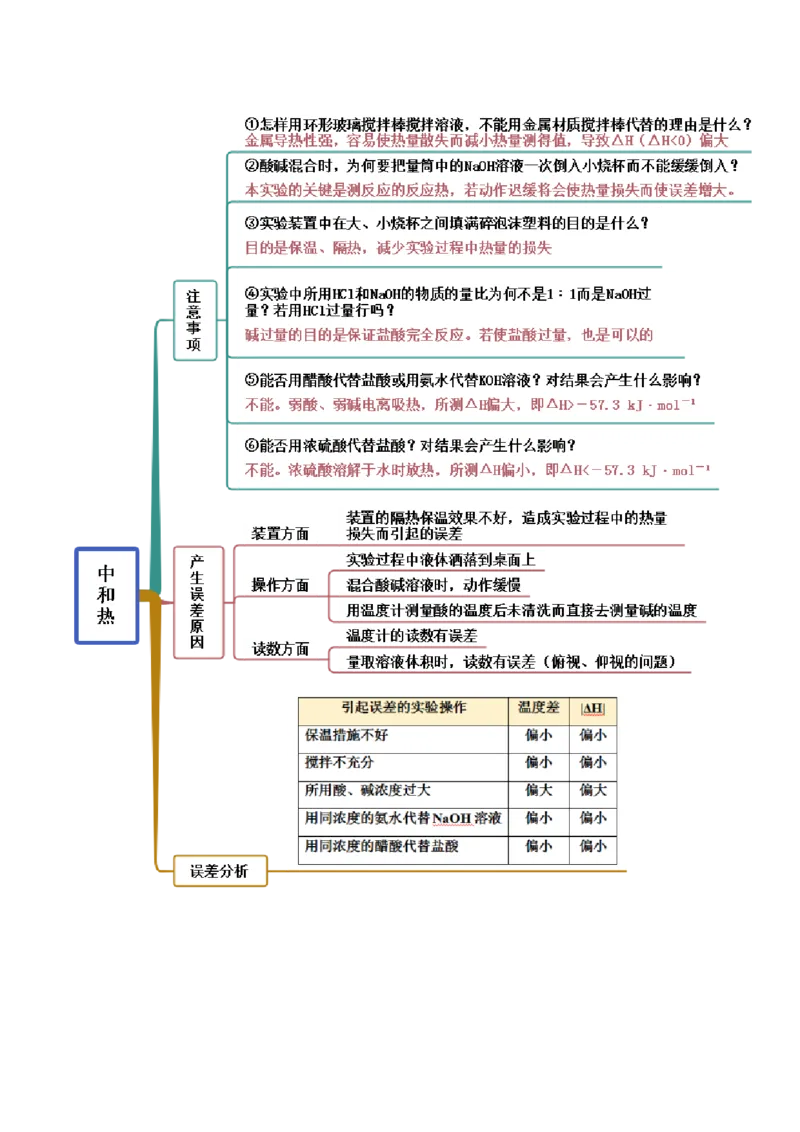
文档内容
1.1 反应热(精讲)
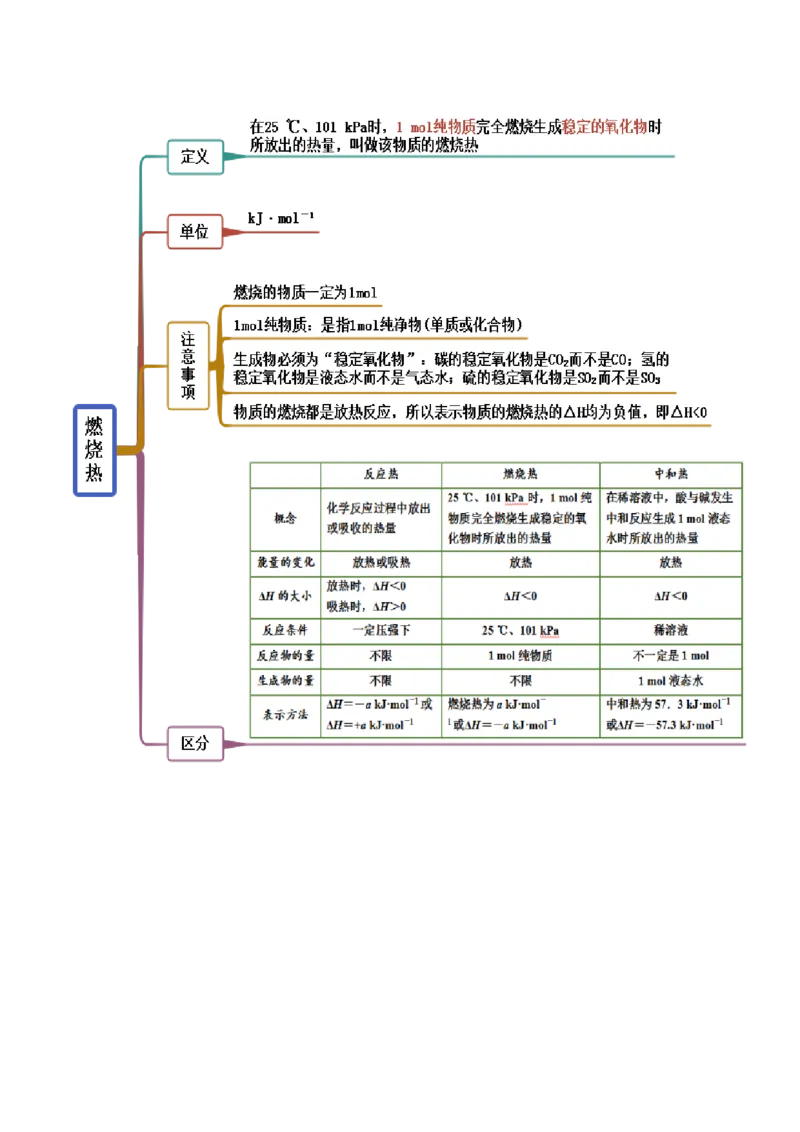
思维导图常见考点
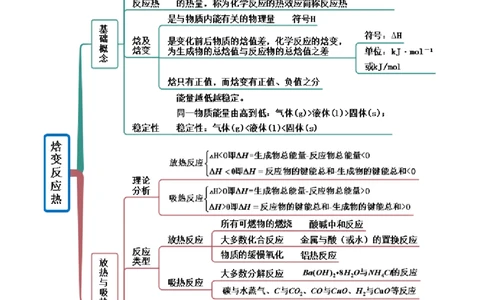
考点一 反应热与焓
【例1】(2022·上海·高二专题练习)已知反应CH(g)+2O(g)=CO (g)+2HO(g)为放热反应,则下列说法
4 2 2 2
中正确的是
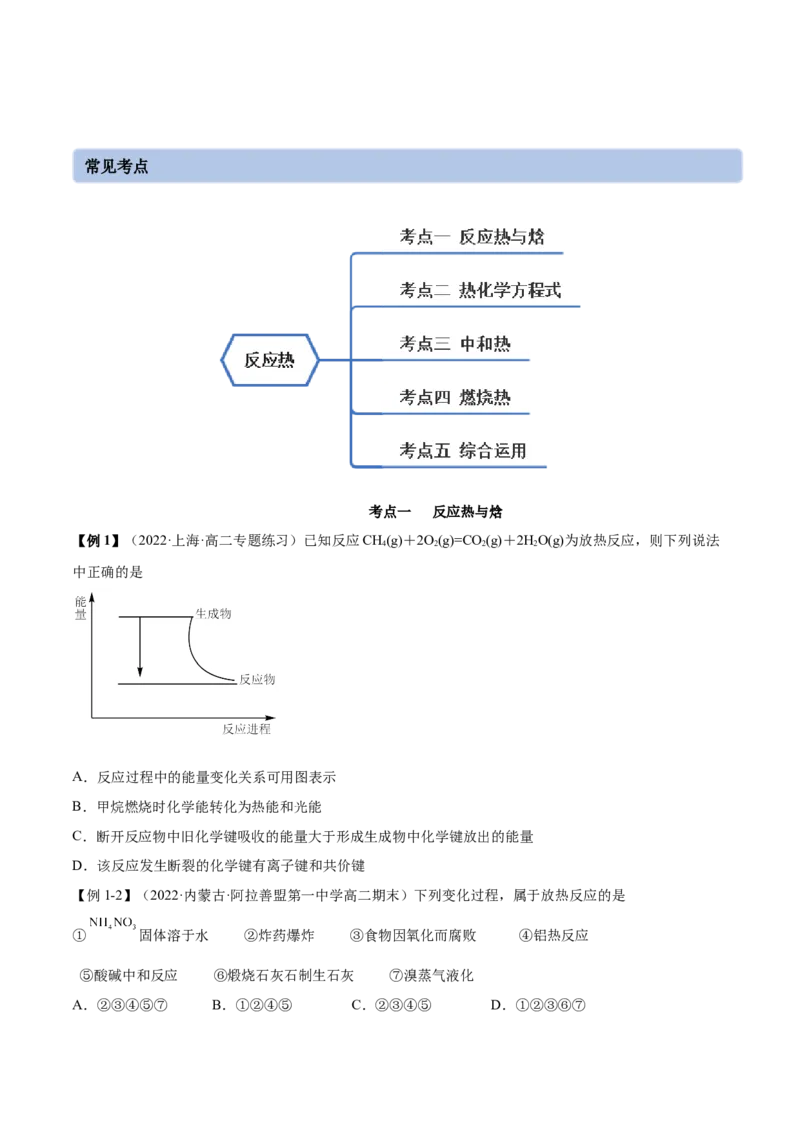
A.反应过程中的能量变化关系可用图表示
B.甲烷燃烧时化学能转化为热能和光能
C.断开反应物中旧化学键吸收的能量大于形成生成物中化学键放出的能量
D.该反应发生断裂的化学键有离子键和共价键
【例1-2】(2022·内蒙古·阿拉善盟第一中学高二期末)下列变化过程,属于放热反应的是
① 固体溶于水 ②炸药爆炸 ③食物因氧化而腐败 ④铝热反应
⑤酸碱中和反应 ⑥煅烧石灰石制生石灰 ⑦溴蒸气液化
A.②③④⑤⑦ B.①②④⑤ C.②③④⑤ D.①②③⑥⑦【一隅三反】
1.(2022·上海·高二单元测试)下列说法正确的是
A.反应焓变是指1mol物质参加反应时的能量变化
B.1mol液态水与18g冰的内能是相等的
C.在加热条件下发生的反应均为吸热反应
D.一个化学反应中,当反应物能量大于反应产物能量时,反应放热,ΔH为“-”
2.已知CH(g)+2O(g)=CO (g)+2HO(l) ΔH= -890 kJ·mol-1。下列说法正确的是
4 2 2 2
A.反应物的焓大于生成物的焓
B.反应物的焓小于生成物的焓
C.根据能量守恒定律,反应物的焓等于生成物的焓
D.该反应为吸热反应
3.下列说法正确的是
A.反应热是1 mol物质参加反应时的能量变化
B.当反应放热时ΔH>0,反应吸热时ΔH<0
C.任何条件下,化学反应的焓变都等于化学反应的反应热
D.在一定条件下,某一化学反应的热效应,取决于反应物和生成物总能量的相对大小
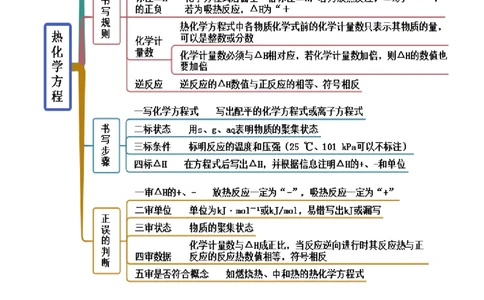
考点二 热化学方程式
【例2】依据实验数据,写出下列反应的热化学方程式。
(1)1 mol C H(g)与适量O(g)反应,生成CO(g)和HO(l),放出1 411 kJ的热量
2 4 2 2 2
(2)1 mol C HOH(l)与适量O(g)反应,生成CO(g)和HO(l),放出1 367 kJ的热量
2 5 2 2 2
(3)2 mol Al(s)与适量O(g)反应,生成Al O(s),放出1 669.8 kJ的热量
2 2 3
(4)18 g葡萄糖与适量O(g)反应,生成CO(g)和HO(l),放出280.4 kJ的热量
2 2 2
(5)1molN (g)与适量H(g)反应生成NH (g)放出92.4kJ热量
2 2 3
______________________ _
(6)1molC(s)与适量HO(g)反应生成CO(g)和H(g),吸收131.5kJ热量
2 2
__________________ __(7)常温常压下,乙烯(C H)燃烧热△H=—1411.0kJ·mol-1
2 4
____________ ___
(8) 常温常压下,乙醇【C HOH】(l)的燃烧热△H=—1366.8kJ·mol-1
2 5
(9)SiH 是一种无色气体,遇到空气能发生爆炸性自燃,生成固体SiO 和液态HO。已知室温下,2gSiH 自
4 2 2 4
燃放出89.2kJ热量
【一隅三反】
1.1mol氨气分解成氮气和氢气需要吸收46.2kJ热量,下列热化学方程式中正确的是
A.
B.
C.
D.
2. 氨气分解成氮气和氢气要吸收 的热量,下列热化学方程式中正确的是
A.
B.
C.
D.
3.写出下列反应的热化学方程式。
(1)N(g)与H(g)反应生成17gNH (g),放出46.1kJ热量。
2 2 3
_ _
(2)1molC HOH(l)完全燃烧生成CO(g)和HO(l),放出1366.8kJ热量。
2 5 2 2
(3)1molCO完全转化为CO 放出283kJ的热量。
2
(4)24gC(s)与足量HO(g)反应生成CO(g)和H(g),吸收262.6kJ热量。
2 2(5)1L1mol·L-1稀盐酸跟1L1mol·L-1NaOH溶液发生中和反应放出57.3kJ热量。
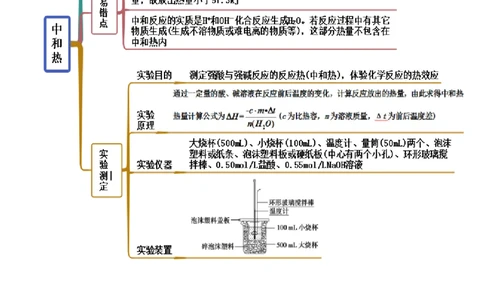
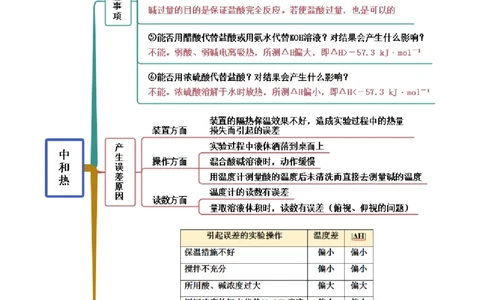
考点三 中和热
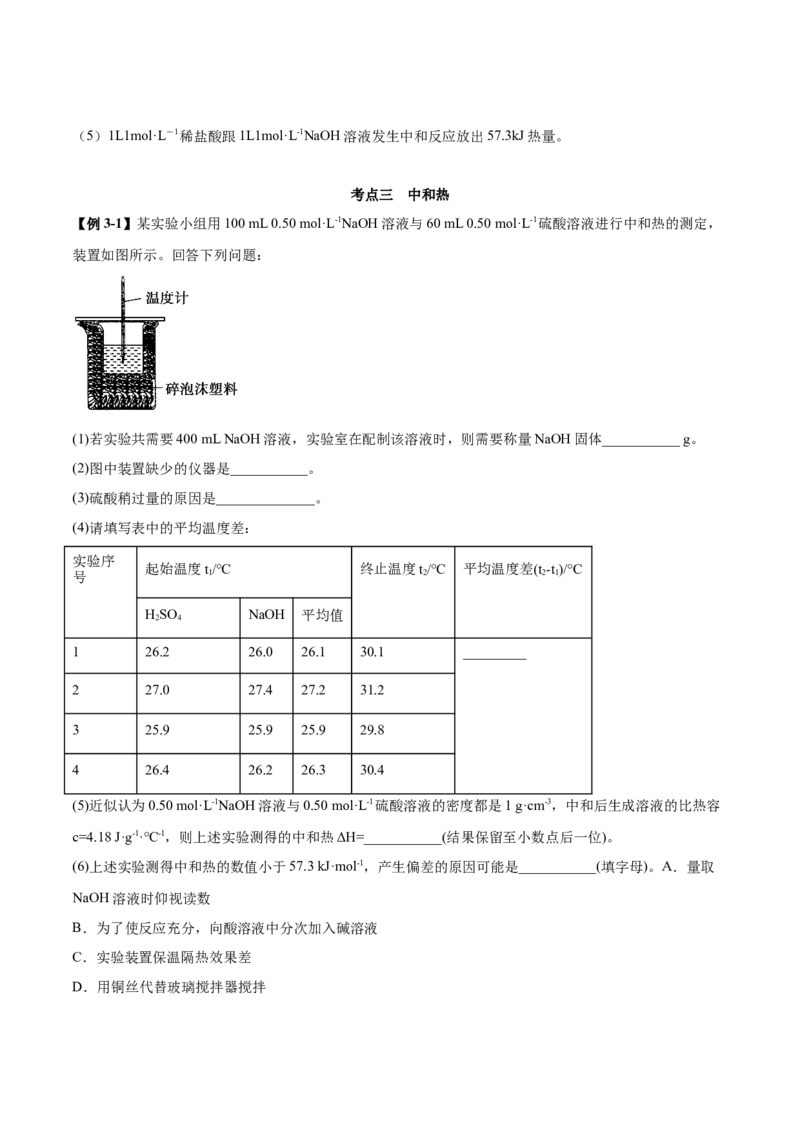
【例3-1】某实验小组用100 mL 0.50 mol·L-1NaOH溶液与60 mL 0.50 mol·L-1硫酸溶液进行中和热的测定,
装置如图所示。回答下列问题:
(1)若实验共需要400 mL NaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体___________ g。
(2)图中装置缺少的仪器是___________。
(3)硫酸稍过量的原因是______________。
(4)请填写表中的平均温度差:
实验序
起始温度t/℃ 终止温度t/℃ 平均温度差(t -t )/°C
号 1 2 2 1
HSO NaOH 平均值
2 4
1 26.2 26.0 26.1 30.1 _________
2 27.0 27.4 27.2 31.2
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
(5)近似认为0.50 mol·L-1NaOH溶液与0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容
c=4.18 J·g-1·℃-1,则上述实验测得的中和热ΔH=___________(结果保留至小数点后一位)。
(6)上述实验测得中和热的数值小于57.3 kJ·mol-1,产生偏差的原因可能是___________(填字母)。A.量取
NaOH溶液时仰视读数
B.为了使反应充分,向酸溶液中分次加入碱溶液
C.实验装置保温隔热效果差
D.用铜丝代替玻璃搅拌器搅拌【一隅三反】
1.中和热测定实验中,用50mL 0.50mol/L盐酸和50mL 0.55mol/LNaOH溶液进行实验,下列说法不正确
的是
A.酸碱混合时,量筒中NaOH溶液应一次性倒入小饶杯中,不断用玻璃棒搅拌
B.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热减少热量损失
C.用量筒量取NaOH溶液时,仰视取液,测得的中和热∆H偏大
D.改用25mL 0.50mol/L盐酸和25mL 0.55mol/LNaOH溶液进行反应,求出的中和热∆H比原来的偏小
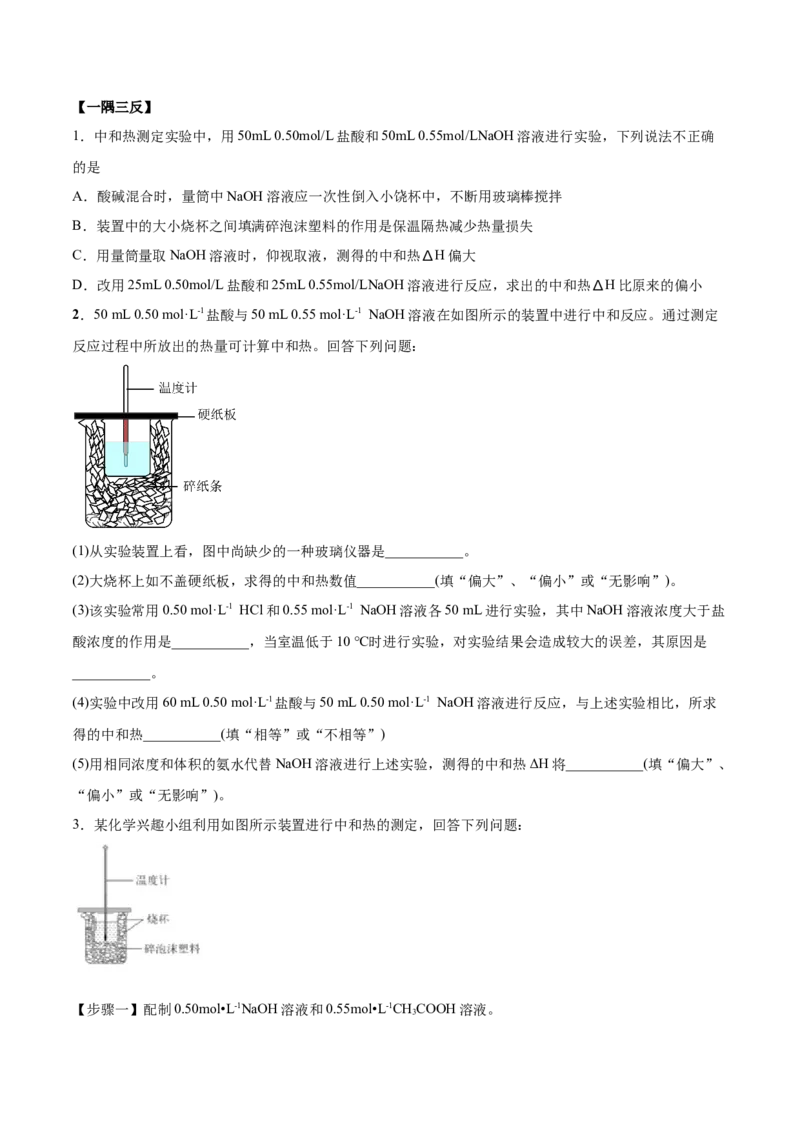
2.50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定
反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是___________。
(2)大烧杯上如不盖硬纸板,求得的中和热数值___________(填“偏大”、“偏小”或“无影响”)。
(3)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1 NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐
酸浓度的作用是___________,当室温低于10 ℃时进行实验,对实验结果会造成较大的误差,其原因是
___________。
(4)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求
得的中和热___________(填“相等”或“不相等”)
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将___________(填“偏大”、
“偏小”或“无影响”)。
3.某化学兴趣小组利用如图所示装置进行中和热的测定,回答下列问题:
【步骤一】配制0.50mol•L-1NaOH溶液和0.55mol•L-1CHCOOH溶液。
3(1)此实验装置中尚缺少的一种玻璃仪器是__。
(2)若实验中大约要使用240mLNaOH溶液,需要托盘天平称量NaOH固体__g。
(3)配制0.50mol•L-1NaOH溶液时需要用到的玻璃仪器是__(从表中选择相应的仪器,填字母)。
名称 托盘天平(带砝码) 小烧杯 容量瓶 玻璃棒 药匙 胶头滴管
仪器
序号 a b c d e f
【步骤二】中和热测定:取50.00mLNaOH溶液和50.00mLCHCOOH溶液进行实验,实验数据如表:
3
起始温度t/℃
温度 1
终止温度t/℃ 温度差平均值(t -t )/℃
2 2 1
实验次数
CHCOOH NaOH 平均值
3
1 26.2 26.8 26.5 29.5
2 26.4 26.2 26.3 32.4
3 25.9 25.9 25.9 28.8
4 27.0 27.4 27.2 30.3
(4)若中和后溶液的比热容为4.18J•g-1•℃-1,醋酸和NaOH溶液的密度都近似认为是1g•cm-3,则此反应中和
热 H=__(取小数点后一位)。
(5)△甲同学通过查找资料得知HCl与NaOH反应的中和热为57.3kJ•mol-1,上述所测值有偏差,产生偏差的
原因可能是___(填字母)。
a.反应时搅拌不充分;b.酸、碱混合时,动作迟缓;c.称量NaOH时,砝码生锈了;d.用温度计测定NaOH
溶液起始温度后直接测定CHCOOH溶液的温度;e.量取NaOH溶液的滴定管只水洗未用所盛NaOH溶液
3
润洗。
乙同学认为所测值与57.3kJ•mol-1数值偏差太大,还可能与反应物醋酸有关,理由是__。
考点四 燃烧热
【例4】已知下列热化学方程式:
①H(g)+ O(g)=HO(l) ΔH=-285kJ·mol-1
2 2 2②H(g)+ O(g)=HO(g) ΔH=-241kJ·mol-1
2 2 2
③C(s)+ O(g)=CO(g) ΔH=-110kJ·mol-1
2
④C(s)+O(g)=CO (g) ΔH=-393kJ·mol-1,
2 2
回答下列问题:
(1)H 的燃烧热为__ _kJ·mol-1;C的燃烧热为_ __kJ·mol-1。
2
(2)燃烧10gH 生成液态水,放出的热量为__ _kJ。
2
(3)写出表示CO燃烧热的热化学方程式_ __。
【一隅三反】
1.下列热化学方程式中, 能表示对应物质的燃烧热的是( )
A.
B.
C.
D.
2.下列关于燃烧热的说法正确的是( )
A.某物质燃烧放出的热量就是该物质的燃烧热
B. 可燃物燃烧所放出的热量就是燃烧热
C. 可燃物完全燃烧生成指定产物时所放出的热量就是燃烧热
D.在 时, 可燃物完全燃烧生成指定产物时所放出的热量是燃烧热
3.现在城市居民使用的管道煤气的主要成分是H、CO和少量CH。H、CO和CH 的燃烧热数据如下表
2 4 2 4
物质 H CO CH
2 4
燃烧热(kJ•mol-1) 285.8 283.0 890.3
(1)请写出H、CO和CH 燃烧的热化学方程式:
2 4(1)__________ ___________;
(2)_________ ___________;
(3)_______ ________________
考点五 反应热的综合运用
【例5】Ⅰ.已知下列热化学方程式:①H(g)+ O(g)=HO(l) ∆H=-285kJ·mol-1,
2 2 2
②H(g)+ O(g)=HO(g) ∆H=-241.8kJ·mol-1,
2 2 2
③C(s)+ O(g)=CO(g) ∆H=-110.5kJ·mol-1,
2
④C(s)+O(g)=CO (g)ΔH=-393.5kJ·mol-1,回答下列问题:
2 2
(1)C燃烧热的热化学方程式为___________;(填序号)
(2)燃烧1gH 生成气态水,放出的热量为___________。
2
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热
化学方程式为H+(aq)+OH-(aq)=H O(l) ∆H =-57.3kJ•mol-1。
2 1
(3)下列各组试剂混合发生反应的离子方程式为H++OH-=H O的是___________(填序号)。
2
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1molH O(l),则反应放出的热量___________(填“大于”“等于”或
2
“小于”)57.3kJ,原因是___________。
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。
(5)据图可判断出反应物的总键能___________(填“>”“<”或“=”,下同)生成物的总键能,则该反应的反应热∆H ___________0。
【一隅三反】
1.(2021·甘肃·民勤县第四中学高二期末)已知下列热化学方程式:
①2H(g) +O (g) = 2HO(l) H = -571.6 kJ/mol
2 2 2
②C(s) + O
2
(g) = CO
2
(g) H△ = -393.5 kJ/mol
③C(s) + H
2
O(g) = CO(g) + H△2 (g) H = +131.5 kJ/mol
请回答: △
(1)上述反应中属于放热反应的是_______(填序号),固体碳的燃烧热为_______。
(2)1molH 完全燃烧生成液态水,放出的热量为_______。
2
(3)依据事实,写出下列反应的热化学方程式。
①1molN (g)与适量O(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为_______。
2 2
②已知HCl稀溶液与NaOH稀溶液反应生成1mol HO时,放出57.3kJ热量,用离子方程式表示该反应的
2
热化学方程为_______。
2.(2021·江西·铅山县第一中学高二阶段练习)化学反应过程中发生物质变化的同时,常常伴有能量的变
化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,
如标准燃烧热和中和反应反应热等。
(1)下列ΔH表示物质标准燃烧热的是_______;表示中和反应反应热的是_______。(填
“ΔH”、“ΔH”、“ΔH”等)
1 2 3
A.2H(g)+O(g)=2HO(l) ΔH
2 2 2 1
B.C(s)+ O(g)=CO(g) ΔH =-Q kJ·mol-1
2 2 1
C.CH(g)+2O(g)=CO (g)+2HO(g) ΔH
4 2 2 2 3
D.C(s)+O(g)=CO (g) ΔH =-Q kJ·mol-1
2 2 4 2
E.Ba(OH) (aq)+HSO (aq)= BaSO(aq)+2HO(l) ΔH
2 2 4 4 2 5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+HO(l) ΔH
2 6
(2)1 g C H 气体完全燃烧生成液态水和CO 气体,放出50 kJ的热量,写出该反应的热化学方程式:
2 2 2
_______。
(3)根据题(1)中B、D判断1 molCO(g)完全燃烧的ΔH=_______。
(4)反应F的ΔH 可以用如图所示的装置进行测量。
6从实验装置上看,图中有两种错误,分别是_______;_______;大烧杯上如不塞碎塑料泡沫,求得的中和
反应的反应热的数值_______(填“偏大”“偏小”或“无影响”)。
3.以下几个热化学方程式中:
①2H(g)+O(g)=2HO(l) ΔH=-571.6kJ·mol-1
2 2 2
②CO(g)+ O(g)=CO (g) ΔH=-283kJ·mol-1
2 2
③C(s)+O(g)=CO (g) ΔH=-393.5kJ·mol-1
2 2
④CaCO =CaO+CO ΔH=+177.7kJ·mol-1
3 2
⑤C(s)+HO(g)=CO(g)+H(g) ΔH=+131.3kJ·mol-1
2 2
⑥HNO(aq)+NaOH(aq)=NaNO (aq)+HO(l) ΔH=-57.3kJ·mol-1
3 3 2
⑦ HSO (l)+NaOH(l)= NaSO (l)+HO(l) ΔH=-57.3kJ·mol-1
2 4 2 4 2
不正确的有___;表示燃烧热的热化学方程式有___,表示中和热的热化学方程式有___。(填序号)倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育